GC-MS/MS法测定食品接触用硅橡胶制品中6种环硅氧烷迁移量
2022-10-22葛丹阳刘桂华祝雨筱商贵芹罗世鹏胡长鹰
葛丹阳, 刘桂华, 姜 欢, 祝雨筱, 商贵芹, 罗世鹏, 胡长鹰*
(1. 暨南大学 食品科学与工程系, 广东 广州 510632;2. 常州工业及消费品检验有限公司, 江苏 常州 213000;3. 南京海关危险货物与包装检测中心, 江苏 常州 213000;4. 江苏理工学院 化学与环境工程学院, 江苏 常州 213000)
硅橡胶因其良好的物理化学性能, 已成为一种应用广泛的食品接触材料。然而, 硅橡胶在聚合过程中由于不完全硫化产生环硅氧烷, 其可以迁移到食品中, 进而影响食品安全[1]。目前国内外尚未制定环硅氧烷的迁移限量, 但由于这些物质在食品接触材料领域属于非有意添加物(Non intentionally added substances, NIAS)[2], 有必要对其迁移风险进行监测或管控。
研究表明, 环硅氧烷会影响环境[3]和生物体[4-5]。挥发性环硅氧烷也可释放到大气或沼气池中进一步在鸟类[6]和鱼类[7]等生物体中富集。长期暴露于八甲基环四硅氧烷(D4)和十甲基环五硅氧烷(D5)中可损伤大鼠的生殖系统, 缩短其衰老周期, 从而加速其衰老[8]。D4、D5和十二甲基环六硅氧烷(D6)已于2018年6月被欧洲化学品管理局(ECHA)列入高度关注物质(SVHC)候选名单。刘宜奇等[9]用毒理学关注阈值(TTC)法对环硅氧烷D4~D6进行毒理学评估, 发现它们属于CramerⅢ类物质, 表明此类物质可能引起的食品安全风险需引起更多关注。
由于食品基质复杂, 在对食品接触材料中的目标物进行迁移风险评估时, 通常使用合适的食品模拟物代替食品进行迁移实验[10-12]。环硅氧烷属于亲脂类物质, 更易向油脂类食品模拟物或其替代溶剂迁移, 其中聚合度较低的环硅氧烷(如D4~D9)在发生迁移后, 相比于聚合度较高和分子量较大的环硅氧烷更容易进入人体代谢, 因此开发环硅氧烷向油脂类食品模拟物和其替代溶剂中迁移量的检测方法对于保障硅橡胶的食品安全至关重要。目前对于环硅氧烷最常见的检测方法包括气相色谱-质谱法(GCMS)[13-16]和气相色谱-串联质谱法(GC-MS/MS)[17], 其中GC-MS/MS法的分离效果更好、灵敏度更高。因此本研究基于GC-MS/MS建立了一种同时测定硅橡胶中6种环硅氧烷(D4~D9)向油脂类食品模拟物(50%乙醇)和常见的油脂类替代溶剂(95%乙醇和异辛烷)中迁移量的检测方法, 以满足市场上食品接触用硅橡胶制品中D4~D9迁移量的检测需要, 并利用建立的方法测定市场上用于食品接触的硅橡胶制品中6种环硅氧烷在食品模拟物中的迁移情况, 为相关监管标准的制定提供参考。
1 实验部分
1.1 试剂与材料
丙酮、正己烷(色谱纯, 上海安谱实验科技股份有限公司), 无水乙醇(常州大恒化工有限公司)。6种标准物质:八甲基环四硅氧烷(D4, CAS号:556-67-2, 纯度≥99. 9%, 坛墨质检科技股份有限公司);十甲基环五硅氧烷(D5, CAS号:541-02-6, 纯度≥99. 0%, 萨恩化学技术(上海)有限公司);十二甲基环六硅氧烷(D6, CAS号:540-97-6, 纯度≥97. 0%, 上海安谱实验科技股份有限公司);十四甲基环庚硅氧烷(D7, CAS号:107-50-6, 纯度≥99. 6%, 坛墨质检科技股份有限公司);十六甲基环八硅氧烷(D8, CAS号:556-68-3, 纯度≥96. 0%, 上海百灵威化学技术有限公司);十八甲基环壬硅氧烷(D9, CAS号:556-71-8, 纯度≥98. 0%, 上海百灵威化学技术有限公司)。
5 mL一次性注射器、0. 22μm尼龙针式过滤器、2 mL玻璃进样瓶(上海安谱实验科技股份有限公司)。
38批次的硅橡胶样品来源于电商平台或线下供应商。
1.2 仪器与设备
Agilent 7890B-7000D气相色谱-三重四极杆质谱联用仪(美国Agilent公司);Milli-Q超纯水纯化系统(美国Millipore公司);XS 204型电子天平(美国梅特勒托利多公司);电热恒温鼓风干燥箱(上海市新苗医疗器械制造有限公司);SIGMA 3-15通用型台式高速离心机(北京博励行仪器有限公司);MVM-2500数显型多管式漩涡混合器(上海泰坦科技股份有限公司)。
1.3 实验方法
1.3.1 溶液配制标准储备液(100 mg/L):分别准确称取D4~D9的标准物质各10. 0 mg于小烧杯中, 用丙酮溶解后转移至10 mL容量瓶, 将小烧杯用少量丙酮清洗3次, 合并清洗液至容量瓶中, 以丙酮定容至刻度, 得到目标物质量浓度为1 000 mg/L的单一标准储备液。准确移取上述标准储备液各1 mL于10 mL容量瓶中, 用丙酮定容至刻度, 得到质量浓度为100 mg/L的D4~D9混合标准储备液, 置于冰箱中保存备用。
50%乙醇标准工作溶液:用丙酮将100 mg/L的D4~D9混合标准储备液进行逐级稀释, 得到目标物质量浓度为5、10、20、50、100 mg/L的标准溶液。分别取上述各浓度的标准溶液100μL至10 mL容量瓶中, 用50%乙醇定容至刻度, 得到目标物质量浓度分别为0. 05、0. 10、0. 20、0. 50、1. 00 mg/L的标准工作溶液。
95%乙醇和异辛烷标准工作溶液:取200μL质量浓度为100 mg/L的混合标准储备液于10 mL容量瓶中, 分别用95%乙醇和异辛烷定容, 得到目标物质量浓度为2. 0 mg/L的95%乙醇和异辛烷基质的标准中间液, 再分别用95%乙醇和异辛烷进行逐级稀释, 得到目标物质量浓度为0. 20、0. 50、0. 80、1. 00、1. 50、2. 00 mg/L的标准工作溶液。
1.3.2 迁移实验按照GB 31604. 1-2015《食品安全国家标准食品接触材料及制品迁移试验通则》[18]和GB 5009. 156-2016《食品安全国家标准食品接触材料及制品迁移试验预处理方法通则》[19]对样品进行预处理, 选择合适的试样接触面积与食品模拟物体积比(S/V), 根据样品类型选择全浸没或灌装法的浸泡方式。每个样品重复浸泡3次, 每次均更换新的模拟物, 将第1次和第3次迁移实验后得到的50%乙醇、95%乙醇和异辛烷食品模拟物(以下称为浸泡液)及时密封, 待后续处理。每个样品均设置3个平行样, 同时设置空白对照。
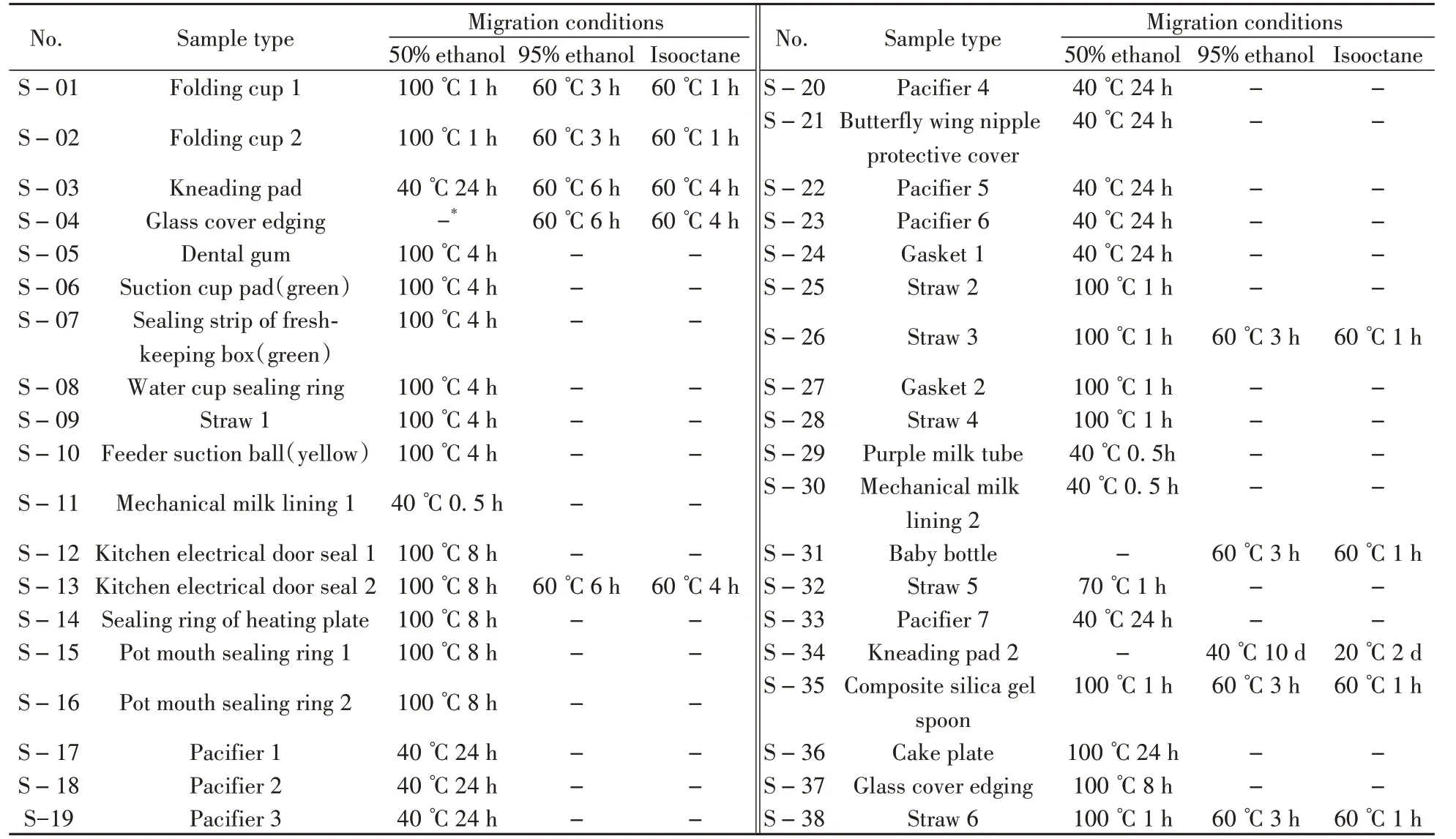
表1 样品信息和迁移实验条件Table 1 Informations and conditions of test samples
1.3.3 食品模拟物的处理取10 mL迁移实验所得的50%乙醇浸泡液于25 mL具盖玻璃离心管中, 加入2 mL正己烷, 旋紧瓶盖后, 以2 000 r/min涡旋萃取3 min, 再以3 000 r/min离心3 min。取上层正己烷提取液过滤至2 mL进样瓶, 待测。
迁移实验得到的95%乙醇和异辛烷无需使用有机溶剂进行萃取处理, 浸泡液经针式过滤器过滤至2 mL进样瓶, 待测。
1.3.4 标准曲线溶液的处理将“1. 3. 1”制备的50%乙醇标准工作溶液按“1. 3. 3”方法进行处理, 分别得到用于相应模拟物定量分析的各目标物质量浓度为0. 05、0. 10、0. 20、0. 50、1. 00 mg/L的标准曲线溶液。95%乙醇和异辛烷的标准曲线溶液无需进行前处理。
1.3.5 仪器条件色谱条件:色谱柱为HP-5 MS(30 m×250μm×0. 10μm);加热程序如下:初始温度为35℃, 保持2 min, 以15℃/min升至240℃, 然后以25℃/min升至280℃, 保持2 min;进样口温度:280℃;注入方式:分流注入, 分流比为3∶1。
质谱条件:溶剂延迟4. 5 min, EI离子源, 离子源温度为280℃, 电子能量为70 eV, 采用多反应监测模式(MRM)。优化的MRM检测参数见表2。
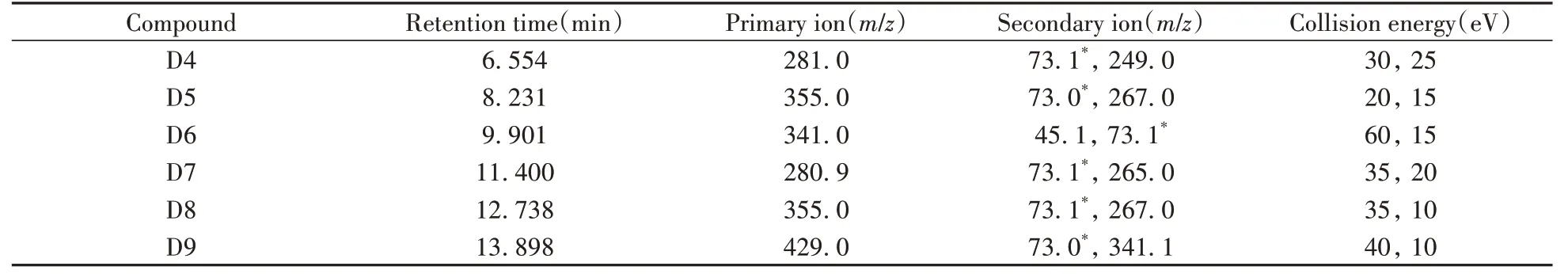
表2 D4~D9的MRM检测参数Table 2 MRM detection parameters of D4-D9
1.3.6 迁移结果计算每个样品中D4~D9的迁移量按下式计算:X=C×V×F/S。式中:X为D4~D9的迁移量(mg/kg);C为迁移得到的浸泡液中D4~D9的质量浓度(mg/L);V为迁移实验中食品或食品模拟物的体积(L);S为迁移实验中样品与食品或食品模拟物的接触面积(dm2);F为样品和食品间的接触面积(dm2)与食品体积或质量(L或kg)的比值。如果样品有实际比值, 根据实际比值进行计算;如果没有实际比值, 则按6 dm2/L或6 dm2/kg计算。
1.3.7 数据分析用Origin 2018作图, 用SPSS 19. 0进行显著性分析。
2 结果与讨论
2.1 实验条件优化
2.1.1 GC条件的选择环硅氧烷化合物具有亲脂性, 而HP-5 MS是高性能通用的非极性石英毛细管柱, 具有较低的柱流失特性, 因此选用HP-5 MS色谱柱进行分离。采用程序升温加热方式, 考察了不同进样口温度下空白样品的响应值和对目标化合物响应的影响, 发现进样口温度在200℃和250℃下, 分子量较大的环硅氧烷(如D8和D9)的响应较差, 而进样口温度在300℃及以上温度时, 空白样品的基线较高, 这可能是由于温度升高而造成了柱流失。因此最终选择进样口温度为280℃, 此温度下既能很好地将目标物汽化又能尽量减少柱流失。
2.1.2 MS条件的选择在全扫描模式下, 确定了6种环硅氧烷的保留时间, 并得到各物质的一级质谱图(图1)。根据一级质谱图选择相对强度较大且具有特征性的离子作为母离子, 如D4的质谱图(图1A), 选择m/z 281. 0的离子作为母离子;而D5虽相对强度最大的离子为m/z 267. 0(图1B), 但选择m/z 355. 0的离子更具有特征性。再通过设定不同的碰撞能量进行优化, 得到各子离子对应的最佳碰撞能, 最终参数如表2所示。
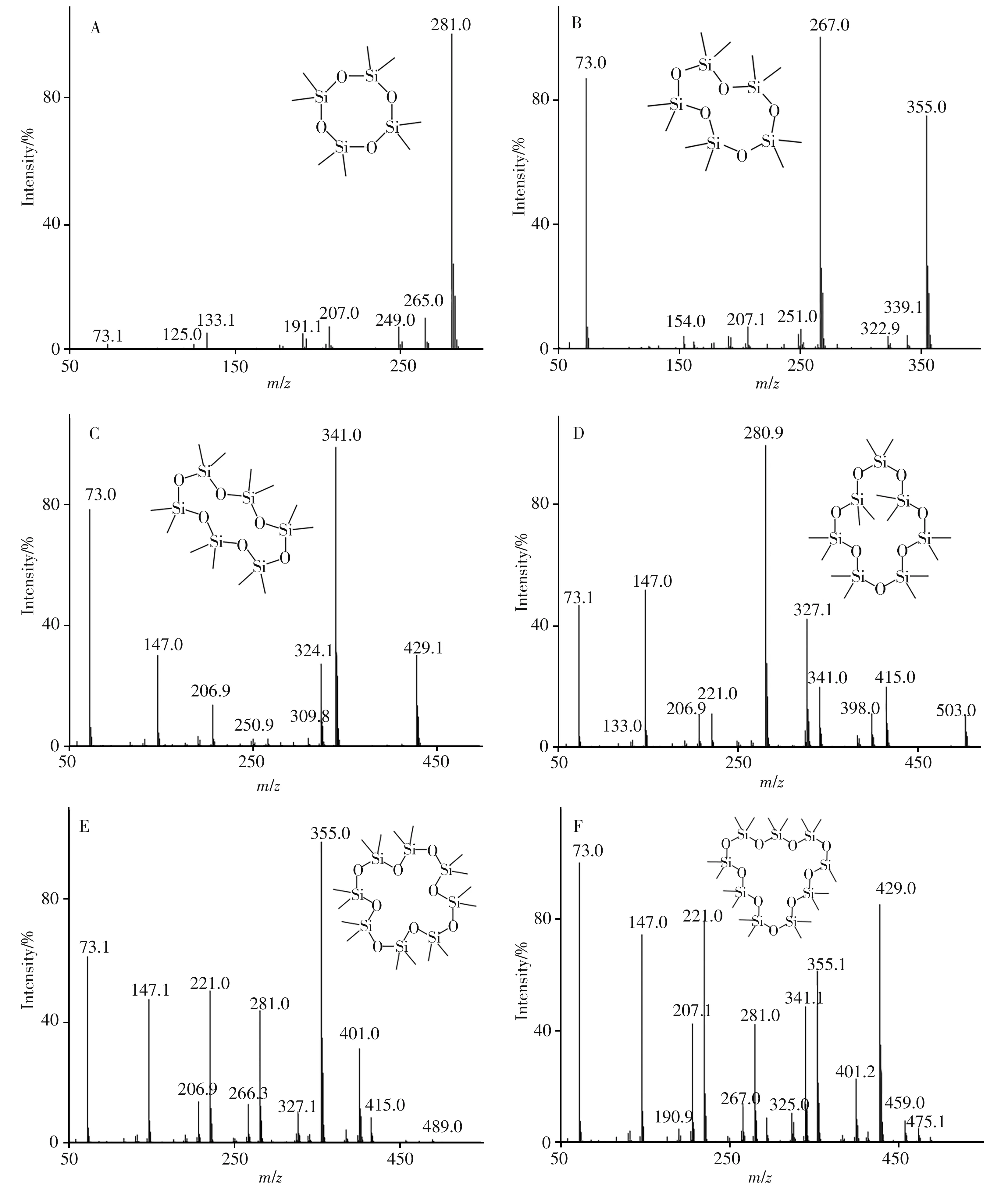
图1 D4(A)、D5(B)、D6(C)、D7(D)、D8(E)与D9(F)的一级质谱图Fig. 1 Primary mass spectra of D4(A), D5(B), D6(C), D7(D), D8(E)and D9(F)
2.1.3 前处理条件的确定由于迁移实验得到的95%乙醇和异辛烷可直接进样, 因此不进行溶剂萃取。而迁移得到的50%乙醇浸泡液中含有高比例的水, 直接进样会损害仪器, 因此选择液液萃取方式将待测物质萃取到有机溶剂后再进行检测。由于环硅氧烷为亲脂性化合物, 在正己烷和二氯甲烷等有机溶剂中均有较好的溶解能力, 并能与水相形成明显的分层, 而使用正己烷进行液液萃取和离心后, 有机相在溶液上层, 易于操作, 因此最终选择正己烷作为萃取溶剂。预实验发现, 加大浸泡液与萃取溶剂的体积比可使D4~D9达到富集效果, 因此为得到更低的检出限, 将浸泡液与萃取溶剂(正己烷)的体积比确定为5∶1。
在优化的实验条件下, 通过MRM模式得到D4~D9混合标准溶液的典型总离子流色谱图如图2所示。
2.2 线性关系、检出限与定量下限
按照“1. 3. 4”处理标准曲线溶液, 然后进行GC-MS/MS测定。以峰面积为纵坐标(y), 以相应标准工作溶液的质量浓度为横坐标(x, mg/L), 绘制各目标物的标准工作曲线。以不低于3倍信噪比(S/N≥3)确定各模拟物中D4~D9的检出限(LOD), 以S/N≥10确定定量下限(LOQ), 结果如表3所示。D4~D9在50%乙醇中的线性范围为0. 05~1. 00 mg/L, 相关系数(r2)不低于0. 996 0;在95%乙醇和异辛烷中的线性范围为0. 20~5. 00 mg/L, r2不低于0. 996 7。D4~D9的检出限为0. 02~0. 07 mg/L, 定量下限为0. 05~0. 20 mg/L, 表明所建立的方法能够满足定量要求。
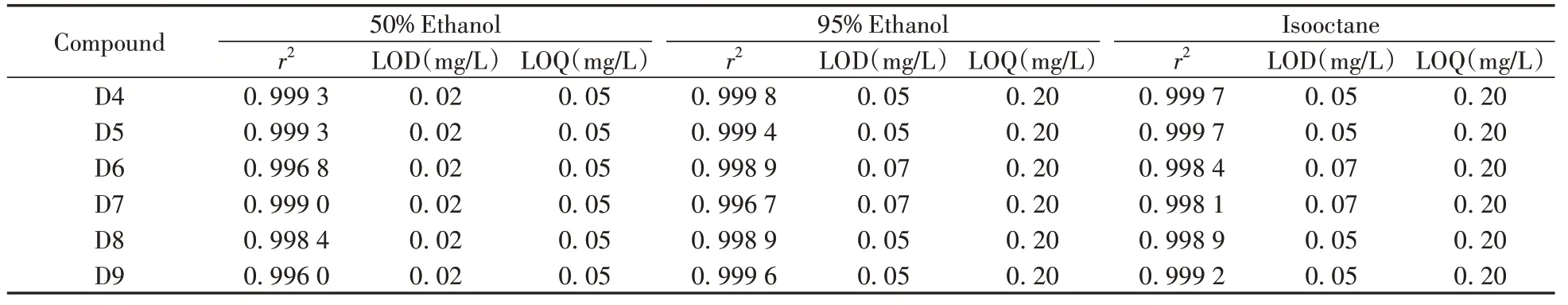
表3 D4~D9的相关系数、检出限与定量下限Table 3 Correlation coefficients, detection limits and quantitation limits of D4-D9
2.3 回收率与相对标准偏差
以不接触样品的50%乙醇浸泡液为溶剂, 制备D4~D9质量浓度分别为0. 05、0. 20、1. 00 mg/L的加标溶液;以不接触样品的95%乙醇和异辛烷浸泡液为溶剂, 制备D4~D9质量浓度分别为0. 20、1. 00、5. 00 mg/L的加标溶液。每种浓度制备6个平行样品, 按“1. 3. 3”方法进行处理并测定。结果显示, D4~D9在50%乙醇中的加标回收率为90. 1%~101%, 相对标准偏差(RSD)为0. 60%~13%;在95%乙醇和异辛烷中的加标回收率为94. 4%~106%, RSD为1. 0%~10%。该方法具有良好的准确度和精密度。
2.4 D4~D9向50%乙醇中的迁移量
以50%乙醇作为食品模拟物对36个样品进行迁移实验, 有12个样品检测到目标物, 占待测样品数量的33. 3%, 且D4~D9向50%乙醇中的迁移总量为0. 06~5. 33 mg/kg。表4列出了12个检出样品中D4~D9向50%乙醇中的迁移结果。
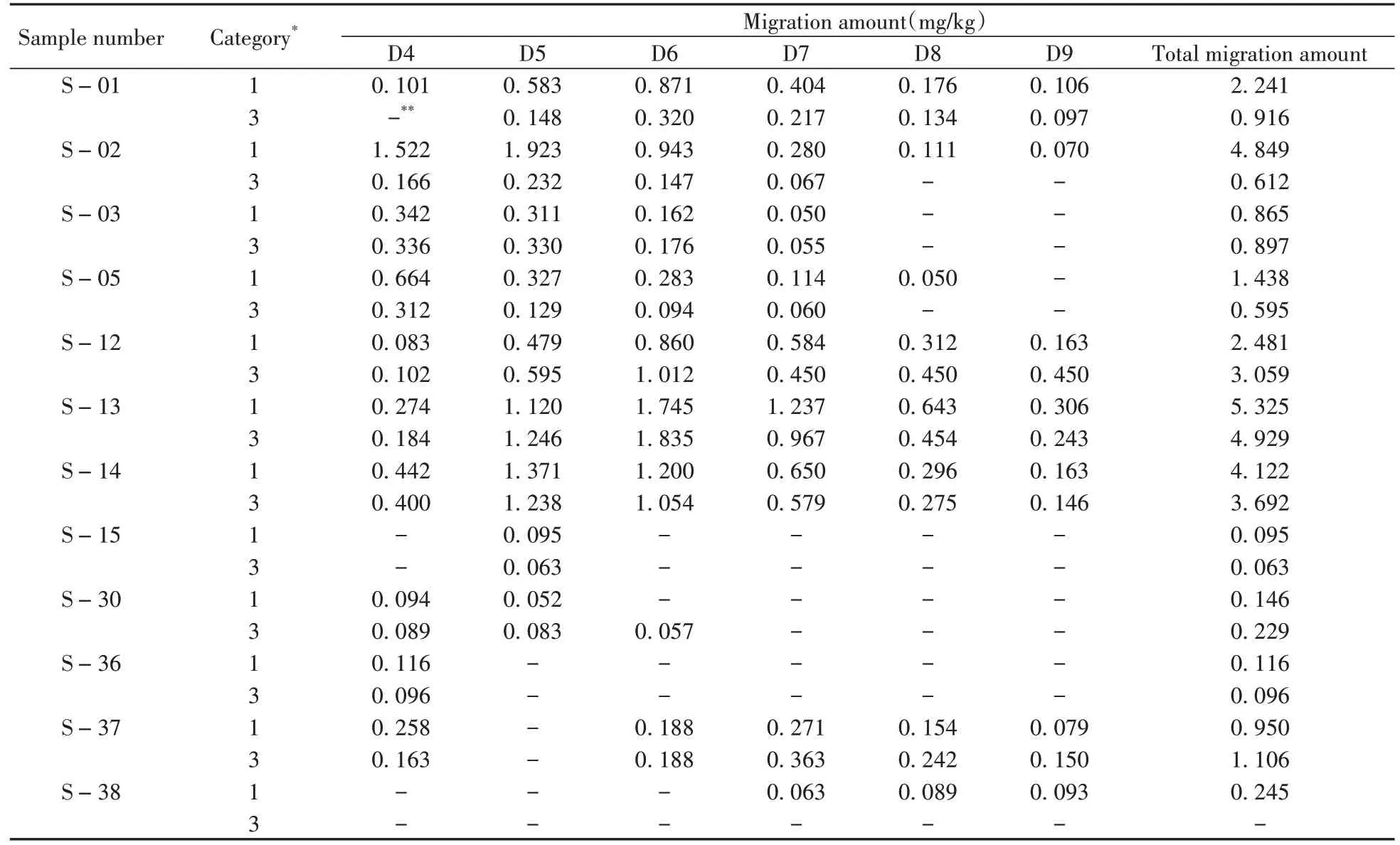
表4 12个检出样品中D4~D9向50%乙醇的迁移量Table 4 Migration amounts of D4-D9 to 50%ethanol found in 12 samples
2.5 D4~D9向95%乙醇和异辛烷中的迁移量
以95%乙醇和异辛烷作为食品模拟物对10个样品进行迁移实验, 有8个样品检测到目标物, 检出率为80%, 迁移结果如表5所示。除了婴儿水杯吸管(S-26)和揉面垫样品(S-34)外, 其他样品均有不同程度的迁移, 且样本间的迁移量差异大。D4~D9在95%乙醇和异辛烷中的最大总迁移量分别为277. 03 mg/kg(S-02蓝色折叠杯)和237. 65 mg/kg(S-13门封条)。可以看出, D4~D9向95%乙醇和异辛烷中的迁移风险显著大于向50%乙醇的迁移风险(P<0. 05)。
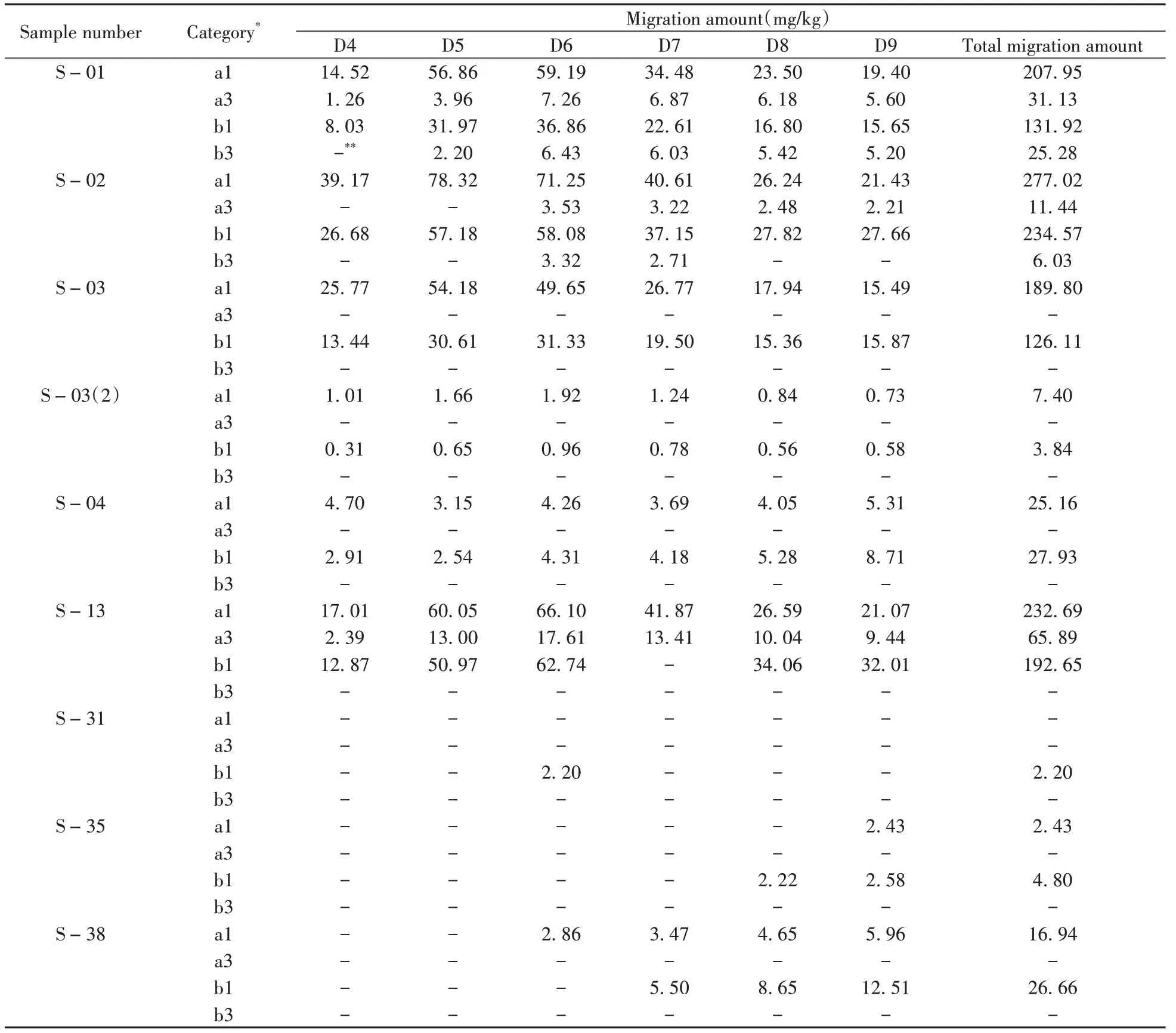
表5 8个检出样品中D4~D9向95%乙醇和异辛烷的迁移量Table 5 Migration amounts of 8 samples D4-D9 to 95%ethanol and isooctane
2.6 迁移次数对D4~D9迁移结果的影响
本研究所有样本在50%乙醇、95%乙醇和异辛烷中第1次和第3次迁移实验中D4~D9的检出率如图3所示。结果显示, 迁移次数对D4~D9在50%乙醇中的检出率无明显影响, 而在95%乙醇和异辛烷中, 第1次迁移实验D4~D9的检出率显著大于第3次迁移实验(P<0. 05)。这可能是由于95%乙醇和异辛烷对硅橡胶中环硅氧烷物质的提取能力较强, 在第1次迁移中, 较多的目标物从硅橡胶样品中迁移出来, 因此在第3次迁移中D4~D9的检出率显著降低。这提醒我们, 在使用全新的硅橡胶产品前, 可以使用高浓度的溶剂(如乙醇)预先浸泡一段时间, 从而降低或避免环硅氧烷物质迁移带来的食品安全风险。
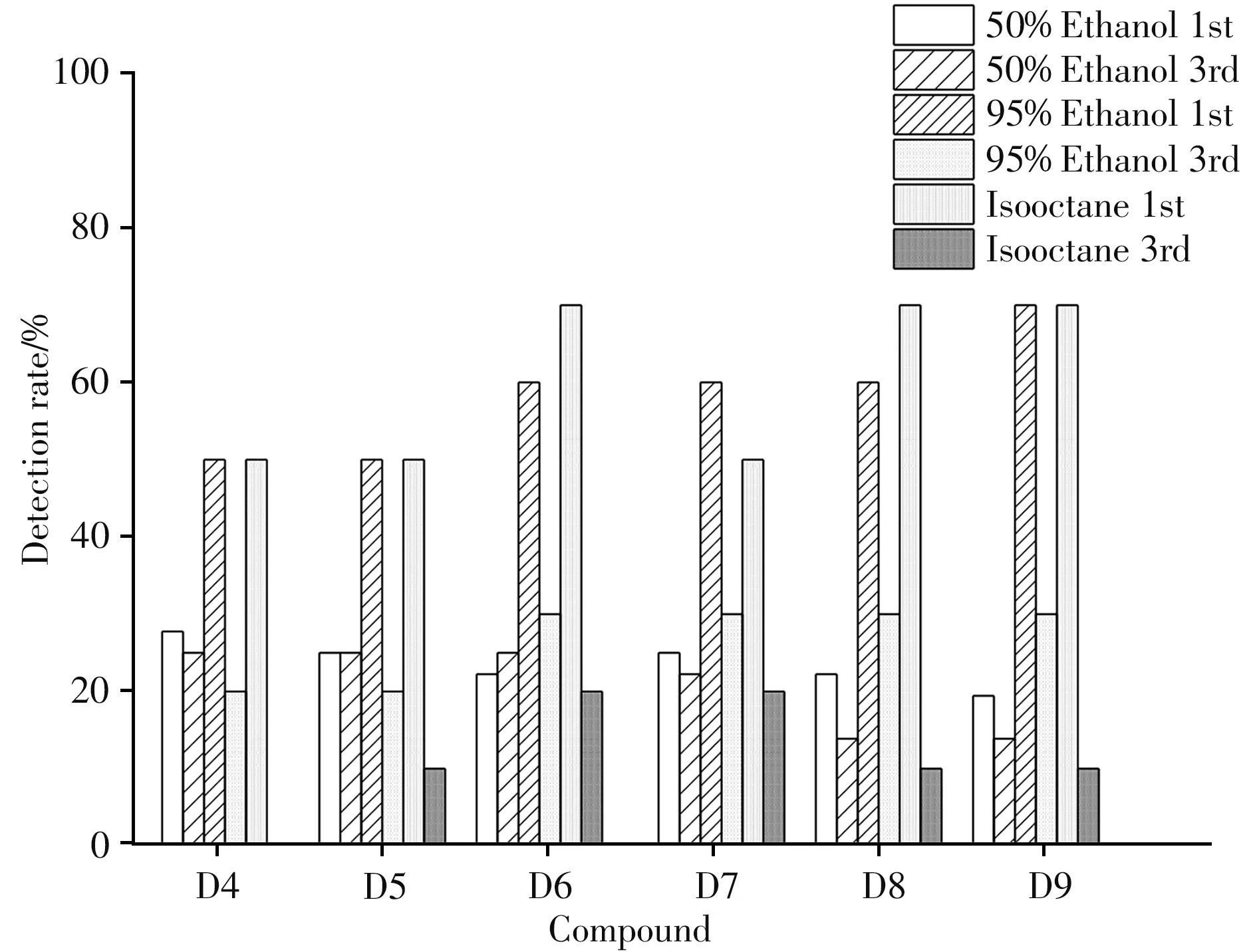
图3 不同迁移次数下D4~D9的检出率(%)Fig. 3 Detection rates of D4-D9 under different migration times(%)
3 结 论
本研究建立了检测食品接触用硅橡胶中D4~D9向50%乙醇、95%乙醇和异辛烷迁移量的GC-MS/MS方法。结果表明, 本方法具有良好的可靠性和准确性, 能够满足市面上硅橡胶制品中D4~D9的检测需求。该方法用于38批次样品中D4~D9迁移量的测定, 发现D4~D9向50%乙醇中迁移量有检出的样品占比为33. 3%, 存在一定的迁移风险;向95%乙醇和异辛烷的检出率和迁移量最大, 安全风险高。建议消费者使用全新的硅橡胶产品时, 使用提取能力较强的溶剂(如乙醇)进行一段时间的浸泡, 以减少或去除环硅氧烷类物质残留。建议在制定相关标准时, 设定环硅氧烷的迁移限量指标, 以减少该类物质迁移造成的食品安全隐患。
