卵巢成熟性囊性畸胎瘤合并卵黄囊瘤1例
2022-10-12袁军刘辉李娜
袁军 刘辉 李娜
患者女,32岁。2021年3月自述扪及下腹部包块,无异常阴道流血、流液,无腹痛、腹胀、恶心、呕吐、腹泻、便秘、尿频、尿急等不适,他院就诊彩超检查提示“下腹部巨大囊实性包块(左侧卵巢来源可能,畸胎瘤可能)”,建议进一步检查,遂来嘉兴市妇幼保健院门诊就诊。门诊拟诊“左侧卵巢囊肿(畸胎瘤可能)”建议手术治疗,收治入院。入院前检查甲胎蛋白(alpha fetal protein,AFP)631.81 μg/L(参考值0~20 μg/L)。入院后阴道彩超检查示子宫前方略偏左侧见一肿块,大小为14.1 cm×12.5 cm×10.2 cm,混合性回声,边界清,内见多个不均质团块状及短条状强回声,部分无回声,液稠,血流信息不明显。提示子宫前方混合性肿块,考虑左侧卵巢畸胎瘤。盆腔增强MRI检查示左侧卵巢未显示,盆腔左侧附件区见一巨大囊实性混杂信号肿块,边界清晰,大小约12.8 cm×10.3 cm×13.6 cm。肿块内见多发分隔及子囊,大部分囊腔T1WI呈低信号、T2WI呈高信号(图1a)。T1WI囊内可见散在条片状高信号影,T1WI压脂序列(T1-weighted image fat inhibition sequence,T1WI/FS)呈低信号。肿块实性部分T1WI呈等信号、T2WI呈稍高信号,扩散加权成像(diffusion-weighted imaging,DWI)呈 高 信 号。MRI增强后肿块分隔及实性成分明显强化(图1b)。膀胱充盈良好,膀胱壁光滑均匀。子宫直肠窝未见异常信号影,盆壁结构正常,盆腔内未见肿大淋巴结。提示:盆腔巨大囊实性肿块,考虑左侧卵巢未成熟畸胎瘤。患者全麻下行左侧附件切除术,进腹探查,未见明显腹水,左侧卵巢肿瘤约14.0 cm×12.0 cm×10.0 cm,包膜完整,光滑无粘连,表面未见结节样瘤灶,质中。右侧卵巢正常大小,外观无殊,双输卵管外观无殊,子宫正常大小,光滑无粘连,术中探查肝、膈下、脾、胃、肠管、大网膜未及明显病灶,腹主动脉旁淋巴结未及肿大。手术切除左侧附件,标本送至病理科进行术中快速冷冻切片,病理诊断为考虑(左侧)卵巢混合性生殖细胞肿瘤。经家属同意,行部分大网膜切除术,手术经过顺利。常规病理检查示肉眼见左侧附件标本,左侧输卵管长6.0 cm,直径0.6 cm,伞端清晰可见,左侧卵巢呈囊实性,大小约14.0 cm×12.0 cm×12.0 cm,内见油脂毛发及头结节,另见一灰黄色肿块,最大径8.5 cm,质偏脆、易碎。大网膜标本为黄色软组织,总体积约15.0 cm×10.0 cm×1.0 cm,未触及明显肿块及质硬区。镜下见:肿瘤形态学结构多样化,表面可见复层鳞状上皮,上皮下可见皮肤皮脂腺、毛囊、汗腺等附件组织,局灶见成熟软骨组织,呈成熟性囊性畸胎瘤典型组织学特征(图2a)。靠近表皮的肿瘤间质呈水肿、黏液样,其中分布小管状腺体(图2b),局部可见含有中心血管的被覆原始生殖细胞的乳头(S-D小体)形成(图2c),背景为由大小不等的相互连通的腔隙组成的疏松网状结构和内衬原始细胞的囊腔,其中微囊内衬扁平细胞,细胞异型不明显,大囊内衬细胞局部较密集,核异型明显,密集区多位于囊腔一端。肿瘤细胞胞质从淡染到透亮不等,密集区域的肿瘤细胞接近原始生殖细胞,表现为胞质少,核异型,核分裂象易见(每个高倍镜视野中可观察到3~4个核分裂象细胞),呈实性排列(图2d),其周围可见乳头状、腺样、微囊等多种结构混杂,部分腔隙内衬鞋钉样细胞(图2e),极个别腔隙的内缘可见嗜酸性变的基膜样物质,间质黏液样(图2f),肿瘤还出现了肠型腺样的分化。免疫组化检查:Sall-like蛋白4(sall-like protein 4,SALL4)弥漫性核着色(图3a),AFP弥漫性胞质和胞核均着色、磷脂酰肌醇聚糖3(glypican 3)呈现出强弱不等的着色,其中实性密集区肿瘤细胞着色较强,乳头状、腺样及囊性区域着色较弱,另外CD117、广谱细胞角蛋白(CK AE1/AE3)也阳性;上皮膜抗原(epithelial membrane antigen,EMA)、雌激素受体(estrogen receptor,ER)、抑制素α(Inhibin α)、孕激素受体(progesterone receptor,PR)、CD30、肾母细胞瘤蛋白(recombinant wilms tumor protein,WT)1、八聚体结合转录因子4(octamer transcription factor,OCT-4)(图3b)均阴性;p53为野生型,Ki-67阳性指数约70%。诊断为左侧卵巢成熟性囊性畸胎瘤合并卵黄囊瘤。行患侧附件切除+部分大网膜切除,术后行博来霉素+依托泊苷+顺泊(bleomycin+etoposide+cisplatinum,BEP)经典方案化疗,定期随访,查体及影像学(B超、CT等)监测,1年半内未见复发与转移。讨论卵黄囊瘤又称内胚窦瘤,最常发生于卵巢,但不限于卵巢[1],其发生率约占卵巢恶性生殖细胞肿瘤的20%,患者的发病年龄从1岁到86岁不等,中位年龄21.5岁,2/3的患 者年龄<20岁[2]。卵黄囊瘤典型临床特征为附件肿块快速增长及伴有腹部疼痛,极个别患者首发为内分泌紊乱(多毛症)[3]。几乎所有的患者都是单侧发生,并且75%的患者在发现时肿瘤直径>15 cm。57%以上的病例为囊性,其中25%的病例表现为多囊性,18%的表现为单囊性,纯实性的肿块很少,且多数较小[4]。肿块切面肉眼表现为褐色、粉红色或者黄色,质地较脆、易碎,常伴有出血和坏死,但是相对较小的肿块却总是呈均匀一致的黄色,可能是与出血较少、坏死有关。较大的肿块容易被发现,但是小肿块特别是<1 cm的肿块很容易被漏诊。当生长在其他肿瘤如成熟性囊性畸胎瘤内时,被认为属于恶性混合性生殖细胞肿瘤范畴,目前报道罕见[5-7]。临床卵黄囊瘤最常见的伴随肿瘤就是成熟性囊性畸胎瘤[8],发生概率约5%,其次是无性细胞瘤,也有极少报道伴发卵巢癌[9-10]。由于畸胎瘤被发现时常常体积较大,且内含较多的油脂毛发组织,较小的卵黄囊瘤(甚至肉眼不可见)极易被漏取材。卵黄囊瘤是一种恶性肿瘤,具有复发和转移的潜能,但通过积极化疗能显著改善患者预后,故漏诊卵黄囊瘤的后果相当严重[11]。本例患者血清学检查提示AFP增高,但低于单纯的卵黄囊瘤,表明该特征对于病理诊断有一定的提示作用。
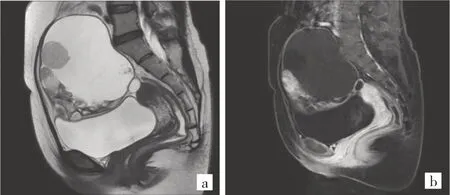
图1 盆腔增强MRI检查所见(a:MRI T2WI矢状位;b:MRI T1WI/FS增强矢状位)

图2 常规病理检查所见[a:成熟性囊性畸胎瘤背景中可见卵黄囊瘤成分;b:靠近表皮的肿瘤间质水肿、黏液样,其中分布小管状腺体;c:含有中心血管的被覆原始生殖细胞的乳头(S-D小体);d:密集区域的肿瘤细胞接近原始生殖细胞,表现为胞质少,核异型,核分裂象易见;e:乳头状、腺样、微囊等多种结构混杂,部分腔隙内衬鞋钉样细胞;f:腔隙的内缘可见嗜酸性变的基膜样物质,间质呈黏液样;HE染色,×100]
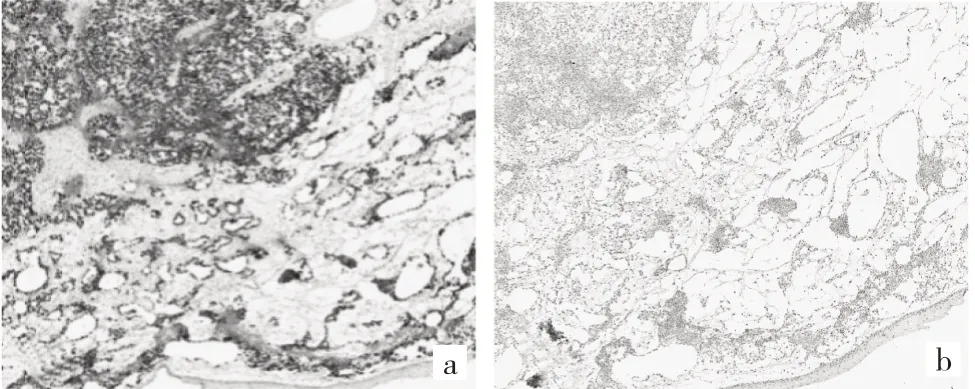
图3 免疫组化染色检查所见(a:SALL4呈弥漫性核着色;b:OCT-4不表达,×100)
卵黄囊瘤在镜下特点丰富、形态多样,最常见的组织学类型为大小不一、相互连通的腔隙组成的不规则的网状结构,约见于70%的病例中;大部分病例可见大小不等的囊状结构,少量可见腺样结构;约1/3可见S-D小体,即特征性的“内胚窦”结构。其他组织学特征包括迷路样结构、管状和囊腔样结构的“帷幕样”排列、多囊亚型的腺纤维瘤样排列、肝样亚型、子宫内膜腺样亚型,极罕见的可见多泡卵黄囊型生长模式[12]。细胞学特征上,肿瘤细胞胞质从淡染到透亮不等,同一肿瘤内细胞形态变化较大,分化好的细胞呈腺样排列及黏液性腺上皮分化,核浆比低,无明显的核异型和核分裂象;分化差的瘤细胞表现为原始生殖细胞样(多衬覆于S-D小体的表面、较大囊腔的内壁及实性区)、缺乏明显的分化方向,细胞核浆比高,核异型显著,核分裂象易见。其他可见的细胞特征包括扁平细胞(多衬覆在微囊内壁)、立方及靴钉样细胞(多衬覆在S-D小体周围腔隙的内壁及乳头的表面)。肿瘤间质的变化主要有富于细胞的间质(多见于多囊亚型)、腺纤维瘤样结构的背景、黏液样至水肿的间质、黄素化间质(妊娠患者)、基底膜样物质沉积、透明小体等。
成熟性囊性畸胎瘤成分的鉴别诊断并不难,故卵黄囊瘤成分是病理鉴别诊断的关键。卵黄囊瘤与卵巢透明细胞癌最易混淆,因为胞质透亮、乳头状结构及靴钉样细胞等在两者均可出现;但透明细胞癌缺乏原始生殖细胞特征及黏液性腺分化,免疫组化染色通常不表达AFP和SALL4。此外透明细胞癌相对的特异性标志物(hepatocyte nuclear factor 1 beta,HNF1-β)对两者的鉴别意义不大,其在卵黄囊瘤的表达率亦可高达80%以上[13]。其次要鉴别卵黄囊瘤与胚胎性癌,胚胎性癌具有腺管状、乳头状结构,亦可见透明小体,这些形态特征与卵黄囊瘤类似;但胚胎性癌肿瘤细胞核常呈空泡状、核膜粗糙不规则,核仁明显,可多个,可见活跃的核分裂象,免疫组化染色表达OCT4和CD30。此外还需要鉴别的是无性细胞瘤,无性细胞瘤往往是实性的,易与实体型的卵黄囊瘤混淆。实体型卵黄囊瘤的AFP阴性,但CK、glypican3阳性,CD117和OCT-4阴性,与无性细胞瘤不同。其他如腺癌及性索间质肿瘤等,则可通过形态学及免疫组化分析CK、AFP、Glypican3、SALL4、inhibin、CD117、OCT-4等来区分。
合并卵黄囊瘤的成熟性囊性畸胎瘤患者治疗同纯卵黄囊瘤。对于年轻患者,应积极保留生育功能[14]。本例采取患侧附件+部分大网膜切除术,术后行BEP经典方案化疗,定期随访,查体及影像学(B超、CT等)监测,1年半内未见复发与转移。由于卵黄囊瘤对化疗极为敏感,大多数患者预后良好,但仍然有部分患者预后较差。Hodroj等[15]发现约30%的患者存在KRAS、KIT和ARID1A基因突变,这为靶向治疗提供了基础。
综上所述,卵黄囊瘤易伴随成熟性囊性畸胎瘤出现,当较小体积的卵黄囊瘤生长于较大体积的成熟性囊性畸胎瘤内时,极易漏诊。本文结合文献及卵黄囊瘤的临床及病理特征,报道卵巢卵黄囊瘤合并成熟性囊性畸胎瘤1例,以期提升临床医生及病理医生对该疾病的认识,减少漏诊率。
