镍锰酸锂正极材料掺杂Cr3+的结构与性能表征
2022-08-30周国江许芷源樊军花杨家智
周国江, 许芷源, 樊军花, 王 浩, 杨家智, 刘 光
(黑龙江科技大学 环境与化工学院, 哈尔滨 150022)
0 引 言
LiNi0.5Mn1.5O4正极材料具有三维锂离子传输通道、约4.7 V的工作电压、650 W·h/kg的能量密度,比市面上的LiCoO2(540 W·h/kg)、LiFePO4(500 W·h/kg)高20%~30%,因此,成为最有潜力的锂离子动力电池正极材料[1-2]。由于其4.7 V过高的充放电平台电压,镍锰酸锂在循环过程中并不稳定。离子掺杂是解决锂离子电池电极材料循环保持率差和倍率性能差问题的最主流的改性方法之一,其操作简单,对设备要求低[3-4]。为避免尖晶石结构中的显著畸变,周期表中靠近镍和锰的掺杂剂,包括 Co3+、Fe3+和 Cr3+等被认为是非常合适的掺杂剂。KaiWai[5]进行了Co元素的掺杂可用作超长循环寿命正极材料,性能的显著提高可归因于杂质相的减少及Cr取代而增强的电子电导率。为了解决镍锰酸锂正极材料的循环性能和倍率性能,笔者采用一定比例的Cr3+去替代不同的镍锰酸锂中的Ni和Mn元素研究其电化学性能。
1 实 验
1.1 材料与设备
实验主要的药品有NiSO4·6H20(w≥98.5%)、MnSO4H20(w≥99.0%)、Na2CO3(w≥99.8%)、氨水(w≥98.5%)、Li2CO3(w≥98.0%)乙醇(w≥99.7%) CrCl3·6H20(w≥99.0%)均为分析纯。实验设备为水热反应釜及恒温鼓风干燥箱。
1.2 实验过程
将NiSO4·6 H20、MnSO4·H20、 Cr Cl3·6 H20按照一定化学计量比γ(表1)溶解于去离子水,搅拌溶解均匀形成混合溶液。将碳酸钠与碳酸氢铵按化学计量比1∶0.5形成沉淀剂,沉淀剂浓度比混合溶液反应浓度比例为1∶1,搅拌溶解均匀。沉淀剂通过蠕动泵以30滴/min的速率滴入混合溶液所在的烧杯中搅拌2 h。将搅拌后的溶液放入高压反应水热釜中,将水热釜放入恒温鼓风干燥箱内以180 ℃加热10 h。随后取得沉淀物通过离心机进行离心,离心后所得的沉淀物经蒸馏水反复洗涤,抽滤后所得的沉淀物在马弗炉中预烧结500 ℃煅烧3 h。得到的预烧结产物加入碳酸锂,锂的实际加入量比理论值高出5%,防止挥发,研磨均匀后放入马弗炉中在800 ℃煅烧12 h,得到LNMO正极材料,制得的产物分别为LiNi0.5Mn1.5O4、LiNi0.5Cr0.05Mn1.45O4、LiNi0.45Cr0.05Mn1.5O4和LiNi0.475Cr0.05Mn1.475O4分别标记为Y、Y-1、Y-2和Y-3。

表1 原材料不同比例制备的样品
1.3 样品表征与电性能测试
文中采用X射线衍射仪的型号为Bruker D8 Advance,使用Cu-Kα射线源表征原材料,电压为40 kV,电流为40 mA,扫射范围是10°~80°,步长为0.02°。利用扫描电子显微镜在加速电压15 kV的情况下观察粉末的表面微观形貌。使用TC53系统测电池进行充放电测试。使用CHI660E电化学工作站进行循环伏安测试(CV)测试参数为3.5~5.1 V,扫描速度为0.1 mV/s及电化学阻抗谱(EIS)进行测试。测试参数为频率0.01~100 kHz,振幅为5 mA。
2 结果与讨论
2.1 结构表征
2.1.1 XRD分析
由表1中所制得样品的XRD元素图谱如图1所示。
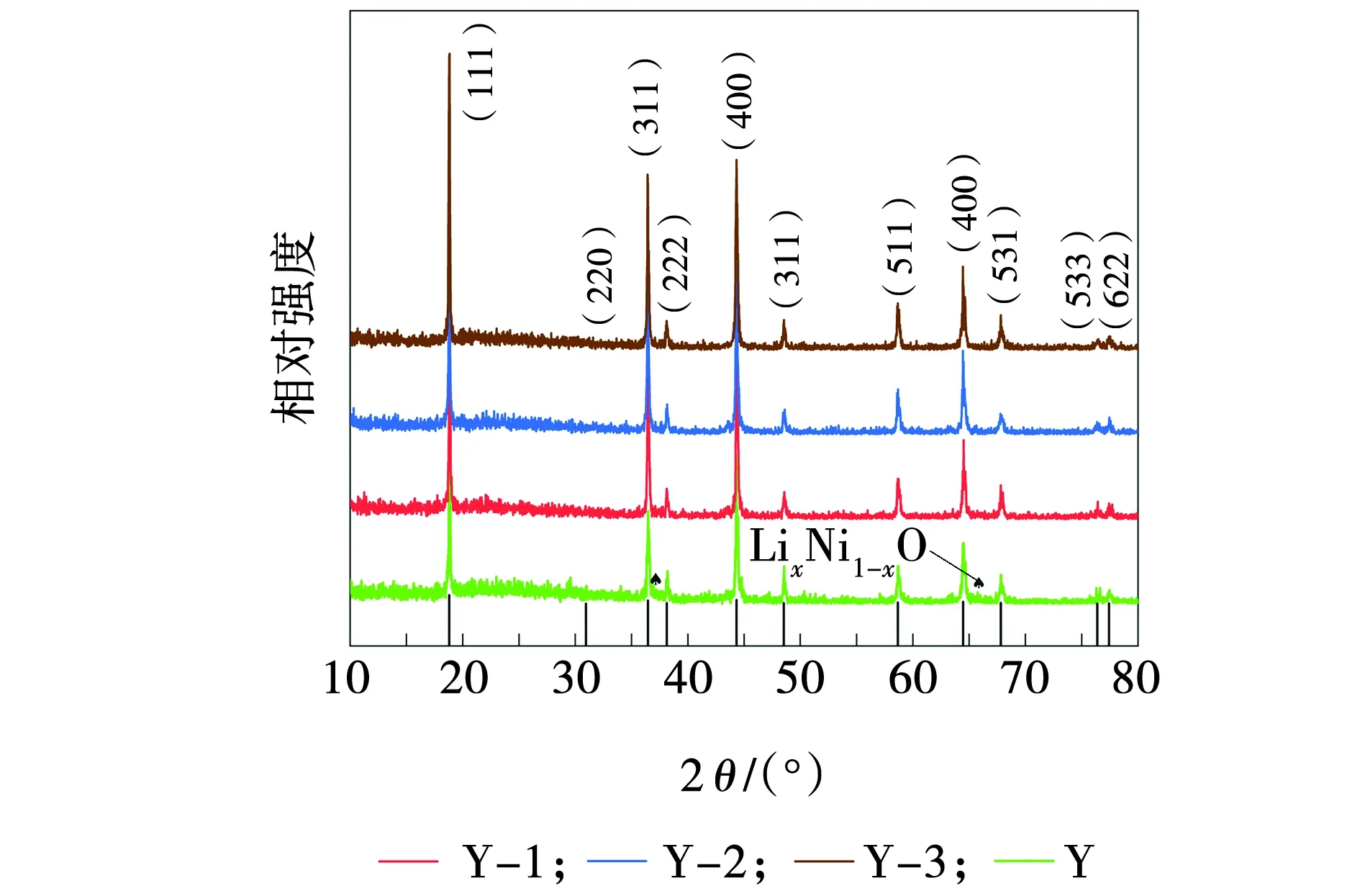
图1 不同的LNMO材料的XRDFig. 1 XRD of different LNMO materials
由图1可见,主衍射峰与JC卡号80-2162吻合,说明制备得到所有样品中都具有无序的Fd-3m构型,这表明所制得的产物为镍锰酸锂(LNMO)。从特征峰可以看出,Cr3+替代了一部分Ni2+和Mn4+,不会有额外的特征峰的出现,以及尖锐且狭窄的衍射峰代表了其良好结晶性。同时发现,在未掺杂Cr3+的LNMO样品中有杂质峰的出现,这种杂质项属于LixNi1-xO[6-10]的存在,是因为煅烧温度超过600 ℃时会出现这样的杂质峰,是一种常见的杂质相。这种杂质相会抑制LNMO的放电容量和速率能力。由于Cr3+的掺杂中,样品的杂质项是几乎不可见的,Cr3+会与O2-有较强的结合能可以减少氧的缺乏,进而抑制LixNi1-xO的产生。
2.1.2 SEM分析
LNMO材料的SEM如图2所示。由图2可以看出,通过水热-共沉淀法可以制备出的LNMO材料中形成了一种球形孔状结构。

图2 不同 Cr3+掺杂位置的LNMOFig. 2 LNMO plot of different Cr3+ doping positions
在这结构中,更多的孔状结构和球形形貌,缩短了Li+的扩散路径。对比图2a~c与图2d图可以看出,Cr3+的掺杂有效地减少了颗粒的团聚现象,颗粒尺寸与未掺杂的相比更小。由图2可以看出,破碎的球状LNMO中是中空球形的LNMO正极材料。这是因为考虑到Cr3+的强氧亲和力,Cr-O键的断裂比Ni-O和Mn-O更困难[11-12]。因此,在煅烧过程中,会形成颗粒相对较小的样品。图2d中的样品中有一部分形貌是半圆或半破碎的形貌,这是由于Cr3+替代了Mn元素的位置,Mn元素的缺失在煅烧过程中形成较大的球形形貌时会破碎,以及部分Mn元素与其余Ni元素会形成粒径较小的球形形貌。图2c样品相比于图2b样品的粒径相对较大,这是由于Cr3+取代Ni元素后,Mn元素并未被替代,而LNMO-2的Cr3+会同时取代Mn元素和Ni元素,从而会形成粒径较小的球形形貌并不会破碎。
2.2 电性能分析
2.2.1 循环性能
所有样品的循环性能如图3所示。由表2可以看出,Y-3在1 C循环时首次充放电的放电比容量最高,其中,Y-3在1 C循环时首圈放电比容量是132.5 mA·h/g,循环200圈后放电比容量是124.5 mA·h/g,容量保持率为94.0%。

图3 不同LNMO材料的循环性能Fig. 3 Cycle properties of different LNMO materials
Y-1在1 C循环时首次充放电的放电比容量最高,Y-1在1 C循环时首圈放电比容量是126.8 mA·h/g,循环200圈后放电比容量是116.3 mA·h/g,容量保持率为91.7%。在1 C循环时,Y-2首次充放电的放电比容量最高,在1 C循环时Y-2首圈放电比容量是 127.0 mA·h/g循环200圈后放电比容量是115.4 mA·h/g,容量保持率为90.8%。而对照组有Y为未掺杂 Cr3+材料的性能在1 C循环时首圈放电比容量是124.8 mA·h/g,循环200圈后放电比容量是115.3 mA·h/g,容量保持率η为92.3%。

表2 不同LNMO材料200次循环后的容量衰减情况
从图3可以看出,Cr3+掺杂位置的不同所导致,由于Y-2中Cr元素替代了部分Mn元素,导致在形成LNMO时不会形成稳定的三维锂离子扩散通道,使自身的循环性能降低。而Y-1由于Cr元素替代了部分Ni元素,替代部分Ni元素后由与LNMO的充放电平台在4.7 V是由Ni的氧化还原,降低了Ni元素会使得4.7 V的放电平台变小导致放电平台降低。但在Y-3中,循环性能及1 C下放电容量提高,这是由于Cr元素在同时替代Ni和Mn元素后,无序度的增加,Cr-O键合强度高,结构存在稳定,同时,Cr3+的存在不会发生Jahn-Teller效应[13-14]。
2.2.2 充放电曲线
所制备的LNMO材料1 C的首次充放电曲线如图4所示。在1 C时Y、Y-1、Y-2和Y-3放电容量分别是124.8、126.8、127.0和132.5 mA·h/g,由图4可以看出,样品都是在4.7 V(vs.Li+/Li)有一个充放电平台。该平台对应着Ni4+/Ni3+,Ni3+/Ni2+的氧化还原对。同时,还会有一个4.0 V(vs.Li+/Li)的放电平台,该平台不太明显,是由于Mn4+/Mn3+的氧化还原[14-16]。其中,Y-3的充放电性能较好,由于自身的粒径较小,球形形貌完整度高的原因,其与对照组Y相比看出,由于Cr3+的掺杂会使Ni4+/Ni3+,Ni3+/Ni2+的氧化还原放电平台略高,这样有利于能量密度的提高。以及掺杂Cr3+后,4.0 V平台的降低会使得Mn3+含量的降低。从而4.7 V的充放电平台会偏高。但由于也有部分Mn元素被替代,自身的4.0 V左右平台相比于Y-1偏短。Y-2与Y-1相比,4.7 V左右的充放电平台相对较长,这是由于Ni元素被部分替代后所导致,但4.0 V左右的充放电平台相对较短。Mn元素未被替代,从而整体上Y-1的放电容量会比Y-2高一点。
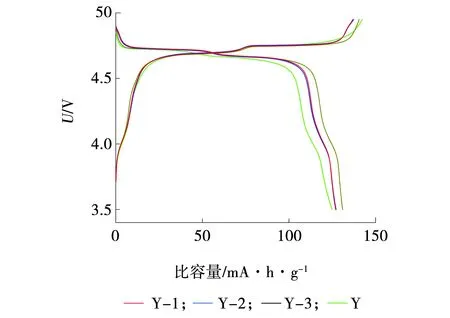
图4 不同LNMO材料的充放电曲线Fig. 4 Charge discharge curves for different LNMO materials
2.2.3 循环伏安曲线
循环伏安曲线一般是用于研究充放电的氧化还原, 不同LNMO材料的循环伏安曲线如图5所示。
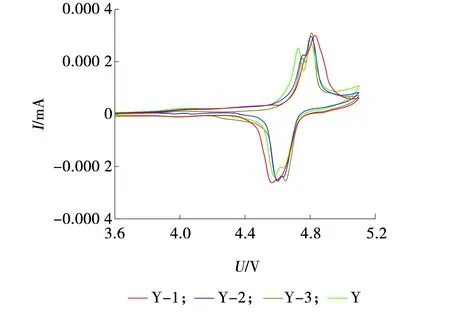
图5 不同LNMO材料的循环伏安曲线Fig. 5 Cyclic voltammetry curves for different LNMO materials
所有样品在4.7 V左右多出了两个氧化还原峰,这是由于Fd3m无序结构的特征。4.7 V左右的峰是对应着Ni4+/Ni3+,Ni3+/Ni2+的氧化还原对。而在4.0 V左右可以看到,有一个微弱的Mn4+/Mn3+的氧化还原对产生的峰[15-17]。Y-3则反应出最高的电化学活性容量,由于Cr3+的掺杂,CV峰的尖锐度也可以反映出锂离子的扩散速率以及氧化还原偶的电化学活性,可以看出,对照组Y的Mn3+含量偏高,也证实了Mn3+离子的含量由于Cr3+的掺杂而变的相对较低。由于Cr3+的掺杂,CV峰的尖锐度也可以反映出锂离子的扩散速率及氧化还原偶的电化学活性。
2.2.4 电化学阻抗图谱
不同LNMO材料的电化学阻抗图谱如图6所示,由图6可以看出,所有样品都显示出了相似的轮廓,由两个半圆和一个相似倾斜的直线构成。
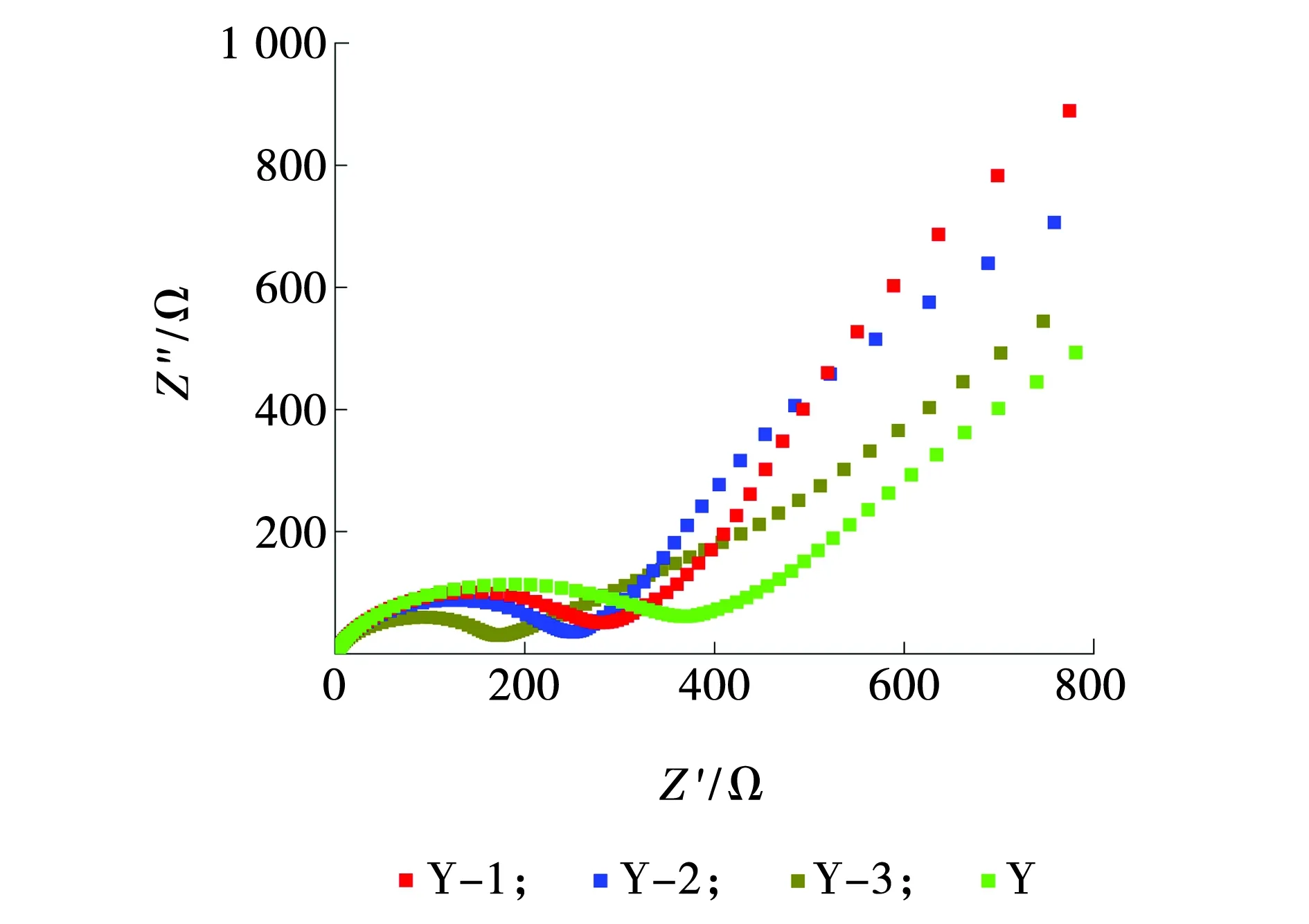
图6 不同材料的电化学阻抗图谱Fig. 6 Electrochemical impedance profiles of different materials
由于在开路电压时,锂离子未发生脱嵌,SEI膜未形成,导致其中中频区的半圆十分不明显。高频区的截距表示电解液,电池材料和分离器所产生的欧姆电阻。高频区的电源是由锂离子在电极表面膜的张力。低频区斜线则是代表Warburg扩散电阻,反映了锂离子在体电极材料的固态扩散[18-20]。从图6可以看出,Y-3具有最小的张力值,可能归功于电镜图中更小的一次粒径及更松散的团聚结构。与对照组Y相比,掺杂 Cr3+可以有效减弱电解液氧化等副反应,可以有效抑制CEI膜的生长,CEI膜层会增加电极阻抗,不利于电化学性能。
3 结 论
(1)采用水热-共沉淀法合成了的镍锰酸锂正极材料, 通过XRD表明,Cr3+的掺杂能够降低LixNi1-xO的杂质存在,以及提高其结晶性, SEM图表明,材料有相对更小的粒径与更完整的中空球形形貌。
(2)Cr3+替代不同元素时会对正极材料充放电平台的长短及电化学性能造成影响。电化学性能表明,LiNi0.475Cr0.05Mn1.475O4具有最佳的倍率性能与循环稳定性。在1 C循环时,首圈放电比容量是132.5 mA·h/g,循环200圈后放电比容量是124.5 mA·h/g,容量保持率为94.0 %。
(3)通过循环伏安法证明了适当增加Cr3+会提高锂离子扩散速率,其中,LiNi0.475Cr0.05Mn1.475O4表现出最佳的氧化还原活性。通过电化学阻抗法证明了,适当掺入Cr3+有效缓解了电解质分解等副反应,有效抑制了CEI膜的生长。
