Cu-3-trz-PMo12的合成、结构及催化氧化碘离子性能
2022-08-17袁常梅张太文
袁常梅,郭 军,,张 丹,张太文
(1.贵州师范大学化学与材料科学学院,贵州贵阳 550001;2.瓮福(集团)有限责任公司中低品位磷矿及其共伴生资源高效利用国家重点实验室)
碘作为基础的化工原料和重要的战略物资,其化工产品被广泛用于医药、农业、染料、冶金、合成橡胶、国防以及尖端技术等领域[1-5]。由于没有天然的碘矿资源,中国主要从海藻及各种天然卤水等资源中提取碘,通过利用氧化剂将碘离子氧化为碘单质进行回收,然而这些资源中的碘含量较低,碘离子氧化为碘单质的过程很慢,造成生产成本较高的同时产率也比较低。为了有效地从各种碘资源中提取、回收碘,采用合适的催化剂去提高氧化反应的速率显得尤为重要。
多金属氧酸盐(POMs,又称多酸)因其制备简单、高催化活性、高选择性及环境友好而广泛应用于催化领域[6-8]。研究表明多钼氧酸盐在催化过氧化氢氧化碘离子方面具有较好的效果[9-10],然而多钼氧酸盐在该反应中为均相催化剂,存在难以分离和回收的问题[11-13]。而直接利用多酸与合适的有机组分连接形成有机-无机杂化物是实现多酸非均相化的一种有效途径[14]。Keggin型的多钼氧酸盐表面有许多的氧原子,这些氧原子具有与金属-有机骨架的金属中心配位的能力,其中过渡金属配合物提供电荷补偿并成为无机多钼酸骨架的一部分[15-18]。利用含N有机组分和过渡金属形成金属配合物对其进行修饰,可形成维度多样的有机-无机杂化材料。基于此,本课题组以3-氨基-1,2,4-三氮唑为有机组分、Cu2+为金属源,合成了一例Keggin型有机无机杂化物(PMo12O40)[Cu6(3-trz)6](PMo12O40)·H2O(简称为Cu-3-trz-PMo12),通过X 射线单晶衍射、傅里叶变换红外光谱(FT-IR)、热分析测试(TG)、X射线衍射分析(XRD)、扫描电子显微镜(SEM)、元素分析对化合物进行了表征,并以过氧化氢为氧化剂,探究其催化碘离子氧化反应的催化性能。
1 实验部分
1.1 实验试剂与仪器
试剂:磷钼酸水合物;3-氨基-1,2,4-三氮唑;盐酸;碘化钾;30%过氧化氢;一水合乙酸铜;二水合氯化铜;浓硫酸;以上均为分析纯。
仪器:APEX-II CCD X 型射线单晶衍射仪;Vario EL Cube 型元素分析仪;Thermo-is5 型傅里叶变换红外光谱仪(KBr 压片);Smartlab9 型X 射线衍射仪;DSC Q2000 型热分析测试仪;PHS-3E 型pH计;PI-1-01 型碘离子选择电极;217-01 型参比电极。
1.2 化合物的合成
将H3PMo12O40·xH2O(0.18 g,0.097 mmol)、CuCl2·2H2O(0.01 g,0.057 mmol)、Cu(CH3COO)2·H2O(0.034 g,0.17 mmol)、3-氨基-1,2,4-三氮唑(0.03 g,0.36 mmol)溶解到10 mL 蒸馏水中,在常温下搅拌30 min,用1 mol/L 的NaOH 调节pH 至2.5,然后将混合溶液加入到25 mL 聚四氟乙烯内衬的不锈钢反应釜中,保持160 ℃反应4 d,得到黑色块状晶体。Cu-3-trz-PMo12的傅里叶红外光谱(FT-IR)ν:1 055.87 cm-1(P—Oa)、957.40 cm-1(Mo—Od)、858.94 cm-1(Mo—Ob—Mo)、789.12 cm-1(Mo—Oc—Mo);Cu-3-trz-PMo12的元素分析数据:理论值(质量分数)C 为3.17%、H为0.53%、N为7.34%;实验值(质量分数)C为3.12%、H为0.774%、N为7.21%。
1.3 化合物晶体结构检测
选取合适的晶粒用于单晶结构测试,置于Bruker APEX-II CCD 衍射仪上,在150 K 下收集衍射数据,射线源为λMo-Ka=0.071 073 nm,同时利用Olex2程序将晶体结构解出,并采用全矩阵最小二乘法进行精修。晶体学参数见表1。
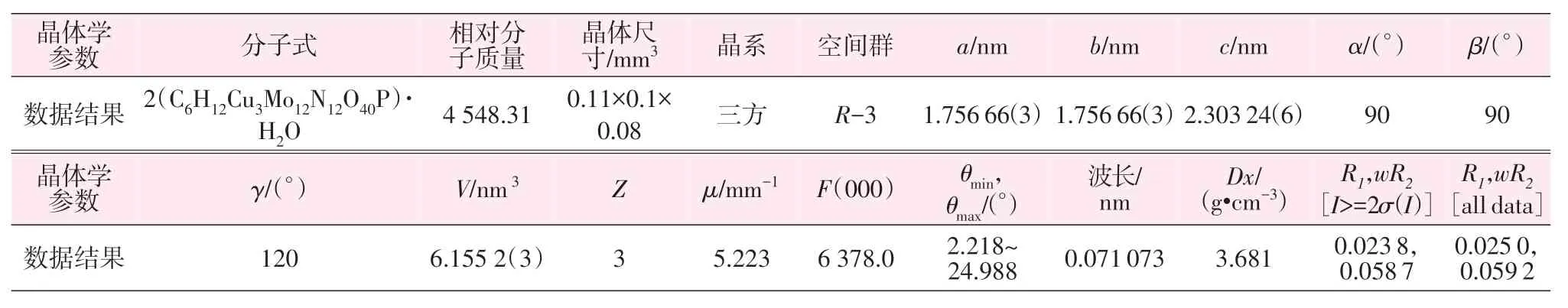
表1 化合物的晶体学数据Table 1 Crystallographic data of compound
1.4 催化性能测试
在c(I-)=4.8×10-3mol/L、c(H2O2)=2.0×10-3mol/L、c(H+)=0.04 mol/L 的体系中加入Cu-3-trz-PMo12,维持体系体积为40 mL。运用离子选择电极法测定反应体系中碘离子的起始浓度c0(mol/L)、反应终点浓度ct(mol/L)及反应时间t(s)。利用二者浓度与时间的关系得到平均反应速率r以及转化率η,并作空白实验与之对照。其公式如下:

2 结果与讨论
2.1 化合物晶体结构
单晶X-射线衍射分析表明化合物结晶在三方空间群R-3中,化合物的分子结构如图1a所示。化合物的基本单元由2 个经典的Keggin 型[PMo12O40]3-、6个晶体学上一致的Cu、6个3-氨基-1,2,4-三氮唑分子和1 个间隙水分子组成的二聚体。在化合物中,每个铜原子采用三角几何,分别与2 个3-trz 的一个N 原子、1 个[PMo12O40]3-的端氧原子Od进行配位(如图1b)。其中,6 个铜原子所在平面可看作以间隙水为中心的正六边形(如图1c)。铜离子周围的间距0.256 2(3)nm(Cu1—O13)键、0.188 5(4)nm(Cu1—N1)键、0.188 3(5)nm(Cu1—N2)。而N—Cu—N角度为167.40(19)°和N—Cu—O的角度范围为89.4(164)~102.5(157)°。
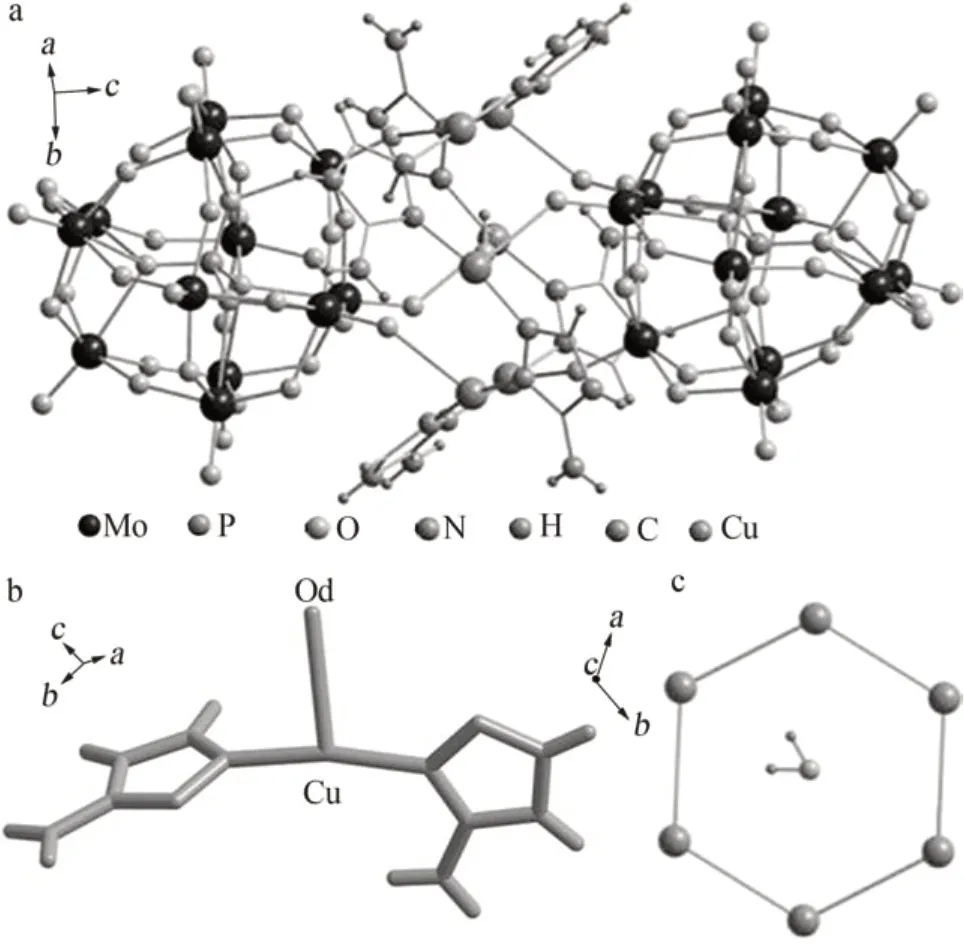
图1 化合物基本单元图(a);铜原子的配位模式(b);6个铜原子形成的正六边形(c)Fig.1 Basic unit diagram of compound(a);coordination modes of copper atoms(b);a regular hexagon formed by six copper atoms(c)
根据价键计算公式[19]s=exp[(R0-R)/B],其中s表示化合物中原子的键价,R为实际键长(nm),R0(nm)为经验键长,而B为经验值取值0.37,R0分别取1.58 nm(Cu—N)、1.679 nm(Cu—O)及1.907 nm(Mo—O)。由此可计算出铜原子的氧化态为0.972,钼原子的氧化态分别为6.57、5.94、6.02、6.10,计算结果表明化合物中铜为+1价,而钼原子皆为+6价。
化合物中相邻的两个基本单元之间,通过有机配体与多酸之间形成的氢键N—H···O、C—H···O连接形成次级单元,见图2a。每个次级单元之间又通过氢键相互作用进而形成一个三维超分子结构,图2b为化合物沿c轴的三维堆积图。具体氢键数据见表2。

图2 氢键的形成过程(a);化合物沿c轴观察的分子结构图(b)Fig.2 Formation process of hydrogen bonds(a);molecular structure of compound viewed along c axis(b)

表2 化合物的部分氢键数据Table 2 Partial hydrogen bond parameters for the compound
2.2 红外光谱分析
化合物的傅里叶红外(FT-IR)光谱如图3 所示,由图3 看出,在700~1 100 cm-1有4 个特征吸收峰,1 055.87、957.40、858.94、789.12 cm-1的吸收谱带分别归属为多阴离子[PMo12O40]3-中的ν(P—Oa)、ν(Mo—Od)、ν(Mo—Ob—Mo)、ν(Mo—Oc—Mo)的伸缩振动峰,而1 100~1 700 cm-1处的特征峰则归属于有机配体3-氨基-1,2,4-三氮唑的特征吸收峰。
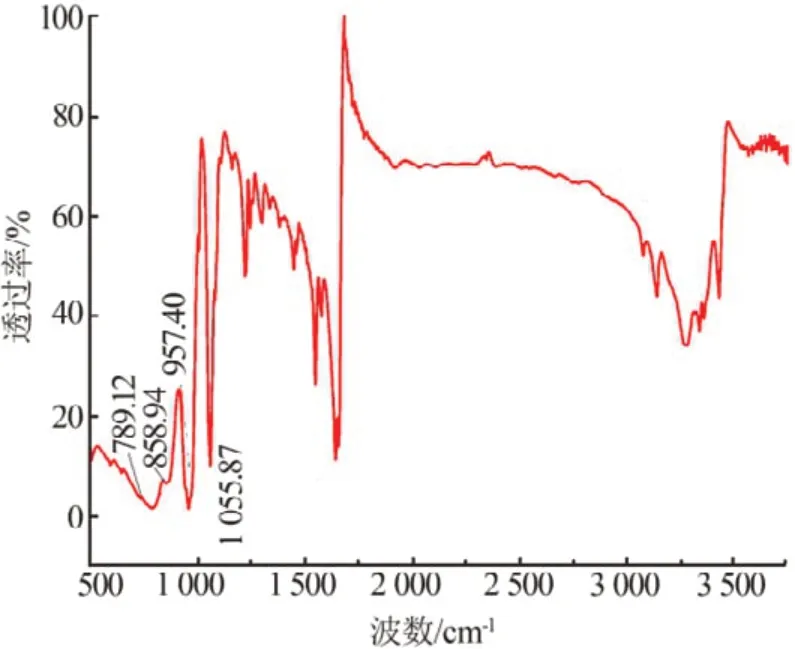
图3 化合物的红外光谱图Fig.3 FT-IR spectrum of the compound
2.3 热重分析
为了研究化合物的热稳定性,对其进行TG 测试,结果见图4。样品在氩气气氛下,升温速率为10 ℃/min,温度范围控制在25~900 ℃。如图4所示,化合物在25~900 ℃质量损失率为23.96%。热重分析展示了化合物的三步失重:第一步,在25~341.2 ℃质量损失率为0.72%,对应于间隙水分子的减少;第二步,在341.2~400.4 ℃质量损失率为15.58%,归属于有机配体与金属形成配合物的逐步分解;第三步,在400.4~900 ℃质量损失率为7.66%,代表了多阴离子结构的降解。
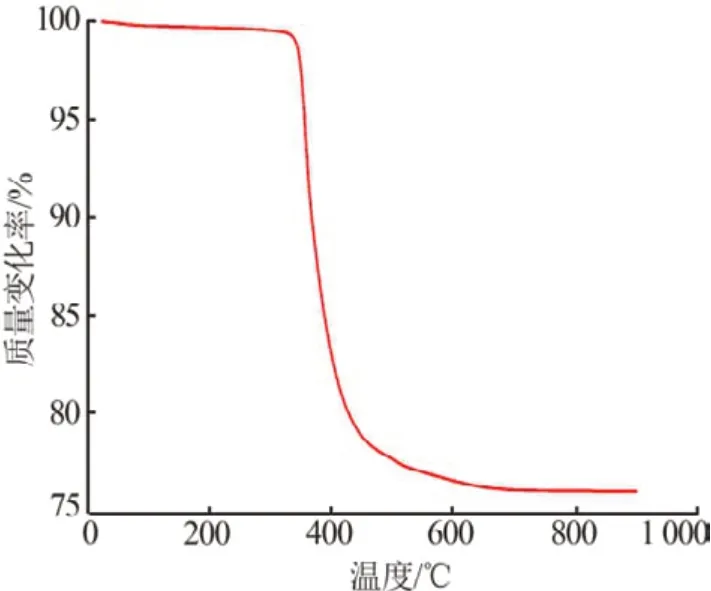
图4 化合物热重曲线图Fig.4 TG curve of the compound
2.4 催化性能研究
对Cu-3-trz-PMo12的催化性能进行了研究,在25 ℃条件下保持体系中c(I-)=4.8×10-3mol/L、c(H2O2)=2.0×10-3mol/L、c(H+)=0.04 mol/L,探究过氧化氢氧化碘离子的性能。该条件下,发现未加催化剂时反应要经历42 h 才能达到终点,而将0.01 g 的Cu-3-trz-PMo12加入到该体系中,反应经25 min 到达终点,此时反应速率达3.20×10-6mol/(L·s)。在体系中剩余碘离子的浓度为3.4×10-3mol/L时,未添加催化剂反应所需时间为42 min,相同条件下,添加催化剂反应仅需1 min,对比结果如图5a,表明Cu-3-trz-PMo12有较好的催化效果。
通过测量碘离子的浓度随时间的变化,分别以ln(ct/c0)、1/c对t作图,并利用作图法求解反应级数,结果见图5b。由图5b可知,以1/c对时间t作图得到一条曲线,ln(ct/c0)对t作图趋近于一条直线,拟合图表明了碘离子催化反应符合准一级反应动力学,动力学方程式表示为ln(ct/c0)=kt,其中k为反应速率常数;c0为反应起始时刻碘离子的浓度,mol/L;ct为t时刻碘离子的浓度,mol/L;该催化剂催化过氧化氢氧化碘离子反应动力学的线性相关系数为0.997 8,该条件下动力学常数为0.232 7 min-1。
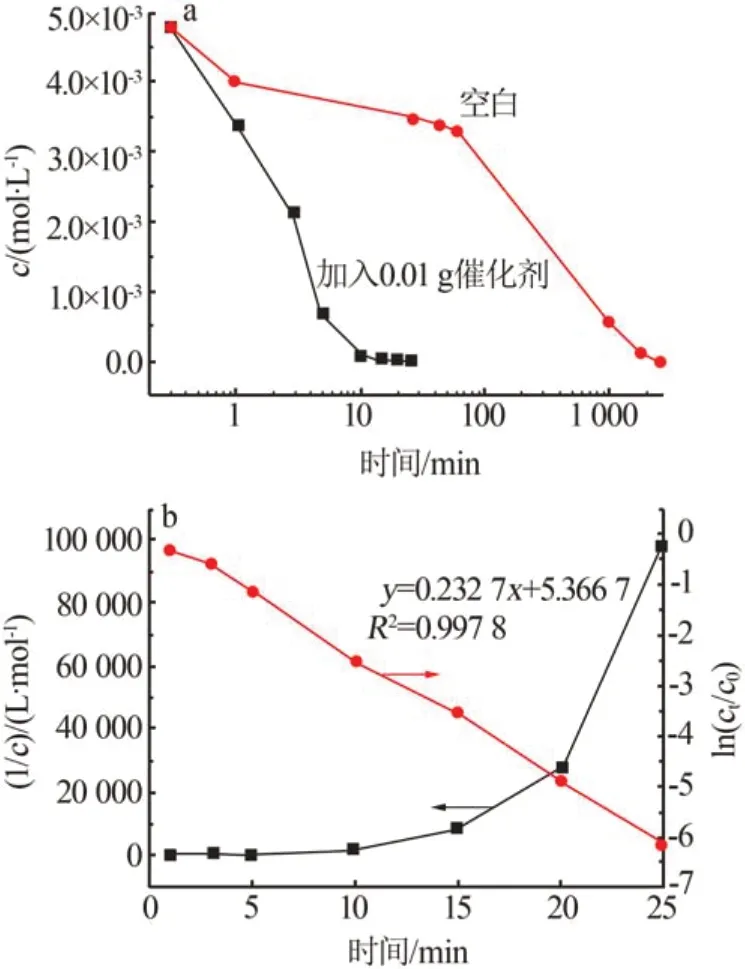
图5 催化剂催化活性评估(a);作图法求解反应动力学级数(b)Fig.5 Evaluation of the activity of catalysts(a);plotting method to solve kinetic progression of catalytic reaction(b)
为考察催化剂的重复使用性能,在25 ℃时催化剂Cu-3-trz-PMo12质量为0.01 g、体系碘离子浓度为c(I-)=4.8×10-3mol/L、c(H2O2)=2.0×10-3mol/L、c(H+)=0.04 mol/L 条件下,对Cu-3-trz-PMo12催化过氧化氢氧化碘离子进行了4次平行实验结果见图6a。由图6a可见,碘离子的4次转化率较为接近,表明该催化氧化实验具有很好的可重复性,之后转化率略有降低,是由于晶体颗粒比较小,在过滤、洗涤过程中有所损失。图6b为催化剂使用前后及单晶X-射线的数据拟合对比图,由图6b 可知,模拟和实验前后得到的组分峰在关键位置吻合较好,表明化合物的粉末为纯相,且催化剂结构特征没发生明显的变化。强度的差异可能是由于样品的取向不同引起的。

图6 催化剂的重复使用效率(a);催化剂的XRD谱图(b)Fig.6 Recycled efficiency of the catalyst(a);XRD patterns of the catalyst(b)
为进一步探究催化反应前后催化剂的形貌是否发生变化,对反应前后的催化剂进行SEM 表征,结果如图7a和图7b所示。由图7a和7b可以看出催化剂表面粗糙且分散不均匀,皆呈现大面积堆积的现象,说明在催化前后并没有改变催化剂的结构,这与XRD分析结果吻合。

图7 催化剂使用前(a)和使用后(b)的SEM照片对比Fig.7 Comparison of SEM images of catalyst before(a)and after(b)use
3 结论
1)Keggin 型[PMo12O40]3-杂多阴离子、金属铜和3-氨基-1,2,4-三氮唑在水热条件下成功得到一例多酸基有机-无机杂化物。晶体结构表明:金属铜通过与有机配体的N 原子、杂多阴离子的端氧原子进行配位形成基本单元结构,基本单元结构之间通过氢键相互连接。
2)性质研究表明,Cu-3-trz-PMo12在催化碘离子氧化中表现出优异的催化活性,25 ℃条件下,当m(Cu-3-trz-PMo12)=0.01 g、c(I-)=4.8×10-3mol/L、c(H2O2)=2.0×10-3mol/L、c(H+)=0.04 mol/L 时其反应速率达到3.2×10-6mol/(L·s),比未加催化剂的反应速率提高了100.9倍。
