纳米片多面体锰基锂离子筛的制备及锂离子吸脱附特性
2022-08-17韩红静吴勇民曹永生韩婷婷汤卫平
韩红静,吴勇民,曹永生,韩婷婷,汤卫平
(1.青海大学新能源光伏产业研究中心,青海西宁 810016;2.上海空间电源研究所)
“双碳”目标的提出带动了光伏及新能源汽车等产业的飞速发展,也间接推动了锂离子电池在电网储能及电动汽车中需求量的持续增加,因此,作为锂电池核心材料的锂在新时代的战略价值堪比石油,被誉为“能源金属、白色石油”[1]。自然界中锂主要以化合物的形式存在于固态含锂矿石及海水、盐湖卤水等含锂的液态资源中。中国锂资源总储量约为450万t,其中盐湖锂资源储量占比超过71%,而且盐湖卤水提锂的成本通常比矿石提锂低30%~50%[2]。但是中国盐湖卤水高镁含量、低锂含量及高镁锂比的特点,增大了锂提取的难度,因此,发展从盐湖卤水中高效提取锂的技术成为盐湖锂资源综合利用与开发的关键所在[2-3]。对于高镁锂比的低品位盐湖卤水,吸附提锂技术被认为是比较高效的方法,成为目前盐湖卤水提锂的主要发展趋势。现阶段常用的吸附剂主要有锰氧化物、钛氧化物及氢氧化铝基等类型[4-5],其中尖晶石型锰氧化物因具有吸附量大、选择性高、操作简单及成本低等优点,在盐湖卤水锂提取方面展现出潜在的应用前景。目前,研究较广泛的锰氧化物型离子筛包括HMn2O4(λ-MnO2),H1.33Mn1.67O4(MnO2·0.31H2O)和H1.6Mn1.6O4(MnO2·0.5H2O)等[6-7]。其中,尽管H1.6Mn1.6O4具有相对较高的理论吸附容量(72.9 mg/g)[7],但酸洗脱附过程中容易发生Mn 的溶损,导致吸附剂结构坍塌而影响使用寿命,严重制约了其工业化推广与应用[8-9]。金属阳离子掺杂改性方法是目前提高锂离子筛结构稳定性、延长其使用寿命的有效方法[10-11]。MA 等[12]研究了Ni2+、Al3+、Ti3+掺杂的锂离子筛HMxMn2-xO4,当x=0.5 时,Al3+掺杂有效降低了Mn 的溶损率。CHEN等[13]以LiOH 和Mn(NO3)2为原料采用水热法制备了Al3+掺杂LiMn2O4,指出Al3+掺杂后,相比于未掺杂样品,Mn 的溶损率降至3.71%,但对Li+的吸附容量也有所下降。徐乃才等[14]采用高温固相法制备了Al3+、La3+掺杂HMnO 型锂离子筛,结果表明,Al-HMnO 和La-HMnO 对溶液中的Li+的吸附容量有所提高。以上基于金属阳离子掺杂改性的研究虽都起到改善Mn溶损、提高结构稳定性的作用,但一般多采用以LiOH及Mn(NO3)2(或MnCO3)等为原料的固相合成法,原料成本高且具有一定的易制爆性,生产工艺耗能高。另外,掺杂金属元素后,吸附容量改善不明显,甚至会出现一定程度的减小。本研究以廉价及安全性高的电解MnO2和LiCl为主要原料,采用水热法合成Al掺杂锂离子筛H1.6(AlxMn1-x)1.6O4,研究了Al掺杂对样品形貌、Li+吸脱附特性及循环稳定性的影响,为优化锰基锂离子筛吸附剂制备工艺及提高其Li+吸脱附特性提供参考。
1 实验
1.1 试剂与仪器
试剂:氯化锂(LiCl),无水氯化铝(AlCl3),氯化铵(NH4Cl),氨水(NH3H2O),氢氧化钾(KOH),以上药品试剂均为分析纯;电解MnO2,分析纯;盐酸(HCl),分析纯;实验用水为一次去离子水。
仪器:BSA224S 型电子天平、PHS-25 型PH 计、KSL-1200X-J 型马弗炉、D/max-2500X 型X 射线衍射仪、JSM-6610LV型场发射扫描电镜、Tecnai G2 20型透射电镜、ESCALAB Xi型X-射线光电子能谱仪、ICAP6300型电感耦合等离子体光谱仪。
1.2 实验方法
1.2.1 纳米片多面体Al掺杂锰基锂离子筛吸附剂的制备
首先将电解MnO2粉末在马弗炉中煅烧15 h,得到Mn2O3粉末。按物质的量比为n(Li)∶n(Mn)∶n(Al)=1.5∶1-x∶x(x=0,0.06,0.1,0.2,0.3,0.4)的比例称取LiCl、Mn2O3和AlCl3,加入去离子水中,同时加入适量KOH 调整溶液的pH 为14,搅拌均匀,倒入100 mL反应釜内衬中,将反应釜放入180 ℃烘箱中反应8 h,得到Li(Mn1-xAlx)O2,样品记为LMO2-Al-x。将所得产物抽滤并干燥,干燥后的产物在马弗炉中热处理4 h,得到Al 掺杂锰基锂离子筛吸附剂前体Li1.6(Mn1-xAlx)1.6O4,样 品 记 为 LMO-Al-x。 将Li1.6(Mn1-xAlx)1.6O4在HCl溶液中酸洗,得到Al掺杂锰基 锂 离 子 筛 吸 附 剂H1.6(Mn1-xAlx)1.6O4,样 品 记 为HMO-Al-x。
1.2.2 纳米片多面体锰基锂离子筛吸附性能研究
取适量锂离子筛HMO-Al-x,加入到50 mL 不同浓度的含Li+溶液中(80 mg/L,100 mg/L,pH=10),在室温下进行搅拌吸附,搅拌24 h后取样测试,研究Li+溶液浓度对样品Li+吸脱附特性的影响。吸附容量可用式(1)[15]进行计算:

式中,Qe为吸附平衡后Li+的吸附容量,mg/g;ρ0为初始锂溶液中Li+的质量浓度,mg/L;ρe为吸附平衡后溶液中Li+的质量浓度,mg/L;V为锂溶液的体积,L;m为锂离子筛吸附剂质量,g。
1.2.3 纳米片多面体锰基锂离子筛循环稳定性研究
锂离子筛循环稳定性的研究过程为称取适量HMO-Al-0.3 对80 mg/L 的Li+溶液进行Li+吸附提取,然后利用0.2 mol/L 的盐酸对提取过程中获得的沉淀进行Li+脱附,重复此吸脱附过程5 次。利用式(1)计算每次的Li+吸附容量。每次循环中Li+洗脱率及Mn3+、Al3+的溶损率可用式(2)[16]进行计算:

式中,RM为Li+洗脱率或Mn3+、Al3+溶损率;ρM为溶液中M离子的质量浓度(M为Li+、Mn3+、Al3+),mg/L;V为锂溶液的体积,L;m为锂离子筛吸附剂质量,g;wM为锂离子筛吸附剂中M离子的质量分数(M为Li+、Mn3+、Al3+)。
2 结果与讨论
2.1 材料结构表征
2.1.1 物相分析
图1为不同锰氧化物的XRD 谱图及LMO-Al-x与HMO-Al-x的晶格参数对比图。从图1a 中可以看出通过水热法制备获得的LMO2-Al-x与LiMnO2标准图谱(JCPDS NO.35-0749)一致。在2θ=28.25°位置出现一个随Al 含量增加而逐渐增强的杂峰。图1b 为LMO-Al-x的XRD 谱图,如图1b 所示,在2θ=18.80、36.56、44.53、64.68°出现的特征衍射峰分别对应(111)(311)(400)(440)晶面,与尖晶石结构锰氧化物Li1.6Mn1.6O4标准图谱(JCPDS NO.52-1841)匹配较好,表明经马弗炉氧化反应后的锰基锂离子筛前驱体为尖晶石结构,且结晶度较好。当Al掺杂含量x=0.4 时,在2θ=28.25、40.44、50.16、66.35°的位置出现杂峰,而酸洗后杂峰相消失,说明杂相具有易溶于酸的特点,由此可初步判断杂峰相可能为AlO(OH)、Al(OH)3或Al2O3相。而且,如图1c所示,酸洗后,对应尖晶石结构的衍射峰强度减弱,表明当Al的掺杂含量过多时,将会导致最终产物出现杂相而且尖晶石相Li1.6Mn1.6O4含量减少。由图1c 可知,酸洗后,HMO-Al-x出现的衍射峰与Li1.6Mn1.6O4标准图谱(JCPDS NO.52-1841)匹配,但衍射峰的位置2θ出现整体的右偏移,这是由于酸洗脱附过程中发生Li+与H+的交换,而H+的离子半径小于Li+,导致晶胞收缩,晶面间距变小。图1d比较了Al掺杂后,晶格参数随Al掺杂含量的变化,由LMO-Al-x(400)晶面的晶格参数变化可以看出,Al掺杂后,晶面间距减小,导致2θ出现微小右移。这主要是由于Al3+的离子半径(0.053 5 nm)比Mn4+(0.054 nm)和Mn3+(0.064 5 nm)小[17],而且Al—O键键能(512 kJ/mol)大于Mn—O键键能(360 kJ/mol)[13],使得Al3+取代Mn3+后产生晶格收缩而导致。HMO-Al-x(400)晶面的晶格参数变化随Al掺杂含量的变化并不明显,主要是由于Li+与H+的交换使晶胞产生较大的收缩所导致。

图1 不同锰氧化物的XRD谱图及晶格参数对比图Fig.1 XRD patterns and lattice parameters comparison chart of different manganese oxides
2.1.2 SEM形貌表征与分析
图2为LMO-Al-0 与LMO-Al-0.3 不同倍率下的SEM照片。由图2a可见,低倍率下未掺杂改性的样品由尺寸约为15 μm的团聚颗粒构成。比较图2a与2c,可以看出Al 掺杂后样品的分散性变好,团聚颗粒尺寸约为5 μm。由图2b 与2d 可知,高倍率下未掺杂改性样品的颗粒主要由尺寸为100 nm 左右的近似球状颗粒组成。Al 掺杂样品主要呈现出尺寸约为100~400 nm纳米片多面体形貌。结果表明,Al掺杂使锰基锂离子筛的分散性及形貌产生显著改变,进而可能会对锂离子筛的吸附性能产生影响。

图2 LMO-Al-0与LMO-Al-0.3不同倍率下的SEM照片Fig.2 SEM images of LMO-Al-0 and LMO-Al-0.3 at different magnification
2.1.3 TEM分析
图3为LMO-Al-0.3 的TEM 照 片。由图3a 可知,纳米粒子的形貌呈现出尺寸约为100 nm的不规则形状。从图3b 的HRTEM 高分辨照片中可以看出,纳米粒子的边缘具有明显的条纹像,计算晶面间距,分别对应尖晶石结构的(111)晶面与(311)晶面。由图3c 的HAADF-STEM 面扫照片及图3d~3f各元素分布图可知,Al元素均匀分布在尖晶石结构的锰氧化物晶格结构中,没有发生明显的团聚或偏聚现象。

图3 LMO-Al-0.3样品的TEM照片及元素分布图Fig.3 TEM images and element distribution maps of LMO-Al-0.3
2.1.4 XPS分析
图4为锰基锂离子筛Al掺杂前后样品的XPS分峰拟合曲线。从图4可以看出,LMO-Al-0.3样品的Mn 2p3/2在643 eV和641.8 eV处可以分出2个峰分别属于Mn4+与Mn3+[18-19],其他样品的Mn 2p3/2同样由Mn4+与Mn3+峰组合而成,表明所有样品中均存在少量的Mn3+。虽然按照化合价理论计算H1.6Mn1.6O4样品中的Mn 全部为+4 价,但由于合成样品中因为氧空位的存在依然含有少量的Mn3+[9]。相对于未掺杂改性的离子筛前驱体LMO-Al-0,LMO-Al-0.3 样品中Mn3+的含量明显降低,验证了Al3+取代的是晶格中Mn3+的位置。酸洗之后,Mn4+和Mn3+峰仍存在,但位置有轻微偏移,而且Mn3+的含量在HMO中均有所减少,说明在酸洗脱附过程中,部分Mn3+发生了歧化反应,这导致了酸洗过程中Mn的溶损。
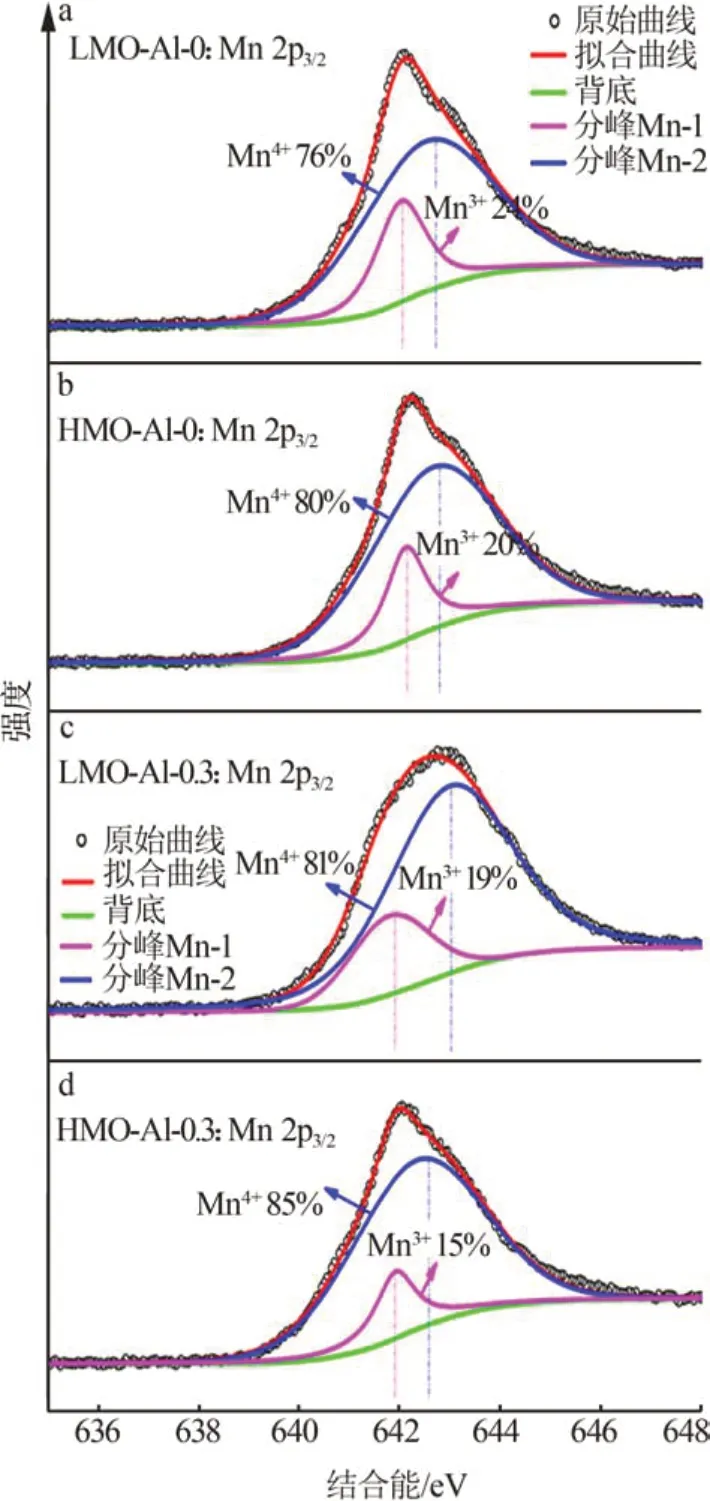
图4 锰基锂离子筛的XPS分峰拟合曲线Fig.4 XPS peak fitting curves of manganese based lithium ion sieves
2.1.5 BET分析
图5为纳米片多面体锰基锂离子筛样品的吸脱附等温线。由图5 可知,所有曲线均与带有回滞环的Ⅳ型等温线形状吻合,表明纳米片多面体锰基锂离子筛样品的吸附为表面介孔层吸附。根据Brunauer-Emmett-Teller(BET)分析,样品的比表面积分别为90.51 m2/g(HMO-Al-0.06)、99.25 m2/g(HMOAl-0.1)、102.58 m2/g(HMO-Al-0.2)和148.98 m2/g(HMO-Al-0.3)。表明通过掺杂Al 元素增大了锰基锂离子筛吸附剂的比表面积,结合SEM 分析结果可以推测这主要是由于Al 元素掺杂后使样品获得纳米片多面体形貌所导致。比表面积的增大使得暴露在表面的吸附位点增加,这将促进Li+与H+的离子交换,从而提高锂离子筛的吸附性能,这与下文锰基锂离子筛吸脱附Li+特性的分析结果一致。
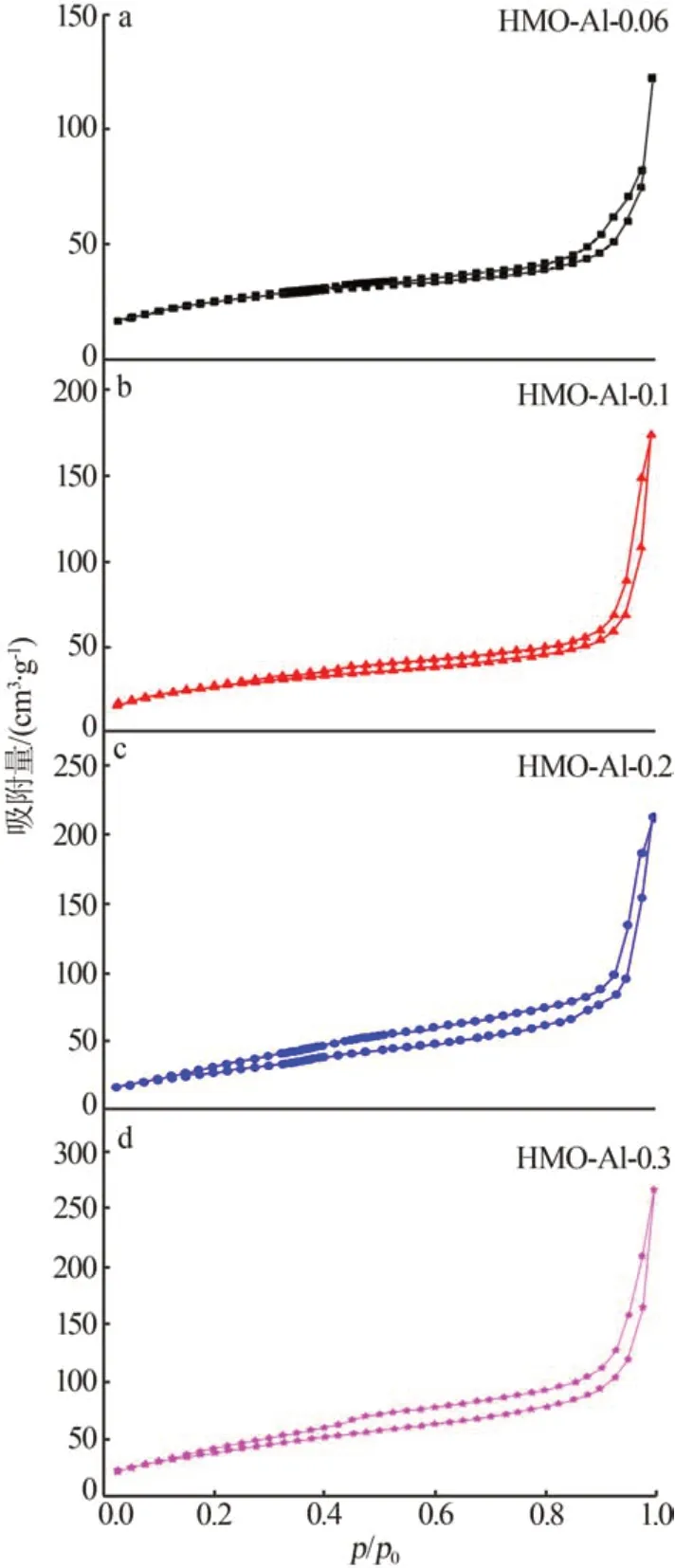
图5 纳米片多面体锰基锂离子筛样品N2-吸脱附等温线Fig.5 N2 adsorption-desorption isotherms of manganese based lithium ion sieves with nanosheet polyhedron morphology
2.2 纳米片多面体锰基锂离子筛吸附剂的Li+吸脱附特性研究
2.2.1 不同Al掺杂含量锂离子筛的吸附性能比较
图6为HMO-Al-x对溶液中Li+平衡吸附容量的对比图。由图6 可知,当Li+溶液初始质量浓度为80 mg/L时,HMO-Al对溶液中Li+的平衡吸附容量随着Al 掺杂含量的增大而增大,HMO-Al-0.3 的吸附容量为32.32 mg/L,高于未掺杂改性样品HMO-Al-0(24.71 mg/L)的吸附容量。当Li+溶液初始质量浓度为100 mg/L 时,HMO-Al 对溶液中Li+的平衡吸附容量随着Al 掺杂含量的变化呈现出类似的规律,HMO-Al-0.3 与HMO-Al-0 的吸附容量分别为34.66 mg/L 与26.92 mg/L。表明Al 元素的掺杂有效地提高了锰基锂离子筛吸附剂对溶液中Li+的吸附性能。这是因为,一方面由SEM与BET表征分析结果可知,Al掺杂后样品呈现纳米片多面体形貌且具有较高的比表面积,使得锂离子筛吸附位点的数目有所增加;另一方面,Al 掺杂使得样品酸洗后可进行离子交换的H+数量有所增加[14]。研究指出,锰基锂离子筛吸附剂对Li+的吸附及脱附能力主要取决于吸附位点的分布、数目及可交换的H+的含量[20]。所以,Al掺杂改性锂离子筛较高的吸附容量可归因于Al 掺杂后微观形貌的改变及可交换H+数目的增加。

图6 HMO-Al-x对溶液中Li+平衡吸附容量的对比图Fig.6 Comparison chart of equilibrium adsorption capacity of Li+in solution by HMO-Al-x
2.2.2 Al掺杂锂离子筛的循环稳定性分析
图7为HMO-Al-0.3 在锂溶液与盐酸溶液中的循环吸脱附性能对比图。由图7a可知,5次循环后,HMO-Al-0.3 对Li+吸附容量降低并不明显,吸附容量由31.77 mg/g降至30.15 mg/g,对Li+的洗脱率可以维持在95%。图7b 为循环过程中Al 与Mn 的溶损率,5 次循环后,Al 的溶损率为0.27%,Mn 的溶损率略高,为3.05%,相比于未掺杂样品Mn 的溶损率(5%)[21]已有明显降低。这主要是因为Al 掺杂后取代了晶格中的部分Mn3+,Al3+(0.053 5 nm)的离子半径小于Mn3+(0.064 5 nm)[17],而且Al—O键的结合力强于Mn—O键,因此,Al3+掺杂有利于使锂离子筛获得稳定的晶体结构,从而表现出优异的循环稳定性[22]。
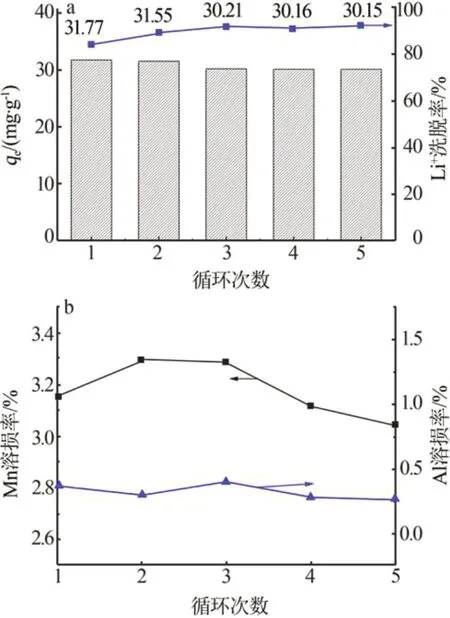
图7 HMO-Al-0.3 样品的循环吸脱附性能Fig.7 Cyclic adsorption and desorption performance of HMO-Al-0.3 sample
3 结论
采用价廉、安全性高的电解二氧化锰与氯化锂为原料,优化水热合成工艺实现了对锰基锂离子筛的Al元素掺杂改性。XRD、TEM结果显示掺杂的Al元素均匀取代了晶格位点的Mn 元素,并且没有改变锰氧化物原有的尖晶石结构。由SEM 及BET 分析结果可知Al掺杂使样品呈现纳米片多面体形貌,且具有较高的比表面积,增加了吸附位点的数目。Li+的吸脱附特性研究结果表明,相比于未掺杂样品,具有纳米片多面体形貌的锰基锂离子筛平衡吸附容量提高了30%,5次循环后,吸附容量保持率为95%。本研究为制备纳米形貌的元素掺杂改性锰基锂离子筛提供了一种有效方法,在保证较高吸附容量的同时可以获得具有优异循环稳定性的锰基锂离子筛吸附剂。
