水力空化联合Fenton/Fenton-Fe氧化降解苯酚废水
2022-07-13陈锐杰孙国龙曹玉琴崔少琦贺琼琼
陈锐杰,孙国龙,曹玉琴,崔少琦,贺琼琼
(1.中国矿业大学材料与物理学院,江苏徐州 211116;2.中国矿业大学化工学院,江苏徐州 211116;3.中国矿业大学安全学院,江苏徐州 211116;4.中国矿业大学国家煤加工与洁净化工程技术研究中心,江苏徐州 211116)
苯酚又名石炭酸,是一种常见的化工废水污染物,主要来源于焦化、石化、医药、塑料、纺织等化工企业,具有来源广、难降解、毒性大等特点[1-2]。高浓度的苯酚废水流入江河,对环境造成严重破坏,同时对人体安全产生巨大威胁。难降解含酚废水的深度净化处理已成为工业上亟待解决的技术难点。
过去,研究人员尝试了不同方法降解含酚废水,包括炭床吸附、生物方法、电化学技术、膜分离技术和其他高级氧化技术[3-5]。但大多存在条件苛刻、降解率低或成本高等缺点。
水力空化(HC)作为一种新型水污染处理技术,近年来成为国内外研究热点[6-8]。HC所产生的微纳气泡在溃灭时会在局部产生热点,瞬态温度达10 000 K,压力约为108Pa[9]。在这种极端条件下,水分子发生热分解反应,分解为高活性的HO·和·H,HO·扩散到本体溶液中与有机污染物发生氧化反应,达到降解污染物的效果。HC协同Fenton高级氧化技术,可进一步提高HO·产量,提高活性氧传质效率的同时强化有机污染物微纳气泡界面反应,从而降低Fenton试剂的用量,减少成本,达到高效降解含酚废水的目的。陈正波等[10]采用微纳气泡联合铁炭微电解法处理盐酸四环素废水,降解率达80.84%。陈利军等[11]采用HC强化H2O2氧化降解水中苯酚,降解率达33.7%。
本文通过自主搭建的HC装置,联合Fenton氧化技术及纳米铁粉强化Fenton技术,探究苯酚废水最优处理工艺,并对其降解过程进行动力学分析,完成含酚废水的高效降解和深度净化,为后续HC技术在水污染处理领域的继续推广提供理论依据。
1 试验材料与方法
1.1 试验药品
用苯酚(分析纯,国药化学试剂有限公司)配制模拟废水,其水质如表1所示。
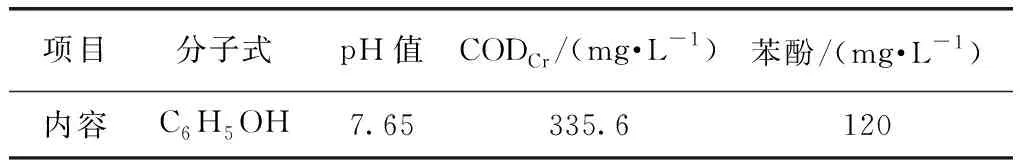
表1 苯酚模拟废水水质Tab.1 Water Quality of Simulated Phenol Wastewater
其他药品:30% H2O2(分析纯,国药化学试剂有限公司);FeSO4·7H2O(分析纯,国药化学试剂有限公司);H2SO4(分析纯,国药化学试剂有限公司);NaOH(分析纯,国药化学试剂有限公司);COD测定试剂;纳米铁粉。
1.2 试验设备
LF-1500微纳米气泡发生器(上海行恒科技有限公司)、JP-020PLUS超声波清洗机、pH计、MS105DU电子分析天平、4802S紫外分光光度计(上海尤尼科仪器有限公司)、水质分析仪、JES-FA200型自旋共振光谱仪(日本电子公司)。
将500 mL的苯酚废水放入储存室,加入Fenton试剂后在离心泵(转速为2 900 r/min,功率为3.0 kW)作用下进入文丘里管,经HC处理后返回储存室,循环工作。其中,文丘里管工作压力为0.5 MPa,流量为40 mL/min,具体试验设备如图1所示。
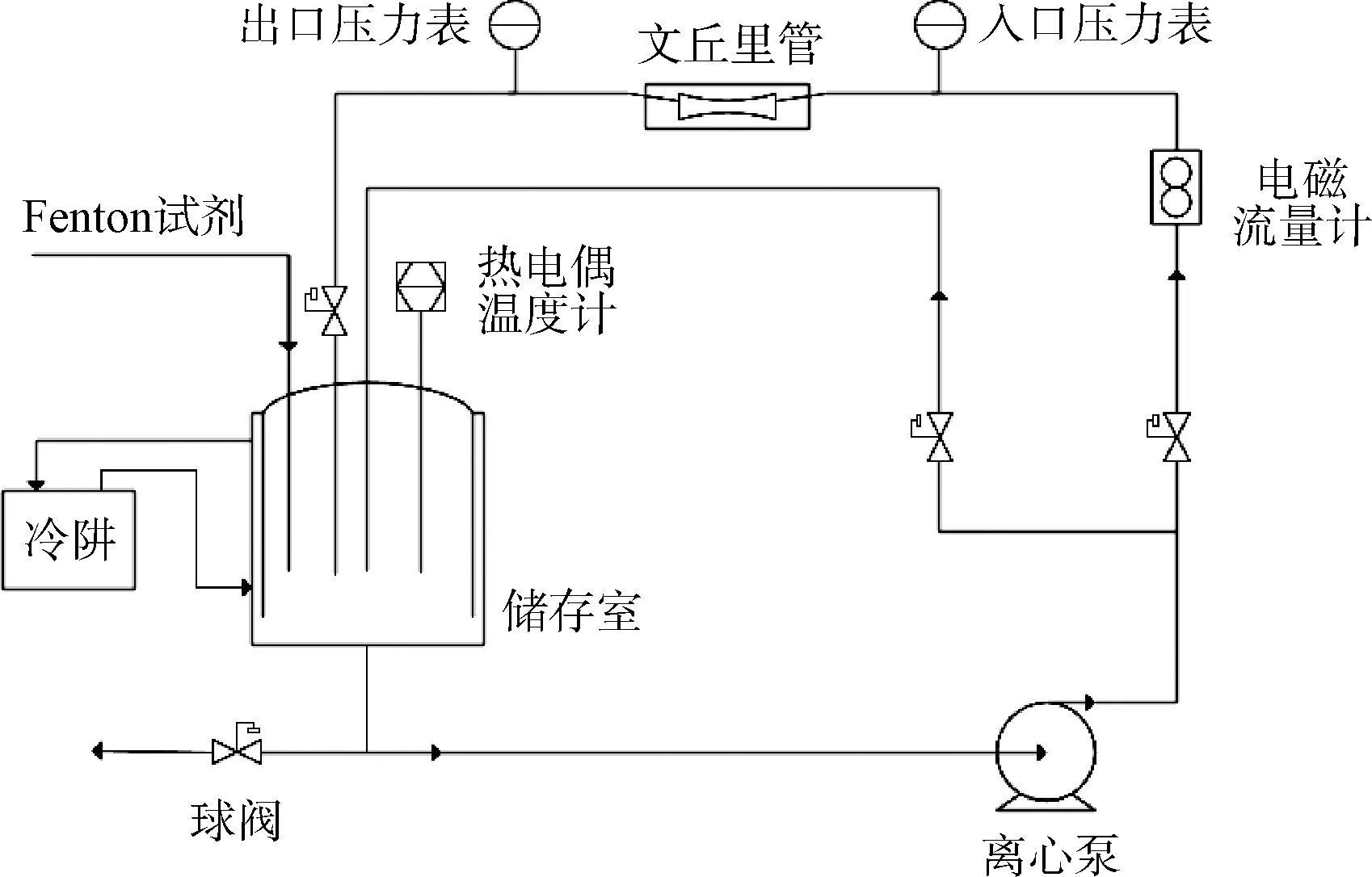
图1 试验设备示意图Fig.1 Schematic Diagram of Experimental Equipment
1.3 试验方法
取500 mL质量浓度为120 mg/L的苯酚溶液,加入NaOH或H2SO4调节pH至所需条件,加入一定量的Fenton试剂,在室温下通入HC装置,改变H2O2用量、FeSO4·7H2O用量、溶液pH、反应时间等因素,研究其对苯酚和CODCr的降解影响。处理完毕后调节溶液pH值至11,并加入2 mL聚丙烯酰胺,将铁离子沉淀,静置数小时后取上层清液测试铁离子与CODCr浓度,并探究多种处理工艺的降解动力学。
1.4 分析方法
CODCr采用快速密闭催化消解法测量[12]。苯酚浓度通过紫外分光光度法测量,设备为UV-9100。为保证吸光度在0~1,将处理完毕的水样稀释10倍,扫描波长为190~1 100 nm,基于比尔-朗伯定律在269 nm波长处测量苯酚溶液的吸光度,将测量值与标准谱线对比,得到降解的苯酚浓度[13-14]。
根据测量数据,分别计算其降解率(η)、动力学反应速率系数(k)和增强因子(f),如式(1)~式(3)。
η=(C0-C)/C0
(1)
ln(C0/C)=kt
(2)
f=(k1+k2)/k3
(3)
其中:C0——处理前苯酚质量浓度,mg/L;
C——处理后苯酚质量浓度,mg/L;
t——反应时间,min;
ki(i=1,2,3)——单独 HC、单独Fenton、HC-Fenton处理工艺的反应速率系数,min-1。
2 结果与讨论
2.1 HC产生的自由基浓度
使用日本电子公司JES-FA200型自旋共振光谱仪X波段(9 GHz)分别测试HC装置对苯酚溶液和水处理60 min所产生的自由基浓度。测试条件:微波功率为0.998 mW,中心磁场强度为314.732 mT,扫描宽度为150 mT,调制频率为100 kHz,调制宽度为2 mT,时间常数为0.03 s,扫描时间为30 s,放大倍数为500倍。其原理是利用自旋捕捉剂与不稳定的自由基发生反应,产生另外一种稳定的、可以用电子自旋共振波谱法检测的新自由基(自旋加合物)。试验采用5,5-二甲基-1-吡咯啉-N-氧化物(5,5-dimethyl-1-pyrroline N-oxide,DMPO)作为自旋捕捉剂捕捉HO·,生成稳定形态的DMPO-OH,可进行ESR分析,其特征图谱为1∶2∶2∶1。具体方程如式(4)~式(5)。
Fe2++H2O2→Fe3++OH-+HO·
(4)
DMPO+HO·→DMPO-OH
(5)
测试结果表明,HC处理60 min苯酚溶液产生的HO·含量为2.099×1018g-1,在水中产生的HO·含量为1.802×1018g-1,同属于一个量级。在苯酚中产生的HO·含量略高于去离子水中含量,表明用HC技术产生HO·处理苯酚溶液是可行的,具体结果如表2与图2所示。

表2 HO·浓度测试结果Tab.2 Test Results of HO· Concentration
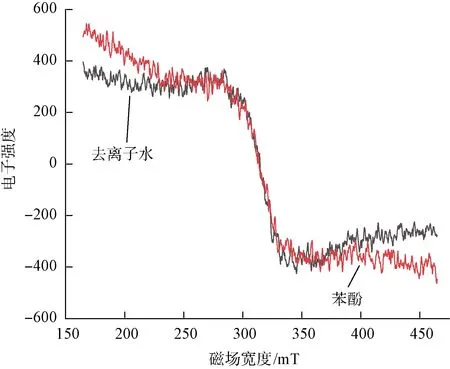
图2 去离子水与苯酚共振谱Fig.2 Resonance Spectrum of Deionized Water and Phenol
2.2 时间对废水降解的影响
在室温下向500 mL质量浓度为120 mg/L的苯酚中加入0.6 mL H2O2、0.20 g FeSO4·7H2O,调节溶液pH值为3,反应时间分别为10、20、30、40、50、60、90、120 min。反应后加入NaOH调节pH值为11,静置数小时后取上层清液测试CODCr与苯酚浓度。另一组在配制完苯酚溶液后直接进行HC处理,相同时间后终止反应,测试CODCr与苯酚浓度。结果如图3所示。
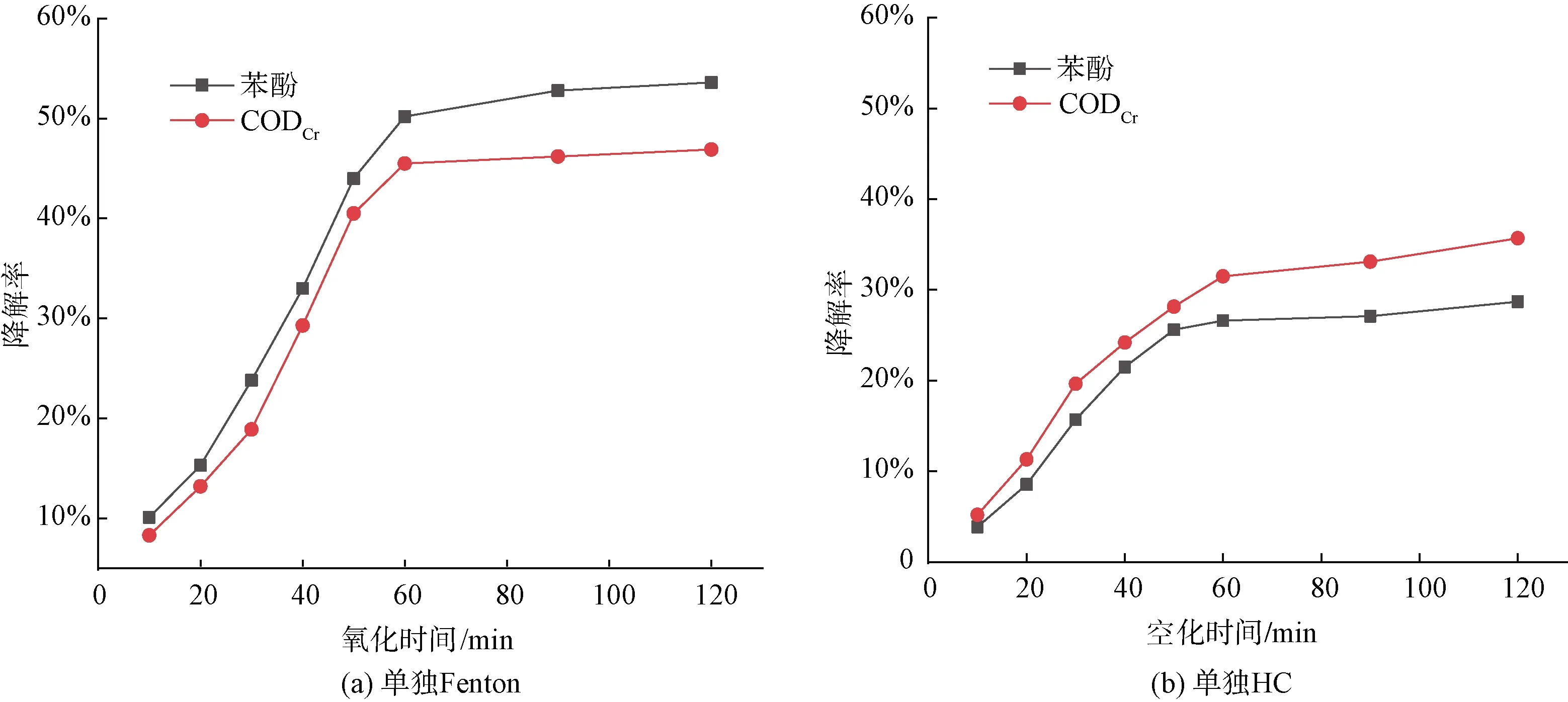
图3 时间对苯酚与CODCr降解的影响Fig.3 Influence of Time on Degradation of Phenol and CODCr
由图3可知,随着时间的增加,CODCr和苯酚的去除率均有增加,且降解速率具有由快而变缓的趋势。由图3(a)可知,在60 min前反应速率较快,此时CODCr和苯酚的降解率分别为45.53%和50.28%,60 min之后反应变缓,直至120 min降解效果无明显增长。原因是Fenton试剂在一开始产生大量的HO·,与苯酚持续发生反应,故反应速率很快,在60 min之后,随着HO·的减少直至耗尽,降解效果的提升无明显变化,因此,选择反应时间为60 min作为优化条件。对于苯酚降解率高于CODCr降解率的原因分析认为,反应初期H2O2在Fe2+的催化作用下,短时间内生成大量HO·,其中一部分HO·与有机污染物发生强烈反应将苯酚氧化为H2O和CO2,另一部分未与苯酚反应而自身发生溃灭,产生苯醌等氧化中间产物,CODCr降解率偏低[13]。同时,苯酚在发生氧化过程中生成羧酸等小分子,而使用的Fenton试剂有限,HO·产生的数量也有限,因此,无法使CODCr进一步降低。Fenton试剂与降解苯酚涉及的方程如式(4)、式(6)~式(8)。
Fe3++H2O2→Fe2++H++HOO·
(6)
HO·+C6H5OH→H2O+CO2
(7)
HO·+HO·→H2O2
(8)
由图3(b)可知,在处理60 min之后,降解速率出现变缓趋势,对于苯酚降解的变缓明显大于CODCr降解的变缓,在60 min时,苯酚和CODCr降解率分别为26.65%和30.74%。原因是HC产生的气泡在溃灭瞬间产生极强的强压力脉冲,在气泡周围形成局部热点,将水蒸气分解为HO·、·H、HO2·和·O等自由基[式(9)],这一过程是持续的,而不是像Fenton试剂在反应开始瞬间产生大量的HO·,这样可大大减少HO·发生自身猝灭。水中所能产生的HO·数量有限,并限于HC装置的功率等原因,在后期出现变缓趋势,另外,在处理后期产物积累饱和,因此,适宜的处理时间为60 min。
H2O+HC→HO·+H·+HO2·+O·
(9)
2.3 废水降解效果影响因素的研究
2.3.1 氧化剂用量对苯酚降解效果的影响
图4是pH值为3、FeSO4·7H2O投加量为0.20 g时,不同H2O2投加量下,60 min的单独Fenton氧化和HC-Fenton处理120 mg/L苯酚溶液的降解效果。可以看出,两种处理方式下,随着H2O2投加量的增大,苯酚和CODCr的降解率都逐渐增大,HC-Fenton处理较单独Fenton氧化处理降解效果更加显著。在H2O2投加量为0.6 mL时,单独Fenton氧化处理下,苯酚和CODCr降解率分别为50.28%和45.53%,HC-Fenton氧化下,苯酚和CODCr降解率分别为84.54%和88.13%,再继续增加药品用量,降解效果并无显著提高。
这是由于H2O2可以提供HO·的载体,随着H2O2投加量的增大,HO·的产生量增大,对苯酚溶液的氧化能力增强;而H2O2又是HO·的捕获剂,过量的H2O2会捕获两种处理方式下产生的HO·,与溶液中的HO·反应产生H2O和O2。徐世贵等[14]对HC-Fenton氧化联合超声吸附处理煤气化废水的研究得到了相同的结论。因此,H2O2的适宜投加量为0.6 mL。其中涉及的机理方程如式(10)~式(12)。
HO·+H2O2→HO2·+H2O
(10)
HO·+HO2·→H2O+O2
(11)
HO2·+H2O2→HO·+H2O+O2
(12)
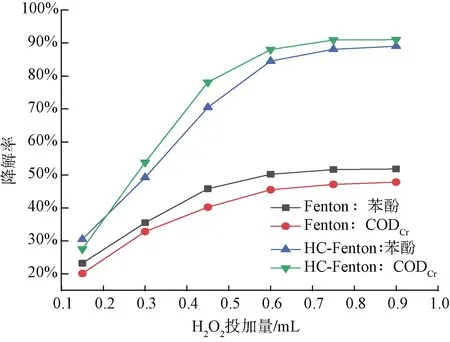
图4 H2O2投加量对苯酚与CODCr降解的影响Fig.4 Effect of H2O2 Dosage on Degradation of Phenol and CODCr
2.3.2 FeSO4·7H2O用量对苯酚降解效果的影响
在pH值为3、H2O2投加量为0.6 mL的试验条件下,改变FeSO4·7H2O投加量,对120 mg/L苯酚溶液进行60 min的单独Fenton氧化和HC-Fenton处理的降解效果影响如图5所示。
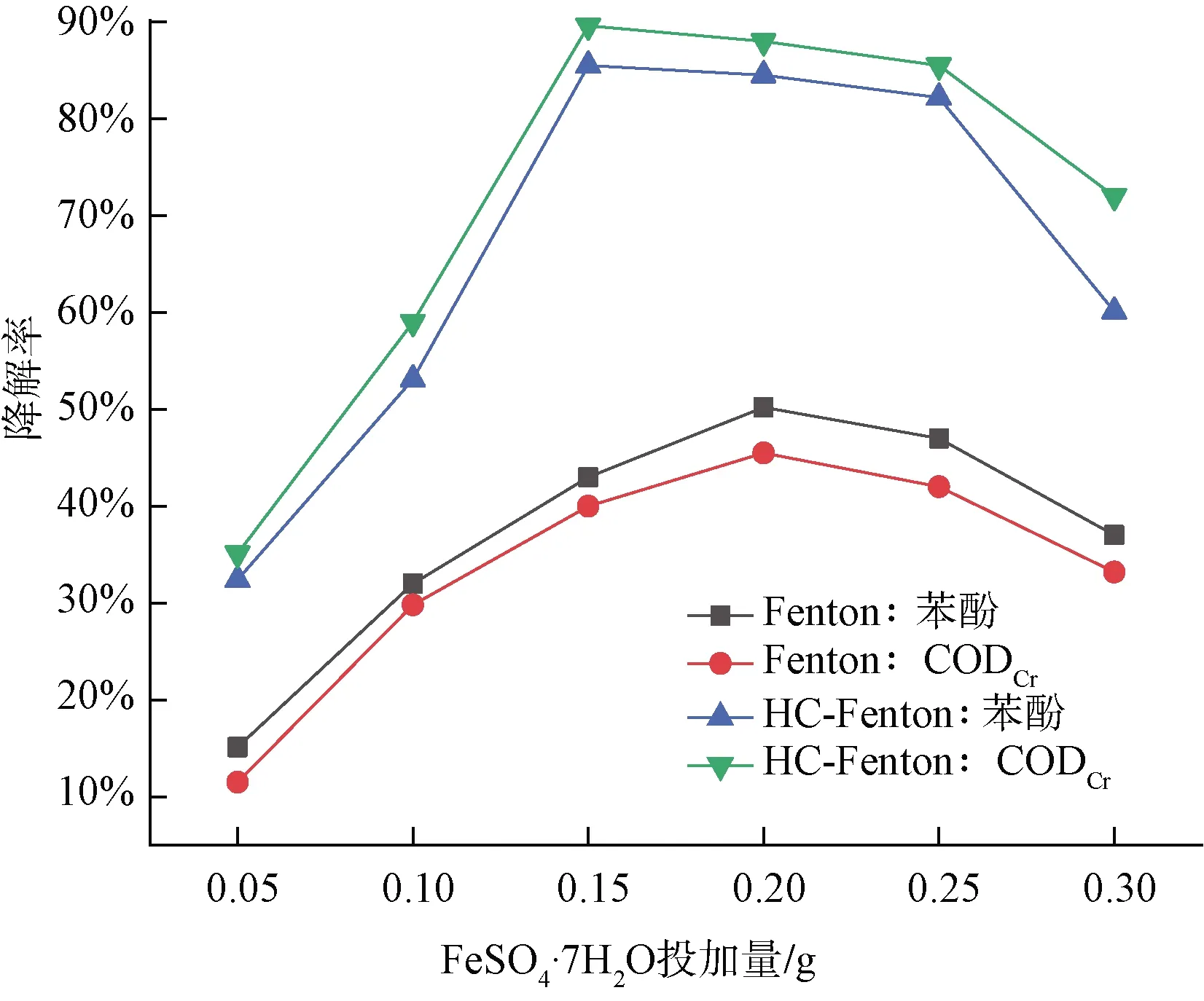
图5 FeSO4·7H2O投加量对苯酚与CODCr降解的影响Fig.5 Effect of FeSO4·7H2O Dosage on Degradation of Phenol and CODCr
由图5可知,两种处理方式下,随着FeSO4·7H2O投加量的增大,苯酚和CODCr的降解率都呈先增加后降低的趋势,且HC-Fenton处理较单独Fenton氧化处理降解效果更加显著。单独Fenton氧化处理时,加入0.20 g的FeSO4·7H2O,苯酚和CODCr的降解率最高,分别为50.28%和45.53%,再继续加量将引起降解率的降低。
分析认为,催化剂用量对单独Fenton和HC-Fenton降解苯酚存在双重作用。过量的Fe2+会与H2O2发生氧化反应变为Fe3+,消耗溶液中的H2O2,使生成HO·速率加快,导致HO·自身湮灭反应的发生,从而降低氧化能力。HC-Fenton氧化中,苯酚和CODCr的降解率最大值出现在FeSO4·7H2O用量为0.15 g时,分析认为HC具有极强传质、催化效果,使用更少量的FeSO4·7H2O即可达到相同效果,提高反应速率,降低试验用量成本。
2.3.3 pH的影响
在FeSO4·7H2O投加量为0.2 g、H2O2投加量为0.6 mL的试验条件下,改变pH,对120 mg/L苯酚溶液进行60 min的单独Fenton氧化和HC-Fenton处理的降解效果影响如图6所示。
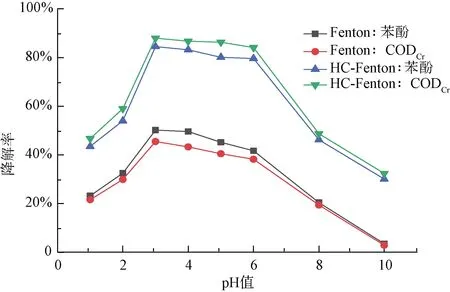
图6 pH值对苯酚与CODCr降解的影响Fig.6 Effect of pH Value on Degradation of Phenol and CODCr
可以看出,两种处理方式下,随着溶液pH的增大,苯酚和CODCr的降解率呈现先增加后降低的趋势,HC-Fenton处理较单独Fenton氧化处理降解效果更加显著。在溶液的pH值为3时,单独Fenton氧化处理下,苯酚和CODCr降解率最高,分别为50.28%和45.53%,在pH值为4~6时pH的大小对于降解效果并无显著影响,pH值<3或>6时影响较大。
分析认为[式(13)~式(15)],酸性条件下有利于H2O2的分解,产生更多的HO·,增强了氧化能力。但在过酸条件下,H+会降低Fe2+的催化效果,同时会与HO·反应,消耗HO·,使氧化能力减弱。碱性条件下,Fe2+易被氧化,形成氢氧化铁络合物,且H2O2会分解为H2O和O2,使生成的HO·减少,降解效率降低[15]。
HO·+H+→+H2O·
(13)
Fe2++OH-+O2→ Fe(OH)3
(14)
H2O2→ H2O+O2
(15)
2.4 处理工艺对苯酚废水的降解效果对比分析
采用多种处理方法对pH值为3、500 mL质量浓度为120 mg/L的苯酚模拟废水进行降解,反应时间为120 min,分别在10、20、30、40、50、60、90、120 min进行取样测试其苯酚和CODCr浓度。其中HC工艺中入口压力为0.6 MPa;Fenton工艺中FeSO4·7H2O投加量为0.20 g,30% H2O2投加量为0.6 mL(Fenton1);Fe2SO4·7H2O投加量为0.40 g,30% H2O2投加量为2.4 mL(Fenton2);HC-Fenton工艺处理条件为上述两者结合;HC-Fenton-Fe工艺中加入的纳米铁粉与FeSO4·7H2O按照摩尔比为1∶1配制,即加入纳米铁粉0.040 3 g。试验结果如图7所示。
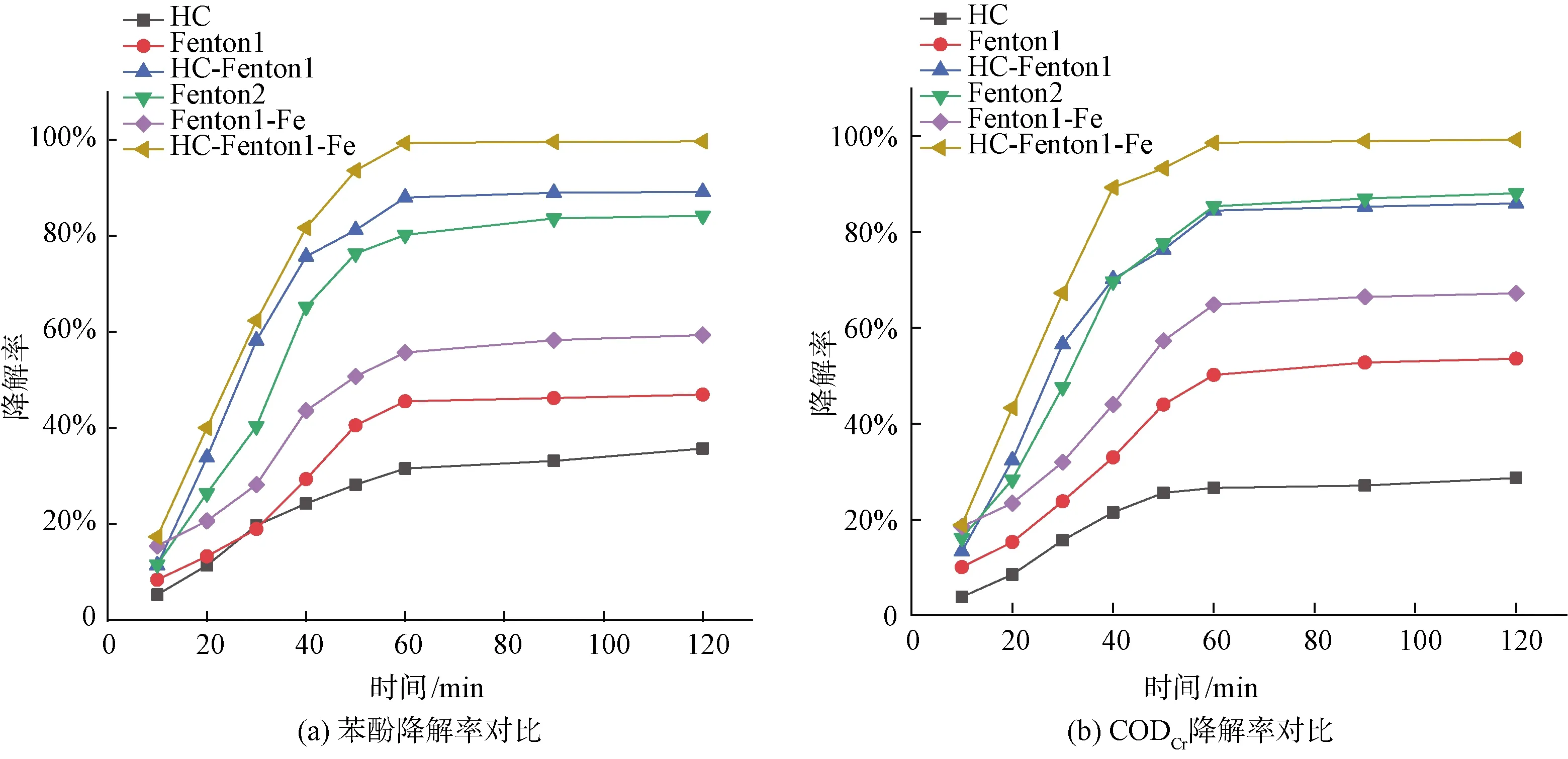
图7 多种处理工艺降解效果对比Fig.7 Comparison of Degradation Effects among Various Treatment Processes
由图7可知,苯酚和CODCr的降解率随着时间的增加而增大,降解主要发生在前60 min,后60 min降解效果则出现变缓趋势。在60 min时,单独HC工艺中苯酚、CODCr降解率分别为26.65%、30.74%,而在120 min时降解率达到28.21%、35.32%。而HC-Fenton工艺在60 min时苯酚、CODCr降解率分别达到88.92%、83.26%,较单独HC处理分别提高62.27%、52.52%。若采用单独Fenton处理,达到此效果需使用H2O22.4 mL、FeSO4·7H2O20.40 g,此时CODCr和苯酚降解率分别为85.41%和80.22%,HC技术的使用可以大大节省药品的成本。对于HC-Fenton处理工艺中加上与Fe2+同样摩尔比的纳米铁粉进行改良,在60 min时苯酚、CODCr降解率可达到98.67%、99.34%。分析原因,Fenton试剂中Fe2+作为良好催化剂可以使H2O2产生大量的HO·,但是在处理过程中Fe2+会参与反应被氧化为Fe3+,从而失去催化作用。一方面,HC技术可以在局部产生高温高压,将水蒸气热解为HO·,使得体系中的自由基含量增加,同时,HC技术产生微纳气泡是一个稳定持续的过程,而不像Fenton试剂在反应初期产生大量HO·,造成HO·本身的部分猝灭现象;另一方面,微纳气泡增大了Fenton试剂与苯酚的接触面积,同时起到搅拌作用,强化活性氧的传质效率,气泡溃灭时产生的强冲击波和微射流理化环境增强了HO·与苯酚的界面反应。在HC-Fenton的工艺中与Fe2+按同摩尔比加入纳米铁粉,可以保护Fe2+不被氧化为Fe3+,获得持续的催化能力,提高Fe2+的利用效率,催化出更多的HO·。使用铁粉而不选择其他还原剂,其一是不会引入其他离子,可以在后续处理中与Fe3+一同沉淀去除,其二是铁粉来源广泛、成本低。具体反应机理涉及式(4)、式(16)。
Fe+Fe3+→Fe2+
(16)
2.5 苯酚废水处理动力学研究
分别将单独HC、单独Fenton以及HC-Fenton这3种处理工艺下苯酚浓度数据进行动力学方程拟合,采用处理时间前60 min的ln(C0/C)与时间t作图,计算得到反应速率常数k和半衰期t1/2。以同种方法对单独HC、Fenton-Fe和HC-Fenton-Fe这3种工艺进行动力学分析,最后计算两种协同方法的增强因子,结果如图 8所示。
由表3可知,单独HC、单独Fenton、HC-Fenton以及加入纳米铁粉的反应过程均符合一级动力学方程,R2均在0.986 00以上,拟合效果较好。反应速率常数依次增大,在HC-Fenton-Fe的处理工艺中,半衰期为1.394 min。这是由于加入的Fenton试剂可以产生一部分HO·,HC技术可持续产生HO·,纳米铁粉使得Fe2+催化剂能稳定存在,并减少H2O2的浪费,产生的HO·总量在多种工艺中最多,同时在HC产生的空化场进一步将HO·强化[16],使得苯酚的降解更为彻底。
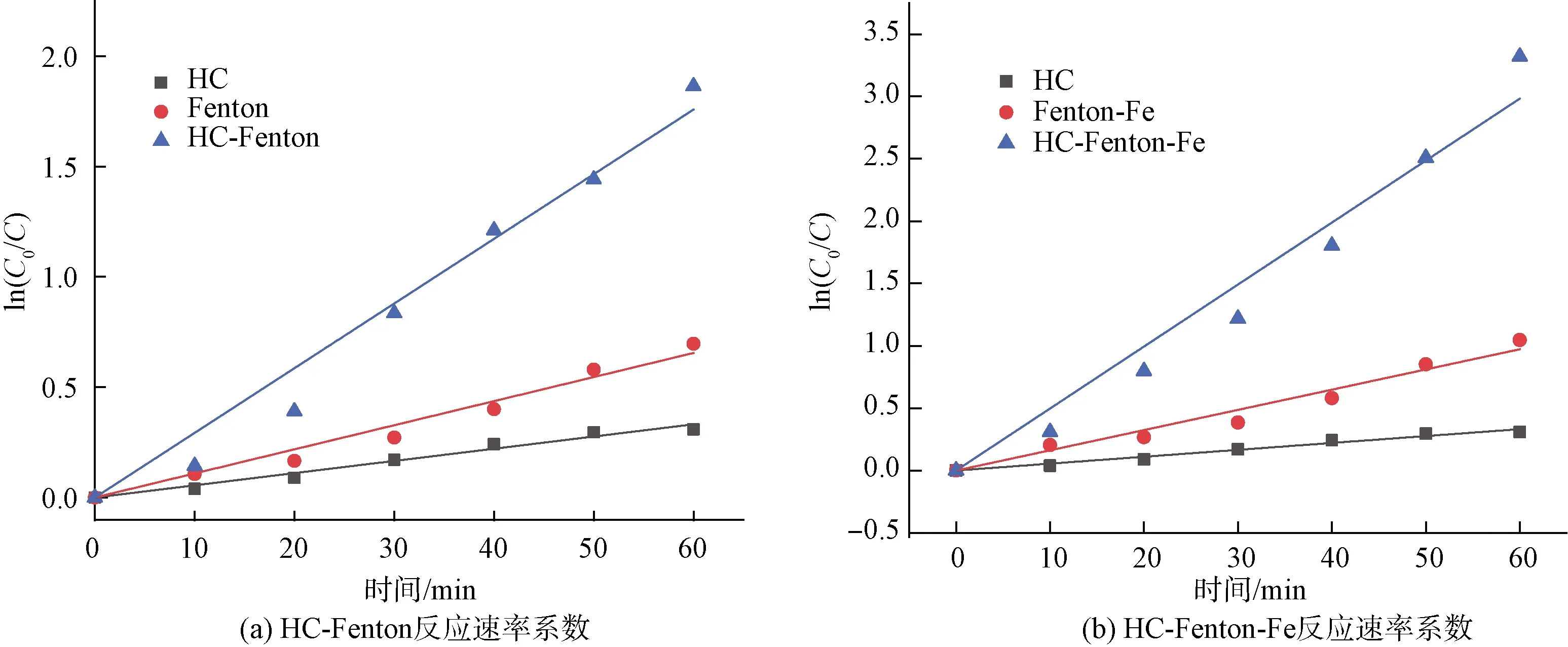
图8 不同处理工艺对反应速率系数的影响Fig.8 Influence of Different Treatment Processes on the Reaction Rate Coefficient

表3 不同工艺处理苯酚的一级动力学方程系数Tab.3 Coefficients of the First-Order Kinetic Equations of Different Processes for Phenol Removal
增强因子计算如式(17)、式(18)。
(17)
(18)
其中:f1——HC-Fenton处理工艺的增强因子;
f2——HC-Fenton-Fe处理工艺的增强因子;
ki(i=1、2、3、4、5)——单独HC、单独Fenton、HC-Fenton、Fenton-Fe、HC-Fenton-Fe的一级动力学反应速率系数,min-1。
HC-Fenton和HC-Fenton-Fe处理工艺的增强因子f均大于1.00,分别为1.78,2.29,说明两种工艺的协同效果对于单独一种工艺处理具有显著的增强效果,对于HC-Fenton-Fe,其增强效果更为明显。
2.6 HC-Fenton-Fe对实际废水的效果
煤焦化实际废水取自江苏徐州某煤焦化厂,pH值为7.95,CODCr质量浓度为722.40 mg/L,含质量浓度为254 mg/L的苯酚及邻甲酚、二甲基苯酚、氰化物、氨类物质。在500 mL的工厂煤焦化废水中加入0.20 g FeSO4·7H2O、0.6 mL 30% H2O2,调节pH值为3.00,空化时间为120 min,空化入口压力为0.4 MPa,流量为40 mL/min。在处理60 min后CODCr和苯酚降解率分别为80.84%和75.22%,此时CODCr质量浓度为138.41 mg/L,达到《污水综合排放标准》(GB 8978—1996)二级排放标准[17](图9)。针对含有多种复杂难降解污染物的煤焦化废水,由于其他水体污染物对HO·的消耗,虽使得苯酚降解率较模拟废水中低23.45%,但采用HC-Fenton-Fe方法处理煤焦化等废水仍具有重要现实意义和显著效果。
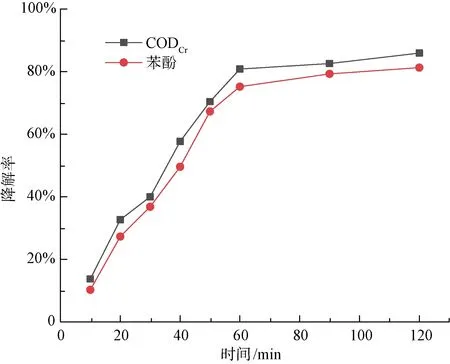
图9 HC-Fenton-Fe对实际煤焦化废水的降解效果Fig.9 Degradation Effect of HC-Fenton-Fe on Actual Coal Coking Wastewater
目前,在煤焦化废水处理中的主流工艺为生物法,主要分为好氧生物处理和厌氧生物处理两种。好氧微生物的特点是易培养、繁殖快、能耗少、价格低廉,但是当废水中的苯酚浓度过高、水质复杂时,生物处理法可能会出现效果不稳定、处理时间长、抗冲击能力差的缺点。而本工艺可快速产生大量HO·,对有机污染物的降解速率快、效率高,且设备操作简单、能够做到二次无污染。在实际处理废水中,需要根据污染物的种类和浓度选择合适的工艺组合。
3 结论
(1)Fenton氧化处理的适宜条件为pH值为3.00、H2O2投加量为0.6 mL、FeSO4·7H2O投加量为0.20 g、处理时间为60 min。此时苯酚和CODCr降解率为50.28%和45.53%,而单独HC处理60 min降解率为26.65%和30.74%。
(2)HC-Fenton处理时CODCr和苯酚降解率达到83.26%和88.92%,比单独使用Fenton氧化达到此效果可节约H2O2用量75%、FeSO4·7H2O用量50%。HC-Fenton-Fe工艺中苯酚和CODCr降解率达到98.67%和99.34%。
(3)单独HC、单独Fenton、HC-Fenton、Fenton-Fe和HC-Fenton-Fe均符合一级动力学方程,HC-Fenton、HC-Fenton-Fe处理工艺的增强因子分别为1.78、2.29,均对苯酚的降解有显著增强效果。
