阿尔泰冷蒿化学成分研究
2022-05-26李知瑾郑丽华
李知瑾 郑丽华 刘 磊*
1.东北师范大学药物基因与蛋白筛选国家工程实验室,吉林 长春 130024; 2.厦门市健康医疗大数据中心(厦门医药研究所)/厦门市天然药物研究与开发重点实验室,福建 厦门 361008
冷蒿(ArtemisiafrigidWilld.)又名白蒿、小白蒿、阿给等,为菊科蒿属(CompositaeArtemisiaLinn.)小灌木植物,具有芳香气味,主要分布于青海、新疆、西藏等以及我国西北、华北、东北各省区,冷蒿是一种中药材,也是藏族、蒙古族常用的一种民间药材[1-3]。冷蒿在不同民族间都有应用,中医药以地上部分入药,蒙医药以全草或地上部分入药,藏医药以地上部分入药,中医药、民族医药、民间医药主要利用冷蒿的地上部分入药[4-7],因此本研究选择阿尔泰冷蒿地上部分作为原材料进行研究。在蒙医药大师占布拉道尔吉编著的《无误蒙药鉴》、藏族经典医书《四部医典》和《晶珠本草》中对冷蒿均有药用记载,蒙药中冷蒿主治出血、关节肿胀、肾热等[5-6],藏药中冷蒿主治痈疖、肺病、肾病等[8],中医在治疗上主治炎症和驱虫等[4]。根据已有文献[9-25]报导,冷蒿化学成分的研究中,涉及产地主要是我国内蒙古自治区、青海省、河北省及加拿大,未见对于新疆地区阿尔泰冷蒿化学成分的研究,在已有研究中,冷蒿的化学成分主要有黄酮类化合物、倍半萜类化合物、苯丙素类化合物、酚类化合物等;对冷蒿的药理作用现今也有很多研究,比如抗癌、抗氧化、调节免疫功能、抗炎消肿等[2,9,12,26-27]。因此,本课题选择阿尔泰冷蒿作为材料,对其化学成分及抗肿瘤活性进行研究。冷蒿是蒿类植物在草原区分布最广的植物[28],阿尔泰冷蒿是生长在阿尔泰地区的种子植物,其资源丰富,这证明阿尔泰冷蒿资源易于获得。虽然阿尔泰地区的冷蒿资源丰富,但是其并未得到有效的利用,因此本课题组与新疆药监局合作,首次选用阿尔泰冷蒿作为原材料对其化学成分及抗肿瘤活性进行研究,研究的意义在于为阿尔泰冷蒿的应用提供前期的理论基础。
1 材料与仪器
本实验药材为阿尔泰冷蒿的地上部分,2011年秋季采集于新疆地区。由新疆药监局提供并鉴定此植物为菊科蒿属(CompositaeArtemisiaLinn.)植物阿尔泰冷蒿(ArtemisiafrigidWilld.),室温阴干,粉碎成粗粉。正己烷、石油醚(PE)、二氯甲烷(CHCl2)、氯仿(CHCl3)、乙酸乙酯(EtOAc)、甲醇(MeOH)、乙醇(EtOH)、丙酮(PA)、正丁醇(nBuOH)、吡啶(Py)、二甲基亚砜(DMSO)等试剂均为分析纯,由北京化工厂生产。柱层析用聚酰胺(天津南开化工厂)、Sephadex LH-20(Pharmacia公司)、硅胶(青岛海洋化工厂)、大孔树脂D101(天津光复)。旋转蒸发仪(上海申生科技有限公司),回流提取器(天津玻璃仪器厂),SHZ-D型循环水式多用真空泵(郑州长城科工贸有限公司),ZK072B真空干燥型电热真空干燥箱(上海市实验仪器总厂)。BRUKER Ultra ShieldTM AV400MHzNMR超导核磁共振波谱仪(德国BRUKER公司),高效液相色谱仪(Aglient 1100),IP X-射线晶体衍射仪(Rigaku IIIA,日本理学株式会社)。人肝癌细胞系(HepG2细胞)购于上海细胞库。
2 提取分离
称取7 kg干燥阿尔泰冷蒿地上部分粗粉,70%EtOH浸没粗粉,回流提取2 h/次,共提取3次,随后合并提取液,减压浓缩得墨绿色浸膏,再悬浮于适量去离子水中,依次用与去离子水等体积的PE、EtOAc、水饱和的nBuOH各萃取3次,分别合并各萃取层,减压浓缩得到萃取物。对石油醚层萃取物(136.0 g)、乙酸乙酯层萃取物(131.3 g)、水饱和的正丁醇层(436.0 g)进行硅胶柱层析、聚酰胺柱层析、葡聚糖凝胶柱层析、大孔树脂柱层析、半制备高效液相色谱的系统分离,每个流份薄层色谱(TLC)或高效液相色谱(HPLC)跟踪检测,最终确定化合物的纯度,得到化合物1~化合物10。
3 结构鉴定
化合物1:白色针状结晶,易溶于CHCl3,化学结构式如图1所示。1H NMR (400MHz, CDCl3):δ1.001(3H,d,J=2.8 Hz) 29位的一个甲基质子信号。13C NMR(100Hz,CDCl3):δ213.19(C=O), 59.48(C-10), 58.23(C-4), 53.10(C-8), 42.79(C-18), 42.14(C-5), 41.52(C-2), 41.29(C-6), 39.69(C-14), 39.25(C-22), 38.29(C-13), 37.44(C-9), 36.00(C-11), 35.62(C-16), 35.34(C-19), 35.01(C-29), 32.77(C-15), 32.42(C-21), 32.08(C-28), 31.77(C-30), 30.50(C-17), 29.99(C-12), 28.16(C-20), 22.27(C-1) , 20.25(C-27), 18.65(C-26), 18.23(C-7), 17.94(C-25), 14.60(C-24)。上述核磁共振波谱数据与已有文献[29]报道的数据基本一致,化合物1鉴定为木栓酮。
化合物2:白色油状,易溶于CHCl3,化学结构式如图1所示。1H NMR (400MHz, CDCl3):δ3.60(1H,m)、3.85(1H,s)为连氧碳上的质子信号,δ5.61(1H,s)为双键碳上的质子信号。13C NMR(100Hz,CDCl3):δ146.23(C-5), 123.87(C-6), 71.36(C-3), 65.35(C-7), 55.71 (C-17), 49.42(C-14), 45.83(C-24), 42.26(C-9),42.30(C-13), 42.00(C-4), 39.17(C-12),37.51(C-8), 37.00(C-1), 37.40(C-10), 36.10(C-20),33.91(C-22),δ31.38(C-2), 25.92(C-23), 28.27(C-16),24.29(C-15), 29.12(C-25), 23.06(C-28),20.70(C-11),18.79(C-27), 19.79(C-26), 19.02(C-21), 18.24(C-19),12.06(C-29), 11.71(C-18),上述核磁共振波谱数据与已有文献[30-31]报道的数据基本一致,因此鉴定化合物2为豆甾-5-烯-3β,7α-二醇。
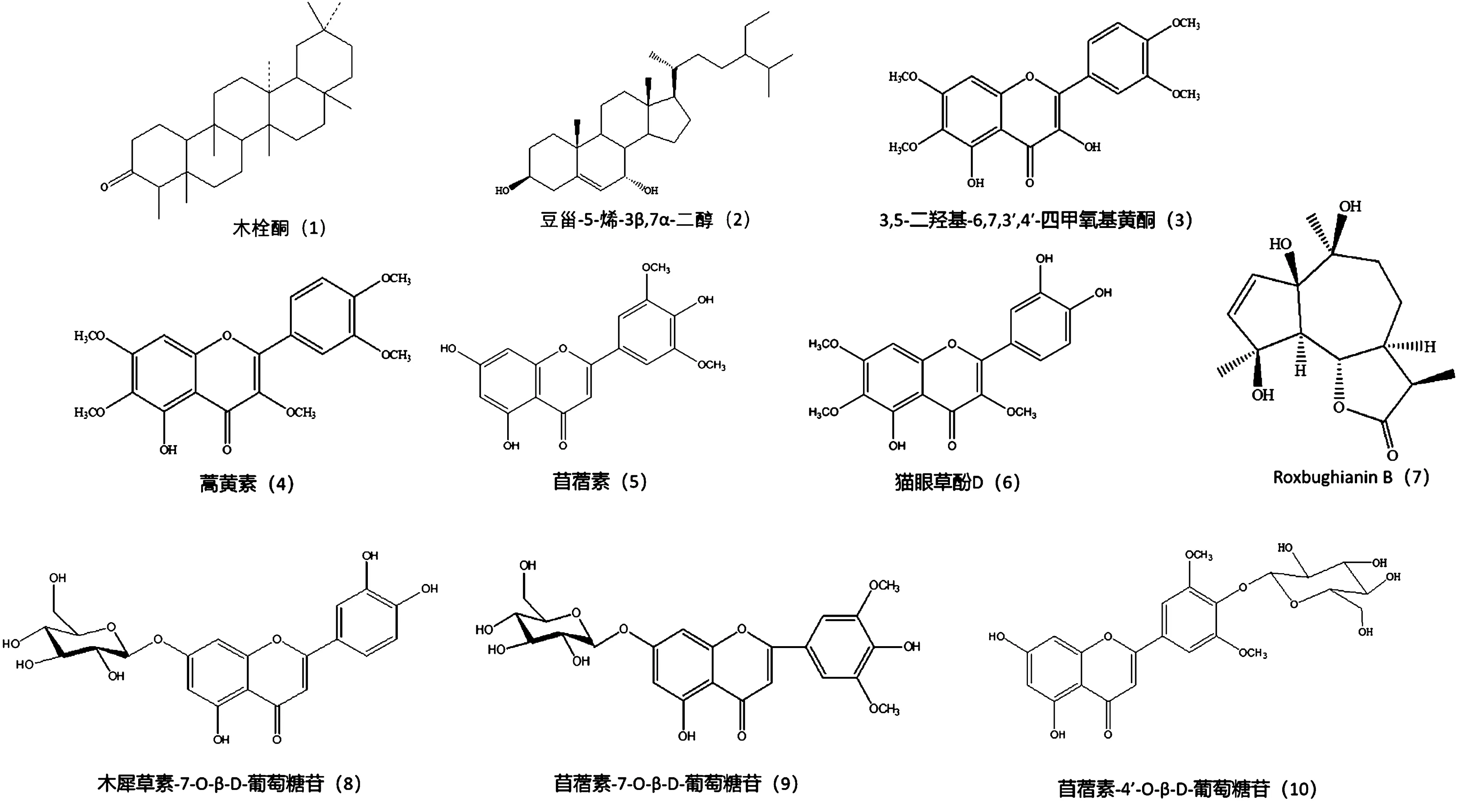
图1 化合物1~10的化学结构式图
化合物3:黄色粉末,易溶于CHCl3、DMSO,化学结构式如图1所示。1H NMR (400MHz, CDCl3):δ7.71(1H,s)、7.66(1H,dd)、7.04(1H,d,J=8.40Hz)、6.50(1H,s)为黄酮骨架结构上2’、6’、5’、8位的质子信号。13C NMR(100Hz,CDCl3):δ178.90(C-4), 158.78(C-7), 155.95(C-2), 152.79(C-5), 152.32 (C-9), 148.35(C-4’), 146.36(C-3’), 138.71(C-3), 122.61(C-6’), 122.48(C-1’), 114.59(C-5’),110.93(C-2’), 106.60(C-10), 90.33(C-8), 60.90(-OCH3),60.18(-OCH3), 56.33(-OCH3), 56.14(-OCH3),上述核磁共振波谱数据与已有文献[32]报道的数据基本一致,化合物3鉴定为3,5-二羟基-6,7,3’,4’-四甲氧基黄酮。
化合物4:黄色结晶,易溶于CHCl3、DMSO,化学结构式见图3。1H NMR (400MHz, CDCl3):δ7.74(1H,dd)、7.69(1H,d,J=1.6Hz)、6.99(1H,d,J=8.4Hz)、6.51(1H,s)为黄酮骨架结构上2’、6’、3’、8位的质子信号。13C NMR(100Hz,CDCl3):δ178.89(C-4), 158.78(C-7), 155.87(C-2), 152.79(C-5), 152.32 (C-9), 151.41(C-4’), 148.80(C-5’), 138.84(C-3), 132.23(C-6), 122.93(C-6’), 122.15(C-1’),111.31(C-2’), 110.87(C-3’), 90.33(C-8), 60.89(-OCH3),60.20(-OCH3), 56.33(-OCH3), 56.10(-OCH3) , 56.01(-OCH3),上述核磁共振波谱数据与已有文献[33]报道的数据基本一致,化合物4鉴定为蒿黄素。
化合物5:黄色粉末,易溶于DMSO,化学结构式如图1所示。1H NMR (400MHz, DMSO-d6):δ12.96(1H,s)为黄酮5位羟基质子信号,δ7.33(2H,s)、6.99(1H,s)、6.56(1H,s)、6.20(1H,s)为黄酮骨架芳香环上的质子信号,δ10.79(1H,s)、9.31(1H,s)为两个羟基的质子。13C NMR(100Hz,DMSO-d6):δ181.77(C-4), 164.09(C-2), 163.62(C-7), 161.37(C-5), 157.30 (C-9), 148.15(C-3’、C-5’), 139.83(C-4’), 120.35(C-1’), 104.36(C-2’、C-6’), 103.70(C-3), 103.56(C-10),98.78(C-6), 94.15(C-8), 56.34(2个-OCH3),上述核磁共振波谱数据与已有文献[34]报道的数据基本一致,化合物5鉴定为苜蓿素。
化合物6:黄色油状,易溶于MeOH、DMSO,化学结构式如图1所示。1H NMR (500MHz, DMSO-d6):δ7.52(1H,d,J=5.0Hz)、7.44(1H,dd)、6.84 (1H,d,J=15.0 Hz)、6.80(1H,s)为黄酮骨架芳香环质子信号。13C NMR(100Hz,DMSO-d6):δ178.13(C-4), 158.56(C-7), 156.06(C-2), 149.41(C-5,C-9,C-4’), 145.40 (C-3’), 137.53(C-3), 131.54(C-6), 120.71(C-1’,C-6’), 115.65(C-5’), 115.28(C-2’), 105.49(C-10), 91.24(C-8),60.02(-OCH3),59.59(-OCH3), 56.44(-OCH3),上述核磁共振波谱数据与已有文献[35-36]报道的数据基本一致,化合物6鉴定为猫眼草酚D 。

图2 化合物7的HMBC图示解析
化合物7:无色结晶,易溶于MeOH、DMSO,化学结构式如图1所示。1H NMR (400 MHz, MeOD):δ6.00(1H,d,J=5.84Hz)、5.88(1H,d,J=5.84 Hz)为一组烯基质子信号,δ4.93与氘代甲醇试剂峰重叠为化合物上6位质子信号,化学位移值在3.00以下的均为此化合物的烷基取代基团。13C NMR(100Hz,MeOD):δ183.46(C-12), 140.48(C-3), 138.57(C-2), 90.03(C-1), 84.55(C-6), 81.07(C-4), 76.13(C-10), 66.24(C-5), 41.75(C-7), 41.10(C-11), 36.95(C-9),28.77(C-14), 26.32(C-15), 24.04(C-8), 11.22(C-13)。HMBC(MeOD):C、H的远程相关,清楚地给出C、H的远程相关关系。通过HMQC(MeOD)波谱给出的信息可以得出以下结论,此化合物的2、3、5、6、7、8、9、11、13、14、15位上直接相连的C、H有相关,如图2所示。上述核磁共振波谱数据与已有文献[37]报道的数据基本一致,并用SHELXTL软件进行数据分析通过对化合物结构的调整使得Goof值接近1,证明此化合物单晶衍射所得到的结果符合此化合物的绝对构型,如图3所示。因此认为化合物7是Roxbughianin B。
化合物8:黄色粉末,易溶于DMSO,化学结构式如图1所示。1H NMR (400MHz, DMSO-d6):δ7.46(1H,d,J=8.48 Hz)、6.91(1H,d,J=8.24Hz)为黄酮骨架结构上2’和6’位的芳香环上的质子信号,δ4.60-δ5.39之间为与黄酮相连的葡萄糖质子信号。13C NMR(100Hz,DMSO-d6):δ181.87(C-4), 164.45(C-2), 162.93(C-7), 161.12(C-9), 156.93 (C-5), 149.92(C-3’), 145.77(C-4’), 121.35(C-6’), 119.15(C-1’), 113.55(C-2’), 105.32(C-10),103.15(C-3), 99.87(C-1’’) , 99.52(C-6), 94.70(C-8), 77.15(C-5”), 76.38(C-3’”), 73.10(C-2’”),69.53(C-4”), 60.60(C-6”),上述核磁共振波谱数据与已有文献[38]报道的数据基本一致,化合物8鉴定为木犀草素-7-O-β-D-葡萄糖苷。
化合物9:黄色粉末,易溶于DMSO,化学结构式如图1所示。1H NMR (400MHz, DMSO-d6):δ12.95(1H,s)和δ9.36(1H,s)为黄酮上羟基质子信号,δ7.36(2H,s)、7.08(1H,s)、6.94(1H,s)、6.46(1H,s)、6.44(1H,s)为黄酮骨架芳香环上的质子信号,δ4.64-δ5.39之间为与黄酮相连的葡萄糖质子信号。13C NMR(100Hz,100MHz, DMSO-d6):δ182.05(C-4), 164.09(C-2,C-4’), 162.99(C-7), 161.06(C-9), 156.85(C-5), 148.19(C-3’,5’), 140.04(C-1’), 120.16(C-10), 104.48(C-2’,6’), 103.77(C-3), 100.12(C-1’’),99.48(C-6), 95.29(C-8) , 77.34(C-5”), 76.47(C-3”), 73.12(C-2”), 69.62(C-4’’), 60.61(C-6”), 56.35(2个-OCH3),上述核磁共振波谱数据与已有文献[39-40]报道的数据基本一致,化合物9鉴定为苜蓿素-7-O-β-D-葡萄糖苷。
化合物10:黄色粉末,易溶于DMSO,化学结构式如图1所示。1H NMR (400MHz, DMSO-d6):δ7.33(2H,s)、7.05(1H,s)、6.57(1H,s)、6.21(1H,s)为黄酮骨架芳香环上的质子信号,δ4.33-δ5.14之间为与黄酮相连的葡萄糖质子信号。13C NMR(100Hz,DMSO-d6):δ181.90(C-4), 164.36 (C-2), 163.01(C-7), 161.40(C-9), 157.42(C-5), 152.89(C-4’), 137.57(C-1’), 125.72(C-10), 104.95(C-2’,6’), 103.84(C-3), 101.95(C-1’’),98.95(C-6), 94.32(C-8) , 77.41(C-5”), 76.62(C-3”), 74.16(C-2”), 69.88(C-4”), 60.79(C-6”), 56.73(2个-OCH3),上述核磁共振波谱数据与已有文献[41]报道的数据基本一致,化合物10鉴定为苜蓿素-4’-O-β-D-葡萄糖苷。
4 抗肿瘤活性
由于本实验从阿尔泰冷蒿中提取分离得到的化合物主要包括黄酮类化合物和倍半萜类化合物,有文献报道显示黄酮类化合物和倍半萜类化合物具有较好的抗肿瘤活性,因此本实验选择对阿尔泰冷蒿中提取分离得到的化合物进行抗肿瘤活性研究。将对数生长期的人肝癌细胞HepG2接种在96孔细胞培养板中,在恒温培养箱中培养24 h后,分别加入0.1、1、10、100 μg/mL不同浓度的药物(用DMSO将化合物配制成10 mg/mL的母液,再用含有3%血清的细胞培养液进行逐级稀释),每孔为100 μL。药物作用48 h后,每孔加入20 μL 2.5 mg/mL MTT溶液,在恒温培养箱中继续培养4 h,之后弃上清,每孔加入100 μL DMSO,使用微量震动器震动10 min之后用多功能酶标仪检测OD490值。对以上10个化合物进行抗肿瘤活性的初步筛选,结果显示化合物2、化合物3、化合物7的IC50值分别为(78.54± 20.51 )μg/mL、(34.58± 2.42) μg/mL 、(149.52± 7.09)μg/mL ,化合物4和化合物8的 IC50值均大于200 μg/mL ,化合物1、化合物5、化合物6、化合物9、化合物10由于在检测时发现有药物在细胞培养板内析出,因此数据不可信。
5 讨论
本论文对阿尔泰冷蒿地上部分的化学成分进行研究,对其70%乙醇提取物的石油醚萃取层、乙酸乙酯萃取层、水饱和的正丁醇萃取层混合物进行分离,经鉴定得到10个单体化合物,其中7个黄酮类化合物、2个甾体类化合物和1个倍半萜类化合物,并首次解析化合物7Roxbughianin B的绝对构型。通过文献查阅可知,蒿属植物中含有大量的黄酮类化合物[42]和倍半萜类化合物[43],其中从黄蒿中提取分离得到的青蒿素即为倍半萜类化合物的典型代表。本实验结果可知,阿尔泰冷蒿中提取分离得到的蒿黄素(4230 mg)和Roxbughianin B(174 mg)含量较其他成分略多。根据文献查阅发现,至今仅有一篇文献[44]在灰苞蒿中提取的到Roxbughianin B,主要提取分离流程分为四步,利用甲醇提取,乙酸乙酯萃取,两次硅胶柱色谱分离得到 Roxbughianin B(6 mg),对比已有文献的提取分离方法可知,本实验对Roxbughianin B的提取分离流程更为简单并且提取率更高,即阿尔泰冷蒿提取分离Roxbughianin B得步骤为三步,70%乙醇提取,乙酸乙酯萃取,一次硅胶柱色谱分离得到Roxbughianin B(174 mg)。因此,以上结果就为蒿黄素和Roxbughianin B的来源提供了新思路。
冷蒿的药理作用方面,有文献[12]研究显示冷蒿总黄酮具有较强的抗氧化能力,本课题通过抗肿瘤活性筛选发现,3,5-二羟基-6,7,3’,4’-四甲氧基黄酮(3)对人肝癌细胞HepG2有较好的抑制作用,3,5-二羟基-6,7,3’,4’-四甲氧基黄酮是一种黄酮类化合物,在此前的研究中并未发现冷蒿中黄酮类化合物具有抗肿瘤活性。然而,本实验提取分离得到的倍半萜类化合物Roxbughianin B对人肝癌细胞HepG2的抑制作用效果不佳,根据之前的文献报道,从冷蒿中提取分离的倍半萜类化合物具有较好的抗肿瘤活性,其中包括去氢-姜黄烯、二氢去氢木香内酯对人子宫颈肿瘤细胞、人脑神经胶质瘤细胞、人肝癌细胞和人黑色素瘤细胞的生长均有影响[9]。从本研究的结果可知,阿尔泰冷蒿的化学成分研究还有很大的空间,因此对于阿尔泰冷蒿的研究还应继续,对其化学成分的深度挖掘将对阿尔泰冷蒿的应用提供前期的理论基础。
