酸碱药对甘草-马钱子配伍汤液沉积相态释放特性研究
2022-05-24郭玉岩李春城魏宇欣杨大宇吕邵娃
郭玉岩,高 滔,李春城,魏宇欣,邵 爽,孙 爽,杨大宇,吕邵娃
酸碱药对甘草-马钱子配伍汤液沉积相态释放特性研究
郭玉岩,高 滔,李春城,魏宇欣,邵 爽,孙 爽,杨大宇,吕邵娃*
黑龙江中医药大学 教育部北药基础与应用研究重点实验室,黑龙江 哈尔滨 150040
探讨甘草-马钱子配伍汤液沉积相态的释放行为,为甘草-马钱子配伍减毒提供科学参考。建立沉积相态释放测定HPLC法,通过体外释放实验,追踪沉积相态在蒸馏水、人工胃液、人工肠液等不同介质中主成分的释放行为,并对其释放结果进行拟合研究分析。甘草酸、马钱子碱以及士的宁在人工肠液中的释放量较大,且马钱子碱>甘草 酸>士的宁。马钱子碱和甘草酸均与一级动力学模型拟合结果最佳,士的宁与Higuchi模型拟合结果最佳。甘草-马钱子沉积相态主要毒效成分呈现出难溶性骨架材料缓释制剂的释放特性,毒(效)成分士的宁可能以沉积共聚体形式存在,在体释放呈缓释行为而减毒;同时,甘草酸的释放对减毒增效起到协同作用。
酸碱药对;甘草;马钱子;配伍汤液;体外释放;沉积相态;减毒
配伍是中医遣方用药之精髓,诸如附子[1-3]、马钱子[4-6]等常用有毒中药,因合理的配伍而能毒减效增[7],“甘缓”“辛散”“酸收”“苦泄”等各具性味的中药常常以药对形式出现在一个组方,群药合煎过程中,伴有溶入水体的次生代谢小分子、生物大分子物质以及无机元素等均影响和改变着合煎汤液的理化性质,使得中药配伍汤液可形成沉积、混悬、胶体及溶液等复杂汤液相态体系,而含酚类、羧酸类成分的中药,与含生物碱类成分的中药配伍,在高温和复杂的化学环境中,生成新的化合物析出沉积形成形态的现象已被充分证实[8]。多项研究表明,汤液相态的特性关乎着汤液中活性组分、毒性物质的释药行为,进而影响药物疗效的发挥和毒性的表达。马钱子为典型有毒中药,其因药理活性显著,为历代医家所推崇。但由于自身固有毒性,应用不慎极易中毒甚至死亡,马钱子主要毒效成分为生物碱类物质马钱子碱和士的宁,过量时可过度兴奋延髓表现出神经系统毒性[9-10]。为有效降低马钱子毒性,临床上常常采用与甘草配伍用药。甘草为国老之药,可解众毒,二者是典型的酸碱药对,大量报道显示[11-13]甘草可解马钱子之毒,但甘草解马钱之毒的确切机制尚不明晰。本课题组前期立足于汤液相态角度,对甘草-马钱子药对配伍汤液中不同相态毒效物质的变化规律进行分析,发现甘草-马钱子汤液的沉积相态可富集近80%的毒效物质,是甘草解马钱子之毒的关键相态[14],而对沉积相态释药特性的分析,可为二者配伍毒减效存规律的深入探讨提供参考。本实验建立了HPLC测定方法,追踪马钱子-甘草配伍汤液关键沉积相态在蒸馏水、人工胃液、人工肠液等不同介质中典型成分的释放特性,从物理药剂学角度出发,为解析甘草配伍马钱子毒减效增的作用机制提供科学参考。
1 仪器与试剂
1.1 仪器与设备
AB265-S型分析电子天平,美国Mettler-Toledo公司;RC806D型溶出试验仪,天津市天大天发科技有限公司;UItiMate3000型色谱仪,美国Thermo Fisher Scientific公司;SB-5200D型超声波清洗机,宁波新芝生物科技股份有限公司;冷冻真空干燥机,埃朗仪器有限公司;Mikro200R型离心机,德国Hettich公司。
1.2 试剂与材料
马钱子、甘草均购自于哈尔滨市同仁药材站,经黑龙江中医药大学王振月教授鉴定,分别为马钱科马钱属植物马钱L.的干燥成熟种子、豆科甘草属植物甘草Fisch.的干燥根和根茎。马钱子碱、士的宁对照品均购自上海源叶生物科技有限公司,批号分别为Y16A7S13272、Z02A7S18869,质量分数均>98%。甘草酸、甘草苷、异甘草苷对照品均购自宝鸡市晨光科技有限公司,批号分别为HI042238196、HL04223898、HI042234198,质量分数均>98%。氢氧化钠,天津市永大化学试剂有限公司;磷酸二氢钾,天津市凯通化学试剂有限公司;胰酶,上海阿拉丁生化科技股份有限公司;盐酸,哈尔滨理工化学试剂有限公司;胃蛋白酶,北京索莱宝科技有限公司;磷酸,天津市科密欧化学试剂有限公司;甲醇,色谱纯,天津市富宇精细化工有限公司;乙腈,色谱纯,北京迪科马科技有限公司;其余试剂均为分析纯。
2 方法与结果
2.1 色谱条件
采用Diamonsil C18(2)(250 mm×4.6 mm,5 μm)色谱柱;以乙腈-0.1%磷酸水溶液为流动相,梯度洗脱:0~10 min,95%~90%乙腈;10~20 min,90%~87%乙腈;20~30 min,87%~85%乙腈;30~40 min,85%~80%乙腈;40~45 min,80%~77%乙腈;45~60 min,77%~68%乙腈;60~80 min,68%~62%乙腈;80~90 min,62%~52%乙腈;90~105 min,52%~35%乙腈;105~115 min,35%~20%乙腈;体积流量1.0 mL/min;柱温25 ℃;检测波长254 nm;进样量10 μL。
2.2 溶液的制备
2.2.1 溶出介质的制备
(1)人工胃液的制备:取稀盐酸(盐酸234 mL,加水稀释至1000 mL)16.4 mL,加水约800 mL,胃蛋白酶10 g,摇匀后,用0.1 mol/L,盐酸溶液调节pH至1.3,加水稀释并定容到1000 mL,即得人工胃液。
(2)人工肠液的制备:取磷酸二氢钾6.8 g,加水500 mL二使其溶解,用0.1 mol/L氢氧化钠溶液调节pH值至6.8;称取胰蛋白酶10 g,加适量水溶解;将上述2种溶液混合后,再加水稀释并定容到1000 mL,即得人工肠液。
2.2.2 对照品溶液的制备 取马钱子碱及士的宁对照品,精密称定,分别置10 mL量瓶中,甲醇溶解定容,得马钱子碱和士的宁质量浓度分别为0.276、0.245 mg/mL和0.014、0.012 mg/mL的2份混合对照品溶液。
精密称取甘草酸、甘草苷、异甘草苷及异甘草素对照品置25 mL量瓶中,用甲醇定容,得到甘草酸、甘草苷、异甘草苷、异甘草素质量浓度分别为0.222、0.193、0.290、0.041 mg/mL和0.011、0.009、0.014 5、0.002 mg/mL的2份混合对照品溶液。
2.2.3 供试品溶液的制备 采用本课题组前述描述的方法[15-16]制备甘草-马钱子合煎液沉积相态。
取马钱子-甘草合煎沉淀相态约0.5 g,精密称定,置具塞锥形瓶中,精密加入浓氨水1 mL和三氯甲烷25 mL置于具塞锥形瓶中,精密称定,密封超声40 min后补足减失的质量,滤过后精密移取续滤液10 mL,水浴蒸干,甲醇复溶并定容于10 mL量瓶中,摇匀,0.22 μm微孔滤膜滤过,即得供试品溶液。
2.2.4 阴性对照溶液的制备 按“2.2.3”项方法制得不含甘草-马钱子配伍沉淀相态的阴性对照溶液。
2.3 方法学考察
2.3.1 专属性实验 按“2.1”项下色谱条件,取对照品溶液、供试品溶液、阴性对照溶液,进样测定,考察马钱子碱、士的宁、甘草酸、甘草苷、异甘草苷、异甘草素检测的专属性。结果在上述色谱条件下,通过与对照品保留时间和UV图谱的对照,确定色谱峰1~6,分别对应马钱子碱、士的宁、甘草苷、异甘草苷、异甘草素、甘草酸6个指标性成分;测试溶液和参比溶液保留时间相同,在相同位置处无干扰峰,专属性良好。根据甘草苷的峰面积计算,分离度≥1.5,理论塔板数≥4000,均符合要求。色谱图见图1。
2.3.2 线性关系考察 分别精密吸取“2.2”项下混合对照品溶液各0.1、0.2、0.5、1.0、1.5、2.0 mL置2 mL量瓶中,甲醇定容,得6个系列质量浓度的对照品溶液。按“2.1”项下色谱条件测定。以进样浓度为横坐标(),峰面积为纵坐标()进行线性回归,得到各成分的回归方程分别为马钱子碱=0.238 5+0.033 2,2=0.999 8,线性范围13.80~276.00 μg/mL;士的宁=0.232 9+0.519 9,2=0.999 7,线性范围12.25~245.00 μg/mL;甘草苷=0.089 8-0.016 5,2=0.999 7,线性范围9.65~193.00 μg/mL;异甘草苷=0.102 1-0.071 8,2=0.999 8,线性范围14.50~290.00 μg/mL;异甘草素=0.169 9+0.016 4,2=0.999 6,线性范围2.05~41.00 μg/mL;甘草酸=0.097 4-0.012 7,2=0.999 8,线性范围11.10~222.00 μg/mL。
2.3.3 精密度实验 精密吸取“2.2.2”项下混合对照品溶液10 µL,按“2.1”项下色谱条件,连续进样6次,测定其峰面积。通过精密度实验,测得马钱子碱、士的宁、甘草苷、异甘草苷、异甘草素、甘草酸各成分的峰面积,其RSD分别为0.31%、0.22%、0.37%、0.25%、0.40%、0.38%,RSD均小于3%,表明该方法精密度良好。
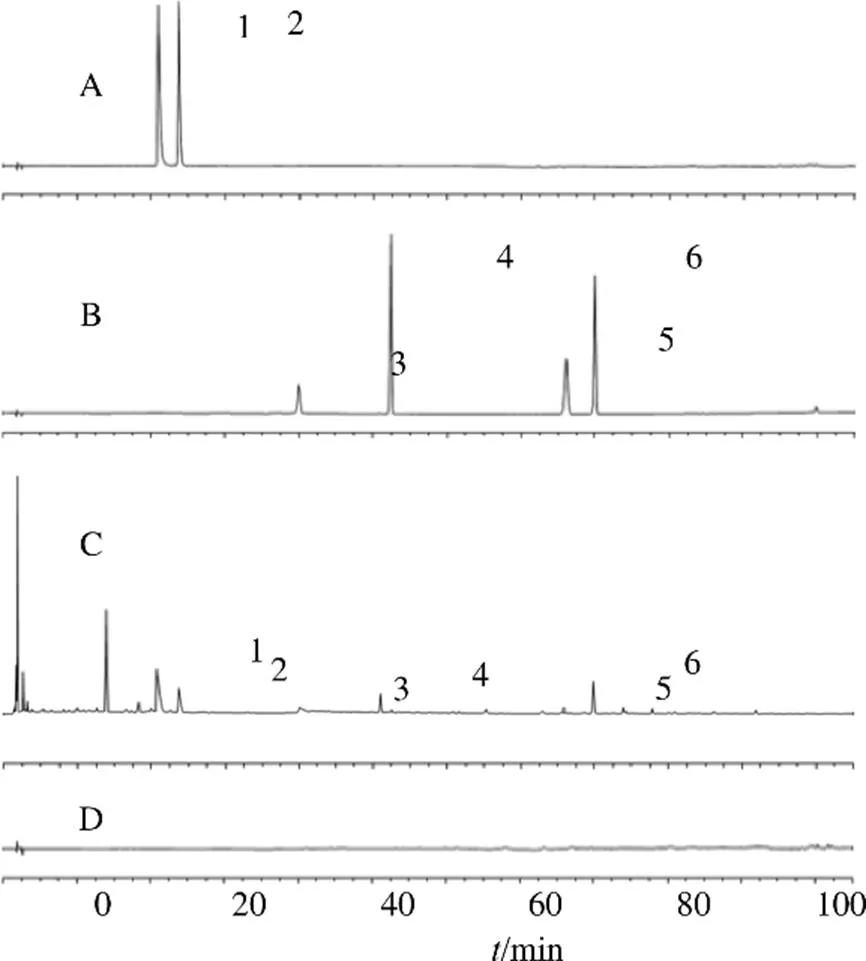
1-马钱子碱 2-士的宁 3-甘草苷 4-异甘草苷 5-异甘草素 6-甘草酸
2.3.4 检测限与定量限 在最优的色谱条件下,当信噪比为10时为定量限;逐步稀释各对照品溶液至信噪比为3∶1,得到各成分的检测限。结果显示马钱子碱、士的宁、甘草苷、异甘草苷、异甘草素和甘草酸的检测限分别为2.48、2.21、3.18、2.90、0.50、2.64 μg/mL;定量限分别为8.28、7.35、7.72、9.67、1.64、8.80 μg/mL。
2.3.5 重复性试验 按“2.2.3”项下平行制备供试品溶液6份,按“2.1”项下色谱条件测定,计算各成分含量差异。测得马钱子碱、士的宁、甘草苷、异甘草苷、异甘草素、甘草酸的RSD分别为0.23%、0.18%、0.19%、0.25%、1.24%、0.59%,RSD均小于3%,表明该方法重复性良好。
2.3.6 加样回收率实验 取已知含量的甘草-马钱子配伍样品6份,每份0.25 g,精密称定,分别加入高、中、低3种个质量浓度的各对照品溶液,按“2.2.3”项下方法制备供试品溶液,按“2.1”项下的色谱条件测定,计算加样回收率。结果马钱子碱、士的宁、甘草苷、异甘草苷、异甘草素、甘草酸的平均加样回收率分别为100.08%、99.85%、100.38%、100.94%、99.77%、99.58%,RSD分别为1.68%、2.03%、1.54%、1.72%、2.09%、1.89%,表明该方法的加样回收率良好。
2.3.7 稳定性试验 取甘草-马钱子配伍沉淀相态蒸馏水、人工胃液、人工肠液样品,按“2.2.3”项下方法制备供试品溶液,按“2.1”项下色谱条件,分别于0、2、4、6、8、12、24 h进样测定马钱子碱、士的宁、甘草酸、甘草苷、异甘草苷、异甘草素的峰面积。结果释放介质为蒸馏水时,马钱子碱、士的宁、甘草苷、异甘草苷、异甘草素、甘草酸的RSD分别为1.04%、1.36%、2.10%、1.25%、2.23%、1.71%;释放介质为人工胃液时,马钱子碱、士的宁、甘草苷、异甘草苷、异甘草素、甘草酸的RSD分别为1.10%、2.02%、1.73%、1.04%、2.35%、1.48%;释放介质为人工肠液时,马钱子碱、士的宁、甘草苷、异甘草苷、异甘草素、甘草酸的RSD分别为1.59%、1.17%、2.11%、1.57%、2.63%、1.71%,表明供试品溶液在蒸馏水、人工胃液、人工肠液中24 h内具有良好的稳定性。
2.3.8 数据处理 采用SPSS 22.0软件进行统计学数据分析,计算RSD值,并进行分析检验。
2.4 释放度测定
按《中国药典》2020年版,量取经脱气处理的水、人工胃液和人工肠液各500 mL注入每个操作容器,调节温度使其保持在(37.0±0.5)℃。称取沉积相态约2.0 g各3份,精密称定,分别投入含有水、人工胃液、人工肠液的容器中,调整转速100 r/min,分别在0.5、1.0、2.0、4.0 h从容器中吸取样液2 mL,同时相同介质补足,0.22 μm滤膜,取续滤液,备用。按选定的方法测定,以沉积相态中马钱子碱、士的宁、甘草酸、甘草苷、异甘草苷、异甘草素成分的含量所含总量为100%,计算累积释放率,并绘制释放曲线,拟合释放动力学模型。沉淀相态在蒸馏水、人工胃液和人工肠液为释放介质的累积释放率,绘制释放曲线,结果见图2。
2.5 体外释药模型的拟合
采用Origin软件将指标性成分累积释药结果分别按零级动力学模型、一级动力学模型、Higuchi模型、Ritger-Peppas模型进行模型拟合,得到相关模型方程及相关系数(2),拟合优度以2进行判断。在蒸馏水、人工胃液和人工肠液体外释药模型最佳拟合结果见表1,马钱子碱、甘草苷、异甘草苷、异甘草素和甘草酸与一级动力学模型拟合结果最佳,士的宁与Higuchi模型拟合结果最佳。
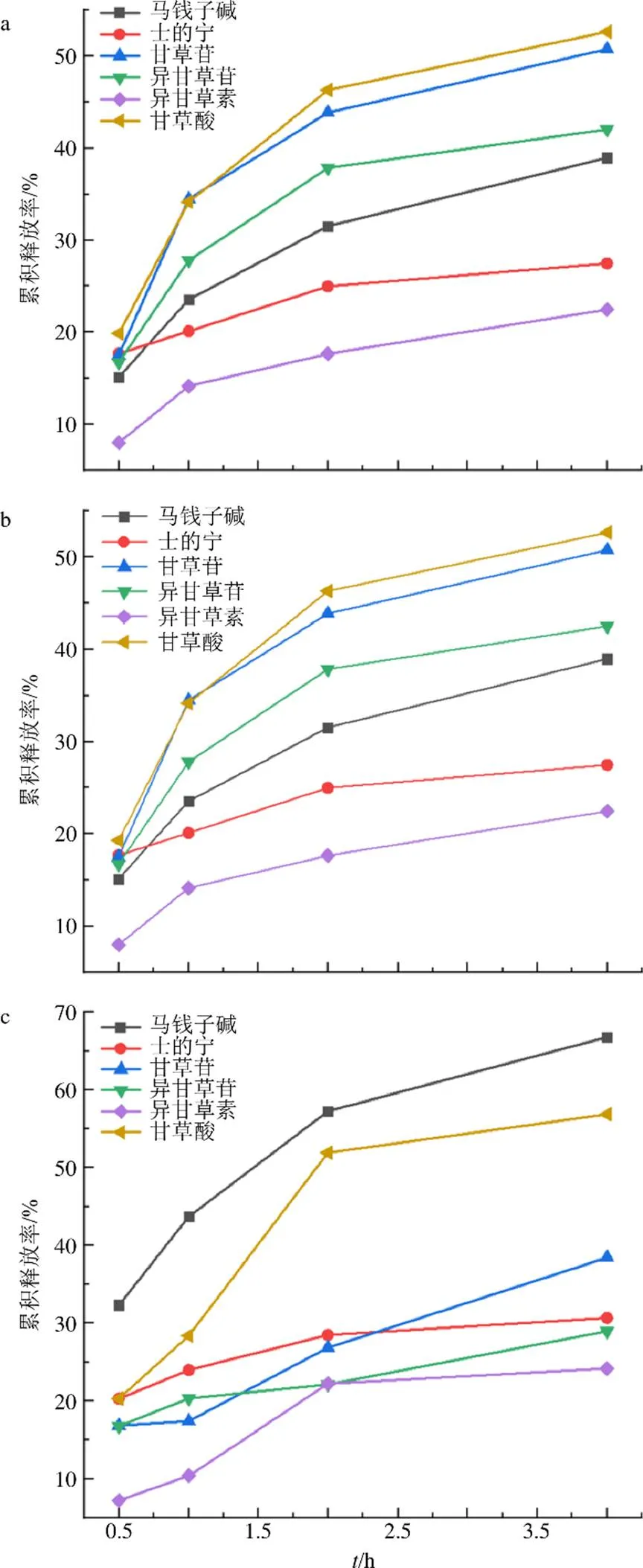
图2 分别以水(a)、人工胃液(b)、人工肠液(c)为溶出介质的释放曲线
3 讨论
中药群药合煎过程中会产生大量沉淀,即使过滤,澄清的药液静置后还会集结成肉眼可见的混悬形态,这些混悬的“药渣”对全方是否可产生增效、减毒或改性等多种药理作用,尚无科学的论断。本实验以甘草-马钱子药对为例,在前期研究工作基础上,将中药在煎煮静置后出现的大量沉积物定义为沉淀相态。经研究发现沉淀相态中聚集了甘草-马钱子合煎液中大多数的毒(效)物质,进一步对甘草-马钱子配伍沉淀相态的释放行为的研究,可为揭示二者配伍减毒增效规律研究提供基础数据。本实验采用HPLC法测定甘草-马钱子配伍沉淀相态中各物质在不同溶出介质中的释放情况。研究表明,马钱子中毒(效)成分马钱子碱和士的宁在人工胃液、人工肠液中的释放量均高于蒸馏水中,且在人工肠液中的释放量最高,原因可能在于马钱子碱和士的宁均为脂溶性生物碱,弱碱类药物通过肠上皮吸收服从pH分配学说,推测沉积相态在释放过程中,马钱子碱和士的宁为咔唑类生物碱,在弱碱性或弱酸性环境中分子之间的作用力降低,易于在人工肠液和人工胃液中释放;甘草苷、异甘草苷为黄酮类化合物,在蒸馏水和人工胃液中的释放相近,均大于人工肠液;异甘草素在人工胃液中释放量最高,而在蒸馏水和人工肠液的释放量相近,这与报道中甘草苷、异甘草苷、异甘草素等在人工肠液中释放较少相一致;甘草酸为三萜皂苷,在人工胃液中的释放量最低,而在水和人工肠液中释放量较高,推测甘草酸结构中具有羧基且呈酸性,在酸性环境中不易解离。

表1 6种指标成分在蒸馏水、人工肠液和人工胃液中最佳拟合结果
药物的吸收以小肠吸收为主,经体外释放研究发现,甘草酸、马钱子碱以及士的宁在人工肠液中的的释放量较大,且马钱子碱释放量>甘草酸释放量>士的宁释放量,可见毒性最强的士的宁释放最慢。由模型拟合结果可知,士的宁释放行为与Higuchi模型拟合结果最佳,呈现出难溶性骨架材料缓释制剂的释放特性,推测沉积相态由于其自身固有溶解特性,毒(效)成分士的宁以沉积共聚体形式存在,在体释放呈缓释行为,这也与课题组前期研究发现甘草-马钱子共煎过程中产生大量絮状沉淀的现象相一致。
另有学者[17]研究发现含有黄酮类与生物碱类中药的经典方剂在煎煮过程中沉淀明显,如四逆汤、麻黄附子甘草汤中的甘草苷、甘草酸等可与附子中的生物碱可结合成难溶盐;同时,甘草次酸与附子中生物碱形成分子络合物,使有毒成分在体内缓慢释放;进一步研究发现附子中毒性生物碱被与甘草成分复合沉积的机制在于生物碱中叔胺N与甘草中羧酸C=O发生缔合,避免了机体在短时间内吸收过量生物碱而引起的毒性反应[18]。由此推测,甘草-马钱子配伍时,其所含的黄酮类成分与生物碱同样可能发生沉积聚合,形成沉淀相态;由于甘草中羧酸的C=O和马钱子中生物碱的N相结合,分子间的作用力增加,可形成类似超分子的沉积共聚物,从而降低毒效成分的释放速率,实现减毒作用。该结果也与甘草配伍雷公藤[19-20]减毒机制相类似。
本研究基于汤液微观物质基础角度,对甘草-马钱子配伍汤剂相态中关键相态沉积相态进行了体外释放评价,探讨配伍汤液沉积相态释放行为,从而为合理阐释甘草与马钱子配伍毒减而效存提供科学依据。
利益冲突 所有作者均声明不存在利益冲突
[1] 魏旭雅, 邱子栋, 陈金龙, 等.有毒乌头类中药炮制与配伍减毒机制的研究进展 [J].中国中药杂志, 2019, 44(17): 3695-3704.
[2] 卢志强, 张艳军, 庄朋伟, 等.附子对急性心力衰竭大鼠血流动力学影响及其机制研究 [J].中草药, 2015, 46(21): 3223-3227.
[3] Jiang Y, Qin L, Lu A J,.CYP3A1 metabolism-based neurotoxicity of strychnine in rat [J]., 2022, 471: 153156.
[4] 陆燕华, 高宁阳.马钱子药理作用及减毒增效方法研究进展 [J].上海中医药杂志, 2019, 53(5): 93-97.
[5] 赵引利, 何燕宁, 杨宇杰, 等.马钱子及其制剂药动学研究进展 [J].中草药, 2015, 46(11): 1710-1714.
[6] 过振华, 马红梅, 张伯礼.马钱子药理毒理研究回顾及安全性研究展望 [J].中西医结合学报, 2008, 6(6): 645-649.
[7] 黄弈涵, 朱姝, 李俊圻, 等.有毒中药减毒方法探究[J].中药材, 2021(8): 2028-2031.
[8] 章津铭.基于毒(效)组分“体外沉积、体内缓释”环节的附子-甘草配伍减毒作用机制研究 [D].成都: 成都中医药大学, 2012.
[9] Ramzan M, Gourion-Arsiquaud S, Hussain A,.release,penetration, anddermatokinetics of ketoconazole-loaded solid lipid nanoparticles for topical delivery [J]., 2022, doi: 10.1007/S13346-021-01058-6.
[10] 唐敏, 伍冠一, 朱婵, 等.马钱子碱镇痛研究进展 [J].中草药, 2014, 45(12): 1791-1795.
[11] 屈艳格, 陈军, 王冬月, 等.马钱子生物碱类成分经口给药后在大鼠体内的药动学研究 [J].中草药, 2013, 44(8): 1008-1012.
[12] 曹玉洁.大黄-甘草药对组方配伍效应与物质基础研究 [D].南京: 南京中医药大学, 2018.
[13] 天津市北辰区中医医院.雷公藤配伍甘草、白芍、莱菔子等解毒中药其特征成分含量变化的研究[Z].李连瑞, 王会杰, 赵琳, 于军, 刘婕, 周士亮, 陈志勇, 冯志新.国家科技成果.2017-12-12.
[14] 陈秋薇.“化学成分-汤液相态-毒效作用”联合分析附子配伍甘草增效解毒作用 [D].成都: 成都中医药大学, 2014.
[15] 郭玉岩, 马文保, 肖洪彬, 等.基于UPLC-MS技术分析马钱子-甘草药对配伍汤液不同相态中毒效物质的变化规律 [J].中草药, 2017, 48(23): 4880-4884.
[16] Guo Y Y, Gao T, Li C C,.Detoxification mechanisms of a combination ofand: A comparative analyses of differences in toxicokinetics and tissue distribution after oral administration of-decoction [J]., 2022, 36: e5321.
[17] 章津铭, 傅超美, 何宇新, 等.附子-甘草配伍前后汤液中沉积物的化学组分对比研究 [J].中草药, 2013, 44(2): 165-169.
[18] Zhang C Z, Zhao R, Yan W Q,.Compositions, formation mechanism, and neuroprotective effect of compound precipitation from the traditional Chinese prescription Huang-Lian-Jie-Du-Tang [J]., 2016, 21(8): 1094.
[19] 王焕君, 马致洁, 董捷鸣, 等.雷公藤配伍甘草减毒大鼠体内尿液中的小分子代谢物以及相应生物代谢通路 [J].世界中医药, 2020, 15(8): 1102-1107.
[20] 李涯松, 杨洁红, 樊守艳, 等.甘草酸对雷公藤多甙治疗类风湿性关节炎增效减毒作用的实验研究 [J].中国中医药科技, 2008, 15(4): 293.
Release characteristics of principal components of acid-base drug pairetcompatibility decoction in sedimentary phase
GUO Yu-yan, GAO Tao, LI Chun-cheng, WEI Yu-xin, SHAO Shuang, SUN Shuang, YANG Da-yu,LYU Shao-wa
Key Laboratory of Basic and Application Research of Beiyao, Ministry of Education, Heilongjiang University of Chinese Medicine, Harbin 150040, China
To investigate the release behavior of the sedimentary phase of the Gancao (et, GRR)-Maqianzi (, SS) compatibility decoction, and provide scientific reference for the toxicity reduction of GRR-SS compatibility.HPLC was used for quantitative detection of effective substances and toxic substances, andmodel release experiment was used to trace the release characteristics of representative components in different media such as distilled water, artificial gastric juice, artificial intestinal juice, and the release results were fitted and analyzed.The release amount of glycyrrhizic acid, strychnine and brucine in artificial intestinal fluid was large, with the sequence of brucine > glycyrrhizic acid > strychnine.Brucine and glycyrrhizic acid were best fitted to the first-order kinetic model, strychnine had the best fitting results with Higuchi model.The main toxic and effective components in the sedimentary phase of GRR-SS show the release characteristics of slow-release preparations of poorly soluble matrix materials, and the toxic components exist in the form of sedimentary copolymer, which show sustained-release behavior with reduce toxicity.At the same time, the release of glycyrrhizin plays a synergistic role in reducing toxicity and increasing efficiency.
acid-base drug pairs;et;; compatibility soup; release; sedimentary phase states; attenuation
R283.6
A
0253 - 2670(2022)10 - 3000 - 06
10.7501/j.issn.0253-2670.2022.10.009
2021-11-26
国家自然科学基金资助项目(82173997);国家自然科学基金资助项目(81703724);黑龙江省博士后科研启动金项目;黑龙江省“头雁”团队;黑龙江中医药大学健康产业专项课题(jkcy04)
郭玉岩(1982—),博士,副教授,从事中药新药开发研究。Tel: 13845046561 E-mail: guoyuyan622@163.com
通信作者:吕邵娃,教授,硕士生导师,主要研究方向为中药及复方的药效物质基础研究。Tel: (0451)87266916 E-mail: 1031892056@qq.com
[责任编辑 郑礼胜]
