椎体强化结合椎旁神经阻滞治疗椎体压缩骨折远处疼痛的效果
2022-05-08史贵训孙伟东王丹锋杨传军郑新峰陈增焕
史贵训 孙伟东 王丹锋 杨传军 郑新峰 陈增焕
脊柱胸腰段是骨质疏松性骨折最常发生的部位。近年来,医院接收的骨质疏松椎体压缩性骨折[1](osteoporotic vertebral compression fractures,OVCFs)患者越来越多。临床中发现,OVCFs引起的疼痛并不局限于骨折椎体部位,在臀部、骶尾、胸前等远离病变椎体的部位也常有明显的疼痛症状,即责任椎远处疼痛[2],发生率较高,给患者带来较大的痛苦,但具体的发生机制仍不明确。经皮椎体成形术(percutaneous vertebroplasty,PVP)是一项已经成熟的微创脊柱外科技术,在OVCFs治疗中被广泛应用,具有创伤小、疗效快、可持续等优势[3]。然而,仍有部分患者PVP术后疼痛缓解并不理想,尤其是术前存在远离骨折部位疼痛的患者[4]。有报道,使用选择性神经根阻滞术治疗OVCFs的疼痛,可以弥补部分PVP疼痛缓解的不足[5]。该研究旨在探讨椎体强化结合局部神经阻滞对椎体压缩骨折患者远处疼痛的治疗效果,现报道如下。
1 资料与方法
1.1 临床资料 选取2019年2月至2021年2月在本院住院行PVP手术治疗的OVCFs患者100例。(1)纳入标准[6]:①骨质疏松性椎体新鲜性压缩骨折,术前经X线、磁共振、CT影像学检查确诊;②患者椎体骨密度在骨质疏松诊断标准范围内;③年龄>60岁;④远端疼痛,疼痛VAS评分>5分,保守治疗不理想,难以耐受长时间卧床者;⑤签署知情同意书。(2)排除标准[7]:①存在PVP手术治疗禁忌证,如三柱骨折、脊柱感染等;②长期口服镇痛药物及糖皮质激素等类药物者;③患有神经根综合征、脊髓压迫综合征等疾病者;④心、肝、肾等重要脏器功能障碍者。根据治疗方法的不同分为观察组和对照组,每组各50例。两组的基线资料比较,差异均无统计学意义(P均>0.05),见表1。本研究经医院伦理委员会批准,所有患者签署知情同意书。
表1 两组的基线资料比较[n=50,(±s)]
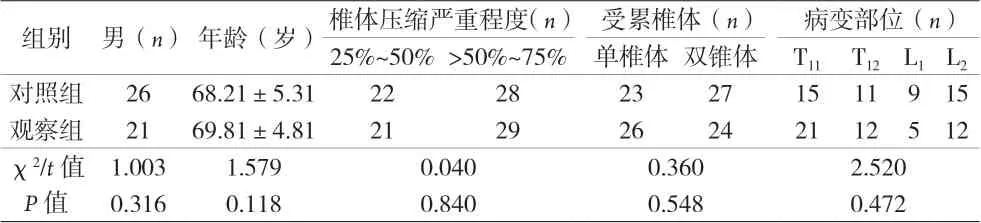
表1 两组的基线资料比较[n=50,(±s)]
组别 男(n)年龄(岁)椎体压缩严重程度(n) 受累椎体(n) 病变部位(n)25%~50%>50%~75% 单椎体 双锥体 T11 T12L1L2对照组 26 68.21±5.31 22 28 23 27 15 11 9 15观察组 21 69.81±4.81 21 29 26 24 21 12 5 12 χ2/t值 1.003 1.579 0.040 0.360 2.520 P值 0.316 0.118 0.840 0.548 0.472
1.2 治疗方法 (1)对照组:仅使用PVP治疗。患者俯卧,手术区域消毒铺巾;术中准备,C臂透视确定手术节段、双侧椎弓根体表投影,确定进针点;1.0%利多卡因5 mL,局部浸润麻醉;3.2 mm的穿刺针双侧经皮穿刺,正位接近椎弓根内缘时,侧位像针尖达椎体后缘,继续穿针至椎体前1/4-1/3处;调制骨水泥在拉丝后期,C臂透视下注入骨水泥,边注射边观察,每个椎体注射4~6 mL,骨水泥弥散至椎体边缘部位时,立即停止。(2)观察组:在PVP治疗的基础上联合采用椎旁神经阻滞。患者取侧卧位,超声探头平行置于病变椎体棘突中线旁2.5 cm处,视野内可见横突及壁层胸膜,穿刺针于超声探头1 cm处刺入椎旁间隙,确保针体处于视野内,对进针方向予以细微调整,从而避开横突至壁层胸膜,在双侧椎旁间隙进行阻滞,注射0.5%罗哌卡因5 mL。
1.3 观察指标 (1)视觉模拟评分法(VAS)评估两组患者在术前及术后1周、1个月、3个月、6个月静息及活动状态下的疼痛程度,总分为10分,评分越高则提示患者疼痛程度越严重。(2)Oswestry功能障碍指数(ODI)量表[8]评估两组患者术前及术后1周、1个月、3个月、6个月时的腰椎活动功能量,各个项目总分为50,评分越高则提示患者功能障碍越严重。(3)采用日常生活能力法(acitivities of daily living,ADL)[9]评估两组患者在术前及术后1周、1个月、3个月、6个月的生活能力水平,5分制,得分越高则提示病痛影响越大。(4)采用SF-12量表[10]评估两组患者术前术后的躯体功能、躯体角色、疼痛、健康状况、活力、社会功能、情绪和心理卫生等生活质量指标,每个维度评分为1~5分,总评分40分,评分越高则提示生活质量越佳。
1.4 统计学方法 采用SPSS20.0统计软件。计量资料符合正态分布以(±s)表示,组间比较采用t检验。以P<0.05为差异有统计学意义。
2 结果
2.1 不同时间点静息及活动状态下两组的VAS评分比较 术后1周、1个月、3个月、6个月,两组患者静息及活动状态下的VAS评分均明显低于术前,且观察组患者静息及活动状态下的VAS评分均明显低于对照组(P均<0.05)。见表2。
表2 不同时间点静息及活动状态下两组的VAS评分比较[分,(±s)]
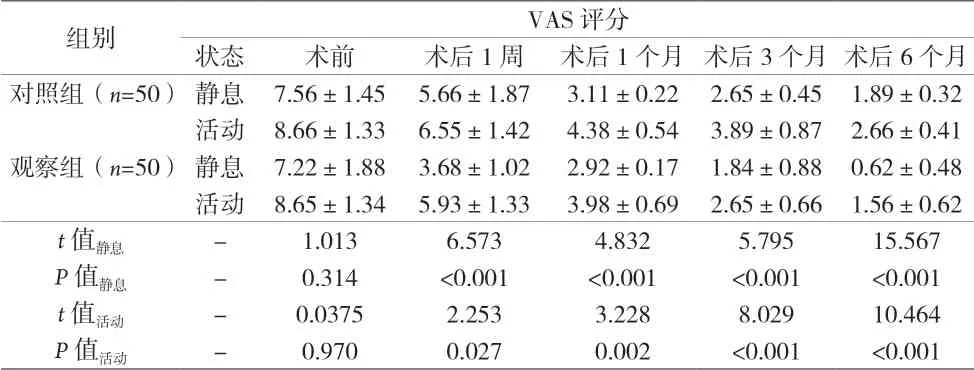
表2 不同时间点静息及活动状态下两组的VAS评分比较[分,(±s)]
组别 VAS评分状态 术前 术后1周 术后1个月 术后3个月 术后6个月对照组(n=50)静息 7.56±1.45 5.66±1.87 3.11±0.22 2.65±0.45 1.89±0.32活动 8.66±1.33 6.55±1.42 4.38±0.54 3.89±0.87 2.66±0.41观察组(n=50)静息 7.22±1.88 3.68±1.02 2.92±0.17 1.84±0.88 0.62±0.48活动 8.65±1.34 5.93±1.33 3.98±0.69 2.65±0.66 1.56±0.62 t值静息 - 1.013 6.573 4.832 5.795 15.567 P值静息 - 0.314 <0.001 <0.001 <0.001 <0.001 t值活动 - 0.0375 2.253 3.228 8.029 10.464 P值活动 - 0.970 0.027 0.002 <0.001 <0.001
2.2 不同时间点两组的ODI评分比较 术后1周、1个月、3个月、6个月,两组患者ODI评分均明显低于术前,且观察组患者ODI评分均明显低于对照组(P均<0.05)。见表3。
表3 不同时间点两组的ODI评分比较[分,(±s)]
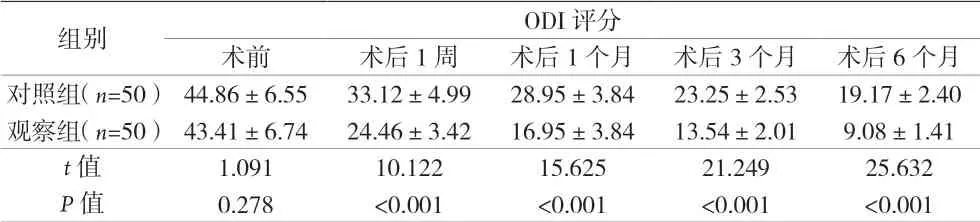
表3 不同时间点两组的ODI评分比较[分,(±s)]
组别 ODI评分术前 术后1周 术后1个月 术后3个月 术后6个月对照组(n=50)44.86±6.55 33.12±4.99 28.95±3.84 23.25±2.53 19.17±2.40观察组(n=50)43.41±6.74 24.46±3.42 16.95±3.84 13.54±2.01 9.08±1.41 t值 1.091 10.122 15.625 21.249 25.632 P值 0.278 <0.001 <0.001 <0.001 <0.001
2.3 不同时间点两组的ADL评分比较 术后1周、1个月3个月、6个月时,两组患者ADL评分均明显低于术前,且观察组患者ADL评分均明显低于对照组(P均<0.05)。见表3。
表3 不同时间点两组的ADL评分比较[分,(±s)]
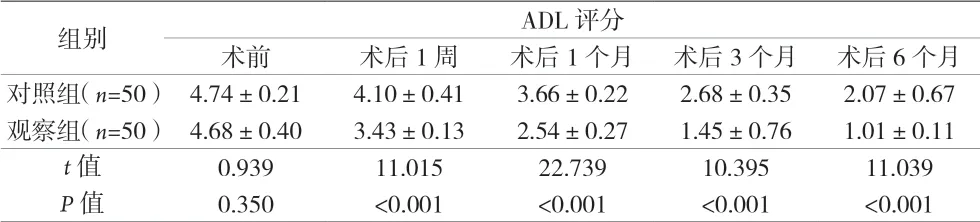
表3 不同时间点两组的ADL评分比较[分,(±s)]
组别 ADL评分术前 术后1周 术后1个月 术后3个月 术后6个月对照组(n=50) 4.74±0.21 4.10±0.41 3.66±0.22 2.68±0.35 2.07±0.67观察组(n=50) 4.68±0.40 3.43±0.13 2.54±0.27 1.45±0.76 1.01±0.11 t值 0.939 11.015 22.739 10.395 11.039 P值 0.350 <0.001 <0.001 <0.001 <0.001
2.4 治疗前后两组的SF-12量表评分比较 术后两组患者SF-12量表中8个维度的评分均明显低于术前,且观察组的SF-12量表评分均明显低于对照组(P均<0.05)。见表4。
表4 治疗前后两组的SF-12量表评分比较[分,(±s)]
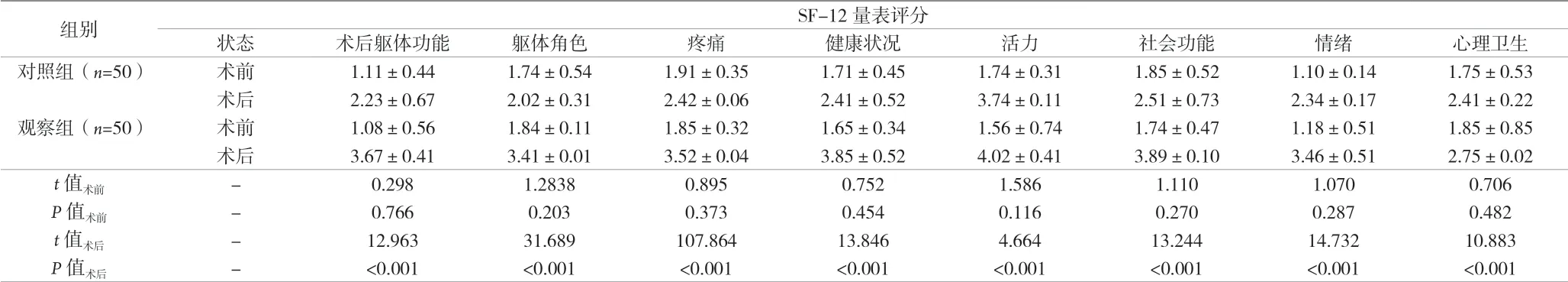
表4 治疗前后两组的SF-12量表评分比较[分,(±s)]
组别 SF-12量表评分状态 术后躯体功能 躯体角色 疼痛 健康状况 活力 社会功能 情绪 心理卫生对照组(n=50) 术前 1.11±0.44 1.74±0.54 1.91±0.35 1.71±0.45 1.74±0.31 1.85±0.52 1.10±0.14 1.75±0.53术后 2.23±0.67 2.02±0.31 2.42±0.06 2.41±0.52 3.74±0.11 2.51±0.73 2.34±0.17 2.41±0.22观察组(n=50) 术前 1.08±0.56 1.84±0.11 1.85±0.32 1.65±0.34 1.56±0.74 1.74±0.47 1.18±0.51 1.85±0.85术后 3.67±0.41 3.41±0.01 3.52±0.04 3.85±0.52 4.02±0.41 3.89±0.10 3.46±0.51 2.75±0.02 t值术前 - 0.298 1.2838 0.895 0.752 1.586 1.110 1.070 0.706 P值术前 - 0.766 0.203 0.373 0.454 0.116 0.270 0.287 0.482 t值术后 - 12.963 31.689 107.864 13.846 4.664 13.244 14.732 10.883 P值术后 - <0.001 <0.001 <0.001 <0.001 <0.001 <0.001 <0.001 <0.001
3 讨论
临床上,胸腰椎OVCFs责任椎引起的疼痛并不局限于骨折椎体部位,常有远离责任椎部位的疼痛症状,如下腰部、臀部、骶尾部,甚至在胸腹部、季肋部及腹股沟区也有放射性疼痛,称之为责任椎远处疼痛[11],也是OVCFs的重要疼痛特点,需要引起重视。临床研究总结,责任椎远处疼痛表现比较弥散、模糊,患者自述多为身体多处、大面积疼痛无法确定具体的位置,呈牵涉痛表现,给患者带来很大的困扰,甚至为解决责任椎远处疼痛作为求医主诉。此外,该病还具有不按躯体感觉神经皮节分布的特点,影像学检查无法得出神经压迫的结论,原理上难以用神经放射痛来解释,给临床医生的诊断和治疗也带来较多的困惑。OVCFs远处疼痛的研究历史很长[12],主流观点认为这种疼痛是由于交感神经传入纤维引起的椎体源性牵涉痛,但仍需要进一步的神经解剖、电生理相关研究证实。另外,其发生还可能与骨折后脊神经根后支受到损伤或刺激有关,还有人认为是肌肉痉挛引起的肌源性疼痛[13]。
椎体强化术即PVP,作为一项临床广泛适用的微创技术,自1994年始用于治疗OVCFs,具有创伤小、恢复快、疗效确切持久等特点[14],不仅可以快速强化骨折椎体,缓解骨折椎体局部的疼痛,改善脊柱功能,还可以迅速缓解椎体骨折导致的责任椎远处疼痛[15]。但是,临床上仍有一部分病例在PVP术后,患者远处部位的疼痛症状不能完全缓解,长期影响患者的活动功能,延长康复周期[16]。研究表明,神经阻滞术可以治疗由神经根炎性刺激诱发的腰腿疼痛和骨质疏松引起的椎体压缩性骨折疼痛,肽能神经和去甲肾上腺素能神经在椎体的骨髓和骨膜中尤为丰富[17]。椎旁神经阻滞可以通过麻醉药物阻断神经的痛觉传导通路,治疗多种腰椎急慢性疼痛,但目前采取椎旁神经阻滞治疗OVCFs相关疼痛的研究报道较少。该研究对接受PVP治疗的患者是否接受椎旁神经阻滞分为对照组和观察组,与仅接受PVP治疗的患者比较,PVP结合局部椎旁神经阻滞治疗患者的VAS评分明显降低、ODI指数明显改善,且并未增加相关并发症发生率,表明接受椎体强化结合局部神经阻滞的椎体压缩骨折患者远处疼痛程度、功能障碍程度和生活质量改善程度均高于仅接受PVP治疗的患者。
综上所述,椎体强化PVP手术结合椎旁神经阻滞治疗OVCFs远处部位疼痛的效果确切,且安全方便。但临床中部分具备PVP手术指征的患者因各种原因会选择拒绝手术治疗,而仅采取椎旁神经阻滞治疗,与该研究中两组比较效果如何,未能进行探讨,是本研究的不足之处。
