HPLC-MS/MS法检测人血中舒芬太尼及代谢物
2022-04-11吕惊晗辛国斌孟令宗石辉丽
吕惊晗,辛国斌,孟令宗,石辉丽
(1. 法庭毒物分析公安部重点实验室,北京 100192;2. 青岛市公安局刑警支队技术处,山东 青岛 266001;3. 临沂大学,山东 临沂 276012)
舒芬太尼(sufentanil)是芬太尼的一种衍生产物,其结构是在芬太尼的4位上引入极性基团N-4取代衍生物[1],镇痛强度是芬太尼的5~10倍,属于强效的阿片类镇痛药物,其作用对象是μ阿片受体[2],具有起效快、药效强、副作用小的特点,因此广泛用于各科手术和术后镇痛[3]。近年来芬太尼类物质已逐渐成为一种新的毒品,滥用或过量致死的案例也时有报道[4],目前国内已有生物检材中舒芬太尼的气相色谱-质谱法[5]和液相色谱-质谱法[6-7]等检测方法的报道,但均存在需浓缩或衍生化[8]、操作复杂等问题,且少有同时检测其代谢产物的报道[9]。为此,本实验建立了高效液相色谱-串联质谱法同时检测人血中舒芬太尼及代谢物去甲舒芬太尼的分析方法,该方法全面、快速、简便、准确、稳定。
1 材料与方法
1.1 仪器与试剂
Qtrap5500质谱仪配备电喷雾电离源(美国AB公司),LC30A超高压液相色谱仪(日本岛津公司)。
舒芬太尼(0.1 mg/mL甲醇液,纯度:99.7%)、去甲舒芬太尼(0.1 mg/mL甲醇液,纯度:95%),舒芬太尼-D5(0.1 mg/mL甲醇液,纯度:99.8%),均购自美国Cerilliant公司;甲醇(德国Merck)、甲酸(≥98%,上海阿拉丁)、甲酸铵(德国Sigma)均为色谱纯;枸橼酸舒芬太尼注射液(1 mL∶50 μg,宜昌人福药业);空白全血(血站提供);实验用水为超纯水;涡旋振荡器、高速离心机、0.22 μm尼龙微孔滤膜等。
1.2 标准储备液的配制
取舒芬太尼和去甲舒芬太尼标准品溶液(0.1 mg/mL)适量,用甲醇配制成质量浓度为100 ng/mL的混合标准储备液;取舒芬太尼-D5标准品溶液(0.1 mg/mL)适量,用甲醇稀释成质量浓度为100 ng/mL的内标标准储备液。-20 ℃保存,实验中根据需要添加或稀释该储备液至测定所需的浓度。
1.3 样本处理
取0.5 mL血样,加入1 mL乙腈,涡旋振荡5 min,高速离心(12 000 r/min)5 min,取上清液过0.22 μm滤膜,待分析。
1.4 分析条件
1.4.1 色谱条件
色谱 柱 为Kinetex C18(100 mm×2.1 mm×2.6 μm,美国Phenomenex公司)液相色谱柱,柱温40 ℃,流速0.3 mL/min,进样量5 μL,流动相A为5 mmol/L甲酸铵和0.1%甲酸的水溶液,流动相B为甲醇,流动相梯度洗脱程序见表1。

表1 流动相梯度洗脱程序Table 1 Gradient elution setup for mobile phase
1.4.2 质谱条件
电喷雾离子源(ESI),正离子扫描,检测模式为多反应监测;碰撞气为氮气;气帘气(CUR)为30 psi,喷撞气(CAD)为Medium,离子化电压(IS)为5 500 V,温度(TEM)为550 ℃,喷雾气(GS1)为60 psi,辅助加热气(GS2)为60 psi,碰撞室入口电压(EP)为10 V,碰撞室出口电压(CXP)为12 V;定性及定量离子对、去簇电压(DP)、碰撞电压(CE)见表2。
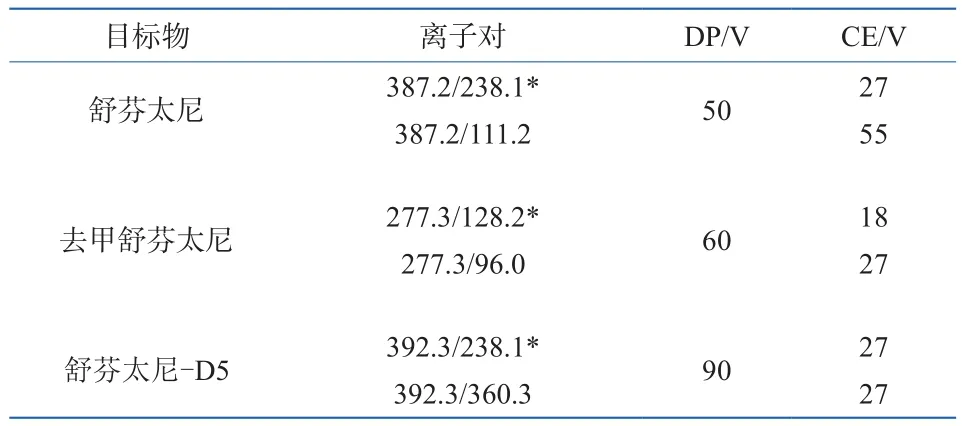
表2 定性/定量离子对、去簇电压(DP)、碰撞能量(CE)Table 2 Qualitative/quantitative ion pair, de-clustering voltage(DP) and collision energy (CE)
2 结果与讨论
2.1 方法学考察
2.1.1 专属性
准备8份不同人的空白血,取其中1份空白血加混合标准储备液及内标标准储备液适量,并将其全部按1.3项处理, 在本试验的条件下进行分析,考察分离度及空白血对目标物的干扰。提取离子色谱图见图1。可见舒芬太尼、去甲舒芬太尼和内标物舒芬太尼-D5峰形良好,分离完全,不受血浆内源性物质干扰,舒芬太尼与舒芬太尼-D5保留时间一致,它们和去甲舒芬太尼的保留时间分别为4.38、3.96 min。
2.1.2 标准曲线、线性范围及检出限
取空白血分别加入混合标准储备液适量,配制成0.1、0.2、0.5、1、2、5、10、15、20 ng/mL 的系列浓度样本,再加入内标标准储备液使内标添加浓度均为2 ng/mL,按1.3项处理后进样。另取空白血加混合标准储备液适量,配制成0.2、0.1、0.05、0.02 ng/mL的低浓度混标添加样本,按1.3项处理后进样,考察检出限。
分析系列浓度的添加样本,以标准品及其内标物定量离子峰面积之比作为纵坐标,标准溶液浓度为横坐标绘图,绘制内标标准工作曲线,经“1/x”权重得到舒芬太尼线性回归方程为:y=0.566 3x+0.004 34,R2=0.999 84,去甲舒芬太尼线性回归方程为:y=0.448 74x-0.005 1,R2=0.999 73,线性范围均为0.1~20 ng/mL。通过分析低浓度混标添加样本,以信噪比(S/N)≥3的添加浓度作为检出限,信噪比(S/N)≥10的添加浓度作为定量限,测得检出限为0.05 ng/mL,定量限为0.1 ng/mL。
2.1.3 精密度和准确度
取空白血,配制浓度分别为0.1 ng/mL(定量下限)、0.2 ng/mL(低浓度)、5 ng/mL(中浓度)、15 ng/mL(高浓度)的标准添加样本(含2 ng/mL内标),每个浓度配制6个样本,在同一天分早中晚分别进行提取分析,确定方法日内检测的精密度和准确度;连续4 d,分别配制这四个浓度标准添加样本,确定方法的日间检测精密度和准确度,结果见表3。不难看出,两种化合物的准确度均在90%~110%,精密度均≤5%,符合法庭科学中毒物检测的要求。
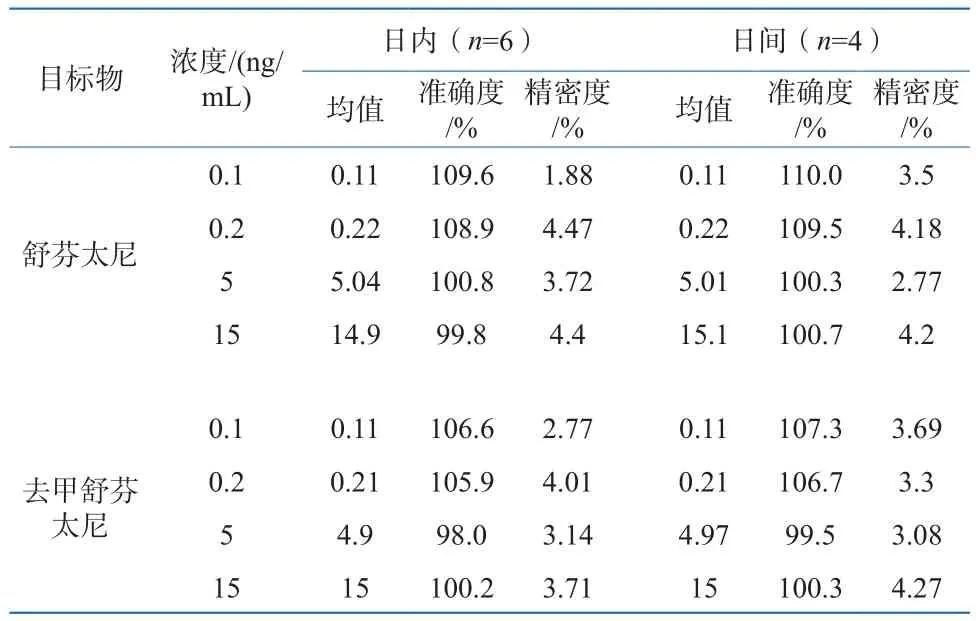
表3 血中舒芬太尼、去甲舒芬太尼精密度和准确度测试结果Table 3 Precision and accuracy of sufentanil and norsufentanil in blood
2.1.4 基质效应和回收率
取空白血,选择0.1、0.2、5、15 ng/mL四个水平添加浓度,分别在样本处理前添加混合标准储备液和2 ng/mL内标(RES),样本按1.3项处理后添加混合标准储备液及2 ng/mL内标于过滤膜后的上清液中(RPES),在甲醇中直接添加混合标准储备液和2 ng/mL内标(RNES),分别测试3种处理条件下的目标物峰面积和内标峰面积的比值,按照以下公式计算样本前处理回收率以及基质干扰率。
回收率%=(RES/RPES)×100%
生物基质影响率%=[(RPES/RNES)-1]×100%
结果如表4所示,计算样本前处理回收率在90%~120%间,基质干扰在-10%~5%之间。方法的回收率及基质干扰均满足要求。
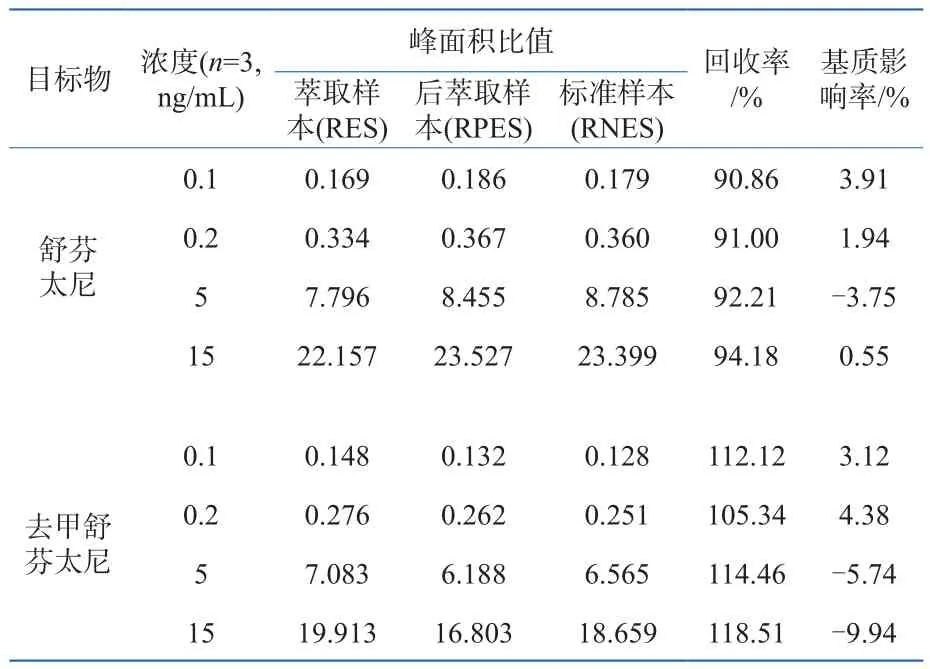
表4 血中舒芬太尼和去甲舒芬太尼回收率及生物基质影响率测试结果Table 4 Recovery rate (%) of sufentanil and norsufentanil in blood and the effect (%) of biological matrix
2.1.5 稳定性
取3份空白血液,配制浓度分别为0.2、4.5、15 ng/mL的舒芬太尼标准添加样本。将血样分别置于-20 ℃(冰箱冷冻)、0 ℃(冰箱冷藏)、20 ℃(室温)三种温度环境中,在0、1、4、7、11、15、25、35、50、70、90 d分别添加2 ng/mL内标后进行检测。
在-20、0、20 ℃条件下质量浓度为0.2、4.5、15 ng/mL的舒芬太尼血样随时间均基本呈下降趋势(见图2),0.2 ng/mL(低浓度)、4.5 ng/mL(中等浓度)在三种温度条件下保存35 d无显著区别且含量最低下降至初始质量浓度的81.7%,而15 ng/mL(高浓度)在-20、0、20 ℃条件下,含量下降至初始质量浓度的80%以上的时间分别为25、11、7 d。综合考虑,检材血液应于7 d内及时送检,尽量冷冻或冷藏保存。
2.1.6 动物实验
两只雄性小鼠(每只约80 g)腹股沟处皮下注射50 μg/mL枸橼酸舒芬太尼注射液约160 μL(即注射剂量为0.1 mg/kg),于给药后20 min、1 h分别通过内眦静脉采血及2 h断颈取血各0.5 mL。按1.3方法处理、检测。超出定量线性范围,空白鼠血稀释后再次分析。
经计算得出小鼠血液中舒芬太尼及去甲舒芬太尼平均质量浓度结果见表5。

表5 小鼠给药后不同时间节点的测试结果Table 5 Sufentanil and norsufentanil tested at different time junctures from mice after administration of the two drugs
2.2 讨论
舒芬太尼主要是通过肝脏代谢,据报道在肝微粒体内由单加氧酶CYP3A4通过N-脱烷基化、O-去甲基化和羟化三种途径而失活[10],然后随尿液和胆汁排出,约1%以原形经尿排出,N-脱烷基化而形成的代谢产物为去甲舒芬太尼(见图3),只有该代谢物具有药理活性,约为舒芬太尼的10%,与芬太尼相当[11],鉴于其特殊的药代学特性,代谢物亦能产生残余效应,从而达到很好的术后镇痛药物效果,因此本实验重点研究代谢物为去甲舒芬太尼的机制与测定。
通过动物实验,不难发现舒芬太尼体内代谢速度较快,20 min后舒芬太尼迅速衰减,2 h时含量极低,这符合舒芬太尼再分布半衰期为15 min左右、清除半衰期为150 min左右的文献报道[12]。
3 结论
近年来,国内外对血中舒芬太尼的分析逐步向灵敏度高、检出限低、重现性好、前处理简便等方向发展,这对建立人血中舒芬太尼及代谢产物的定性定量检测方法有较强的指导意义。本方法中,通过在人血中添加舒芬太尼和代谢物去甲舒芬太尼,使用舒芬太尼-D5作为内标,无需衍生化;采用乙腈沉淀蛋白的前处理方法直接进样分析,操作简单、快速,可避免因操作繁琐引起的误差;通过反向C18色谱柱分离目标物,电喷雾串联四级杆质谱进行检测,选取两个离子对定性,准确度好。经验证该方法特异性、准确度、精密度、灵敏度、线性、基质效应和回收率均满足毒物动力学和毒品检验的要求,且建议该检材血液应低温保存并于7 d内及时送检,4.5 ng/mL血样在20 ℃条件下40 d后检测结果升高、70 d后下降,其变化较为复杂,有待于进一步研究。本方法前处理简便、可标准化,可用于法庭科学中舒芬太尼滥用案件的分析检测。
