帕博丽珠单抗对PD-L1高表达的晚期肺腺癌患者的影响
2022-04-11李奕璇赵敏陈娜马静
李奕璇 赵敏 陈娜 马静
河南大学淮河医院呼吸内科,开封 475000
肺腺癌是肺癌中的一种,属于非小细胞癌,在女性肺癌患者中多见,多起源于支气管黏膜上皮[1]。同其他类型的肺癌一样,在肿瘤切除完全的情况下可增加生存率,但仍有近30%左右的患者术后会有复发的现象,对患者的身心均造成了不小的伤害[2]。而晚期肺腺癌患者因机体功能低下,且癌细胞的广泛扩散,不能支持手术。肿瘤的发生与发展与机体的免疫机制有着密切联系,免疫治疗在癌症系统性治疗中占据了重要位置[3]。程序性细胞死亡受体-1(PD-L1)是一种重要的免疫抑制分子,具有下调免疫系统感应的作用,可使肿瘤细胞获得免疫逃逸,促进肿瘤的恶性发展[4]。PD-L1 抑制剂可通过抑制 PD-1/PD-L1 信号通路,阻断两者结合,激活T 细胞的免疫反应,对肿瘤细胞进行识别、杀伤和清除,是目前临床认为最为有效的治疗方法[5]。帕博丽珠单抗作为PD-L1 抑制剂在肺癌患者中的应用得到临床的广泛关注,称为肺癌的治疗新星,基于此,本研究对河南大学淮河医院采用帕博丽珠单抗治疗的晚期肺腺癌患者进行疗效观察,探讨其对细胞角化素蛋白片段 19(Cyfra21-1)、人半乳糖凝集素-3(Galectin-3)水平及PD-L1阳性表达率的影响。
资料与方法
1、一般资料
经河南大学淮河医院伦理委员会审核通过,选取2019年5月至2021年5月在河南大学淮河医院治疗的70例晚期肺腺癌且PD-L1呈高阳性表达患者,男21例,女49例,年龄45~74(59.45±6.68)岁。(1)纳入标准:①经病理学及影像学确诊为晚期肺腺癌患者;②PD-L1 蛋白阳性表达率≥50%;③患者及家属对本研究目的了解并同意入组。(2)排除标准:①合并其他恶性肿瘤者;②预计生存期不足6 个月者;③配合度较差者;④对本研究药物及方法有禁忌者。
2、治疗方法
患者在化疗期间均给予营养支持及抗感染等基础治疗。药品:帕博丽珠单抗注射液[注册证号S20180019,爱尔兰MSD Ireland(Carlow),100 mg/4 ml];用法:静脉注射;用量:200 mg;时间:每3周1次。共持续使用12周,4个周期。
3、观察指标
3.1、近期疗效评估 参照《实体瘤治疗疗效评价标准》[6]对此次治疗效果进行评估,分为完全缓解(CR)、部分缓解(PR)、疾病稳定(SD)、疾病进展(PD)4 级。以影像学表现为标准,当治疗后病灶完全消失为CR;病灶范围缩小30%及以上为PR;病灶范围缩小不到30%或增大未超过20%为SD;病灶范围增大20%及以上或有新病灶出现为PD。
3.2、血清学指标 于治疗前及治疗2、4周期后,抽取所有入组患者的空腹静脉外周血,检测Cyfra21-1、Galectin-3水平及PD-L1阳性表达率。检测方法:采用酶联免疫吸附试验(ELISA)(试剂盒:上海酶联生物科技有限公司)检测患者Cyfra21-1、Galectin-3 水平;采用Western blot法检测PD-L1 阳性表达率[一抗:PD-L1 多克隆抗体试剂采自武汉益普生物科技有限公司;二抗:羊抗小鼠免疫球蛋白G(IgG)单克隆抗体试剂盒采自北京百奥莱博科技有限公司]。
3.3、不良反应 记录入组患者在治疗期间出现淋巴细胞计数减少、血红蛋白减少、肝功能异常等不良反应发生情况。
4、统计学处理
对本研究所得相关数据采用SPSS 21.0 统计学软件进行分析,计数资料用例(%)表示,将满足正态分布且方差齐的计量资料用()表示,组间差异采用两样本独立t检验比较,组内多个时间点比较采用重复测量资料的方差分析,当P<0.05提示差异有统计学意义。
结 果
1、70例肺腺癌患者近期临床疗效情况
在治疗 4 周期结束后,PR 26 例(37.14%),SD 34 例(48.57%),PD 10例(14.29%),总疾病控制率为85.71%。
2、70例肺腺癌患者治疗前后血清学指标变化情况
由表 1 可知,Cyfra21-1、Galectin-3 水平及 PD-L1 阳性表达率在治疗后有显著下降趋势,且随着治疗周期的推移,Cyfra21-1、Galectin-3 水平及 PD-L1 阳性表达率下降明显(均P<0.05)。
表1 70例PD-L1高表达的晚期肺腺癌患者治疗前后血清学指标变化情况()
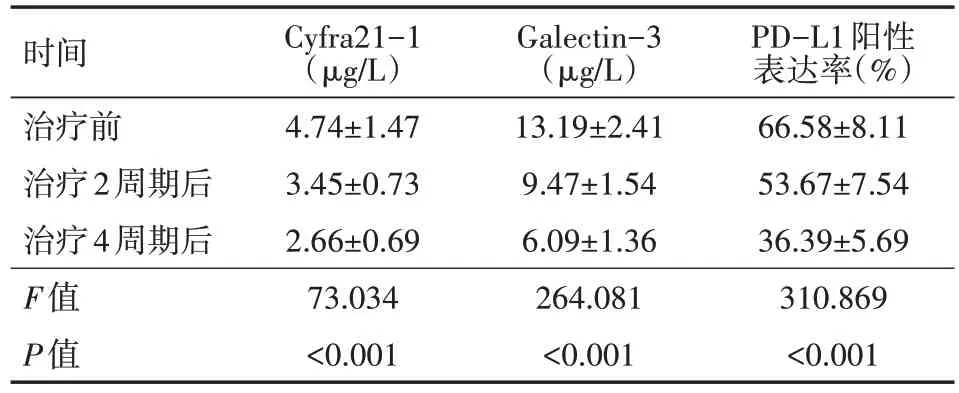
表1 70例PD-L1高表达的晚期肺腺癌患者治疗前后血清学指标变化情况()
注:PD-L1为程序性细胞死亡受体-1,Cyfra21-1为细胞角化素蛋白片段19,Galectin-3为人半乳糖凝集素-3
PD-L1阳性表达率(%)66.58±8.11 53.67±7.54 36.39±5.69 310.869<0.001时间治疗前治疗2周期后治疗4周期后F值P值Cyfra21-1(µg/L)4.74±1.47 3.45±0.73 2.66±0.69 73.034<0.001 Galectin-3(µg/L)13.19±2.41 9.47±1.54 6.09±1.36 264.081<0.001
3、不同疗效肺腺癌患者治疗前后血清学指标变化比较
由表 2 可知,在治疗 4 周期后,疗效为 PR 和 SD 的患者,较治疗前比较,Cyfra21-1、Galectin-3 水平及 PD-L1 阳性表达率均有下降(均P<0.05);疗效为PD 的患者,Cyfra21-1、Galectin-3 水平及PD-L1 阳性表达率与治疗前比较差异均无统计学意义(均P>0.05)。治疗4 周期后PR+SD 患者的Cyfra21-1、Galectin-3 水平及 PD-L1 阳性表达率明显低于PD患者(均P<0.05)。
表2 不同疗效PD-L1高表达的晚期肺腺癌患者治疗前后血清学指标变化比较()
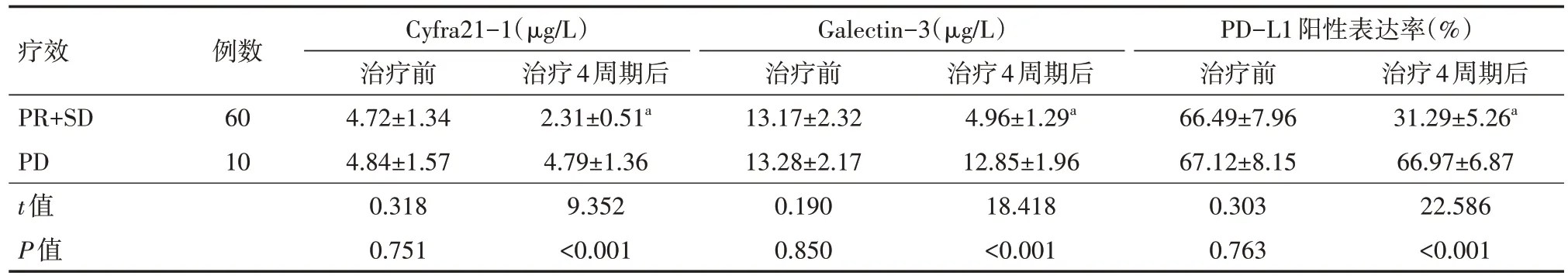
表2 不同疗效PD-L1高表达的晚期肺腺癌患者治疗前后血清学指标变化比较()
注:PD-L1为程序性细胞死亡受体-1,Cyfra21-1为细胞角化素蛋白片段19,Galectin-3为人半乳糖凝集素-3;PR为部分缓解,SD为疾病稳定,PD为疾病进展;与同组治疗前比较aP<0.05
治疗4周期后31.29±5.26a 66.97±6.87 22.586<0.001疗效PR+SD PD t值P值例数60 10 Cyfra21-1(µg/L)治疗前4.72±1.34 4.84±1.57 0.318 0.751治疗4周期后2.31±0.51a 4.79±1.36 9.352<0.001 Galectin-3(µg/L)治疗前13.17±2.32 13.28±2.17 0.190 0.850治疗4周期后4.96±1.29a 12.85±1.96 18.418<0.001 PD-L1阳性表达率(%)治疗前66.49±7.96 67.12±8.15 0.303 0.763
4、70例晚期肺腺癌患者治疗过程中不良反应发生情况
在治疗过程中,70 例晚期肺腺癌患者中有5 例出现淋巴细胞计数减少,3 例出现血红蛋白减少,有2 例出现肝功能异常,总不良反应发生率为14.29%。不良反应均为Ⅰ~Ⅲ级,未出现Ⅳ级不良反应。
讨 论
肺癌在我国恶性肿瘤中的发病率居于首位,严重威胁着我国人民的健康,肺腺癌是其中一种,起源于支气管黏膜上皮,属于腺上皮恶性肿瘤。肿瘤的预防和治疗一直是医学研究的热点,近年来,随着对肿瘤生理过程的深入研究,在机体免疫治疗方向取得了很大的突破。PD-L1在诸多肿瘤细胞组织中呈高表达状态,其通过与肿瘤细胞中的PD-1 结合,使肿瘤细胞逃离免疫系统的识别,从而促进肿瘤细胞的恶性发展[7]。帕博丽珠单抗作为PD-L1 免疫抑制剂的一种,具有肺癌治疗新星之称,对于中晚期肺腺癌患者、不适于手术治疗者,免疫治疗无疑是最佳选择。本研究显示,在治疗4 周期结束后,总疾病控制率高达85.71%,说明帕博丽珠单抗治疗PD-L1高表达的晚期肺腺癌患者有着较好的疗效。
本研究显示,70 例晚期肺腺癌患者经治疗后,Cyfra21-1、Galectin-3 水平及 PD-L1 阳性表达率在治疗后有显著下降趋势,且随着治疗周期的推移,Cyfra21-1、Galectin-3 水平及PD-L1 阳性表达率下降明显。Cyfra21-1 是上皮源性的肿瘤标志物,广泛分布于正常组织的上皮组织中,正常情况下在机体外周血以及淋巴结肿处于低水平状态,当上皮组织癌变出现后,使Cyfra21-1 大量释放,溶于组织液、体液及血液中,呈高表达状态[8]。杨颖等[9]研究提到,Cyfra21-1 是非小细胞肺癌最有价值的血清肿瘤标志物。Galectin-3属于半乳糖凝集素家族,存在于细胞核与细胞质间,有着调节细胞生长、分化和凋亡的作用,在肿瘤细胞中多有高阳性表达状态[10],在齐德林等[11]的研究中显示,Galectin-3水平的表达与肺癌肿瘤细胞淋巴结转移有关。PD-L1/PD-1 信号通路是肿瘤免疫机制重要的途径之一,抑制PD-L1 是免疫治疗最主要的机制。这说明,Cyfra21-1、Galectin-3 水平及 PD-L1 阳性表达率可能可以作为疗效评估的指标。本研究发现,在治疗4 周期后,疗效为PR 和SD 的患者,较治疗前比较,Cyfra21-1、Galectin-3水平及PD-L1 阳性表达率均有下降;疗效为PD 的患者,Cyfra21-1、Galectin-3 水平及 PD-L1 阳性表达率与治疗前比较均无明显差异。这提示,在治疗过程中监测Cyfra21-1、Galectin-3 及 PD-L1 阳性表达率变化,对疗效评估具有一定的价值。本研究发现,70 例晚期肺腺癌患者的总不良反应发生率仅为14.29%,且均未发生Ⅳ级不良反应。王芸等[12]的研究中提出,帕博丽珠单抗治疗晚期非小细胞癌患者未见明显不良反应,本研究与其部分相似,说明帕博丽珠单抗的不良反应较小。
综上所述,帕博丽珠单抗对PD-L1 高表达的晚期肺腺癌患者的疾病控制效果较好,可明显降低Cyfra21-1、Galectin-3 及PD-L1 的阳性表达率,且不良反应较小。Cyfra21-1、Galectin-3 及 PD-L1 可作为治疗效 果 的 观察指标。
利益冲突所有作者均声明不存在利益冲突
