合并心原性休克的急性心肌梗死患者行急诊经皮冠状动脉介入治疗后1年内死亡预测因素分析
2022-04-06胡昊吴佳纬李丹施超李龙伟孔祥勇周俊岭陈鸿武马礼坤
胡昊 吴佳纬 李丹 施超 李龙伟 孔祥勇 周俊岭 陈鸿武 马礼坤
急性心肌梗死(acute myocardial infarction,AMI)合并心原性休克(cardiogenic shock,CS)是一种临床常见的复杂综合征,可引起低心排血量和低血压,并伴有多器官功能障碍。即使在早期血运重建,包括经皮冠状动脉介入治疗(percutaneous coronary intervention,PCI)或冠状动脉旁路移植术(coronary artery bypass grafting,CABG)后,其死亡率仍在40%~60%[1]。为了稳定这些危重患者的病情,临床除了正性肌力药物外,还有诸如主动脉内球囊反搏(intra-aortic balloon pump,IABP)、经皮左心室辅助装置(例如Impella)或静脉动脉体外膜肺氧合(extracorporeal membrane oxygenation,ECMO)等机械辅助装置来支持血流动力学,其中机械辅助装置IABP已成为一项成熟的技术,这是目前在急性泵衰竭中最常用的机械辅助方法[2]。虽然目前IABP降低CS患者死亡率的结论仍存在争议[3-6]。死亡率的高低是否可能归因于其他危险因素,这一点尚未明确。本文纳入中国科学技术大学附属第一医院符合入选条件的所有登记患者,分析患者临床特点、死亡预测因素并绘制生存曲线,探讨影响AMI合并CS患者死亡率可能相关的危险因素。
1 对象与方法
1. 1 研究对象
2014年1月至2018年1月在中国科学技术大学附属第一医院心血管内科因AMI入院行急诊PCI术的患者共2193例,其中符合入选条件并完成随访的患者298例(13.6%)。患者在PCI术前均签署知情同意书。登记所有入选患者基本临床资料、实验室检查结果及PCI资料。所有入院诊断AMI合并CS患者,在IABP辅助下行急诊PCI;部分患者为PCI术后发生CS而补救性置入IABP也予以入选。根据患者1年随访时的生存情况分为死亡组111例(37.2%)和存活组187例(62.8%)。
1. 2 临床指标标准
A M I 诊断标准:按照第3版心肌梗死全球定义[5]。CS诊断标准:(1)收缩压≤90 mmHg(1 mmHg=0.133 kPa)或平均动脉压下降≥30 mmHg,或高血压病患者原收缩压下降60 mmHg,至少持续30 min;(2)心排指数(cardiac index,CI)≤2.2 L/(min·m2);(3)肺毛细血管楔压≥15 mmHg;(4)脏器低灌注:神态改变、发绀、肢体发冷、尿量减少[<0.5 ml/(kg·h)]。心肌梗死溶栓治疗试验(thrombolysis in myocardial infarction,TIMI)血流分级标准:0级,血管闭塞远端无前向血流;Ⅰ级,对比剂部分通过闭塞部位,但不能充盈远端血管;Ⅱ级,对比剂可完全充盈冠状动脉远端,但对比剂充盈及清除速度较正常冠状动脉血流延缓;Ⅲ级,对比剂完全、迅速充盈远端血管并迅速清除。
1. 3 PCI及药物治疗
患者术前或术后经股动脉置入IABP,采用常规方法进行冠状动脉造影和PCI,PCI策略由术者根据病情决定。所有患者术前给予负荷剂量双联抗血小板药物治疗(阿司匹林300 mg和氯吡格雷300 mg或替格瑞洛180 mg)。术后阿司匹林100 mg、每日1次和氯吡格雷75 mg、每日1次或替格瑞洛90 mg、每日2次维持。常规给予他汀类药物调脂,以及其他冠心病二级预防治疗。泵衰竭患者结合临床表现给予改善心力衰竭等血管活性药物。
1. 4 随访方法和临床事件的定义
患者持续接受随访至少12个月。分别在PCI术后12个月记录终点事件。全因死亡为主要终点事件。
1. 5 统计学分析
所有数据采用SPSS 22.0统计软件进行分析。计数资料用率(构成比)表示。采用Kaplan-Meier法进行生存分析,采用多因素Cox回归分析与患者死亡相关的危险因素,组间比较采用Log-rank检验。建立模型计算不同危险因素的风险比(hazard ratio,HR)、95%置信区间(confidence interval,CI)及多因素校正分析。估计影响死亡率预测因子的效应大小。在纳入统计模型之前,对所有变量进行共线性评估。对于共线变量,只选择最合适的变量。回顾调整前后效应大小的变化,估计混杂效应的影响,并进行敏感性分析。以P<0.05为差异有统计学意义。
2 结果
2. 1 患者基线资料和1年累积生存分析曲线
298例AMI患者中,293例(98.3%)患者完成1年随访,有5例(1.7%)患者失访。住院期间死亡患者共64例(21.5%),3个月随访时全因死亡患者达100例(33.6%),1年随访时全因死亡达111例(37.2%)。死亡组和生存组在年龄≥75岁、2型糖尿病、肌钙蛋白≥10 ng/ml、PCI术后TIMI血流分级≤Ⅱ级、左心室射血分数(left ventricular ejection fraction,LVEF)<40%及首次医疗接触至球囊扩张(first medical contact to balloon,FMC-to-B)时间等方面比较,差异均有统计学意义(均P<0.05,表1)。Kaplan-Meier生存曲线显示AMI合并CS患者3个月内死亡率高(图1)。
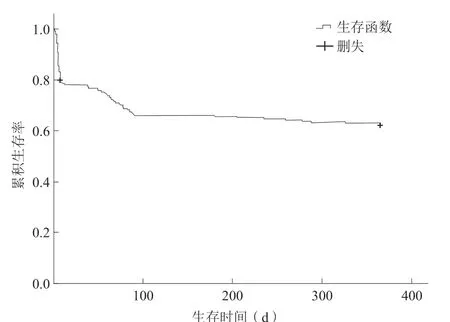
图1 患者随访1 年的Kaplan-Meier 生存曲线
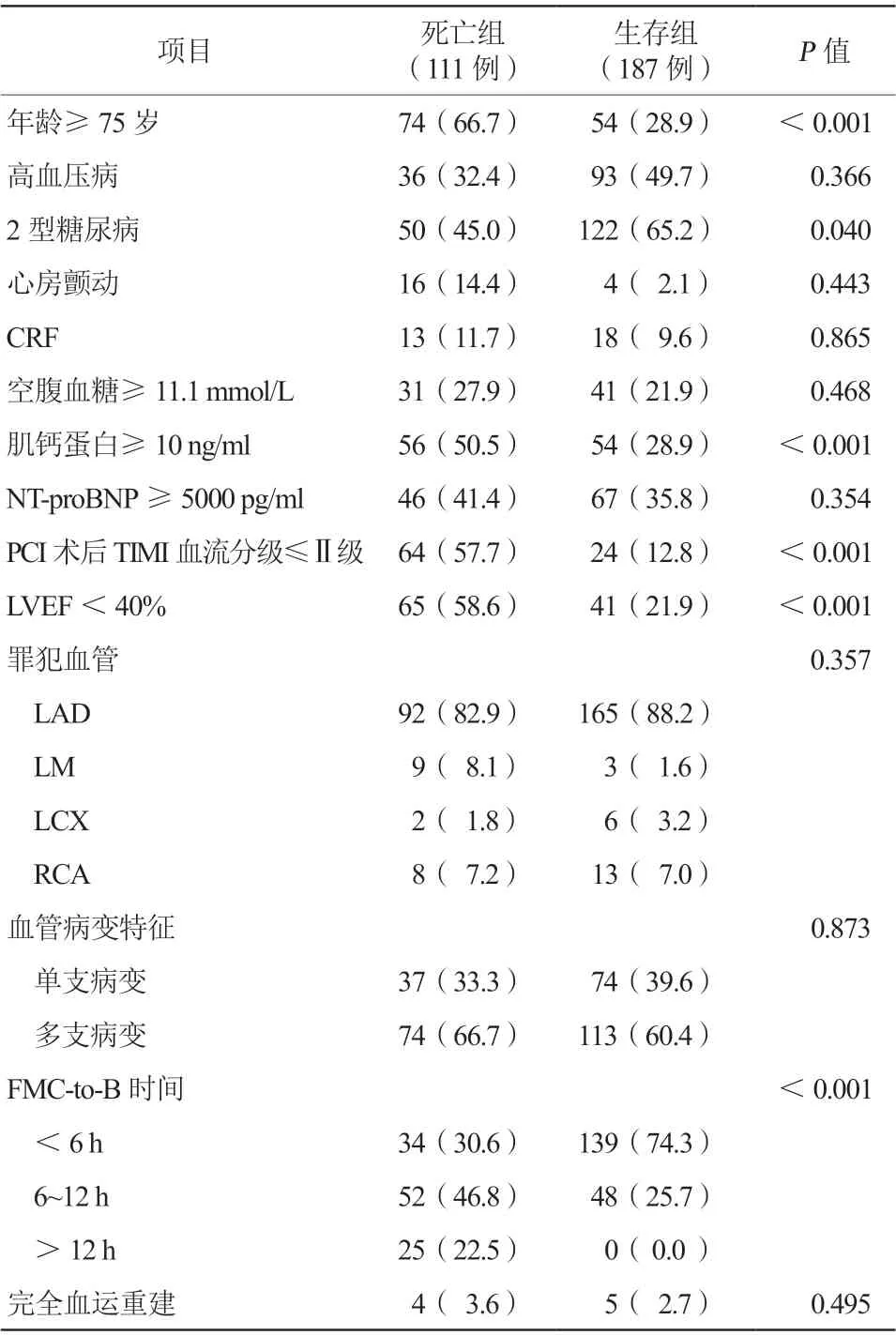
表1 两组患者基线资料特征比较[例(%)]
2. 2 相关危险因素对死亡率高低的预测价值
通过单因素Cox回归分析发现影响死亡率的危险因素有年龄≥75岁以及合并高血压病、2型糖尿病、心房颤动、肌钙蛋白≥10 ng/ml、PCI术后TIMI血流分级≤Ⅱ级、LVEF<40%、左主干病变、FMC-to-B时间>6 h。但通过建立多因素Cox回归分析发现,年龄≥75岁(HR1.68,95%CI1.31~2.16,P<0.001)、PCI术后TIMI血流分级≤Ⅱ级(HR3.57,95%CI2.06~6.18,P<0.001)、LVEF<40%(HR0.45,95%CI0.26~0.78,P=0.004)以及FMC-to-B时间>12 h(HR7.52,95%CI3.28~17.24,P<0.001)为影响死亡率的危险因素(表2)。按影响死亡率预测因子重要性分层则依次为FMC-to-B时间>12 h、LVEF<40%、PCI术后TIMI血流分级≤Ⅱ级、年龄≥75岁。

表2 影响患者1 年死亡率的预测因子分析
通过对这四个因素不同分组情况分别绘制生存分析曲线,Kaplan-Meier生存分析结果见图2。从结果看FMC-to-B时间>12 h是最强的死亡预测因素(HR7.52,95%CI3.28~17.24,P<0.001),患者预后极差。
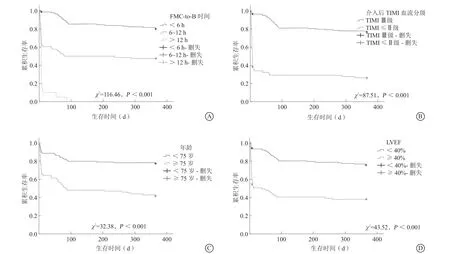
图2 A. 不同FMC-to-B 时间经皮冠状动脉介入治疗后累积生存分析;B. 不同介入术后TIMI 血流经皮冠状动脉介入治疗后累积生存分析;C. 不同年龄段经皮冠状动脉介入治疗后累积生存分析;D.不同LVEF 值经皮冠状动脉介入治疗后累积生存分析(Log-rank 检验,P<0.001)
3 讨论
AMI发生CS比例为5%~7%,死亡率高[1]。在目前的指南中,IABP被推荐用于AMI合并CS的患者。IABP的主要血流动力学效应包括通过球囊充气改善舒张期冠状动脉血流量,减轻心脏后负荷以减少心肌氧耗和增加心输出量。目前国际上IABP被广泛应用在CS患者的治疗中[5]。但IABP是否能够真正改善AMI合并CS患者的预后目前尚缺乏证据。AMI合并CS患者预后差,早期识别高危患者极为重要。简易、经济和有效的风险评估方法有利于临床医师尽早采取更积极的干预措施,进而有助于改善患者预后[7]。
本研究人群为真实世界中AMI合并CS的患者。既往的研究主要结果发现,成功的PCI是AMI合并CS患者生存的重要决定因素之一[8-10],通过单因素分析发现年龄、高血压病、糖尿病、心房颤动、肌钙蛋白水平、术后TIMI血流分级、LVEF、罪犯血管(左主干病变)及FMC-to-B时间等均是影响患者死亡率的预测因子,但是多因素分析里有些因素不再具有显著性意义。实际上通过多因素分析真正具有显著意义的危险因素是:高龄(≥75岁)、PCI术后TIMI血流分级≤Ⅱ级、LVEF(<40%)以及FMC-to-B时间(>12 h)。尽管有IABP等机械辅助装置支持,血流动力学持续恶化的患者死亡率仍然居高不下[8-9]。所以进一步提高患者术后生存率的关键是识别和消除预测不良后果的因素或事件。
对于AMI合并CS患者应用IABP是否能改善患者心功能和维持血流动力学稳定的结果尚存在争议。目前最大的随机对照研究IABP-SHOCK Ⅱ研究[6]结果表明置入IABP对AMI合并CS患者30 d死亡率仅是中性结果(P=0.69)。但也有些研究表明IABP辅助后的结果是积极的。前瞻性多中心随机对照研究(BCIS-1)[11]结果表明,严重缺血性心肌病患者PCI术中使用IABP长期随访5年全因死亡率下降34%。
如上所述,尽管IABP-SHOCK Ⅱ研究结果呈中性,但IABP仍被认为是AMI合并CS患者的合理选择。不可否认的是,与以前的指南推荐相比,目前的推荐等级降低了。根据2004年美国心脏病学会/美国心脏协会(American College of Cardiology/American Heart Association,ACC/AHA)指南[12],IABP为Ⅰ类适应证,推荐应用于CS患者。但在2013年ACC/AHA指南[13]中,IABP为Ⅱa类适应证。欧洲相关指南推荐IABP为Ⅱb类适应证[14]。基于多个指南推荐,目前IABP仍可能继续用于CS患者,除非有更好的替代装置。需要认识的是,对于一些高危且合并死亡预测因素较多的患者,可能仅仅依靠IABP的辅助是远远不够的[15]。因此,一些新型机械循环辅助装置如ECMO、Impella等可能给该类高危患者提供更多支持,但临床疗效是否优于IABP,尚有待进一步研究证实。现有的研究结果表明,针对AMI合并CS患者,联合应用机械循环辅助装置可更好地改善患者预后[15-16]。
本研究非随机双盲对照研究,入选样本量相对较小。本研究中AMI合并CS患者发生率高于文献报道的发生率,可能原因与部分AMI患者未能及时行急诊介入治疗,导致合并CS患者较多有关,同时也发现有少数患者是术后发生CS而行补救性IABP置入,期待更多大规模多中心前瞻性随机对照临床研究探讨AMI合并CS患者行急诊PCI后远期发生死亡的预测因素。
利益冲突 所有作者均声明不存在利益冲突
