马来酸阿伐曲泊帕治疗化疗相关血小板降低症的效果
2022-04-06苏玉婷戴春华
丁 延 苏玉婷 戴春华
(江苏大学附属医院 放疗科, 江苏 镇江 212000)
血小板减少症是指血液中血小板计数小于100×109/L,分为原发性和获得性,前者是遗传因素(如Fanconi贫血、先天性伴畸形无巨核细胞等)所致,后者是血液性疾病、风湿免疫性疾病、放化疗损伤等因素所致[1]。其中恶性肿瘤化疗相关性血小板减少症(chemotherapy-induced thrombocytopenia, CIT)是恶性肿瘤化疗药物对患者体内骨髓巨核细胞产生抑制作用,导致血液中血小板计数大量减少,低于100×109/L[2]。CIT轻则引起出血、延长住院时间,重则影响化疗药物剂量及恶性肿瘤的治疗效果,对患者生命安全造成严重威胁[3-4]。临床医师主要根据病情程度采用输注血小板和药物治疗,常见治疗药物为重组人血小板生成素(recombinant human thrombopoietin, rhTPO)和重组人白介素-11(recombinant human interleukin-11, rhIL-11),治疗效果良好,且不良反应较少。而马来酸阿伐曲泊帕是全球首个获批用于治疗慢性肝病(chronic liver disease, CLD)相关血小板减少症的药物,临床疗效良好,除了CLD相关血小板减少症外,其已在CIT以及特发性血小板减少性紫癜(idiopathic thrombocytopenic purpura, ITP)中开展研究,但此类临床研究较少[5]。因此本研究拟观察马来酸阿伐曲泊帕联合rhTPO对CIT患者血小板参数的影响,旨在验证其对CIT患者的临床疗效和安全性,以期为CIT临床治疗提供新的选择。
1 资料与方法
1.1 一般资料
选取2019年6月~2021年6月在本院确诊的50例肿瘤化疗相关3级及以上血小板减少症(CIT)患者的临床资料,进行回顾性分析。将患者根据不同治疗方案分为观察组(n=23)和对照组(n=27)。纳入标准:①符合CIT诊断标准[6];②卡氏(KPS)评分>70分;③均接受化疗。排除标准:①外周血血小板计数>50×109/L;②对治疗药物存在过敏者;③合并其他血液疾病者;④合并严重感染者;⑤合并严重心脑血管疾病者;⑥合并严重器官功能障碍者。本研究经医院伦理委员会通过(No: KY2021K0902),患者及家属了解并知情同意。
1.2 治疗方法
对照组患者在化疗第2周期结束6~24 h内皮下注射rhTPO(厂家:沈阳三生制药有限责任公司;规格:15 000 U: 1 mL;批号:国药准字S20050048)300 U/kg,1次/天,连续注射不超过14 天,血常规检查根据血小板计数进行,血小板计数低于50×109/L,1次/天,高于50×109/L,1次/3天。若血小板计数≥100×109/L时,应立即停药。对于出血明显和血小板计数<10×109/L,联合血小板输注进行治疗。观察组对于rhTPO的使用同对照组,并联用马来酸阿伐曲泊帕片(厂家:日本Kawashima Plant, Eisai Co.,Ltd.;规格:20 mg×10片;批号:国药准字H20200005)进行口服治疗,在择期化疗前10~13天开始服用,1次/天,与食物同服。若患者血小板计数<40×109/L,3片/天,反之则2片/天,连续服用5天。若血小板计数≥100×109/L时,应立即停药。若服药过程中血小板计数无明显升高或出现严重不良反应则立即停药,采用血小板输注进行治疗,确保血小板升高至目标水平。
1.3 观察指标
两组患者自化疗第2周期结束之日开始随访,随访2周。①比较血小板恢复情况,包括化疗后血小板升高至50×109/L、75×109/L、100×109/L的治疗时间和治疗费用;②比较血小板开始升高时间以及治疗过程中血小板最低值和最高值;③治疗7天后,比较两组患者凝血功能相关指标,包括凝血酶原时间(prothrombin time, PT)、活化部分凝血活酶时间(activated partial thromboplastin time, APTT)、凝血酶时间(thrombin time, TT)、纤维蛋白原(fibrinogen, FIB)、D-二聚体;④治疗7天后,比较两组患者治疗前后血清肝肾损伤相关指标,包括谷草转氨酶(aspartate aminotransferase, AST)、谷丙转氨酶(alanine aminotransferase, ALT)、血清尿素氮(blood urea nitrogen, BUN)、血肌酐(serum creatinine, Scr)。
治疗期间密切监测患者血常规以及生命体征,包括心电图、心肺功能等,随时记录两组患者治疗期间的不良反应发生情况。
1.4 统计学处理
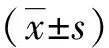
2 结果
2.1 两组患者一般资料比较
两组患者年龄、性别等一般资料无统计学差异(均P>0.05),见表1。

表1 两组患者一般资料比较
2.2 两组患者血小板恢复时间和治疗费用情况比较
观察组血小板计数升高至50×109/L、75×109/L、100×109/L的治疗时间明显短于对照组,差异均具有统计学意义(均P<0.05),两组治疗费用差异无统计学意义(P>0.05),见表2。

表2 两组患者的血小板恢复时间和治疗费用情况比较
2.3 两组患者的血小板计数变化情况比较
治疗后观察组血小板开始升高时间明显短于对照组,血小板最高值明显高于对照组,差异均具有统计学意义(均P<0.05);两组血小板最低值无明显差异(P>0.05),见表3。

表3 两组患者的血小板计数变化情况比较
2.4 两组患者凝血功能相关指标比较
治疗前两组患者凝血功能相关指标无统计学差异(均P>0.05)。与治疗前相比较,治疗后两组患者凝血功能相关指标APTT、PT、FIB、TT以及D-二聚体水平差异均具有统计学意义(均P<0.05)。但治疗后观察组APTT水平低于对照组,TT水平则高于对照组(均P<0.05),PT、FIB、D-二聚体水平差异无统计学意义(均P>0.05),见表4。

表4 两组患者凝血功能相关指标比较
2.5 两组患者的肝肾损害情况比较
与治疗前相比,两组患者治疗后的ALT、AST、BUN、Scr水平均无明显差异(均P>0.05);对照组和观察组相比,治疗前和治疗后的ALT、AST、BUN、Scr水平差异均无统计学意义(均P>0.05),见表5。

表5 两组患者的肝肾损害情况比较
2.6 两组患者的不良反应发生情况比较
观察组患者出现1例发热,1例肌肉酸痛,总不良反应发生率为8.70%;对照组患者仅出现1例发热,总不良反应发生率为3.70%。两组患者治疗期间总不良反应发生率无明显差异(P=0.588),且两组不良反应症状较轻微,经对症处理后均恢复正常,无严重不良反应发生,见表6。

表6 两组患者的不良反应发生情况比较
3 讨论
CIT可引起出血等并发症甚至死亡,严重影响了患者化疗的正常进行[7-8]。血小板输注虽是临床针对CIT最有效且起效最快的治疗手段,但血液制品供应紧缺,且血小板的多次输注机体容易出现耐受,引起继发性输注无效,同时也容易增加血液传染疾病的感染风险[9]。
rhTPO通过与血小板生成素受体(myeloproliferative leukemia, MPL)特异性结合,促进巨核细胞增殖分化为血小板并抑制巨核细胞的凋亡,同时促进更多的肝细胞进入增殖周期,使巨核系祖细胞池得以扩增[10]。马来酸阿伐曲泊帕是第二代血小板生成素(thrombopoietin,TPO)受体激动剂。既往研究显示[11-12],其在多种病因引起的血小板减少症,如ITP、CIT、围手术期血小板减少症等均具备一定的疗效。其通过模拟TPO效应,加速骨髓祖细胞的巨核细胞增殖分化周期,从而增加血小板的生成[13]。本研究结果表明,观察组患者血小板计数恢复至相应水平所需治疗时间以及开始升高时间均短于对照组,但治疗费用无明显差异。这一结果提示,马来酸阿伐曲泊帕联合rhTPO的临床疗效显著,相较单用rhTPO的起效时间更快,血小板升高能力更强,提高疗效的同时不进一步增加患者经济负担。分析其原因,马来酸阿伐曲泊帕与TPO受体特异性结合位点和rhTPO不同。马来酸阿伐曲泊帕与TPO受体的跨膜区相结合,而rhTPO则与TPO受体的胞外区特异性结合,因此两者不存在竞争抑制,可联合发挥更好的临床疗效[14]。另外,可能与其累加效应有关。相关研究表明[15],马来酸阿伐曲泊帕作用机制虽然与TPO相似,但没有抑制TPO与其受体结合,二者可能同时作用于受体。在TPO发挥最大效应的情况下,加入马来酸阿伐曲泊帕可使巨核细胞数量再增加约1倍,对促进巨核细胞的生成方面存在叠加作用,从而提高了治疗效果。此外,本研究结果显示,联用阿伐曲泊帕和rhTPO较单用rhTPO达到治疗目标所花费的时间缩短了近1倍多,且治疗所需剂量明显降低,因此两种治疗费用无明显差异。
既往研究显示[16-17],阿伐曲泊帕应用于慢性肝病相关血小板减少症和ITP患者,耐受性较优,不良事件少且轻微,而I期临床研究显示,其应用于CIT患者中并未出现严重不良反应,如血栓形成以及肝毒性事件。但目前阿伐曲泊帕应用CIT的临床研究较少,其安全性仍需进一步评估。本研究结果表明,治疗后两组患者凝血功能得到显著改善并且总不良反应发生率无明显差异,但观察组TT、APTT以及血小板最高值与对照组有明显差异,并且两组患者D-二聚体较正常范围略升高,差异无统计学意义。这提示两组患者经过治疗后凝血功能均得到增强的同时,没有明显增加血栓风险以及不良反应的发生。相关临床试验结果显示[18],马来酸阿伐曲泊帕与具有相同作用机制的药物类似,其具有血栓性和血栓栓塞性并发症的轻微风险,特别是门静脉血栓的发生风险。本研究结果与其不同,观察组患者均无血栓发生,可能与联合使用剂量较少有关,也有可能是样本量较少,对统计学结果造成影响所致。与降低血小板活化阈值的rhTPO相反,马来酸阿伐曲泊帕不增加血小板表面P-选择素和活化糖蛋白2b/3a测定的循环活化血小板数量,也不增加血小板对低浓度或高浓度凝血酶受体激活肽和二磷酸腺苷的反应性,与相关文献报道类似[19-21]。本研究结果显示,治疗前后两组患者ALT、AST、BUN、Scr水平差异均无统计学意义,这提示该药物无肝肾毒害性。
综上所述,马来酸阿伐曲泊帕能快速升高恶性肿瘤CIT患者血小板计数,与rhTPO联合运用,在提高疗效的同时未出现严重不良事件,且无肝肾毒害性。但本研究样本量较少,可能对统计学结果造成影响,且本研究只观察了马来酸阿伐曲泊帕联合rhTPO的效果,对于单用效果尚未明确。其应用于CIT的效果值得探索,安全性及有效性有待大规模临床研究进一步验证。
