阿法替尼联合培美曲塞和卡铂化疗治疗吉非替尼耐药肺腺癌患者的临床效果▲
2022-03-29王小文谢金龙朱晓芸谭可为
王小文 谢金龙 朱晓芸 谭可为 陈 林
(1 中国人民解放军联勤保障部队第九二二医院血液肿瘤科,湖南省衡阳市 421002,电子邮箱:xlvbxv@163.com;2 南华大学附属第二医院呼吸与危重医学科,湖南省衡阳市 421001)
肺腺癌属于非小细胞肺癌的一种类型,是呼吸系统中最常见的恶性肿瘤,且发病率呈现逐年升高的趋势,严重威胁患者的生命健康[1]。近年来,分子靶向药物已经成为治疗肺腺癌的主要方法之一,吉非替尼属于表皮生长因子受体(epidermal growth factor receptor,EGFR)酪氨酸激酶抑制剂(tyrosine kinase inhibitor,TKI)药物,其作用机制为阻碍EGFR通路传递信号,最终达到抑制肿瘤细胞增殖、促进肿瘤细胞凋亡的目的[2]。虽然与常规化疗药物相比,肺腺癌患者对EGFR-TKI吉非替尼的耐受性较好,但有研究显示,绝大多数患者的治疗有效性并不持久,多在用药7~12个月后出现耐药现象,临床表现为病灶进一步生长或者转移[3]。因此寻找有效治疗吉非替尼耐药的肺腺癌患者的药物,对抑制病灶进一步生长、改善预后具有重要的意义。基于此,本研究探讨阿法替尼联合培美曲塞+卡铂化疗治疗吉非替尼耐药肺腺癌患者的疗效。
1 资料与方法
1.1 临床资料 选取2017年3月至2018年3月中国人民解放军联勤保障部队第九二二医院、南华大学附属第二医院收治的149例吉非替尼耐药肺腺癌患者为研究对象。纳入标准:(1)符合《中国非小细胞肺癌放射治疗临床指南(2020版)》[4]中肺腺癌的诊断标准,经病理组织学确诊,且处于中晚期;(2)对吉非替尼耐药,治疗失败;(3)预计生存期≥3个月;(4)卡氏功能状态评分≥60分。排除标准:(1)合并其他肿瘤者;(2)不能耐受本研究药物者;(3)局部病灶或者远处转移病灶不可测量和评估者;(4)心、肝、肾、骨髓等功能明显异常者;(5)合并严重感染性疾病者;(6)精神障碍、沟通障碍者。按照随机数字表法将患者分为化疗组74例和联合组75例。化疗组中男性35例、女性39例,患者年龄35~67(48.45±12.65)岁;原发肿瘤-区域淋巴结-远处转移分期:Ⅲ期32例,Ⅳ期42例;病灶部位:右上肺叶8例,右下肺叶7例,左上肺叶31例,左下肺叶28例。联合组中男性31例、女性44例,患者年龄35~65(47.50±11.75)岁;原发肿瘤-区域淋巴结-远处转移分期:Ⅲ期33例,Ⅳ期42例;病灶部位:右上肺叶9例,右下肺叶10例,左上肺叶30例,左下肺叶26例。两组患者的性别、年龄、原发肿瘤-区域淋巴结-远处转移分期和病灶部位比较,差异均无统计学意义(均P>0.05),具有可比性。患者及家属均对本研究知情同意,本研究经中国人民解放军联勤保障部队第九二二医院和南华大学附属第二医院医学伦理委员会批准。
1.2 方法
1.2.1 治疗方法:化疗组患者采用培美曲塞+卡铂化疗方案进行治疗。在开始化疗前给予患者叶酸、地塞米松预处理。化疗方案为500 mg/m2培美曲塞(南京先声东元制药有限公司,国药准字:H20133216)于第1天静脉滴注;400 mg/m2卡铂(中国齐鲁制药有限公司,国药准字:H10920028)于第2天静脉滴注;21 d为1个化疗周期,连续行2个化疗周期。联合组在化疗组的基础上口服阿法替尼治疗,患者餐前至少1 h或者餐后2 h口服40 mg阿法替尼(上海勃林格殷格翰药业有限公司,国药准字:J20170029),1次/d,21 d为1个疗程,连续用药2个疗程。
1.2.2 肿瘤标志物检测:于治疗前、两个疗程结束后1 d抽取患者清晨空腹静脉血3 mL,常温下3 000 r/min离心15 min(离心半径为3 cm)分离上层血清,-80℃保存待检。采用酶联免疫吸附法(enzyme-linked immunosorbent assay,ELISA)检测肿瘤标志物糖类抗原199、癌胚抗原、人细胞角蛋白19片段抗原21-1(cytokeratin 19 fragment antigen 21-1,CYFRA21-1)水平。检测仪器为罗氏Cobas e601全自动电化学发光分析仪。糖类抗原199 ELISA试剂盒由上海臻科生物科技有限公司提供(货号:ZK-2042),癌胚抗原 ELISA试剂盒由上海奥陆生物科技有限公司提供(货号:F2725-B),CYFRA21-1 ELISA试剂盒由上海富雨生物科技有限公司提供(货号:FY-03722H2)。RNA提取试剂盒购自深圳市纽邦生物技术有限公司(批号:55000)。
1.2.3 肿瘤增殖、凋亡基因及长链非编码RNA相对表达水平的检测:于治疗前、两个疗程结束后1 d抽取患者外周静脉血3 mL,分离出单个核细胞,之后采用TRIzol法提取单个核细胞中的总RNA,RNA提取试剂盒购自深圳市纽邦生物技术有限公司(批号:55000)提取完成后进行RNA纯度、含量测定,使用TaKaRa公司的试剂盒将其反转录为cDNA,反转录试剂盒购自上海羽哚生物科技有限公司(批号:YDJQ3013),采用实时荧光定量PCR法测定患者外周血单个核细胞中B细胞淋巴瘤-2(B-cell lymphoma-2,Bcl-2)mRNA、Bcl-2相关X蛋白(Bcl-2 associated X protein,Bax)mRNA及小核仁RNA宿主基因(small nucleolar RNA host gene,SNHG)12、SNHG15、SNHG16的表达。PCR反应试剂盒购自北京百奥莱博科技有限公司(批号:RFT100-JXV)。反应体系包括上下游引物各0.4 μL、cDNA模板1 μL、SYBR Green 10 μL,加蒸馏水至20 μL。反应条件为95℃预变性1 s、95℃ 5 s、60℃ 31 s,共进行40个循环。Bcl-2引物序列:上游5′-GACTTCGCCGAGATGTCCAG-3′,下游5′-CGGTGCTTGGCAATTAGTGG-3′;Bax引物序列:上游5′-ATGGAGCTGCAGAGGATTCG-3′,下游5′-AATGTCCAGCCCATGATGGT-3′;SNHG12引物序列:上游5′-AATTCTCGGCAATCACCACT-3′,下游5′-AGCGAGGAGAGGACTGGAAT-3′;SNHG15引物序列:上游5′-CCTAGTGAGGAGTGGAGCTGA-3′,下游5′-CTCATTCTGGAAGCAGAGAACC-3′;SNHG16引物序列:上游5′-GACTACAGGCGCGTACCTTC-3′,下游5′-GAAGCTGAGGCAGGCAGAT-3′;β-肌动蛋白(内参)引物序列:上游5′-CTGGCACCACACCTTCTACAATGAGC-3′,下游5′-GAGGATCTTCATGAGGTAGTCAGT-3′。使用2-ΔΔCt法计算上述各基因的相对表达水平。
1.2.4 临床疗效评价:两个疗程结束后1 d参照实体瘤疗效评价标准RECIST 1.1[5]评估两组患者的临床疗效。临床疗效分为完全缓解、部分缓解、疾病稳定、疾病进展。患者所有目标病灶均消失为完全缓解;患者基线病灶最大径之和至少减少30%为部分缓解;患者基线病灶最大径之和减少但未达到部分缓解标准,或者基线病灶最大径之和增加但未达到疾病进展标准为疾病稳定;患者基线病灶最大径之和至少增加20%,或者出现新的病灶为疾病进展。临床缓解率=(完全缓解+部分缓解)例数/总例数×100%。
1.2.5 毒副反应发生情况:依据世界卫生组织颁布的抗癌药物急性与亚急性毒性反应评估标准[6],记录在治疗过程中患者发生白细胞减少、脊髓抑制、消化道反应(恶心、呕吐)、肝肾功能损害等药物毒性反应的情况。
1.2.6 生存情况:两个疗程结束后对患者进行为期2年的随访,统计其生存情况,包括无进展生存期、总生存期以及2年存活率,其中从治疗开始至肿瘤进展或复发的时间为无进展生存期,从治疗开始至死亡或者末次随访的时间为总生存期。
1.3 统计学分析 采用SPSS 20.0软件进行统计学分析。计量资料以(x±s)表示,组间比较采用独立样本t检验,组内比较采用配对t检验;计数资料以频数和百分比表示,组间比较采用χ2检验。采用GraphPad Prism制作生存曲线,采用log-rank检验比较生存曲线间的差异。以P<0.05为差异具有统计学意义。
2 结 果
2.1 两组患者肿瘤标志物水平的比较 治疗前,两组患者的糖类抗原199、癌胚抗原、CYFRA21-1水平差异均无统计学意义(均P>0.05);治疗后,两组患者的糖类抗原199、癌胚抗原、CYFRA21-1水平均低于治疗前,且联合组以上指标水平低于化疗组(均P<0.05)。见表1。

表1 两组患者肿瘤标志物水平的比较(x±s,μg/L)
2.2 两组患者肿瘤增殖和凋亡基因mRNA相对表达水平的比较 治疗前,两组患者的Bcl-2和Bax的mRNA相对表达水平比较,差异均无统计学意义(均P>0.05);与治疗前相比,治疗后两组患者的Bcl-2 mRNA相对表达水平降低,Bax mRNA相对表达水平升高,且联合组Bcl-2 mRNA相对表达水平低于化疗组,Bax mRNA相对表达水平高于化疗组(均P<0.05)。见表2。
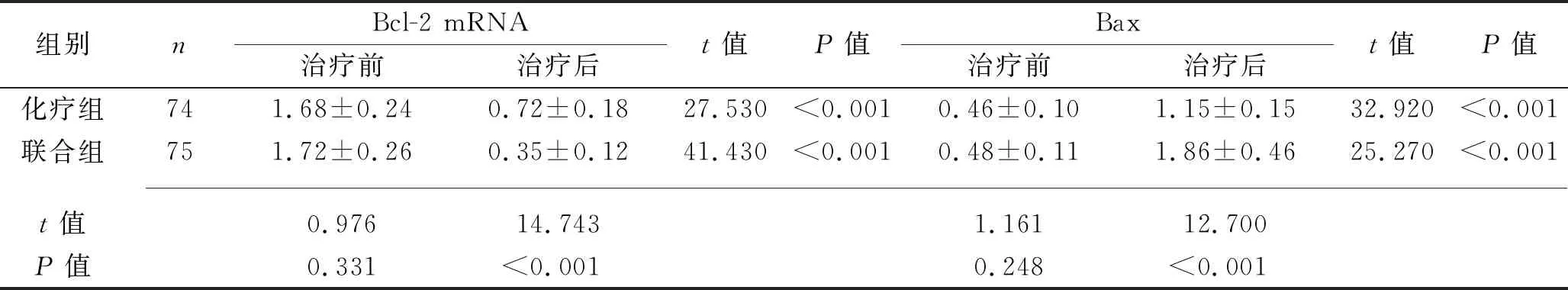
表2 两组患者肿瘤增殖和凋亡基因mRNA相对表达水平的比较(x±s)
2.3 两组患者SNHG12、SNHG15和SNHG16相对表达水平的比较 治疗前,两组患者的SNHG12、SNHG15和SNHG16相对表达水平比较,差异均无统计学意义(均P>0.05);治疗后,两组患者的SNHG12、SNHG15、SNHG16相对表达水平均低于治疗前,且联合组均低于化疗组(均P<0.05)。见表3。

表3 两组患者SNHG12、SNHG15、SNHG16相对表达水平的比较(x±s)
2.4 两组患者临床疗效的比较 联合组、化疗组患者的临床缓解率分别为62.67%(47/75)、45.95%(34/74),前者高于后者(χ2=4.198,P=0.041)。见表4。

表4 两组患者临床疗效的比较(n)
2.5 两组患者毒副反应发生情况的比较 化疗组、联合组的毒副反应总发生率分别为14.86%(11/74)、17.33%(13/75),差异无统计学意义(χ2=0.168,P=0.682)。见表5。

表5 两组患者毒副反应发生情况的比较(n)
2.6 两组患者生存情况的比较 联合组患者的中位无进展生存期为35.58个月,长于化疗组的30.52个月(χ2=11.756,P=0.008)。见图1。联合组患者的中位总生存期为42.63个月,长于化疗组的36.00个月(χ2=11.021,P=0.009);联合组患者的2年存活率为93.33%(70/75),高于化疗组患者的59.46%(44/74)(u=4.860,P=0.001)。见图2。

图1 两组患者无进展生存曲线图
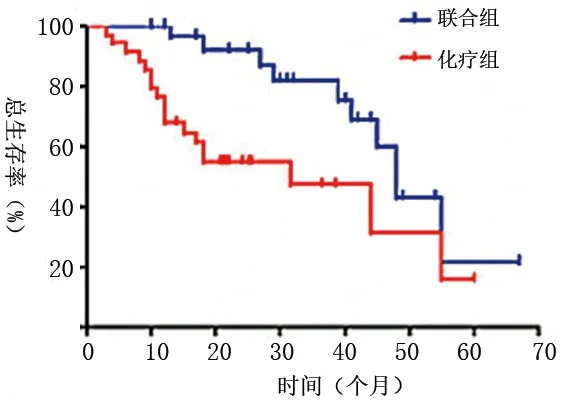
图2 两组患者总生存曲线图
3 讨 论
目前肺癌已经成为我国居民死亡的重要因素,其中肺腺癌是最为常见的类型。化疗为此病的主要治疗手段,但随着化疗药物应用时间的延长,肿瘤细胞会出现耐药现象,再次接受该化疗药物时效果甚微[7]。临床研究显示,肺腺癌患者多存在EGFR酪氨酸激酶结构域突变,虽然多数EGFR基因突变患者对吉非替尼等EGFR-TKI敏感,但存在不同程度的耐药现象[8]。目前肺腺癌患者的吉非替尼耐药率明显升高,这严重影响患者的预后[9]。因此寻找有效地延长吉非替尼耐药患者生存期、改善预后的药物具有重要的意义。
对吉非替尼耐药肺腺癌患者,临床上多采用化疗药物治疗,培美曲塞+卡铂化疗方案属于较为常见的方案之一。其中培美曲塞是一种新型的多靶点叶酸拮抗剂,其可同时阻断二氢叶酸还原酶、胸苷酸合成酶、甘氨酸核糖核苷甲酰基转移酶等多种与叶酸相关的酶,从而阻碍肿瘤细胞的嘧啶和嘌呤合成,最终抑制肿瘤细胞的RNA和DNA合成,从而发挥抗肿瘤的作用[10-12]。阿法替尼是一种不可逆的EGFR-TKI,其可用于治疗伴有EGFR外显子19缺失或者外显子21替代突变的晚期肺癌患者[13]。临床研究显示,阿法替尼可分别与EGFR上的残基半胱氨酸(cysteine,Cys)797、Erb-B2受体酪氨酸激酶4上的Cys803、Erb-B2受体酶氨酸激酶2上的Cys805以共价的形式相结合,抑制酪氨酸激酶活性,进而导致细胞内酪氨酸残基磷酸化,抑制信号转导,因此其对EGFR突变的肺腺癌具有较强的抗肿瘤作用[14-16]。本研究结果显示,治疗后,与化疗组患者相比,联合组患者糖类抗原199、癌胚抗原、CYFRA21-1水平、Bcl-2 mRNA相对表达水平更低,Bax mRNA相对表达水平更高,临床缓解率和2年存活率更高(P<0.05),提示与单纯培美曲塞+卡铂化疗方案相比较,阿法替尼联合该方案治疗吉非替尼耐药肺腺癌,可更好地抑制肿瘤细胞增殖,降低肿瘤标志物的表达,改善患者预后。
长链非编码RNA的转录本长度大于200 nt,其可经染色质修饰、转录激活、基因组印迹、X染色体的基因沉默、核内转运等方式调控基因的表达,参与肺腺癌的发生和发展,且与患者预后具有一定的相关性[17-18]。目前已经证实SNHG12在多种恶性肿瘤组织(包括肺腺癌组织)中呈高表达,且与患者对多种药物的反应密切相关,可作为此类患者发生多重耐药后的治疗靶点[19-20]。SNHG15属于长链非编码RNA家族中的一员,其可作为内源性竞争RNA,通过与微小RNA结合来促进恶性肿瘤的进展[21]。临床研究显示,SNHG15在肺腺癌中呈高表达,可作为肺腺癌的生物标志物[22]。SNHG16可诱导多种恶性肿瘤细胞的产生,是恶性肿瘤的促癌因子,其在肺腺癌组织中高表达,且与患者的化疗耐药、临床特征密切相关,SNHG16表达量越高患者生存期越短[23-24]。本研究结果显示,治疗后联合组患者的SNHG12、SNHG15、SNHG16相对表达水平较治疗前降低,且低于化疗组(均P<0.05),提示阿法替尼联合培美曲塞+卡铂化疗可能通过抑制SNHG12、SNHG15、SNHG16表达,发挥抑制肿瘤进展、改善患者预后、延长生存期的作用。
本研究结果还显示,采用阿法替尼联合培美曲塞+卡铂化疗方案治疗的患者临床缓解率和2年存活率升高,中位无进展生存期和中位总生存期延长,提示该方案可提高临床疗效,延长患者生存期。采用阿法替尼联合培美曲塞、卡帕化疗方案治疗的患者的毒副反应发生率相对于采用单纯培美曲塞+卡帕化疗方案治疗的患者更高,但差异无统计学意义(P>0.05),表明采用阿法替尼联合培美曲塞、卡帕化疗方案治疗具有较好的安全性。
综上所述,与单纯培美曲塞+卡铂化疗方案相比,阿法替尼联合该方案治疗吉非替尼耐药肺腺癌,可更有效地抑制肿瘤细胞增殖,下调SNHG12、SNHG15、SNHG16表达,从而抑制肿瘤进展,提高临床疗效,延长患者生存期。
