一维TiO2锐钛矿/金红石异相结的制备及光催化降解甲醛性能
2022-03-16查凤娟王建友林雨寒王传义李英宣
查凤娟 刘 庆 王建友 林雨寒 王传义 李英宣*,
(1陕西科技大学环境科学与工程学院,西安 710021)
(2榆林市榆神工业区能源科技发展有限公司,榆林 719302)
甲醛(HCHO)已被世界卫生组织认定为致癌和致畸性物质,是现代室内空气主要的气体污染物之一。某些室内装饰材料、家具、地毯等会持续释放HCHO气体,长期影响室内环境和人体健康[1-2]。因此,如何在室温下高效去除空气中的HCHO是解决HCHO污染问题的关键,也一直是当前气体净化研究领域关注的焦点。虽然金属铂(Pt)纳米粒子可在室温下活化空气中的O2分子,快速将HCHO气体转变为无毒的二氧化碳(CO2)[3-5],但是Pt在自然界中的丰度较低、价格昂贵,限制了其规模化应用。
半导体光催化是以成本低廉、安全绿色的半导体为催化剂,直接利用自然光或人工光源在温和条件下催化氧化还原反应的过程,在空气及水体污染物处理、分解水制氢、CO2还原等环境和能源领域具有明显的竞争优势[6-13],而利用光催化技术将空气中的HCHO降解为无毒的CO2更是引发了人们的广泛关注[14]。迄今为止,有超过100种光催化材料被报道[15],其中,二氧化钛(TiO2)由于具有光催化活性强、化学稳定性好、环境友好和成本廉价等优点而成为光催化领域的研究焦点,也被广泛地用于HCHO的光催化降解的研究中[16]。但是,传统的TiO2制备方法仍然存在着反应温度过高、合成中加入腐蚀性或有毒试剂、可控制备难以实现等问题,严重限制了TiO2光催化活性的进一步提高和大规模应用[17-19]。因此,低温、可控、“绿色”制备TiO2仍然是一个挑战。
TiO2主要有锐钛矿、金红石、板钛矿3种晶型[20],其中锐钛矿和金红石均为四方结构,在光催化反应中应用最为广泛[21]。研究发现纯相TiO2电荷分离的效率低,光催化活性不能够满足实际应用的需求[22]。目前通常采用金属掺杂[23]、半导体复合[24]、金属负载[25]、形貌与晶面调控[26]、异相结构建[27]等手段提高TiO2的光催化活性。其中异相结的构建被认为是一种低成本、简单、有效地提高TiO2光催化活性的方法[28-30],其原理是将同一种半导体的2种物相进行复合,当2种不同的物相紧密接触时就会形成异相结。由于2种物相能带结构的差异会在异相结的两侧形成空间电势差和内建电场,从而加速光生电子-空穴对的分离,进而提高半导体的光催化活性。李灿等通过将锐钛矿相TiO2沉积到金红石相表面构建了锐钛矿/金红石异相结,并发现其光催化分解水制氢的效果得到显著提高[31]。张晓东等通过高温(600℃)煅烧合成的锐钛矿/金红石异相结TiO2在光催化降解气态甲苯和液相四环素的过程中表现出较好的活性[32]。
除了构建异相结外,合理调控TiO2的形貌也被认为是一种提高其光催化活性的有效方法,其中一维(1D)纳米结构的TiO2因具有高的比表面积、可控的结构和快速的电子传递速率等优点,在光催化领域引起了研究者的广泛关注[33]。目前,通过简单、方便的方法构建一维纳米TiO2异相结材料的报道还十分有限[34]。我们采用一步水热法,在较低温度下(180℃)成功制备出了一维TiO2锐钛矿/金红石异相结,并通过调节水热时间实现了异相结中锐钛矿和金红石含量的调控。实验结果表明,180℃下水热24 h制备的TiO2在光催化氧化HCHO方面表现出了最佳的性能:在光强为12.26 mW·cm-2的365 nm LED灯照射下,120 mg·L-1HCHO气体25 min内的降解率为92%。这种简单、温和制备一维TiO2异相结的方法为开发基于TiO2的廉价、高效光催化材料提供了新思路。
1 实验部分
1.1 试剂与仪器
1.1.1 实验试剂
实验所用化学药品均为分析纯。二(2-羟基丙酸)二氢氧化二铵合钛(C6H18N2O8Ti)购自成都化夏化学试剂有限公司,无水乙醇购自天津市天力化学试剂有限公司,HCHO购自阿达玛斯试剂有限公司。
1.1.2 实验仪器
主要仪器:在线光声红外多气体监测仪(INNOVA Air Tech Instruments model 1412);X 射线衍射仪(XRD,德国Bruker,D8-advance,Cu Kα射线,λ=0.154 18 nm,工作电流为30 mA,工作电压为40 kV,扫描角度为20°~80°);扫描电子显微镜(SEM,日本Hitachi公司,S4800,电子枪为冷场发射电子源,加速电压为0.5~30 kV);透射电子显微镜(TEM,日本电子公司出产的JEOLJEM-2100F,加速电压为200 kV);物理吸附仪(美国麦克默瑞提克仪器有限公司,ASAP 2460);紫外可见漫反射(日本岛津公司,UV-2600);电化学工作站(上海辰华公司,CHI660E);光催化反应釜。
1.2 催化剂的制备
室温下,在100 mL聚四氟乙烯内衬中加入70 mL去离子水,再加入2 mL C6H18N2O8Ti,搅拌30 min,接着将该内衬装入水热反应釜内,放入烘箱中,于180 ℃下分别水热反应10、14、24、36 h,然后取出冷却至室温后倒去上清液,样品用无水乙醇和去离子水各洗涤3次,最后置于60℃恒温干燥箱中烘干,即可得到一维TiO2异相结催化剂。不同时间制备的催化剂分别记为TiO2-10、TiO2-14、TiO2-24和TiO2-36。
1.3 电化学测试及光催化降解HCHO性能测试
采用典型的三电极体系(饱和甘汞电极、铂网以及涂有催化剂的导电玻璃分别作为参比电极、对电极和工作电极,0.5 mol·L-1Na2SO4溶液为电解液),在带有石英窗口的电解池中测量光电流响应值(以波长为365 nm的LED灯作为光源)和电化学阻抗谱。
光催化降解HCHO实验是在密闭的不锈钢反应器(带有石英窗口)中进行,反应器体积约为300 mL,光源为100 W的365 nm LED灯。将0.25 mg样品与5 mL超纯水充分混合后,均匀旋涂在玻璃片上,再在60℃的烘箱中干燥后置于反应器中。用微量进样器向反应器中注入气态HCHO和O2的气体混合物(气态HCHO是由固体HCHO在120℃下进行挥发得到的),然后在磁力搅拌器的不断搅拌下进行HCHO氧化的性能测试。在循环实验之前将反应后的TiO2粉末在100℃下加热60 min,去除吸附的HCHO分子,再重复进行HCHO催化氧化实验。HCHO的起始浓度为120 mg·L-1左右,暗吸附30 min达到吸附-脱附平衡,然后开灯反应50 min。通过在线光声红外多气体监测仪测定HCHO浓度的变化。HCHO的降解率(η)用下式计算:

其中,c0为初始浓度,ct为实时浓度。
2 结果与讨论
2.1 催化剂形貌结构分析
采用XRD对不同水热反应时间制备的TiO2晶体结构进行了测定,结果如图1所示,水热不同时间得到的TiO2的XRD峰分别与标准卡片PDF No.21-1272(锐钛矿相TiO2)和PDF No.21-1276(金红石相TiO2)的位置相匹配,其中 2θ=25.3°、37.8°、48.1°、53.9°和62.7°的衍射峰分别对应锐钛矿相TiO2的(101)、(004)、(200)、(105)和(204)晶面。而 2θ=27.4°、36.1°、41.2°、44.1°、54.2°、56.6°、64.0°和69.8°的衍射峰则分别对应金红石相 TiO2的(110)、(101)、(111)、(210)、(211)、(220)、(310)和(112)晶面。XRD测试证明制备的TiO2是由锐钛矿和金红石两相组成的混合相。对于制备的不同TiO2的异相结中不同相的含量可通过公式2进行计算[35-36]:

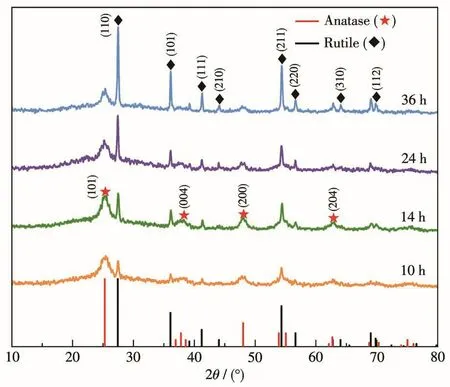
图1 不同水热时间下制备的TiO2的XRD图Fig.1 XRD patterns of TiO2prepared at different hydrothermal times
其中 I1和 I2分别为 27.4°(金红石相)和 25.3°(锐钛矿相)的XRD峰强度,w1和w2分别为金红石相TiO2和锐钛矿相TiO2的质量分数。通过计算可知,在水热反应 10、14、24和36 h的条件下,锐钛矿相TiO2在TiO2-10、TiO2-14、TiO2-24和TiO2-36中的占比分别为51%、49%、33%和23%。如图1所示,归属为金红石相TiO2的衍射峰峰形尖锐,而归属为锐钛矿相TiO2的衍射峰较宽,说明锐钛矿相TiO2在异相结中的粒径较小,其粒径尺寸可以根据谢乐公式3计算:

其中,D为粒径尺寸,λ为X射线波长(通常取0.154 nm),β为半峰宽(弧度),θ为相应的衍射角。计算得到锐钛矿相TiO2纳米粒子的平均粒径为(9.5±0.5)nm。
为了研究TiO2催化剂的形貌和微观结构,对TiO2-24进行了TEM测试。从图2a的低倍TEM照片可以看出,制备的TiO2样品是由整体分布比较均匀、表面略显粗糙的一维纳米棒构成,纳米棒的长度为(400±50)nm,直径为(60±5)nm。从放大后的TEM照片(图2b)可以清楚地发现纳米棒的表面均匀、高密度地负载了大量的纳米颗粒,纳米颗粒粒径分布均一(约10 nm)。TiO2-24的高分辨透射电镜(HRTEM)照片如图2c所示,可以清楚地看到存在2组不同的晶格条纹,表面纳米粒子的(红色圈示意)晶格条纹间距为0.35 nm,对应锐钛矿相TiO2的(101)晶面,说明纳米粒子为锐钛矿相TiO2,这一结果与XRD结果相符合。黄色矩形标记的晶格条纹间距为0.32 nm,对应金红石相TiO2的(110)晶面[37],结合XRD的结果证明纳米棒的主体为金红石相TiO2,表面纳米粒子的结构主要为锐钛矿相TiO2,进一步证明了一维锐钛矿/金红石异相结的成功构建。通过图2c还可以发现,锐钛矿相与金红石相TiO2之间形成了紧密接触界面,这为载流子的转移提供了方便。此外,负载在一维纳米棒上的锐钛矿相纳米粒子会增加材料表面的粗糙度,有利于入射光的散射,使材料对光的吸收增强,进而提高其光催化活性[38]。

图2 TiO2-24的(a)低倍照片、(b)高倍TEM照片和(c)HRTEM照片Fig.2 (a)Low-magnification TEM image,(b)high-magnification TEM image,and(c)HRTEM image of TiO2-24
2.2 紫外可见漫反射吸收光谱
样品的光吸收特性是影响光催化活性的一个重要因素,通过紫外可见漫反射吸收光谱研究了不同水热时间制备的异相结TiO2光催化剂对光的吸收性能。从图3中可以观察到,所有异相结TiO2样品在400 nm以内的紫外光区都有良好的响应。TiO2样品的禁带宽度通过经验公式4计算获得[39]:

其中α是吸收系数,hν是光子能量,A为常数,Eg为半导体禁带宽度。如图3中插图所示,通过外推切线,TiO2-10、TiO2-14、TiO2-24、TiO2-36曲线的横截距(即样品的带隙值)分别为 2.79、2.75、2.75、2.78 eV,均低于文献报道的块状TiO2(锐钛矿为3.2 eV,金红石为3.0 eV)[40]的带隙值,这可能是因为一维TiO2锐钛矿和金红石异相结的成功构建,使样品的能带结构变窄[32]。该结果表明构建的一维TiO2锐钛矿/金红石异相结明显提高了电子-空穴对的分离效率,使光激发产生的电子-空穴对更容易到达催化剂的表面。
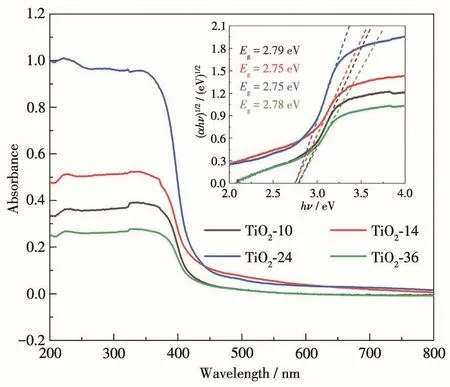
图3 TiO2样品的紫外可见漫反射吸收光谱及(αhν)1/2-hν曲线Fig.3 UV-Vis diffuse reflectance absorption spectra of TiO2samples and(αhν)1/2-hν curves(Inset)
2.3 TiO2光催化降解HCHO性能测试
通过测试不同TiO2样品的光催化降解HCHO性能,来评价其光催化活性。不同样品降解HCHO过程中,HCHO浓度的降低和相应CO2浓度的增加情况分别如图4a和4b所示。在光催化剂作用下,反应系统中的HCHO浓度不断降低(图4a),同时CO2浓度不断增加(图4b),表明所制备的TiO2催化剂均能在室温下将HCHO氧化为CO2。图4a和4b表明不同的催化剂在室温下的光催化氧化HCHO性能明显不同,25 min后在 TiO2-10、TiO2-14、TiO2-24和TiO2-36催化剂作用下HCHO浓度从120.0 mg·L-1分别下降到了 47.0、38.0、10.0及 61.5 mg·L-1,ΔcCO2(实验过程中CO2浓度相对实验前浓度的差值)也相应地增加至69.0、80.5、105.0及52.0 mg·L-1。可见催化剂TiO2-24对HCHO的降解率最高,25 min后达到了92%。
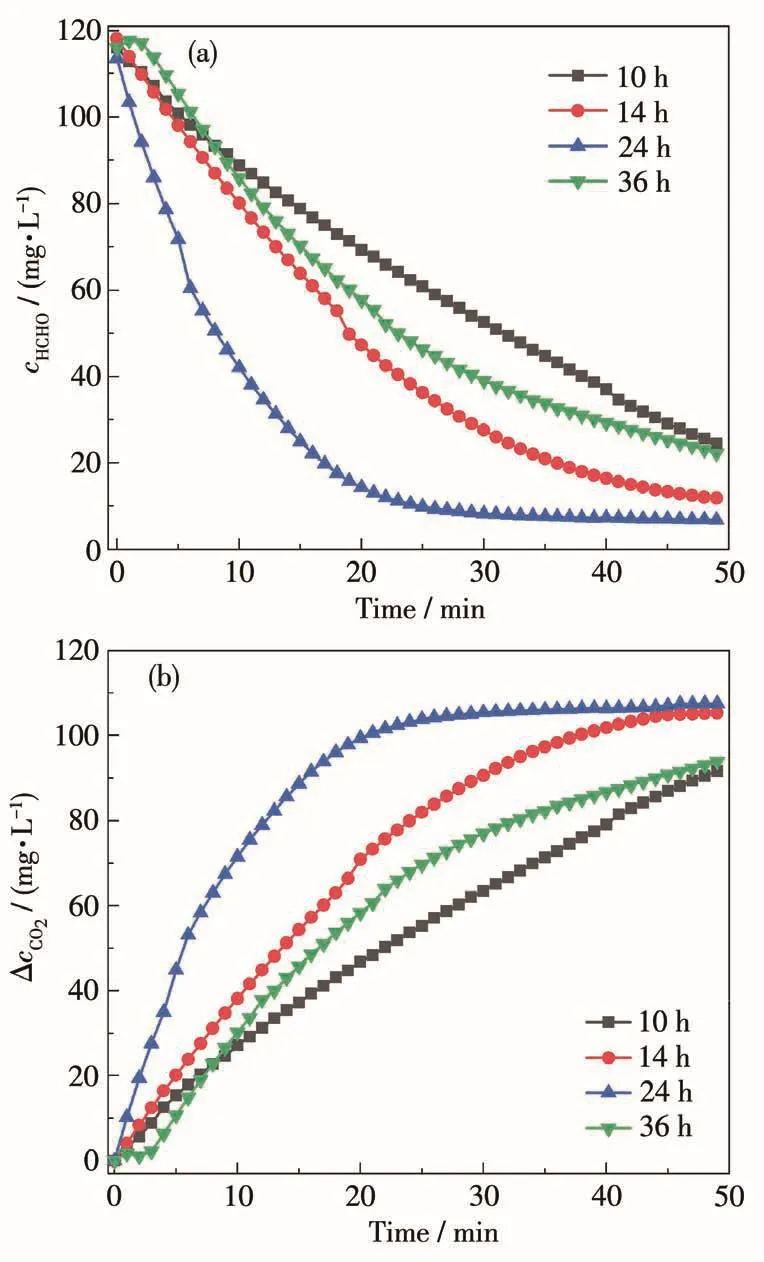
图4 TiO2样品在催化氧化HCHO实验过程中HCHO浓度(a)与ΔcCO2(b)随反应时间的变化曲线Fig.4 Changes of HCHO concentration(a)andΔcCO2(b)as a function of reaction time on TiO2samples
为了探究该系列材料光催化性能提高的影响因素,测试了TiO2-10、TiO2-14、TiO2-24和TiO2-36的N2吸附-脱附等温线(图5)。根据BDDT(Brunauer-Deming-Deming-Teller)分类[41],所有样品的吸附-脱附曲线都是典型的Ⅳ型吸附等温线,具有H3型回滞环,表明介孔结构的存在。根据吸附等温线,TiO2-10、TiO2-14、TiO2-24和TiO2-36的BET(Brunauer-Emmett-Teller)比表面积(SBET)分别为45、42、30和29 m2·g-1。样品的SBET随着水热时间延长逐渐降低,这可能与材料发生团聚有关。结合图4的催化活性结果,可以证实比表面积不是影响TiO2异相结降解HCHO性能的主要因素。因此,异相结中不同相的比例应该是导致该类材料性能差异的主要原因。
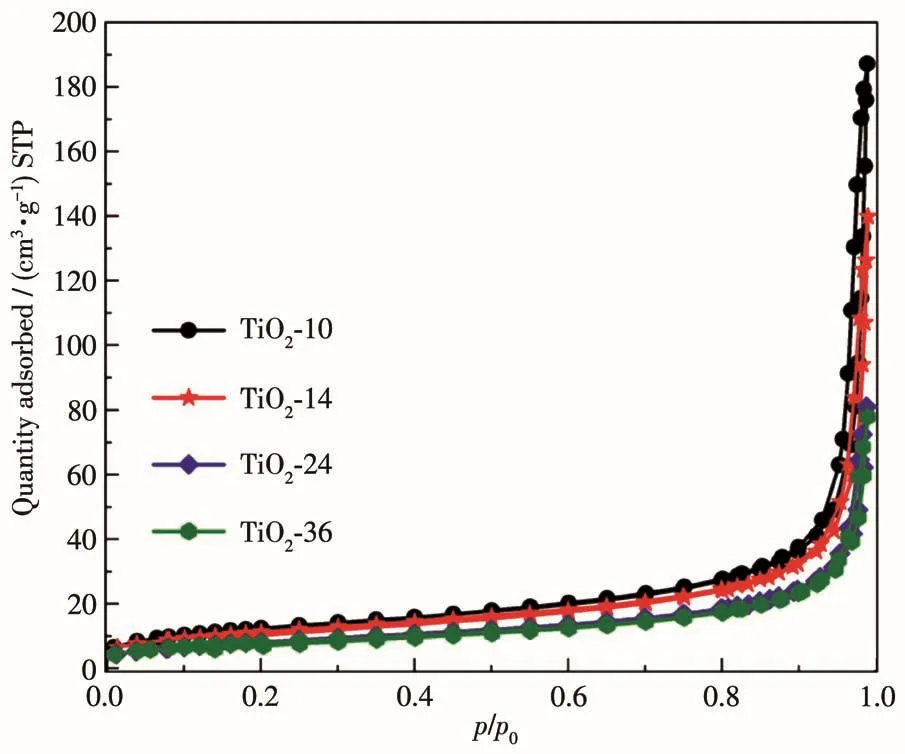
图5 TiO2-10、TiO2-14、TiO2-24和TiO2-36的N2吸附-脱附等温线Fig.5 N2adsorption-desorption isotherms of TiO2-10,TiO2-14,TiO2-24,and TiO2-36
催化剂的稳定性和循环性在实际应用中至关重要。图6为TiO2-24光催化剂在室温下光催化氧化HCHO的循环性能。从图中可以观察到TiO2-24光催化剂在5次循环实验后,HCHO的减少量和相应的CO2增加量均没有明显的变化,即该样品对HCHO的降解率仍然维持在92%左右,这表明TiO2-24催化剂具有良好的光催化活性和化学稳定性,在室温光催化降解室内空气中HCHO方面具有一定的应用前景。
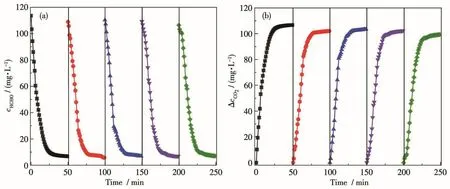
图6 TiO2-24在5次循环试验中HCHO浓度(a)和ΔcCO2(b)随时间的变化曲线Fig.6 Changes of HCHO concentration(a)andΔcCO2(b)as a function of reaction time for TiO2-24 in five repeated tests
2.4 光催化反应机理
为了研究TiO2催化剂在受到光激发后产生的光生电荷的迁移和复合情况,在室温下测试了TiO2-10、TiO2-14、TiO2-24和TiO2-36的稳态荧光和时间分辨荧光光谱。图7a为所有TiO2催化剂在激发波长为325 nm时的稳态荧光谱图,其中,TiO2-24的荧光强度最低,说明TiO2-24的光生电荷复合率最低,荧光谱图的强度顺序为TiO2-36>TiO2-10>TiO2-14>TiO2-24,该顺序与催化剂光催化活性的顺序一致。图7b为锐钛矿/金红石异相结TiO2的荧光寿命光谱图,根据公式5可得到荧光寿命:
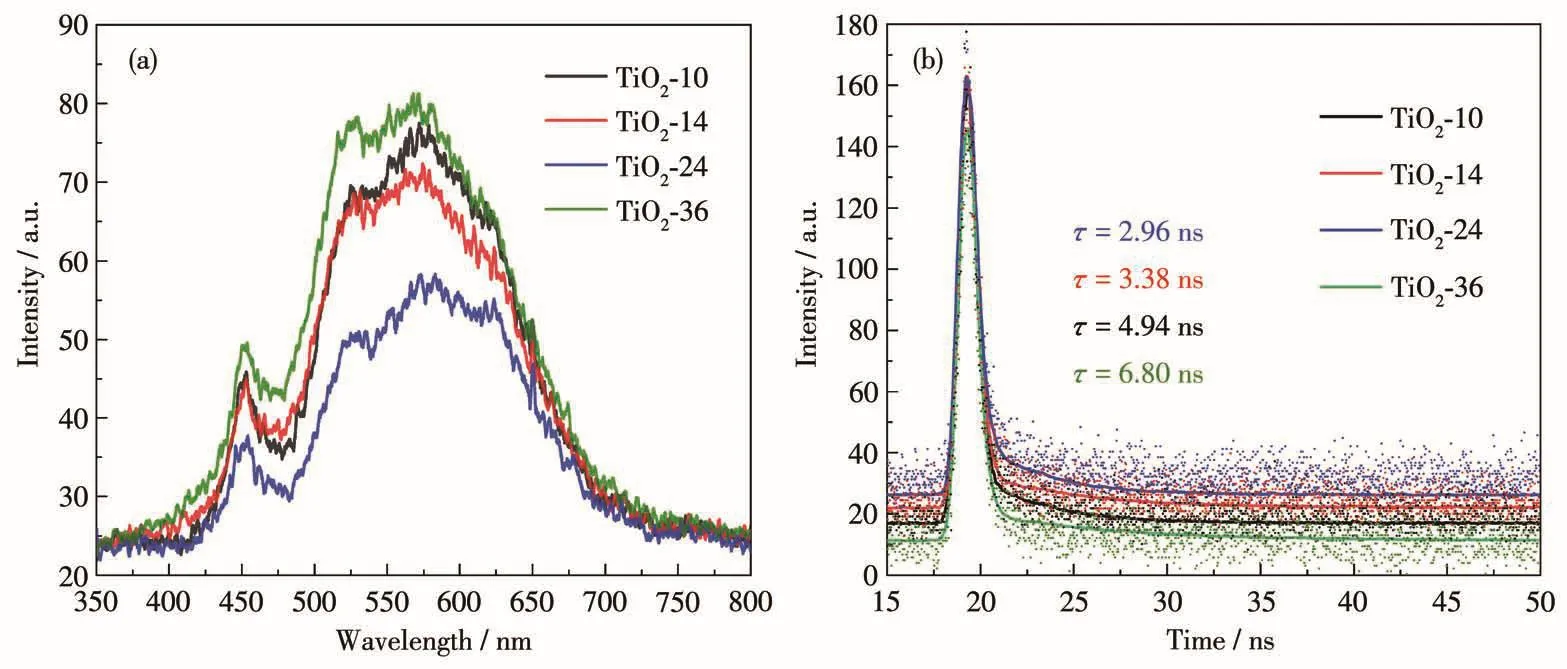
图7 TiO2样品的(a)稳态荧光光谱图和(b)时间分辨荧光光谱图Fig.7 (a)Steady-state fluorescence spectra and(b)time-resolved fluorescence decay spectra of TiO2samples
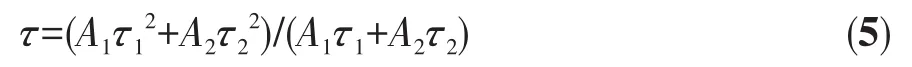
其中,τi(i=1、2)为寿命,Ai为指数衰减拟合的振幅。计算得到 TiO2-24 的平均寿命(τ)为 2.96 ns,短于TiO2-10(4.94 ns)、TiO2-14(3.38 ns)和 TiO2-36(6.80 ns)的寿命。这是由于TiO2-24的光诱导电荷可以从金红石相TiO2上通过紧密接触的界面快速有效地转移到锐钛矿相TiO2表面[42],这表明制备的异相结TiO2-24具有较高的载流子分离和迁移效率。
为进一步探究TiO2的光电化学性质,分别对不同TiO2样品进行了光电流和电化学阻抗测试,结果如图8a和8b所示。从图8a中可以看出,TiO2-24(6.1µA·cm-2)的光电流强度明显高于TiO2-10(4.6µA·cm-2)、TiO2-14(5.8 µA·cm-2)和 TiO2-36(3.8 µA·cm-2),这表明异相结TiO2-24对光生电子-空穴对的分离效果最好。此外,Nynquist曲线如图8b所示,异相结TiO2-24的弧半径小于TiO2-10、TiO2-14和TiO2-36的半径,同样表明异相结TiO2-24具有最优的电荷分离效率。以上(光)电化学性能测试结果与光催化降解HCHO活性测试结果一致,说明光生电荷的高效分离和快速转移是TiO2异相结光催化降解HCHO性能提高的关键因素。
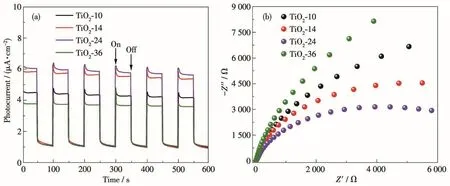
图8 TiO2样品的(a)瞬态光电流响应图和(b)Nyquist曲线Fig.8 (a)Transient photocurrent responses and(b)Nyquist plots of TiO2samples
自2018年余家国教授提出了梯型(S-scheme)异质结光催化机制以来,该机制受到了广泛关注。我们推测本研究中一维TiO2锐钛矿/金红石异相结的光催化氧化HCHO的机理也符合梯型异质结机制[43]。一维TiO2锐钛矿/金红石异相结光催化降解HCHO的可能反应机理如图9所示(图中Ef表示的是费米能级)。锐钛矿和金红石的禁带宽度分别为3.2和3.0 eV[41],金红石和锐钛矿相TiO2的价带(VB)和导带(CB)相对位置如图9a所示[44],该异相结锐钛矿相TiO2具有更高的VB电位,属于氧化型半导体光催化剂,而金红石结构的TiO2具有更低的CB电位,可作为还原型半导体光催化剂。当2种不同结构的TiO2发生紧密接触(图9b)形成异相结后,电子从费米能级高的金红石结构的TiO2流入费米能级低的锐钛矿相TiO2,使金红石相TiO2的能带向上弯曲,形成正电荷聚集区域,与此同时,锐钛矿相TiO2得到电子,使其带边向下弯,形成负电荷聚集区域,进而在2种不同结构TiO2界面处形成一个内建电场,有利于形成电子传输通道。如图9c所示,在紫外光照射下,锐钛矿和金红石均被激发产生光生电子(e-)-空穴(h+)对。由于内建电场的存在,锐钛矿相TiO2的光生电子穿过界面迁移至金红石相TiO2的VB,使电子和空穴分别聚集于金红石相TiO2和锐钛矿相TiO2氧化还原活性位点,大幅提高光生电荷的利用率。空穴在锐钛矿相TiO2表面与吸附的HCHO分子发生反应,最终将HCHO氧化成无毒无害的CO2,电子聚集在金红石相TiO2与吸附的O2发生还原反应生成·O2-,随后可能还会继续与H+反应生成HO2·等。HCHO光催化降解过程中可能发生的氧化还原反应可以用下列方程式表示[45-46]:
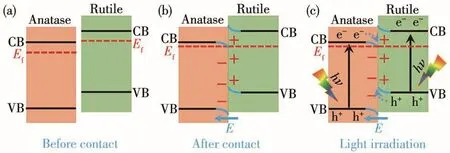
图9 异相结TiO2光催化降解HCHO机理示意图Fig.9 Mechanism diagram of photocatalytic degradation of formaldehyde by TiO2heterophase junction

氧化反应:
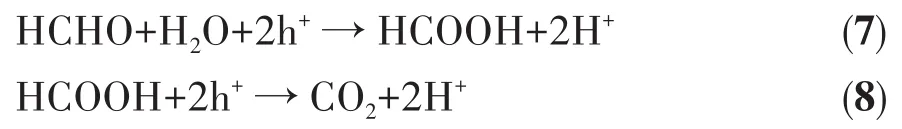
还原反应:

3 结论
采用简单、可控的一步水热法在较低温度下成功合成了一维的含量可控、界面紧密接触的锐钛矿/金红石异相结TiO2,其中水热时间为24 h、锐钛矿相含量为33%的催化剂TiO2-24在HCHO的光催化降解HCHO中表现出最优的性能。在波长为365 nm,光强为12.26 mW·cm-2的LED灯照射下,浓度约为120 mg·L-1的HCHO气体在反应器内反应25 min后,HCHO矿化为CO2的降解率达到了92%。TiO2-24催化剂的高活性被认为与以下两方面有关:(1)通过形貌调控,粒径分布均匀的锐钛矿相TiO2纳米粒子高密度、单分散地负载在金红石相TiO2纳米棒上,这种界面结构增加了反应的活性位点,增强了光吸收能力,同时异相结之间的紧密接触也有利于光生电荷的传输;(2)异相结结构对电荷的分离具有定向驱动作用,使催化剂具有更高效的光生电荷分离和传输效率。本实验采用的简单、可控、温和的异相结制备方法为TiO2光催化剂的广泛应用奠定了基础,为光催化氧化HCHO提供了一种可行的解决方案。
