不同品牌校准品对血清碱性磷酸酶检测结果可比性的影响
2022-03-14林斐然欧元祝刘文彬虞啸炫葛丹红
林斐然,欧元祝,刘文彬,虞啸炫,葛丹红,赵 冉
(上海市临床检验中心,上海 200126)
碱性磷酸酶(alkaline phosphatase,ALP)水平是诊断和鉴别诊断骨骼、肝胆系统疾病的常用指标,其检测结果的准确性对疾病诊断和预后管理至关重要。国家卫生健康委临床检验中心正确度验证计划和上海市临床检验中心正确度验证计划结果均显示,ALP正确度验证计划合格率一直较其他酶学项目低[1]。
国际临床化学和检验医学联合会于2011年正式公布了ALP酶学国际参考方法[2]。基于参考测量程序,体外诊断试剂厂商可通过连续溯源链赋值,将测量结果准确传递给校准品。但是,传递过程中偏差的引入和校准品中的化学物质都有可能影响各检测系统检测结果的准确性和不同检测系统检测结果的可比性。本实验室以AU校准品、C.f.a.s.校准品、ALP国家二级标准物质[GBW(E)090920 ALP血清(液体)标准物质,简称标准物质]作为校准品,通过对比、分析使用不同校准品校准后的ALP检测结果,为进一步开展血清ALP检测标准化工作和临床检验结果互认提供参考。
1 材料和方法
1.1 样本来源
收集上海交通大学医学院附属仁济医院新鲜血清样本25例,覆盖低、中、高浓度;另收集2018年第2次上海市临床检验中心5个浓度水平常规化学室间质量评价样本。
1.2 仪器与试剂
美国贝克曼库尔特公司AU5800全自动生化分析仪(简称AU5800)及配套试剂(批号5728)、校准品(批号1120,溯源性Beckman Master Calibrator,冻干粉),瑞士罗氏公司cobas c501全自动生化分析仪(简称c501)及配套试剂(批号337631)、校准品[批号25013301,溯源性Original formulation IFCC5(1983),冻干粉]。ALP国家二级标准物质GBW(E)090920[标准值222.6 U/L,扩展不确定度(k=2)为5.6 U/L;溯源性Original formulation IFCC9(2011);冰冻人血清]。
1.3 方法
使用c501配套C.f.a.s.校准品和标准物质对c501的ALP项目进行校准,分别为罗氏配套系统和标准物质-c501系统;使用AU5800配套校准品和标准物质对AU5800上的ALP项目进行校准,分别为AU5800配套系统和标准物质-AU5800系统;见表1。校准通过后,检测25例新鲜血清样本和5个浓度水平室间质量评价样本,每个样本测定2次,计算均值。以标准物质校准后的检测值为参比系统,采用Excel软件分别计算c501配套系统与标准物质-c501系统检测结果均值之间的相对偏移、相关性和AU5800配套系统与标准物质-AU5800系统检测结果均值之间的相对偏移和相关性。以样本序号为X轴,相对偏移为Y轴,绘制散点图。

表1 检测系统具体情况
使用标准物质、C.f.a.s.校准品、AU校准品分别对2台仪器的ALP项目进行校准。校准通过后检测25例新鲜血清样本及5个浓度水平室间质量评价样本,每个样本测定2次,计算均值。以c501检测值为参比系统,用Excel软件计算2台仪器检测值之间的相对偏移、相关性(标准物质-c501系统与标准物质-AU5800系统、c501配套系统与C.f.a.s.-AU5800系统、AU校准品-c501系统与AU5800配套系统、c501配套系统与AU5800配套系统),以样本序号为X轴,相对偏移为Y轴,绘制散点图。
2 结果
2.1 不同系统检测结果
c501配套系统与标准物质-c501系统、AU5800配套系统与标准物质-AU5800系统的相关性良好(r值)均>0.999。两两系统间偏移均<10%,c501配套系统与标准物质-c501系统比较均为负偏移,AU5800配套系统与标准物质-AU5800系统比较均为正偏移,室间质量评价样本与临床血清样本的相对偏移均无明显差异。见表2、图1。
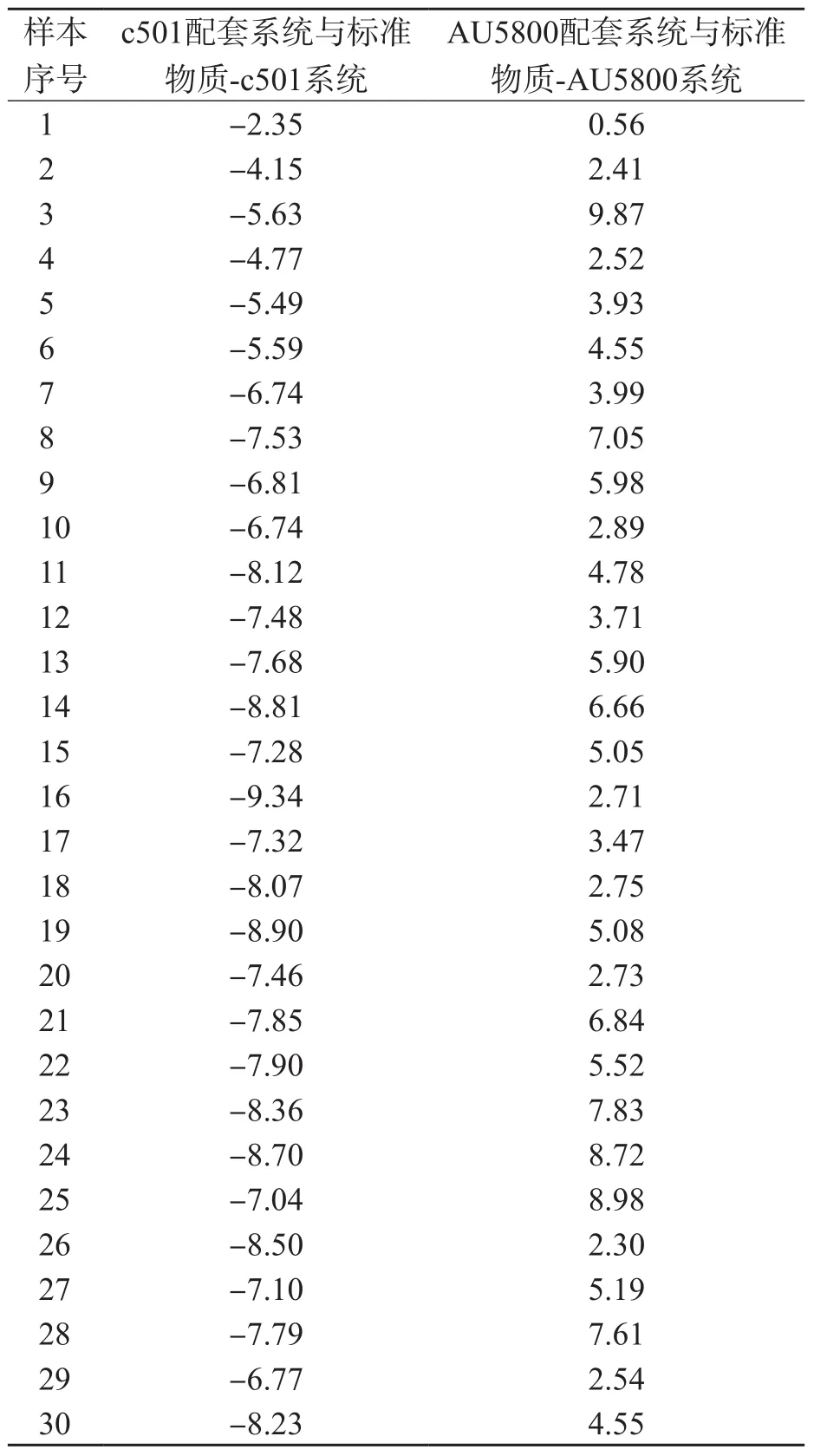
表2 各配套系统与以标准物质为校准品的检测系统ALP检测结果的相对偏移 %
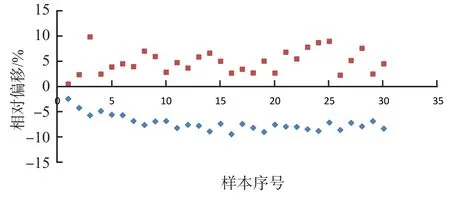
图1 各配套系统与以标准物质为校准品的检测系统的相对偏移分布
2.2 不同标准物质校准后2台仪器检测结果
使用标准物质、C.f.a.s.校准品、AU校准品分别校准c501和AU5800,2个系统之间ALP检测结果相关性良好(r值均>0.999)。使用标准物质校准后,2个系统临床血清样本检测结果的相对偏移在±4%以内,而室间质量评价样本检测结果的相对偏移为9%~16%。使用C.f.a.s.校准品校准后,检测临床样本时,2个系统临床血清样本检测结果的相对偏移为负偏移(18%~25%),室间质量评价样本检测结果的相对偏移为负偏移(7%~10%)。使用AU校准品校准后,检测临床样本时,2个系统临床血清样本检测结果的相对偏移为负偏移(-22%~-14%),室间质量评价样本检测结果的相对偏移为负偏移,缩至-10%~-4%。使用配套校准品校准后,检测临床样本时,2个系统偏移为正偏移(3%~17%),检测室间质量评价样本时,增至25%~31%。见表3、图2。
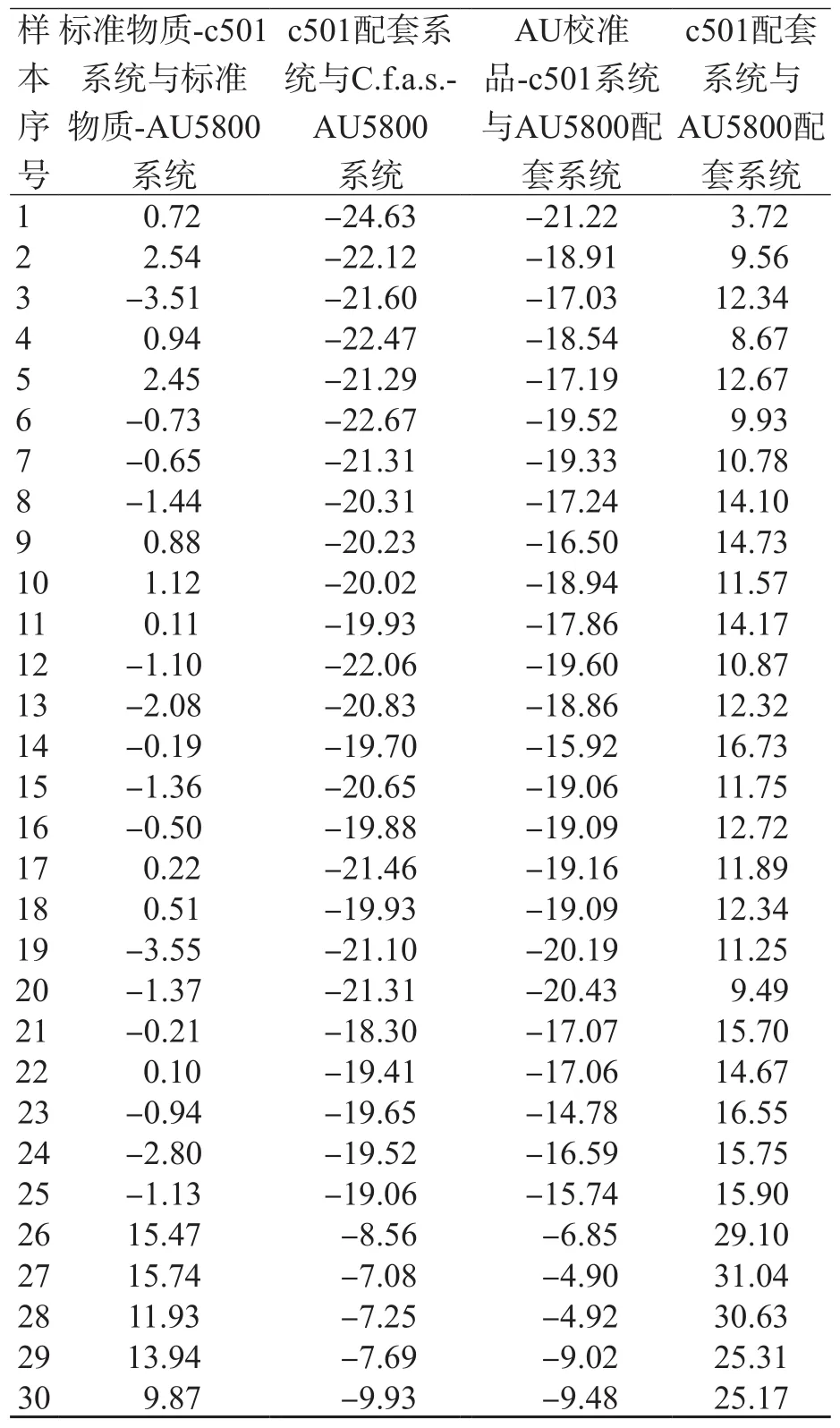
表3 不同校准品校准的检测系统间ALP检测结果的相对偏移 %
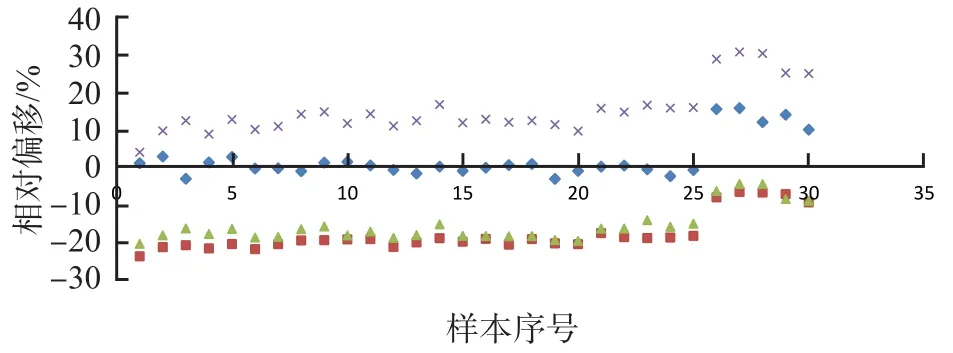
图2 不同校准品校准的检测系统间偏移分布图
3 讨论
在不同ALP检测系统之间,影响检测结果的主要因素是缓冲液种类和试剂配方[3]。目前,商品化ALP试剂品牌较多,统计近几年上海市临床检验中心和国家卫生健康委临床检验中心室间质量评价上报的ALP试剂信息和检测方法,以及不同品牌的ALP试剂说明书,发现国内90%以上,上海100%都是基于国际临床化学和检验医学联合会推荐的方法,使用2-氨基-2-甲基-1-丙醇缓冲液。进一步分析上海市临床检验中心ALP室间质量评价和正确度验证统计结果,截至2020年,均值差异最大且呈规律性差异的主要为瑞士罗氏公司试剂和美国贝克曼库尔特公司试剂。体外诊断试剂检测系统准确性需通过校准品的不间断比较链进行量值传递。校准品量值传递的有效性、可靠性是厂商保证其检测结果准确、可追溯的重要工具[4]。基于临床实验室ALP试剂使用情况,从校准品角度出发,本研究选取了具有代表性的AU5800系统配套校准品、c501系统配套C.f.a.s.校准品和标准物质,通过分析不同品牌、基质校准品对临床血清样本和室间质量评价样本ALP检测结果可比性影响,为进一步开展血清ALP检测标准化工作和临床结果互认提供参考。
本研究结果显示,检测临床血清样本时,使用各检测系统配套校准品校准,与使用标准物质校准结果相比较,c501配套系统呈负偏移,AU5800配套系统呈正偏移,与国家卫生健康委临床检验中心正确度验证结果和意大利的一项研究结果一致[1,5]。标准物质是溯源到2011年ALP酶学参考方法,已知2011的ALP推荐程序与1983年Tietz方法(30 ℃)[6]相比,改变了2-氨基-2-甲基-1-丙醇浓度和测量温度(从30 ℃到37 ℃)。本研究所使用的C.f.a.s.校准品是溯源至1983年的方法,美国贝克曼库尔特公司宣称AU校准品可溯源至Master校准物,可追溯性尚不明确,这可能是导致2个系统检测结果偏移的主要原因,目前瑞士罗氏公司已逐渐将中国市场的校准品溯源调整至国际临床化学和检验医学联合会(37 ℃)的方法。本研究发现,使用标准物质校准与使用配套校准品校准相比,c501和AU5800 ALP血清样本检测值相对偏移由约15%降至±4%。而2台生化分析仪即使使用相同厂商校准品,相对偏移依然不能缩小,且超过了使用各自配套系统校准品校准后的相对偏移。使用C.f.a.s.校准品校准后,AU5800检测值较c501检测值更低,而使用AU校准品校准后,c501检测值较AU5800检测值更高,使得配套系统校准品校准时为正偏移,而2台仪器使用相同厂商校准品校准时,却均为负偏移。校准品只能专用于指定型号仪器、试剂、方法和检测程序组成的检测系统,才能发挥其校准和溯源作用[7]。可见,使用非配套校准品会为检测结果引入更大偏差,无法互通。罗氏公司和贝克曼库尔特公司试剂采用的都是国际临床化学和检验医学检测值联合会推荐的方法,以2-氨基-2-甲基-1-丙醇作为缓冲液。虽然成分用量略有不同,但是使用具有互换性的标准物质校准后,2个检测系统检测结果的偏移是可以被明显缩小的。有文献指出,为了使校准品能更稳定,实验室进行了更多前处理,以去除更多血清中的成分,这样的参考物质与患者新鲜血清样本的互换性产生了严重问题[8]。本研究2个品牌的校准品虽然也是人血清基质,但附加了化学添加物及非人类来源相关酶,存在基质效应,无法用于非配套检测系统。而标准物质为冰冻人血清,减少了杂物引入,降低了校准品传递过程中基质效应的影响,且通过了互换性评价,使得2个检测系统检测结果偏移缩小,更有利于各检测系统和实验室间检测结果一致性和可比性。
本研究结果显示,室间质量评价样本检测结果与临床血清样本比较,呈现出一些不同,使用配套系统校准与标准物质校准后的偏移结果同检测血清样本结果基本保持一致;但使用配套校准品分别校准后,相对偏移几乎是校准纯血清时的2倍,使用标准物质校准后,相对偏移有所缩小,但仍比校准纯血清时偏移要大,有基质效应的室间质量评价样本放大了2个系统间的相对偏移,也说明只有具有互换性的室间质量评价样本才能真实反映检测系统间的差异。而使用非配套校准品同时校准2台仪器后,相对偏移反而缩小到10%以内,可能是因为校准品和室间质量评价样本同为处理过的血清物质,均为冻干品,基质效应的影响反而有所缩减。提示有基质效应的室间质量评价样本并不能完全展示各系统的真实检测结果,有可能会放大或缩小系统间差异。
综上所述,血清ALP检测标准化以及临床结果互认工作任重而道远。人血清ALP测定的常规程序中主要使用的是2-氨基-2-甲基-1-丙醇和二乙醇胺[9]。近几年,国家卫生健康委临床检验中心和上海市临床检验中心上报的试剂信息统计结果显示,我国临床实验室采用的ALP检测方法基本统一,都是基于国际临床化学和检验医学联合会推荐的方法,缓冲液为2-氨基-2-甲基-1-丙醇。虽然国际临床化学和检验医学联合会于2011年正式公布了ALP酶学国际参考方法,但2个品牌ALP检测试剂并没有及时更新为新的国际参考方法。此外,使用具有溯源性和互换性的血清参考物质作为校准品,能大大提高不同检测系统间检测结果的准确性和可比性,有利于不同实验室间检测结果的标准化和一致性。而多数商品化校准品存在基质效应,未经互换性评价,仅服务于指定配套检测系统,无法互通。由于缺乏可交换性,使用通用物质进行校准,并不会促成检测结果的一致性[10]。试图通过使用同一品牌校准品校准未经验证的不同检测系统,而达到不同检测系统间结果一致性的方法不可取。临床实验室在日常工作中,应尽可能选用经验证、有溯源性的配套校准品,建立实验室的参考区间,以保证检测结果的准确、可靠。临床实验室作为检测系统的终端用户,必须确保其使用的校准品可追溯到最高水平[9]。使用无基质效应血清样本的正确度验证计划与使用含有基质效应的室间质量评价可以更准确地反应不同系统间检测结果的差异。为了提高ALP检测结果的准确性和可比性,还需要试剂厂商、临床实验室和各级临床检验中心的共同努力。
