磷酸锂渣制备电池级碳酸锂工艺研究
2022-03-11郭春平周有池文小强刘雯雯黄叶钿
郭春平,周有池,文小强,刘雯雯,洪 侃,黄叶钿
(赣州有色冶金研究所有限公司,江西赣州 341000)
锂及其化合物作为21世纪能源和轻质合金的理想原材料,在宇航、冶金、轻工、石油化工、电子、橡胶、玻璃、陶瓷、医疗等高科技及传统工业领域得到广泛应用,被称为“能源金属”和“推动世界前进的重要元素”[1-4]。其中碳酸锂作为锂的主要无机化合物之一,是制备各种锂化合物的关键原料[5-6]。近年来,随着锂电产业的蓬勃发展,锂的需求量呈现爆发性增长[7-8]。根据国家统计局资料,2020年末中国新能源汽车保有量达492万辆,其中纯电动汽车保有量占比达81.32%[9]。预计2025年全球碳酸锂的需求量为80万~110万t,这是一个庞大的市场需求[10]。
中国是全球最大的锂盐生产国,但绝大部分仍然依赖于进口锂原料加工,其中进口锂辉石加工占60%、进口高浓卤水加工占15%、中国矿石提锂占17%、中国卤水提锂仅占8%[11]。根据摩根士丹利预计,2017—2025年锂需求增长率为每年12%[12]。随着新能源动力汽车、能源转换、航空航天等高新技术产业的迅猛发展、矿石资源的开采条件限制及盐湖锂资源的季节影响导致无法满足未来这些高新产业的发展需要,多渠道开拓和循环利用锂源已成为国内外锂产业持续发展的必然。
在对沉锂后产生的废水进行排放前处理时,通常加入可溶性磷酸盐以去除水中的重金属、碱土金属和锂,形成大量含磷酸锂的废渣。目前针对高效回收磷酸锂废渣中锂技术的研究报道较少,所报道的回收方法主要有辅料焙烧法[13]、高酸全溶解法[14]、硫酸锂转化法[15]、低酸转化法[16]等。
笔者以江西赣县某厂回收得到的磷酸锂废渣为原料,在低酸条件下直接实现转化反应,经除杂、沉淀制得碳酸锂产品。经检测产品达到YS/T 582—2013《电池级碳酸锂》的要求。该方法工艺简单、操作方便、易于工业化生产,具有较好的经济效益,为磷酸锂的高效循环回收利用提供了可靠的途径。
1 实验部分
1.1 原料和仪器
原料:磷酸锂渣,江西某企业将废旧锂离子电池正极材料提取高价值元素后回收废液产生的含磷酸锂的废渣(组成见表1);浓盐酸、氯化钙、氢氧化钙、氢氧化钠、纯碱均为工业级。

表1 磷酸锂渣的组成及含量Table 1 Composition and content of the slag containing lithiumphosphate
仪器:JJ-1型精密增力电动搅拌器;HH-S4恒温水浴锅;LEAD-2型蠕动泵;SHZ-D(Ⅲ)循环水式真空泵;101A-2型电热鼓风恒温干燥器。
1.2 实验原理
磷酸为三元酸,在不同pH下与金属离子结合可生成正盐或酸式盐,而在相同条件下不同金属离子形成的酸式盐有非常明显的溶解性差异,因此可以通过控制体系pH实现磷酸锂中Li+与PO43-的分离。以钙盐为例,此反应可表述如下:

用HSC软件计算可知,上述反应过程在0~100℃的吉布斯自由能(ΔGTΘ)与温度的关系见图1。从图1看出,0~100℃氯化钙与磷酸锂在酸性条件下反应的ΔGTΘ皆远小于0,即反应可自发进行,且随着温度的升高ΔGTΘ越负,说明随着温度的升高自发反应的趋势越强。另外,磷酸锂与酸的反应为放热反应,可提高反应体系的温度,进而促进反应的进行。
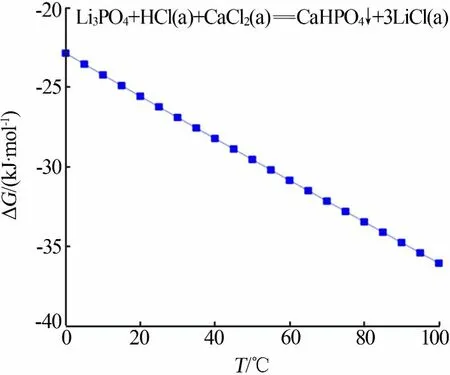
图1 吉布斯自由能与温度的关系Fig.1 Relationship between Gibbsfreeenergyand temperature
1.3 实验方法
称取一定量磷酸锂渣于烧杯中,加入去离子水并搅拌均匀,添加适量的浓盐酸反应一段时间,再加入CaCl2溶液反应30 min,过滤所得滤液即为转化后的氯化锂溶液,溶液除杂后在95℃以上用碳酸钠沉淀法制备Li2CO3并用热去离子水洗涤,烘干即得到电池级Li2CO3。工艺流程见图2。
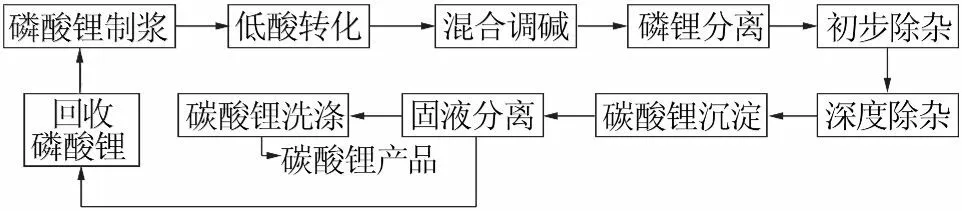
图2 磷酸锂渣回收制备碳酸锂工艺流程图Fig.2 Processflow diagramfor recoveringlithiumcarbonate fromthe slag containing lithiumphosphate
2 结果与讨论
2.1 盐酸用量对转化钙渣中锂残余量的影响
磷酸锂在低酸条件下与钙转化剂反应生成钙的磷酸酸式盐及锂溶液。如果加酸量过大,将会使磷酸锂完全溶解,反应混合物体系回调pH时耗碱量大,影响转化成本;当酸量不足时,磷酸锂反应不完全,部分仍以磷酸锂的形式存在,直接影响锂的转化效率。因此,需要选择合适的盐酸用量。称取62.5 g磷酸锂渣于烧杯中,加入去离子水并搅拌均匀,研究不同盐酸用量对转化钙渣中锂残余量的影响,结果见图3。由图3看出,随着盐酸用量的增加,转化钙渣中锂残余量呈现递减趋势。当盐酸用量为65 mL时,盐酸与固体原料的液固体积质量比为1.04 mL/g,转化钙渣中锂残余量最低,即磷酸锂中锂的损失率最低,为3.20%,此时转化至溶液中的锂为96.8%。继续增加酸的用量,转化钙渣中锂残余量增加,磷酸锂的转化效率反而呈现下降趋势。主要原因是,回调pH时耗碱量增大,导致溶液局部碱过量又生成部分磷酸锂,而随着pH升高磷酸锂转化能力减弱,使得转化钙磷渣中锂残余量增加,锂转化率反而呈现下降趋势。因此,选择盐酸用量为65 mL较为合适。

图3 盐酸用量与转化钙渣中锂残余量的关系Fig.3 Relationship between the amount of hydrochloric acid and theresidual amount of lithiumin converted calciumslag
2.2 体系终点pH与磷酸锂转化率的关系
由于磷酸二氢锂与磷酸二氢钙、磷酸氢钙的溶解度差异巨大(20℃时磷酸二氢锂在100 g水中的溶解度为16.6 g,磷酸二氢钙的溶解度为1.8 g,磷酸氢钙的溶解度仅为4.303×10-3g),因此可以通过控制转化体系pH使Ca2+与HPO42-或H2PO4-结合,以CaHPO4、Ca(H2PO4)2的固体形式沉淀下来,从而使锂与磷酸根有效分离。实验探索了pH在2.5、3.5、4.0、5.0时对钙沉淀率和磷酸锂转化效果的影响,结果见图4。从图4看出,随着pH升高钙的沉淀量逐渐增加,pH为4.0时钙的沉淀率已达到95.11%,保持弱酸性体系再增大pH对钙沉淀率的影响不大,可能的原因是在该条件下钙磷渣的主体已为磷酸氢钙。转化钙渣中锂残余量也随着pH增大而略微增加。主要原因是:当pH较低时,反应体系中的磷主要以H2PO4-的形式存在,转化钙渣主成分为Ca(H2PO4)2,因Ca(H2PO4)2溶解度偏大,使得溶液中存有大量的H2PO4-和Ca2+,后续净化时需要的碱量增大,pH上调过程因局部过碱而使部分锂重新生成磷酸锂,使已溶解的部分锂又重新包裹在钙渣中,致使转化钙渣中锂残余量增加,反而降低了磷酸锂的转化效率;保持体系的弱酸性,随着体系终点pH升高,钙与磷充分反应生成溶解度更低的CaHPO4,溶液中游离的Ca2+、HPO42-浓度都较低,所获富锂溶液与低pH终点相比杂质离子要低得多,后续净化时需碱量和生成渣量极少,溶液中锂损失量低,磷酸锂的转化效率相对也更高。当体系终点pH为4.0后,钙沉淀趋于平衡,转化钙渣中锂残余量为3.18%。故体系终点pH选择4.0左右较为适宜。

图4 转化体系pH与钙沉淀率、转化钙渣中锂残余量的关系Fig.4 Relationship between pH of conversion systemand calciumprecipitation rateand residual lithium in converted calciumslag
2.3 氯化钙用量与锂转化率的关系
磷酸锂在低酸条件下与转化剂(CaCl2)反应生成钙的酸式磷酸盐及锂溶液(氯化锂)。转化剂用量过小时,不足以与磷酸根完全结合,使得磷酸锂转化率降低;转化剂用量过大时,虽然可以使磷酸根完全转化至钙磷渣中,但是过量的钙将增大后续除杂负担,另外过量的转化剂将增加转化成本,使净化渣量增加,锂损失量大。因此,需对磷酸锂转化时转化剂用量进行严格控制。磷酸锂、盐酸用量同前,依据磷酸锂渣的含磷量加入不同化学计量比的氯化钙,过滤分析滤液中的总锂量和磷酸盐副产品的锂含量,并计算其转化率,结果见图5。图5显示,随着氯化钙用量增加,锂转化率先增大后基本不变,较佳的氯化钙用量为磷酸锂中含磷物质的量的0.9倍左右。而随着氯化钙用量过量,磷酸锂转化率虽有微量提升,但是溶液中残余钙离子较多,增加了后续除杂压力,并增加了净化渣量,进而影响锂的总收率。故选择氯化钙用量为磷酸锂中含磷物质的量的0.9倍。
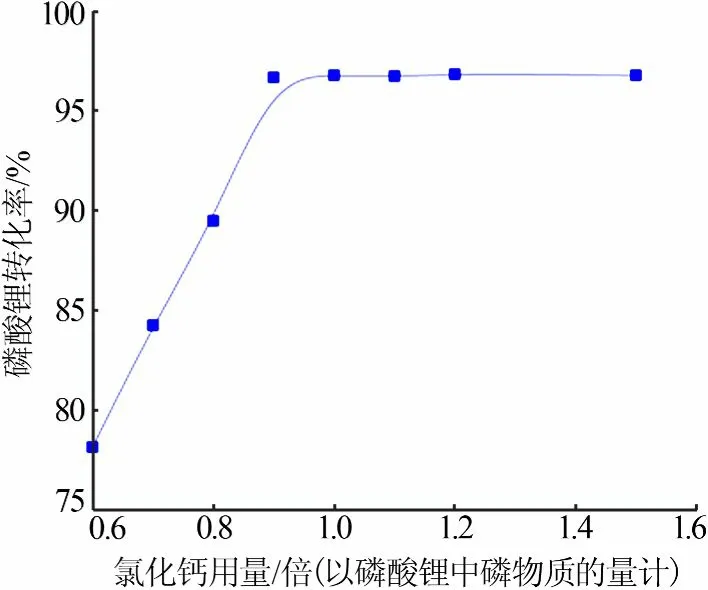
图5 氯化钙用量与磷酸锂转化率的关系Fig.5 Relationship between the amount of calciumchloride and the conversion rate of lithiumphosphate
2.4 盐酸体系液固比、转化时间与锂转化率的关系
磷酸锂固液直接转化法类似于矿物浸出的固液体系,转化体系的液固比、转化时间将影响锂的转化率及锂液的浓度。原辅材料取量同前,经过不同转化液固比、转化时间对锂转化率的影响实验,分析计算锂的转化率,结果见图6。从图6看出,磷酸锂的转化率随着液固比的增大、转化时间的延长呈现先增大后几乎不变的趋势。液固比对锂转化率影响规律的原因是,首先液固比较小时,固体生成物会包裹部分固体反应物,使得该部分原料难以与液相充分接触,转化反应不充分,降低了磷酸锂的转化率;其次是液固比较小时,各离子浓度高,固液分离后钙磷渣中残存液相所含锂也相应增加,洗涤时难以洗出,也在一定程度上影响了锂的转化效率。转化时间对锂转化率影响规律的原因是,该反应体系是固液相互转化过程,在该体系下转化反应速率主要取决于游离的HPO42-及转化剂所含金属离子的浓度,初始时两者浓度都比较高,所以转化速率也高,随着转化时间的推移,HPO42-与Ca2+结合生成溶解度小的CaHPO4,使两种游离离子的浓度降低,转化速率随之下降。故转化前期转化率升高较快,至一定时间后转化反应趋于平衡,转化率几乎不再有明显变化。
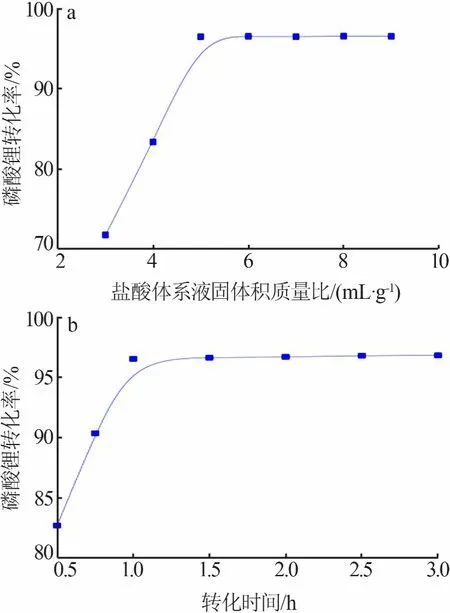
图6 盐酸体系液固比(a)、转化时间(b)与磷酸锂转化率的关系Fig.6 Relationship between liquid-solid ratio(a),conversion time(b)and lithiumphosphate conversion rate under hydrochloric acid system
2.5 浸出液净化
将所得滤液取样后送检,经分析可知滤液主要杂质为Ca2+、Mg2+、Ni2+、Fe3+、Al3+及PO43-。依据金属离子完全沉淀时pH差异,先将pH调节至5.0~5.5,除去大部分Fe3+、Al3+及部分PO43-,再调节pH至11~12,同时加入少量Na2CO3,沉淀除去Ca2+、Mg2+、Ni2+和PO43-,并加入吸附剂吸附去除PO43-(吸附剂加入量为3 g/L),再经离子交换深度除杂得到锂完成液,用于制备Li2CO3。除杂前后的杂质含量对比见表2。从表2看出,除杂前后溶液中Ca2+含量减少了93.21%、P含量减少了94.69%,除杂效果明显,而Mg2+和Fe3+在转化液中的含量已较低,因此除杂后降低幅度较小。

表2 浸出液除杂前后杂质含量对比Table 2 Comparison of impurity content in leaching solution before and after impurity removal
2.6 碳酸锂沉淀
碳酸锂的溶解度随着温度的升高而降低,完成液中其余盐类的溶解度则是随着温度的升高而升高,故沉锂温度选择≥90℃。碳酸钠经溶解、粗滤、精密过滤得到精制碳酸钠溶液,在保证温度≥90℃条件下,以精制碳酸钠溶液为沉淀剂,严格控制加料方式、加料速度及锂液浓度,将锂完成液与精制碳酸钠溶液混合均匀,搅拌反应20 min后趁热过滤,用热水洗涤多次,干燥得到碳酸锂产品。取碳酸锂样品,参照YS/T 582—2013《电池级碳酸锂》检测样品的杂质含量(结果见表3),并进行XRD分析(结果见图7)。XRD表征结果表明,样品XRD谱图与标准 卡吻合度较高。

表3 自制碳酸锂与YS/T 582—2013《电池级碳酸锂》化学成分对比Table3 Comparisonofchemicalcompositionbetweenself-madelithiumcarbonateand YS/T582—2013“batterygradelithiumcarbonate”

图7 自制碳酸锂XRD谱图Fig.7 XRDpattern of self-made lithiumcarbonate
检测结果表明,自制碳酸锂平均Li2CO3质量分数为99.65%,杂质含量也在电池级碳酸锂行业标准要求范围内,说明严格控制沉锂完成液的质量及沉锂条件可以直接获得电池级碳酸锂。沉锂母液残存锂可以磷酸锂的形式返回工艺前段进行回收或蒸发浓缩后回收,碳酸锂沉淀洗液返回碳酸钠溶解段。通过碳酸锂沉淀获得的锂质量约占原料锂总质量的81.8%,通过沉锂母液回收的锂质量约占原料锂总质量的11.6%,锂总回收率不低于93.4%。该工艺可以充分利用杂质含量高的磷酸锂渣,拓宽了中国锂资源的渠道。
3 结语
通过对磷酸锂渣在酸性条件下与转化剂反应的热力学分析,得出在常温条件下加入适当的转化剂,磷酸锂即可与转化剂在混合体系内自发地进行固液反应,将锂从难溶的磷酸锂中转化成易溶性的锂盐,实现Li+、PO43-的高效分离。通过实验研究盐酸添加量、体系终点pH、转化剂添加量对磷酸锂转化率的影响,确定了磷酸锂较佳的转化条件:盐酸添加量与固体原料的液固体积质量比为1.04 mL/g,体系终点pH为4.0,转化剂氯化钙的加入量为原料含磷物质的量的0.9倍。在该条件下磷酸锂中锂的转化率达到96.8%。转化锂液经化学、物理方法二次深度净化,严格控制沉锂的方式可以直接获得电池级碳酸锂,沉锂母液再回收利用后锂的总收率达到93.4%。工艺特点:酸用量较少,设备设施普适性强;可自发进行固液反应,实现锂与磷酸根的分离,转化效率可达96.8%;严格控制沉锂条件,能稳定获得电池级碳酸锂产品;工艺简捷,无环境危害物产生,极具工业化前景。
