细胞因子风暴及其中药防治的研究❋
2022-03-08张彬彬于国华史渊源
张彬彬, 于国华, 史渊源,2△
(1.北京中医药大学生命科学学院, 北京 100029; 2.深圳北京中医药大学研究院, 广东 深圳 518118)
人冠状病毒(hCoV)可分为低致病性和高致病性冠状病毒。低致病性冠状病毒感染上呼吸道,并引起轻度感冒样呼吸道疾病。相比之下,高致病性hCoV(如严重急性呼吸综合征CoV(SARS-CoV)、中东呼吸综合征CoV(MERS-CoV)以及新型冠状病毒(2019-nCoV)主要感染下呼吸道并引起致命性肺炎。高致病性冠状病毒引起的严重肺炎通常与病毒快速复制、大量炎性细胞浸润以及促炎性细胞因子和趋化因子应答升高有关[1]。这些高致病性冠状病毒可通过逃避宿主的抗病毒免疫反应,促使炎症性细胞因子上调以引起急性感染,这种免疫失调被称为细胞因子风暴(cytokine storm,CS)。CS可能致命,也是感染患者死亡率上升的重要潜在因素[2]。
不同病毒感染诱导的CS涉及的细胞因子种类有所差别,因此在治疗策略上可能也会有所差别。本文述评了人类高致病性冠状病毒(SARS-CoV、MERS-CoV、2019-nCoV)的免疫病理学过程,分析其中的相同之处和不同之处,剖析不同病毒感染诱导的CS不同特点,为治疗CS提供一定的理论依据。同时针对不同的人类高致病性冠状病毒(SARS-CoV、MERS-CoV、2019-nCoV),分别总结归纳中药防治的药理作用,旨在为中药干预CS提供有意义的临床指导意见。
1 人类高致病性冠状病毒引起的CS
1.1 共同之处:干扰素(Interferon,IFN)反应失调
炎症细胞因子的过度诱导和细胞因子信号的失调,可能促使机体产生相关的炎症[3]。对病毒最有效和最迅速的宿主反应是产生I型IFN[4],IFN是抵抗病毒感染的第一道防线[5],也是抗病毒先天免疫系统的重要组成部分。首次与病毒接触产生的IFN会使病毒繁殖减慢甚至停止,延长生物体时间,并有助于建立适应性免疫反应[4]。但SARS-CoV、MERS-CoV、2019-nCoV在侵入人体初期均具有IFN响应延迟和被抑制现象,通过减慢被感染组织细胞中的IFN及其抗病毒基因的表达,病毒可以在感染的最初关键阶段获得时间,以便在宿主中不受阻碍的繁殖[6]。SARS-CoV可通过所编码的nsp3抑制STAT1磷酸化,从而抑制IFN响应[4,7]。MERS-CoV的M,4a,4b蛋白和木瓜蛋白酶(PLpro)会抑制I型IFN和NF-κB信号通路,从而促进先天性免疫逃逸、病毒清除延迟、嗜中性粒细胞浸润增强以及特异性T细胞应答受损[8]。2019-nCoV感染引起的总中性粒细胞和淋巴细胞变化与SARS、MERS变化类似。2019-nCoV可能会在感染早期促使I型IFN响应延迟,导致病毒复制失控[9]、宿主先天免疫应答失调,同时中性粒细胞和单核/巨噬细胞的流入,也会导致促炎细胞因子的大量产生。
IFN-α的缺乏促进对病毒的抗原呈递,从而削弱强大的抗病毒适应性Th-1免疫应答发展[10]。IFN反应失调可能最终导致人类宿主从高先天免疫转向保护性适应性免疫应答的失败[11]。此外,易受COVID-19影响的人是那些具有潜在疾病的人,包括糖尿病、高血压和心血管疾病患者。这些事实有力地表明,先天免疫应答是疾病转归的一个关键因素[9]。
1.2 不同之处
经过查阅文献并总结归纳3种高致病性冠状病毒引起CS的发病机理,发现每种冠状病毒均有其独特的部分,关注于此将为临床提供有效的参考依据。
1.2.1 SARS 核衣壳(nucleocapsid,N)蛋白、刺突(spike,S)蛋白与NF-κB相互作用启动细胞因子释放 Zhang等[12]研究发现,SARS-CoV的 N蛋白与宿主转录因子NF-κB相互作用调节IL-6的表达。Wang等[13]研究发现,SARS-CoV 的S蛋白与鼠巨噬细胞之间的相互作用,可以诱导细胞因子IL-6和TNF-α的释放,S蛋白触发NF-κB的激活,然后启动细胞因子的释放,这些研究将为探索SARS-CoV 的N蛋白和S蛋白的功能机制、SARS-CoV发病机理提供新的见解,同时为预防和治疗SARS-CoV引起的细胞因子风暴提供新的思路。
1.2.2 MERS:MERS-CoV感染T细胞和诱导细胞凋亡可能与MERS的高致死率有关 尽管MERS与SARS高度相似,但MERS的致死率超过35%[14],是SARS的3倍。与SARS-CoV和2019-nCoV不同,MERS-CoV的功能受体为二肽基肽酶4(DPP4)。DPP4是T细胞的激活标记,在T细胞的大量表达可能使细胞更易受MERS-CoV感染。MERS-CoV有效感染CD4+和CD8+T细胞,并下调受感染细胞中的表面DPP4[15]。MERS-CoV能够有效地从外周血、脾脏和扁桃体感染人T细胞,并且感染MERS-CoV能够诱导T细胞大量凋亡,其中涉及外部和内在凋亡通路的激活,这可能是MERS高致死率的重要原因。另外,SARS-CoV和MERS-CoV引起淋巴细胞减少的潜在机制可能是不同的,而这种不同可能是T细胞直接感染和感染诱导细胞凋亡的结果。除凋亡外,MERS-CoV感染后T细胞中表面DPP4的急剧消耗,可能会严重破坏T细胞的增殖和细胞功能[15]。
1.2.3 COVID-19 IL-6可能在CS中起关键作用 许多基质细胞和免疫系统细胞,包括B淋巴细胞、T淋巴细胞、巨噬细胞、单核细胞、树突状细胞、肥大细胞和其他非淋巴细胞等均可产生IL-6[16]。COVID-19尽管病死率不高,但感染人数很多,仍有大量患者死亡。随着越来越多临床数据的整理和发布,大量数据表明重症患者存在轻度或重度CS,这是COVID-19患者死亡的重要原因。Michot等通过临床观察发现,2019-nCoV引起的CS与白介素和趋化因子失调有关,从首次成功用抗IL-6受体治疗严重的COVID-19患者观察结果可以看出,IL-6是引发新冠肺炎患者炎症风暴中的关键炎症因子[17]。因此,如果有可能阻断IL-6的信号传导途径,则有望成为治疗重症COVID-19患者的新方法[18]。
1.2.4 细胞因子和趋化因子的过度产生 表1示,通过临床研究分析,SARS-CoV、MERS-CoV、2019-nCoV促使受感染细胞分泌大量的趋化因子和细胞因子,但分泌的趋化因子和细胞因子不尽相同。
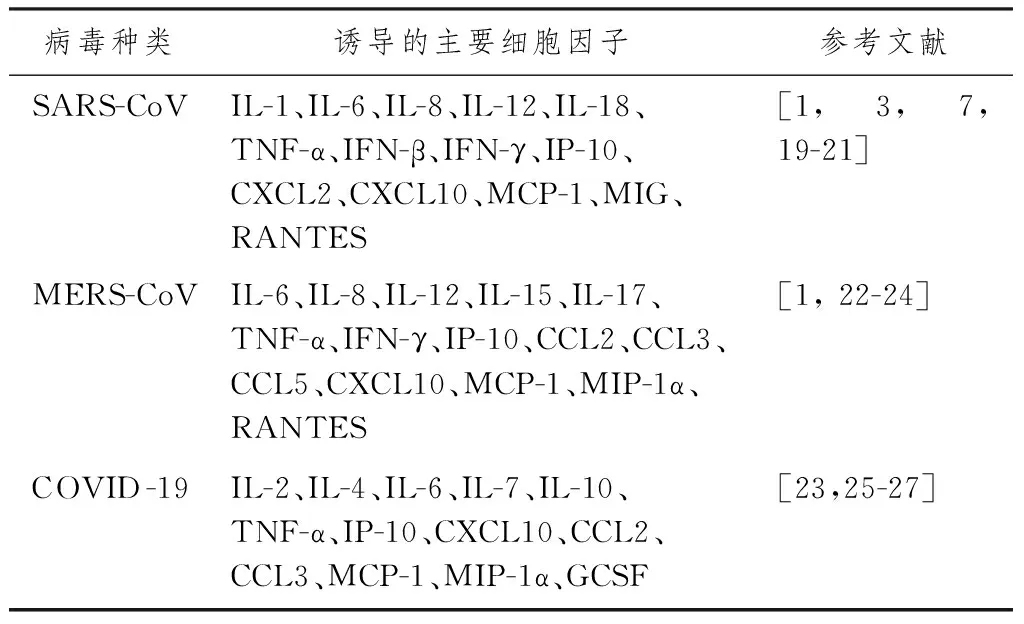
表1 3种高致病性冠状病毒诱发CS涉及的主要细胞因子
2 中药对CS的干预作用
经过对文献的查阅,总结归纳分别用于SARS-CoV、MERS-CoV、2019-nCoV的单味中药及中药处方如下。
2.1 中药对SARS-CoV引起的CS干预作用
在SARS疫情期间中医药发挥了重大作用,而后出现了大量关于中药治疗SARS-CoV引起的免疫失调的研究。姜代勋等[28]研究发现,芦根、大青叶、金银花、连翘、紫苏叶、薄荷、黄芪这7味药可能通过抑制cAMP-PDE(cAMP-磷酸二酯酶)活性,抑制炎性细胞因子的释放和中性粒细胞的活化,从而实现抗SARS的作用。甘草酸影响细胞信号通路,如蛋白激酶C(PKC)、酪蛋白激酶Ⅱ(CK-Ⅱ)、转录因子和NF-κB。此外,甘草酸及其苷元代谢物18β甘草次酸上调巨噬细胞诱导型氧化亚氮合酶的表达,并促进氧化亚氮的产生。Cinatl等[29]初步结果表明,甘草酸在Vero细胞中诱导氧化亚氮合酶的生成,当氧化亚氮供体(NONOate DETA)加入培养基时,病毒复制被抑制。Lau等[30]的研究结果表明,鱼腥草水提取物可以显著且剂量依赖性地刺激小鼠脾淋巴细胞的增殖。通过流式细胞仪发现,鱼腥草增加了CD4+T和CD8+T细胞的比例,此外还引起小鼠脾淋巴细胞IL-2和IL-10分泌显著增加。在抗病毒方面,鱼腥草对SARS-CoV 3C样蛋白酶(3CLpro)和RNA依赖性RNA聚合酶(RdRp)表现出显著的抑制作用。
大量实验表明,清开灵注射液、鱼腥草注射液、板蓝根冲剂对肺部急性炎症、肺指数、炎性因子、炎性渗出均有明显的改善作用[31]。常秀娟等[32]通过CS探讨热毒宁注射液对脂多糖(LPS)致大鼠急性肺损伤(ALI)的治疗作用及机制,结果表明热毒宁注射液能够降低ALI模型大鼠肺脏IL-1β、TNF-α、IL-4、IL-6、IL-8、IL-10、ICAM-1、NF-κB水平,改善大鼠肺组织形态学变化。在SARS爆发期间,Lau等[33]探索在高危人群中使用中药预防呼吸道病毒感染的可能性研究。在2周内3160名医护人员食用由桑菊饮和玉屏风散加另外2种抗病毒特性中药大青叶和黄芩研制成的制剂,其中37人检查了血清的免疫反应。在服用中药制剂时,CD4/CD8比值出现短暂性升高,B淋巴细胞持续下降,研究结果显示,抗病毒中药制剂在服用过程中可能产生有益的免疫调节作用。
2.2 中药对MERS-CoV引起的CS干预作用
国家卫生计生委发布《中东呼吸综合征病例诊疗方案(2015年版)》,清开灵注射液、参麦注射液分别被列为中医中药治疗MERS(邪毒壅肺、正虚邪陷)推荐药物[34]。
清开灵注射液是在传统名方“安宫牛黄丸”基础上加减而成[35],被誉为“中药抗生素”。张平等[36]观察清开灵注射液对急性肺损伤大鼠免疫功能的影响,结果发现清开灵注射液能增加CD4+T细胞数目,改善CD4+/CD8+比值,对大鼠急性肺损伤具有明显的修复作用。梁爱华等[37]研究发现,清开灵注射液可以抑制内毒素诱导的体内炎性因子TNF-α和IL-6的产生,同时可抑制内毒素诱导的血小板数目降低。
参麦注射液是《症因脉治》中 “参麦饮”的衍变方[38],经现代科学技术、大量药理研究、临床验证而成功研制的静脉注射剂,主要功能是益气固脱、养阴生津[39]生脉,增强机体免疫力[40]。范晓春等[41]研究发现,参麦注射液能够降低重症肺炎患者TNF-α、IL-1β、IL-6水平,提高IL-10水平,具有保护黏膜屏障的功能、调节炎症因子释放、减轻肺部炎症反应等作用。
很多中药成分对病毒蛋白酶有抑制作用,如草质素(Herbacetin)、补骨脂乙素(Isobavachalcone)、蜡菊亭(Helichrysetin)[42]、丹参酮等能抑制MERS-CoV 3C样蛋白酶(3CLpro)活性,从而发挥抗病毒复制作用[43]。另外,多酚[44]、丹参酮[45]、肉桂酰胺[46]、泡桐树果实的甲醇提取物等[47]产生了许多能够靶向PLpro的小分子,具有PLpro的抑制活性作用。而PLpro会抑制I型干扰素(IFN)和NF-κB信号通路,因此上述中药成分可能具有抑制先天性免疫逃逸功效。
2.3 中药对2019-nCoV引起CS的干预作用
2.3.1 新型冠状病毒肺炎诊疗方案(试行第七版)中与CS相关的中成药 新型冠状病毒肺炎诊疗方案(试行第七版)指出,建议重症及危重症患者使用清肺排毒汤、化湿败毒方、喜炎平注射液、血必净注射液、热毒宁注射液、痰热清注射液、醒脑静注射液、苏合香丸、安宫牛黄丸、参附注射液、生脉注射液、参麦注射液等中成药。经过查阅文献发现,上述中成药基本都有调节细胞因子、趋化因子的作用,从而对CS有一定的干预作用(见表2)。
2.3.2 具有潜在调节2019-nCoV引起CS作用的中药 IL-6是引发新冠肺炎患者炎症风暴中的关键炎症因子,寻找对IL-6有调节作用的中药对临床用药有重大意义,因此有必要认真总结对IL-6起调节作用的中药(见表3)。
3 讨论
CS发病前征兆少,发病后救治难度大且后果严重。目前针对CS大多采用西药治疗,西药虽有效但其安全性仍存在争议[73]。新型冠状病毒肺炎诊疗方案(试行第七版)强调中药治疗,中药作用靶点广泛,在CS的发生、进展、转归阶段均有一定的效果,并在此方面有着独到优势,因此从中医药领域寻找有效方治疗COVID-19重症及危重症下的CS是值得重点关注的问题。

表2 新型冠状病毒肺炎诊疗方案(试行第七版)与CS相关的中成药汇总比较

表3 对IL-6起调节作用中药的比较
本文分析了人类高致病性冠状病毒(SARS-CoV、MERS-CoV、2019-nCoV)引起CS的机理异同点,并归纳总结了中药对3种冠状病毒引起CS的免疫调节作用,发现其中有很多中药均可用于3种病毒引起的CS,如清开灵注射液、参麦注射液、热毒宁注射液等,因其机理有许多共同之处,如调控TNF、NF-κB等信号通路抑制炎症反应,降低血清IL-6、IL-8、TNF-α水平等。同时也有些中药成分具有针对其中某种病毒的作用,如多酚、丹参酮、肉桂酰胺、泡桐树果实的甲醇提取物等产生了许多能够靶向PLpro的小分子,具有对PLpro的抑制活性作用,从而抑制MERS-CoV引起的先天免疫逃逸。表3示,因IL-6是2019-nCoV诱发CS的关键细胞因子,因此重点关注对IL-6具有调节作用的中药,将对临床治疗COVID-19有很好的指导作用。关注CS机理的共同之处和不同之处,在未来的研究中可以更好地了解病毒诱发CS的全过程,将CS的发病机理与中药防治CS的机制紧密联合起来,高效筛选治疗药物并探讨其作用机制[74],这对于研发“广谱类”抗CS中成药及“针对性”抗CS中成药具有重要参考价值。然而不同冠状病毒引起CS的机理尚未完全研究清楚,中药干预CS的机制亦是如此。本文只是简单地比较3种高致病性冠状病毒引起CS机理的异同以及简单归纳中药干预CS的机制,为临床治疗CS提供一定的用药思路,而中医药防治CS仍需探索。
