一种减少胸部肿瘤放疗图像引导配准误差的方法
2022-03-04杨定强戴红娅周一兵
杨定强,戴红娅,周一兵
陆军军医大学第二附属医院 肿瘤科,重庆 400037
引言
随着放疗技术发展,现代放疗技术已进入高精度放疗时代,采用图像引导放射治疗(Image Guided Radiotherapy,IGRT)技术可以提高治疗的位置精度,减少对周围正常组织照射量。放疗IGRT设备众多如锥形束CT(Cone Beam CT,CBCT)、电子射野影像系统(Electronic Field Imaging System,EPID)、泰影像验证系统(Image Verification System,IVS)等。采用IGRT技术治疗时图像的验证配准方式是影响位置精度的主要因素[1]。IVS为二维验证设备,与三维验证设备比较存在图像采集配准复杂、分辨率较低、组织器官重叠严重等局限性[2],使得技师在图像配准时难度增大。在头颈部肿瘤放疗中二维验证设备只能保证在平移方向位置的准确性[3],上述原因导致技师在行二维图像验证时配准偏差较大,使得技师在放射治疗中医生和技师进行图像匹配时出现匹配结果不一致的情况。本研究运用气管隆嵴结合主动脉弓为匹配特征点配准,找到技师自主配准更精确的配准方法,对比分析胸部肿瘤在图像引导的匹配结果数据进行分析,此方法能够提高技师自主摆位精度,现报道如下。
1 材料和方法
1.1 一般资料
选取2019年10月至12月在我院行胸部调强放疗患者30例123次位置验证,其中男性19例,女性11例,体重50~70 mg,年龄25~70岁,中位年龄45岁,卡氏评分均≥70分,所有患者均能平静呼吸。中心型肺癌13例;周围型肺癌5例;食道癌3例;胸椎骨转移8例;胸腺瘤1例。主要设备为Elekta直线加速器,oncntra计划系统、飞利浦CT模拟机、雷泰影像验证系统IVS。
1.2 患者体位固定及CT扫描
患者平躺于模拟机平板床的体位固定板上,热塑模固定。通过激光三点以等中心放疗技术确定marker和左右两侧的十字交叉线[4]。在患者身上和热塑膜上均做好摆位标记,以确保治疗前复位和治疗中的摆位的准确性。CT扫描范围:上界为第4颈椎椎体上缘,下界至肋膈角下缘约3 cm,扫描层厚为5 mm,层间距为5 mm。CT扫描图像经网络传入oncntra计划系统。
1.3 结构勾画
胸部肿瘤靶区的勾画受到较多因素的影响,如影像学特点、窗宽窗位的选择、医师的经验、医师的临时状态等[5]。为了避免勾画肿瘤靶区体积变化过大的影响,30例患者均由三名医生讨论后勾画,靶区勾画范围需得到三位医生共同认可。靶区勾画定义参照ICRU50和23号报告,勾画大体肿瘤靶区(Gross Tumor Volume,GTV)、临床靶区(Clinical Target Volume,CTV),同时勾画正常组织器官,GTV为CT图像下可见病灶,据对肿瘤生物学的了解及临床经验,在GTV外周加一定边界以包括亚临床浸润病灶构成CTV[6],PCTV外放根据病灶位置不同而有所变化,食道癌在CTV基础上左右外扩5 mm,上下外扩10 mm,胸腺瘤和胸椎转移患者在CTV基础上均匀外扩5 mm,肺癌患者运用4D-CT扫描方式在ITV基础上均匀外扩5 mm,勾画敏感器官和需保护重要组织。
1.4 TPS计划及图像后处理
将CT扫描所做的三个“十”字标记线在模体内相交点位置作为坐标“0”位点,TPS根据靶区形态自动选择治疗等中心。根据放疗原则尽可能减少正常组织器官剂量的同时使靶区得到更高剂量照射进行IMRT计划设计。计划确认后在TPS上设置大机架为0、90°、270°小机头均为0的三个射野,三个射野x、y、z坐标和计划坐标保持一致。分别生成0、90°、270°的二维验证图像,并传入IVS位置验证系统。患者经CT模拟机复位并在热塑模上标记出治疗等中心。
1.5 验证CT图像获取
所有患者均在ELEKTA直线加速器上治疗,射线能量为6 MV,验证系统为雷泰影像验证系统IVS。每位患者以CT复位数据作为摆位依据,运用激光灯摆放体位。如图1所示,根据患者病灶位置确定拍摄0、90°或0、270°两张二维验证图像,通常病灶位于患者正中矢状面之左时选择0、90°拍摄两张二维验证图像,反言之则拍摄0、270°两张二维验证图像。2个角度加速器分别出束1 MU,总计出束2 MU,射野大小均为27 cm×27 cm。IVS系统载入参考图像与获取的二维验证图像进行配准。
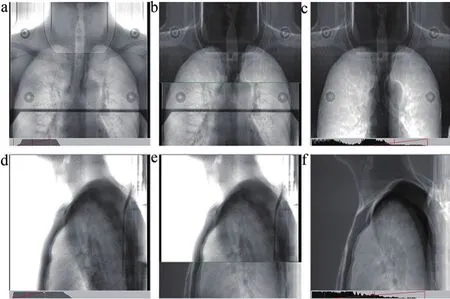
图1 IVS位置验证图
1.6 图像匹配与数据获取
30例患者共计123组IVS图像,在图像匹配中为避免不同人员匹配时存在的误差,医生在对每组IVS图像进行配准时均由3名医生共同讨论后得出匹配误差,同样技师对IVS图像配准时也由3名技师共同讨论后得出匹配误差。每组IVS图像均用3种方式行图像手动匹配。A组:在无医生参与下行图像匹配,技师对胸部病灶进行图像匹配时采用独立自主的配准方式进行图像匹配。B组:由医生自行做图像匹配,医生对胸部病灶进行图像匹配时采用独立自主的配准方式进行图像匹配。C组:技师采取气管隆嵴结合主动脉弓作为匹配特征点对胸部病灶进行图像匹配。分别获取背腹位(Dorsoventral,VRT)、头脚位(Head Pin,LNG)和左右位(Lateral,LAT),以B组医生匹配结果作为标准,两两对比分析AB、BC之间的匹配误差。
1.7 统计学分析
应用IBM SPSS 19.0软件,模体位置验证三个方向的误差值运用散点图对数据进行处理。所有患者使用A、B、C三种方法获得的三个方向的摆位误差数据进行简单分析,用均值±标准差(±s)表示,运用配对样本t检验对数据进行处理,检验水准P<0.05为差异有显著性。
2 结果
每组统计例数为123例,如表1所示,A组技师自主配准在LAT、VRT、LNG方向匹配误差分别为(0.05±0.25)cm、(0.04±0.26)cm、(0.09±0.62)cm。B组医师自主配准在LAT、VRT、LNG方向最大匹配误差分别为(0.04±0.30)cm、(0.05±0.34)cm、(0.01±0.67)cm。C组技师运用特征点匹配在LAT、VRT、LNG方向匹配误差分别为(0.04±0.27)cm、(0.05±0.28)cm、(0.03±0.63)cm。A组技师匹配误差与B组医生匹配误差比较,在LAT、VRT方向误差比较,差异无统计学意义(P>0.05);在LNG方向匹配误差,差异有统计学意义(P<0.05);C组技师运用特征点匹配误差与B组医生匹配误差比较,在LAT、VRT、LNG方向匹配误差差异均无统计学意义(P>0.05)。
表1 三个方向摆位误差数据(cm,±s)

表1 三个方向摆位误差数据(cm,±s)
注:a表示A组与B组比较;b表示B组与C组比较。
?
3 讨论
IGRT技术的应用能够及时矫正摆位误差,从而提高放疗精确度[7]。IGRT准确性是以加速器机械参数准确为前提,因此加速器校准成为IGRT准确性的关键。根据TG142报告要求首先校准加速器治疗治疗等中心、辐射野与灯光野一致性、大机架旋转精度、激光灯等。
精确放疗是当今放疗的常规选择,而照射靶区位置的准确性是放射治疗中重要和基本的一个环节,位置验证的目的就是评估和调整治疗时的体位,达到定位和计划时的体位,保证所确定的靶区和重要器官以及照射的空间位置与计划的相符,使靶区得到准确的照射[8-9]。前人研究结果认为当摆位误差大于l cm,会导致周边靶区丢失大于6 mm[10-11]。胸部患者在放疗过程中,摆位位置误差、肺部呼吸运动、器官自身运动、机械参数误差、人为因素均可导致计划精确的降低,使得靶区漏照或敏感器官超量的风险增加[12]。放疗技术进步很快,当前已进入精确定位、精确计划、精确治疗的“三精”时代[13],IMRT技术已成为当今放疗主要趋势,由于IMRT计划和靶区高度适形却剂量跌落较大,故对患者治疗精度要求更高。临床上常用CTV外扩PCTV方式来解决系统误差和随机误差,从而达到治疗靶区不漏照目的。IVS获取的位移值精度,是否在我科PCTV外放误差范围内,校准位移精度也是一项重要任务。
医师从每位患者的接诊、定位、靶区勾画、计划审核、治疗都全程参与,对病人一般情况、病理特性、病灶和周围组织器官的位置关系了然于心,因此医师的图像匹配结果可作为匹配准确性的标准值。而技师对特定患者解剖学结构、病灶和周围组织器官关系等因素与医生考虑的角度之间存在差异,图像配准结果会受到图像体素尺寸大小等因素的影响,且配准是否准确靠技师来判断,这就将技师的认真程度和经验也纳入影响定位精度的范畴,增加了随机误差[14-15],综上原因均能左右图像匹配结果。有研究表明在自由呼吸状态下隆突的平均移动在左右方向为(1.5±0.7)mm,在头脚方向为(5.3±1.6)mm,在腹背方向(2.3±1.4)mm[16],左右方向位移误差较小,头脚方向位移误差较大,不能单一作为匹配标志。研究表明胸椎位置固定,与主动脉弓比较在头脚、腹背方向移动度较小,无统计学差异,主动脉弓在头脚、腹背方向可做为匹配标志[17-19]。上述文献表明胸部肿瘤配准时单一选择气管隆嵴或者主动脉弓均无法提高配准精度。从本文研究结果证明运用气管隆嵴结合主动脉弓为匹配特征点配准,在LAT、VRT方向,医师、技师独立自主配准、特征点配准匹配结果无统计学差异。在LNG方向医师与技师独立自主配准结果有明显统计学差异,技师在LNG方向存在较大配准误差。医师独立自主配准与技师运用气管隆嵴辅助主动脉弓为匹配特征点配准结果,在LNG方向无明显统计学差异。气管隆嵴结合主动脉弓为匹配特征点能够运用临床匹配三个方向的位移误差,能够提高技师在图像配准时的精度。
EPID是附加于直线加速器的影像设备,可以进行二维图像位置验证,有操作方便、成本较低和实时进行拍片的优点,是多数进行三维精确放疗单位使用的位置验证设备和监测治疗实施过程中质量控制的手段[20]。雷泰影像验证系统IVS是安装在医科达加速器的EPID探测板处,替换原有的EPID探测板,因此IVS图像是MV级二维图像,具有EPID行二维图像位置验证功能。相对于EPID验证系统IVS经数据算法处理在成像质量、分辨率、照射剂量、软组织分辨率等方面均有所提高,但和XVI(KV-CBCT)比较亦有所欠缺,尤其是胸椎、胸椎间隙、肋骨等部位,由于MV-X线康普顿效应及组织重叠等原因,边界模糊,用于图像配准较为牵强。而隆突、主动脉因相邻组织器官密度反差较大,图像较清晰,容易判断结构边界,是可作为IGRT配准标志的影像学依据。二维验证时由于MV-X线使其软组织显影质量较差,组织结构重叠严重等使其配准难度增加,在由于技师对特定患者解剖学结构、病灶和周围组织器官关系等因素与医生考虑的角度之间存在差异,技师如何选择配准方式成为难点。笔者运用气管隆嵴结合主动脉弓为匹配特征点配准,和医师配准结果无明显差异,能够提高技师在图像配准时的精度,且配准速度快、成本较低适用于临床应用。IVS验证系统是通过加速器MV级X射线获取二维验证图像,加速器出束量的多少是影响图像质量关键因素,对于体重50~70 mg患者出束1 MU图形质量较好,当体重超过或少于该体重范围时图形质量就有所降低,患者体重大于70 mg时出束1.5 MU图形质量较好,而我科医科达加速器初始最小出束量为1 MU,出束1.5 MU需调整加速器参数,导致图像验证和治疗之间需修改加速器参数,反而增加了治疗时间,加速器参数反复调整也容易造成医疗事故。目前我科将IVS验证系统用于50~70 mg胸部肿瘤患者,在此体重范围外患者主要还以CBCT为主的验证方式。如何运用IVS验证系统在不增加出束量的同时提高图形质量,在日后工作中需进一步研究,以提高IVS在胸部肿瘤中的应用范围。
