高效液相色谱法测定混合重组人胰岛素注射液中异天冬氨酸的含量*
2022-02-13晏菊姣王婧张一唱喻悦周朝晖李恒
晏菊姣,王婧,张一唱,喻悦,周朝晖,李恒
(1.武汉药品医疗器械检验所,国家药品监督管理局药物制剂质量研究与控制重点实验室,武汉 430075;2.美国东北大学化学与生物化学系,巴奈特化学与生物分析研究所,波士顿 02115)
糖尿病是一种以高血糖为特征的代谢性疾病,其中1型糖尿病主要表现为胰岛β细胞的功能受损,主要是体内胰岛素的绝对缺乏,其患者主要通过注射胰岛素进行治疗。鱼精蛋白是以精氨酸为主的30多种氨基酸组成的碱性多肽混合物[1],在含有少量锌离子和苯酚的中性条件下,带负电荷的胰岛素与带正电荷的硫酸鱼精蛋白结合形成棒状晶型的白色沉淀,使其在人体液中溶解度降低从而达到延时释放的目的[2]。混合重组人胰岛素注射液是双时相胰岛素制剂[3],是将普通胰岛素(regular insulin,RI)与鱼精蛋白锌胰岛素(protamine zinc insulin,PZI)按一定比例混合而成,从而得到一个来自速效或短效部分的餐时胰岛素以及中效部分的基础胰岛素,发挥餐时胰岛素和基础胰岛素的效果。重组人胰岛素由51个氨基酸组成,含有3个天冬酰胺(Asn)残基,可能发生脱酰胺化反应,从而改变其结构和功能,导致其活性下降[4-6]。脱酰胺作用的程度可由蛋白中形成的异天冬氨酸(isoaspartic acid,isoAsp)浓度反映[6]。混合重组人胰岛素注射液中既有RI,又有PZI,鱼精蛋白与胰岛素的结合可能使胰岛素的结构发生变化,从而使isoAsp的检测更加复杂。生物技术药物近年来蓬勃发展,为人类战胜疾病发挥积极意义,我国对生物技术药物中脱酰胺化的研究处于探索阶段,历版《中华人民共和国药典》及法规未对脱酰胺的检测和评价方法形成明确规定。笔者在本研究选取混合重组人胰岛素这种分子量较小的生物药作为研究目标,测定其脱酰胺化产生的isoAsp含量,为研究其他更大分子量的生物技术药物中脱酰胺化提供借鉴与参考。
1 试药与仪器
1.1试药 30/70混合重组人胰岛素注射液(商品名:甘舒霖®30R,通化东宝药业股份有限公司,批号:3M12019065353,3M12020086763);精蛋白锌重组人胰岛素混合注射液(商品名:优泌林®70/30,Lilly France,礼来苏州制药有限公司分装,批号:C924352A,D135743A);精蛋白重组人胰岛素混合注射液(30/70)(商品名:优思灵,珠海联邦制药股份有限公司中山分公司,批号:202007C117);精蛋白锌重组赖脯胰岛素混合注射液(25R)(商品名:优泌乐®25,Lilly France生产,礼来苏州制药有限公司分装,批号:D215343);精蛋白锌重组赖脯胰岛素混合注射液(50R)(商品名:优泌乐®50,Lilly France生产,礼来苏州制药有限公司分装,批号:D179806A,D176504A);重组人胰岛素标准品(批号:140633-201907,规格:27.2 U·mg-1);赖脯胰岛素标准品(批号:140729-201702,规格:27.6 U·mg-1),购自中国食品药品检定研究院;ISOQUANT®Isoaspartate Detection Kit,MA1010[Promega公司,批号:0000387327,包含S-腺苷-L-高半胱氨酸(S-adenosyl-homocysteine,SAH)(14.97 μmol·L-1)、Isoasp-DSIP(96.1 μmol·L-1)、S-腺苷-L-甲硫氨酸(S-adenosyl-methionine,SAM)(1 mmol·L-1)、异天冬氨酸甲基转移酶(protein isoaspartate methyltransferase,PIMT)、5倍反应缓冲液,0.3 mol·L-1磷酸];牛胰蛋白酶(Sigma-Alderich公司,批号:SLBG6452V);磷酸二氢钾(批号:20190509)、磷酸氢二钾(批号:20180109)、无水硫酸钠(批号:20181023)、磷酸(批号:20160425)、乙醇胺(批号:20200807)均为分析纯试剂,盐酸(批号:20190118)优级纯,购于国药集团化学试剂有限公司;甲醇色谱级(Scharlau公司,批号:20277613);超纯水。
1.2仪器 Agilent 1260 Infinity Ⅱ高效液相色谱仪(安捷伦科技有限公司),METTLER TOLEDO XS205BU电子天平(梅特勒-托利多仪器公司,感量:0.01 mg),METTLER SevenEasy pH计(梅特勒-托利多仪器公司),ELGA纯水机,VORTEX-Kylin-Bell涡旋仪(海门市其林贝尔仪器制造有限公司),DK-S26电热恒温水浴锅(上海精宏实验设备有限公司),SK250LHC超声波清洗仪(上海科导超声仪器有限公司),R1750R高速离心机(湖南湘仪实验室仪器开发有限公司)。
2 方法与结果
2.1溶液的制备
2.1.1磷酸钾缓冲液 取磷酸二氢钾1.08 g,磷酸氢二钾0.25 g,加水使溶解并稀释至1000 mL,用磷酸调节pH值至6.2[7]。
2.1.2胰蛋白酶溶液 取牛胰蛋白酶适量,加50 mmol·L-1醋酸-磷酸钾缓冲液(pH值6.2)(1:9)溶解,并制成含胰蛋白酶2 mg·mL-1的溶液。
2.1.3Isoasp-DSIP对照品溶液 取试剂盒中Isoasp-DSIP对照品,用水稀释20倍,制备含Isoasp-DSIP 4.805 μmol·L-1的溶液(冰上配制)。
2.1.4主反应混合物(master mix,MM)溶液 取SAM适量,用水稀释10倍,制成100 μmol·L-1的SAM溶液,再依次加水、5倍反应缓冲液、SAM溶液、PIMT按1:1:1:1制备混合溶液(冰上配制)。
2.1.5SAH对照品溶液 用水稀释SAH对照品,制备浓度分别为0.25,0.50,0.75,1.25,2.50,3.75 μmol·L-1系列SAH对照品溶液适量,置200 μL进样瓶中。
2.2酶反应
2.2.1胰蛋白酶消化 取甘舒霖®30R(批号:3M12019065353)且室温放置30 min,摇匀,精密量取200 μL,加入胰蛋白酶溶液4 μL,混匀,作为样品溶液。同时取超纯水同法制备空白样品溶液。将上述两种溶液,在37 ℃孵育1 h,立即置-18 ℃冰箱中止反应。
2.2.2PIMT反应 取经“2.2.1”项下消化后的样品溶液、空白样品溶液和Isoasp-DSIP对照品溶液各30 μL,分别置200 μL离心管中,各加入MM溶液 40 μL,轻轻涡旋混匀,离心(4 ℃,12 000 r·min-1),以确保所有液体均在管底。将离心管置于30 ℃水浴中保持30 min。取出放置冰上,立即加终止液(0.3 mol·L-1磷酸)10 μL,放置5~10 min至反应完全,轻轻涡旋混匀,离心(4 ℃,12 000 r·min-1,有效离心半径8.56 cm),取上清液置200 μL进样瓶中(避光保存)。
2.3HPLC检测
2.3.1色谱条件 用十八烷基键合硅胶为填充剂:Agilent Eclipse XDB-C18色谱柱(150 mm ×4.6 mm,5 μm);柱温:25 ℃;流速:1.0 mL·min-1;采用DAD检测器,检测波长:260 nm。以甲醇和磷酸钾缓冲液为二元溶剂体系,梯度洗脱:0~2 min,10%甲醇;>2~10 min,10%→30%甲醇;>10~12 min,30%→90%甲醇;>12~13 min,90%甲醇。
2.3.2测定法 取各SAH对照品溶液、“2.2.2”项下4种溶液各20 μL,分别注入液相色谱仪,记录色谱图,见图1。
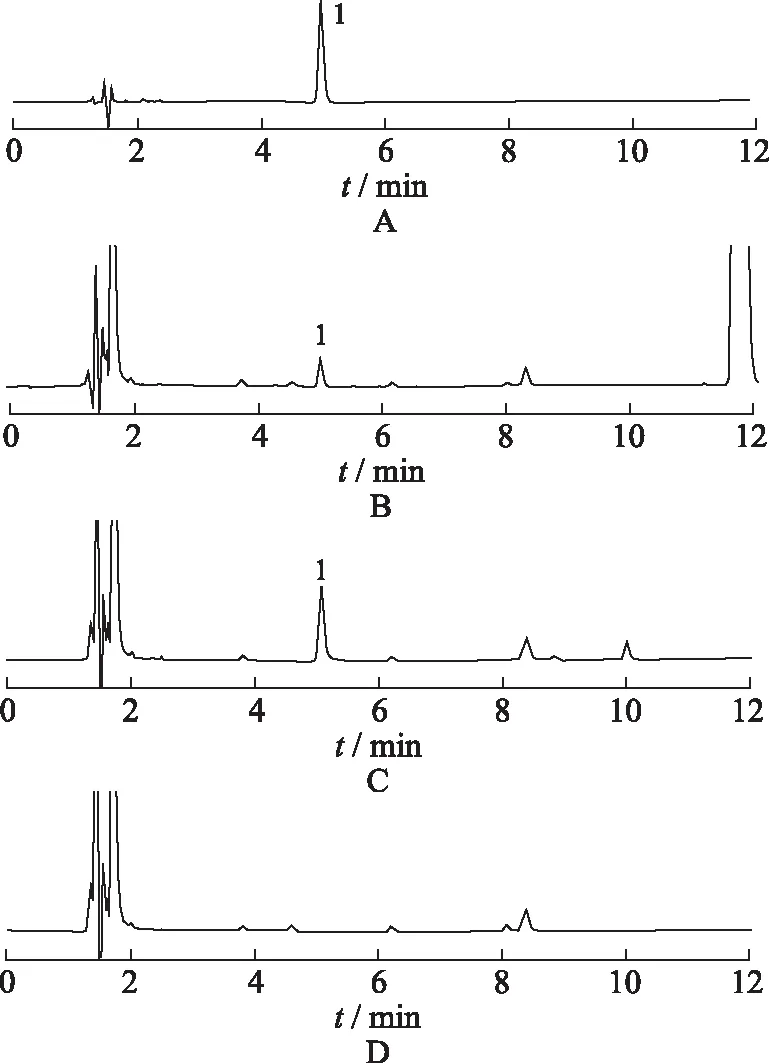
A.SAH对照品;B.样品;C.isoAsp-DSIP对照品;D.空白;1.SAH。图1 混合重组人胰岛素注射液isoAsp含量检测HPLC色谱图A.SAH reference;B.Sample;C.isoAsp-DSIP reference;D.blank control;1.SAH.Fig.1 HPLC chromatograms of isoAsp quantification in mixture of recombinant human insulin injection
2.3.3线性关系考察 精密量取浓度为0.25,0.50,0.75,1.25,2.50,3.75 μmol·L-1系列SAH对照品溶液,按照“2.3.1”项色谱条件,进样20 μL,记录色谱图,以所得 SAH峰面积为纵坐标(Y),SAH进样量(X)为横坐标,绘制标准曲线,线性方程为Y=0.893 2X-0.886 0,r=0.999 3,结果显示SAH对照品浓度在0.25~3.75 μmol·L-1,线性关系良好。
2.3.4精密度和稳定性 为了确保整个过程的准确性和稳定性,实验中总共进样6次2.5 μmol·L-1SAH对照品溶液,开始、中间和结束时各2次(10 h),以便在实验的不同阶段考察系统的适用性。结果保留时间为(5.067±0.003) min,RSD为0.06%,峰面积为42.89±0.23,RSD为0.54%。
2.3.5Isoasp-DSIP对照品的测定 添加的isoAsp-DSIP对照品为4.805 μmol·L-1,测定的isoAsp含量结果为4.963 μmol·L-1(+3.3%),符合测定结果在±10%范围内的要求,表明本实验检测有效。
2.3.6重复性实验 取30/70混合重组人胰岛素注射液样品(批号:3M12019065353),照“2.2”项下方法平行制备6份,注入液相色谱仪,记录,代入标准曲线计算,结果峰面积RSD为2.63%,isoAsp含量为(1.88±0.05) nmol·mL-1,RSD为2.44%。
2.3.7回收率实验 取“2.2.1”项下样品溶液15 μL与SAH(14.97 μmol·L-1)对照品各1,4,10 μL,加水至30 μL,混合均匀,制备低、中、高3种加标溶液各3份,分别置200 μL离心管中,照“2.2.2”项下进行实验,测得的9份回收溶液SAH的量,计算加标回收率。低、中、高浓度加标回收率测定结果分别为114.0%,104.6%,97.29%,平均为105.3%,RSD为6.9%。表明实验体系无干扰,保证实验所得数据的准确度。
2.3.8检出限 对照品SAH在进样量5 pmol时,色谱峰的信号(S/N)为13.5,符合定量要求。
2.3.9样品的测定 对不同厂家的样品进行isoAsp含量进行测定,结果见表1。
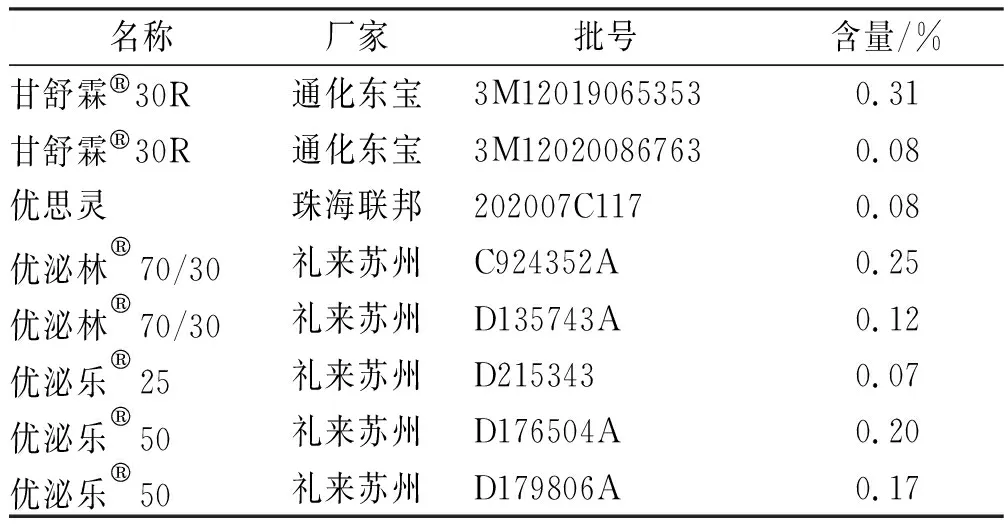
表1 不同厂家的isoAsp含量Tab.1 The content of isoAsp in samples from different companies
3 讨论
本研究先用胰蛋白酶将混合重组人胰岛素注射液中的蛋白成分进行消化,产生分子结构更小的多肽片段,再利用PIMT(EC:2.1.1.77)的特异性作用,催化SAM上甲基转移至isoAsp成为异天冬氨酸甲酯,SAM失去-CH3生成SAH,结合HPLC法,采用外标校正法检测SAH的浓度,进而间接检测isoAsp的浓度,建立混合重组人胰岛素注射液中isoAsp的质量控制方法。
本研究对样品消化时间(0.5,1 和2 h)、胰蛋白酶溶液配制溶剂(50 mmol·L-1醋酸-磷酸钾缓冲液、50 mmol·L-1醋酸)进行考察,最后选择缓冲液溶解的胰蛋白酶消化1 h处理样品效果较好。
通常酶消化后的样品采用磷酸终止反应,而本研究采取在-18 ℃立即冷冻停止反应。实验中发现在下一步PIMT反应中,加入的磷酸使样品溶液pH值较低,会影响PIMT酶的活性(PIMT酶在pH值6~8活性较高),阻断SAM与样品中的isoAsp的反应。
《中华人民共和国药典》2020年版三部收载A21脱氨胰岛素[8]的测定方法。参考该方法测定各厂家样品的A21脱氨胰岛素含量,并将测定结果与isoAsp含量相比较,发现样品中isoAsp测定结果较A21脱氨胰岛素高,表明样品中可能存在其他位点的脱酰胺化[9]。
利用胰蛋白酶消化样品可能存在一定假阳性风险,LIU等[10]发现,在pH值 4.5条件下,Glu-C同样可以有效地酶解样品,且样品在酶解过程中几乎不发生新的脱酰胺化,从而使测得的脱酰胺水平更接近样品中的真实值。isoAsp的产生是个动态变化的过程,建立准确定量的检测方法[11-13]非常必要。
