西洋参药材的等级标准及质量评价研究
2022-01-16张洋蔡广知刘小康贡济宇
张洋 蔡广知 刘小康 贡济宇


摘 要 目的 建立西洋參药材的等级标准,并对不同等级药材的质量进行评价。方法 以24批西洋参药材为样本,采用Pearson相关性分析方法对定性分析指标(主根长度、主根直径和单根药材质量)与内在成分指标(醇溶性浸出物及人参皂苷Rg1、人参皂苷Re、人参皂苷Rb1、人参皂苷Rc、人参皂苷Rb2、人参皂苷Rd、拟人参皂苷F11的含量)间的相关性进行分析,结合化学计量学方法筛选出西洋参等级划分的参考指标,并制定等级划分标准。建立24批西洋参药材的高效液相色谱-蒸发光散射检测器(HPLC-ELSD)指纹图谱并进行相似度评价,通过与对照品比对进行色谱峰的指认,然后结合聚类分析对不同等级西洋参药材进行质量评价。结果 经筛选,确定主根直径、单根药材质量和人参皂苷Rd含量为西洋参药材等级划分的参考指标。根据上述3个指标,将西洋参药材分为特等、一等和二等3个等级。根据K-均值聚类的中心值,算出特等药材的总得分>135.40,一等药材的总得分为61.82~135.40,二等药材的总得分<61.82。从24批西洋参药材的HPLC-ELSD指纹图谱中,共确定了25个共有峰,并指认了其中7个特征峰;特等、一等、二等西洋参药材的色谱图与对照指纹图谱的相似度分别为0.980~0.989、0.962~0.968、0.940~0.949。聚类分析结果显示,不同等级西洋参药材可被明显区分开。结论 本研究建立了西洋参药材的等级标准和HPLC-ELSD指纹图谱,可应用于西洋参药材的专属鉴别,并为其质量控制及等级划分提供参考。
关键词 西洋参;等级标准;高效液相色谱-蒸发光散射检测器;质量评价;指纹图谱
中图分类号 R282 文献标志码 A 文章编号 1001-0408(2022)01-0051-07
DOI 10.6039/j.issn.1001-0408.2022.01.09
ABSTRACT OBJECTIVE To establish the grade standard for Panax quinquefolium and to evaluate the quality of different grades of medicinal materials. METHODS Totally 24 batches of P. quinquefolium were used as test samples. Pearson correlation analysis method was used to analyze the correlation between qualitative analysis indicators (taproot length, taproot diameter and weight of single root) and internal component indicators (ethanol-soluble extract, and the contents of ginsenoside Rg1, ginsenoside Re, ginsenoside Rb1, ginsenoside Rc, ginsenoside Rb2, ginsenoside Rd, pseudo-ginsenoside F11). Combined with chemometrics methods, the reference indexes for the classification of P. quinquefolium were selected, and the classification standards were formulated. HPLC-ELSD fingerprints of 24 batches of P. quinquefolium were established and their similarity evaluation was also performed. The chromatographic peaks were identified by comparison with the reference substance, and then the quality of different grades of P. quinquefolium was evaluated by cluster analysis. RESULTS After screening, taproot diameter, the weight of single root and the content of ginsenoside Rd were taken as the reference indexes for the classification of P. quinquefolium. According to above 3 indexes, P. quinquefolium were divided into 3 grades: special grade, first grade and second grade. According to the center value of K-means clustering, the total score of special-grade medicinal materials was more than 135.40, that of first-grade medicinal materials was 61.82-135.40, and that of second-grade medicinal materials was less than 61.82. In the HPLC-ELSD fingerprints of 24 batches of P. quinquefolium, 25 common peaks were confirmed, and 7 characteristic peaks were identified. The similarity of the chromatograms of P. quinquefolium of special grade, first grade and second grade with fingerprints ranged 0.980-0.989, 0.962-0.968, 0.940-0.949, respectively. The results of cluster analysis showed that different grades of P. quinquefolium could be identified significantly. CONCLUSIONS The grade standard and HPLC-ELSD fingerprints of P. quinquefolium are established, which can be applied for exclusive identification of P. quinquefolium, and provide reference for its quality control and grade classification.
KEYWORDS Panax quinquefolium; grade standard; HPLC- ELSD; quality evaluation; fingerprint
西洋参为五加科人参属植物西洋参Panax quinquefolium L.的干燥根[1],始载于清代《本草从新》。西洋参味苦,性寒,微甘,味厚气薄,能补肺降火、生津液、除烦躁[2]。现代研究表明,西洋参含有皂苷类、挥发油类等成分,其中以人参皂苷为主要有效成分,如人参皂苷Rg1、Re、Rb1、Rd等[3]。西洋参具有提高免疫力、降低血糖、抗疲劳及抗衰老等多种药理作用[4-6],市场需求量较大。
西洋参最初是从北美洲引种到我国,目前在吉林、黑龙江和山东等地均有大量栽培[7-8]。由于其市场需求量越来越大,出现了大量掺伪、掺假的现象,如利用人参等同科属植物进行掺伪[9]。与此同时,市场流通的西洋参质量参差不齐,现行的西洋参等级标准仅遵循“辨状论质”原则,从表面形状、断面等将其划分为3个等级(特等、一等和二等)[2]。然而,西洋参药材的质量受多种因素影响,根据主观性状描述无法对其进行全面评价[10-13]。
西洋参和人参的化学成分基本相似,均以人参皂苷(如人参皂苷Rb1、Re、Rg1等)为主要活性成分。虽然人参皂苷的种类多、分离困难,但有些皂苷类成分是西洋参所特有的,如拟人参皂苷F11[14]。目前,大多数的研究都是采用高效液相色谱(high pressure chromatography,HPLC)法对西洋参的质量进行控制和评价,并且多与紫外检测器或二极管阵列检测器联用[15-19],但西洋参中拟人参皂苷F11等特征性成分并无紫外吸收,上述方法难以对西洋参进行全面的成分分析。蒸发光散射检测器(evaporative light-scattering detector,ELSD)具有适用范围广且可以消除溶剂峰干扰等优点[20]。选用ELSD为检测器建立西洋参的HPLC-ELSD指纹图谱,可对西洋参更为全面地进行质量评价。鉴于此,本研究通过测定西洋参的外观性状指标,采用HPLC-ELSD法测定西洋参中7种人参皂苷类成分的含量,并结合化学计量学方法对外观性状指标和内在成分指标进行分析,合理划分西洋参药材的等级;同时,建立西洋参药材的HPLC-ELSD指纹图谱,并结合聚类分析方法评价不同等级西洋参药材的质量,以期为西洋参药材的质量控制及等级划分提供参考。
1 材料
1.1 主要仪器
本研究所用主要仪器有Anters-1200Ⅰ型HPLC仪(上海科哲生化科技有限公司,包括在线脱气系统、1050A型高压液相色谱泵、HS-1000型柱温箱、AS3000B型自动进样系统、ELSD-3000KS型ELSD)、AB135-S型十万分之一电子分析天平(瑞士Mettler-Toledo公司)。
1.2 主要药品与试剂
人参皂苷Rb1(批号B21310)、人参皂苷Re(批号B21311)、人参皂苷Rg1(批号B21310)、人参皂苷Rc(批号B21215)、人参皂苷Rb2(批号B21312)、人参皂苷Rd(批号B21210)和拟人参皂苷F11(批号B21218)的对照品均购自上海源叶生物科技有限公司,纯度均不低于98%;乙腈、甲醇为色谱纯,其他试剂均为分析纯,水为超纯水。
1.3 供试药材
本研究所用的24批西洋参药材(生长年限均为4年,商品规格均为短粒)均购自东方红西洋参药业股份有限公司,经长春中医药大学中药鉴定学教研室蔡广知副教授鉴定均为五加科植物西洋参P. quinquefolium L.的干燥根。药材具体来源信息见表1。
2 方法
2.1 外观性状指标的选择及测定
参照2020版《中国药典》(一部)中关于西洋参的性状描述及《中药材商品规格等级(226种)》对西洋参药材外观性状的考察[1,8],本研究选择了主根长度、主根直径及单根药材质量作为西洋参药材的外观性状指标。为保证结果的准确性,在每批药材中分别随机抽取20个样本进行测量:先使用电子天平称定单根药材质量,然后再分别以直尺和数显游标卡尺测定药材的主根长度和主根直径,取平均值。结果,24批西洋参药材的主根长度为4.73~8.08 cm、平均长度为6.55 cm,主根直径为0.87~1.17 cm、平均直径为1.05 cm,单根药材质量为2.25~6.91 g、平均质量为4.57 g。西洋参药材外观性状指标测定结果见表2。
2.2 醇溶性浸出物
按照2020版《中国药典》(四部)醇溶性浸出物测定法项下的热浸法(通则2201)进行测定,溶剂为70%乙醇[1]。结果,24批西洋参药材的醇溶性浸出物含量范围为33.34%~53.98%,平均含量为44.16%,结果见表2。
2.3 HPLC-ELSD法測定西洋参药材中7种人参皂苷类成分的含量
2.3.1 供试品溶液的制备 精密称取西洋参药材粉末1 g,精密加入水饱和正丁醇溶液50 mL,称定质量,水浴加热回流提取1.5 h,冷却后用水饱和正丁醇溶液补足减少的质量,摇匀,过滤,收集续滤液。精密量取续滤液25 mL,回收溶剂至干,残渣用70%甲醇定容至10 mL量瓶中;以0.22 μm微孔滤膜过滤,收集滤液,即得。
2.3.2 混合对照品溶液的制备 精密称取各人参皂苷对照品适量,加甲醇制成分别含人参皂苷Rg1 0.204 mg/mL、人参皂苷Rb1 0.198 mg/mL、人参皂苷Re 0.206 mg/mL、人参皂苷Rb2 0.219 mg/mL、人参皂苷Rc 0.213 mg/mL、拟人参皂苷F11 0.214 mg/mL和人参皂苷Rd 0.223 mg/mL的混合对照品溶液。
2.3.3 色谱条件 采用大连依利特Hypsil C18色谱柱(250 mm×4.6 mm,5 μm);以乙腈(A)-水(B)为流动相进行梯度洗脱(0~15 min,19%A;15~30 min,19%A→29%A;30~42 min,29%A;42~45 min,29%A→33%A;45~65 min,33%A→40%A;65~70 min,40%A);进样量为20 μL;柱温为25 ℃;流速为1.0 mL/min;漂移管温度为50 ℃;载气流量为1.0 L/min。
2.3.4 方法学考察 依据2020版《中国药典》(四部)分析方法验证指导原则进行方法学考察[1]。专属性试验结果如图1所示,空白溶剂(甲醇溶液)对待测成分的测定无影响,各待测色谱峰与相邻峰间的分离度均大于1.5。以各待测成分峰面积的对数值(y)作为纵坐标、进样量的对数值(x)作为横坐标进行方程拟合,得到人参皂苷Rg1、人参皂苷Re、人参皂苷Rb1、人参皂苷Rc、人参皂苷Rb2、人参皂苷Rd、拟人参皂苷F11的回归方程分别为y=0.971 9x+3.305 3(R2=0.999 6)、y=1.542 3x+2.369 4(R2=0.999 3)、y=0.983 4x+3.246 8(R2=0.999 5)、y=1.630 9x+2.110 7(R2=0.999 1)、y=1.974 6x+1.763 0(R2=0.999 2)、y=1.229 8x+3.381 6(R2=0.999 1)、y=1.185 5x+ 3.280 8(R2=0.999 3),分别在0.2~3.2、5.1~14.5、6.6~32.8、1.4~10.9、0.1~0.7、0.6~4.4、0.3~2.5 μg进样量范围内与其峰面积的线性关系良好;精密度试验中,峰面积的RSD分别为1.74%、1.06%、1.45%、1.86%、1.73%、1.05%、1.61%(n=6);重复性试验中,含量的RSD分别为1.04%、1.72%、1.08%、1.65%、1.48%、1.54%、1.41%(n=6);稳定性试验(室温放置24 h)中,峰面积的RSD分别为1.02%、0.86%、1.21%、1.35%、1.49%、1.43%、1.75%(n=6);平均加样回收率分别为95.23%、96.82%、96.38%、97.25%、97.58%、97.04%、95.78%(n=6)。结果表明,本方法的专属性、精密度、重复性、准确性良好。
2.3.5 含量测定 取24批西洋参药材,按“2.3.1”项下方法制备供试品溶液,再按“2.3.3”项下色谱条件进样测定,记录峰面积,根据标准曲线计算样品中各成分的含量。每个样品重复进样测定3次,取平均值。结果,24批西洋参药材中人参皂苷Rg1、人参皂苷Re、人参皂苷Rb1、人参皂苷Rc、人参皂苷Rb2、人参皂苷Rd、拟人参皂苷F11的含量分别为0.37~2.58、15.21~29.01、21.79~49.23、2.96~4.98、0.38~1.15、1.36~4.83、0.56~4.96 mg/g。西洋参药材中7种人参皂苷类成分的含量测定结果见表3。
2.4 西洋参药材等级标准的建立
2.4.1 各指标间的相关性分析 利用SPSS 23.0 统计学软件,采用Pearson相关性分析方法对各指标间的相关性进行分析,确定内在指标成分与外观性状指标间的相关性,并选出相关性较高的内在指标成分和外观性状指标,初步确定西洋参药材等级划分的参考指标。各指标间的Pearson相关性分析结果见表4。
由表4结果可知,主根长度与人参皂苷Rd含量呈显著正相关(P<0.05),说明主根越长,人参皂苷Rd的含量越高。主根直径与人参皂苷Rg1、拟人参皂苷F11的含量均呈显著负相关(P<0.05),与人参皂苷Rc含量呈显著负相关(P<0.01),说明主根越粗,人参皂苷Rg1、人参皂苷Rc和拟人参皂苷F11的含量越低。单根药材質量与人参皂苷Rg1、人参皂苷Re、人参皂苷Rc和拟人参皂苷F11的含量呈显著负相关(P<0.05),与人参皂苷Rd含量呈显著正相关(P<0.05),说明单根药材质量越大,人参皂苷Rg1、人参皂苷Re、人参皂苷Rc、拟人参皂苷F11的含量越低,人参皂苷Rd含量越高。因此,本研究初步选取主根长度、主根直径、单根药材质量和人参皂苷Rg1、人参皂苷Re、人参皂苷Rc、人参皂苷Rd、拟人参皂苷F11含量共8个指标为等级划分的参考指标,进行主成分分析(principal component analysis,PCA)。
2.4.2 PCA 以“2.4.1”项下筛选的8个参考指标为变量,采用SIMCA-P 14.1软件对24批西洋参药材进行无监督的PCA,得分图见图2。模型拟合结果显示,第1主成分的特征值为3.494、贡献率为43.669%,第2主成分的特征值为1.349、贡献率为16.861%,第3主成分的特征值为1.054、贡献率为13.172%,3个主成分的累计贡献率为73.702%,表明提取的3个主成分可以很好地反映药材的大部分信息。PCA结果显示,24批西洋参药材被分成3类:样品S1、S5、S7、S15、S16、S18、S20和S24为第1类,样品S2、S3、S4、S6、S10、S14、S17和S22为第2类,其他样品为第3类。
2.4.3 偏最小二乘法-判别分析 PCA将24批西洋参药材初步分为3类,为进一步找到3类样品间的差异性指标,本研究以“2.4.1”项下初步筛选的8个指标为变量,采用SIMCA-P 14.1软件对24批药材进行有监督的偏最小二乘法-判别分析(partial least squares discriminant analysis,PLS-DA),得分图见图3。PLS-DA结果显示,24批西洋参样品初步分为3类,与PCA结果一致。
变量投影重要性分析值(variable importance in projection,VIP)可用来描述PLS-DA分析中变量的变异程度:若某变量的VIP>1,说明对应变量的变异程度较大[21]。本研究提取了模型中8个指标的VIP,结果见图4。结果显示,在8个变量指标中,单根药材质量(VIP=1.505 8)、主根直径(VIP=1.449 4)和人参皂苷Rd含量(VIP=1.005 1)的VIP均大于1,表明上述3个指标是影响西洋参等级差异的重要指标。
2.4.4 西洋参药材的等级划分标准 根据PCA与PLS-DA结果,本研究拟将西洋参药材划分为3个等级,分别为特等、一等和二等;再根据VIP结果,确定以单根药材质量、主根直径和人参皂苷Rd含量为西洋参药材等级划分的参考指标。采用SPSS 23.0软件对24批西洋参药材中上述3个指标进行K-均值聚类分析,得到等级标准制定中各指标的中心值,结果见表5。
采用SPSSAU统计分析软件中CRITIC权重法对上述3个指标赋予权重系数,得到主根直径、单根药材质量、人参皂苷Rd含量的权重系数分别为0.13、0.55、0.32。根据各指标的权重系数,建立综合评分公式:主根直径得分=(主根直径/主根直径均值)×0.13×100,单根药材质量得分=(单根药材质量/单根药材质量均值)×0.55×100,人参皂苷Rd含量得分=(人参皂苷Rd含量/人参皂苷Rd含量均值)×0.32×100;总得分=主根直径得分+单根药材质量得分+人参皂苷Rd含量得分。将K-均值聚类得到的中心值代入总得分公式,计算出各等级间总得分分界值分别为135.40、61.82。因此,本研究将西洋参的等级标准制定如下:特等药材的总得分>135.40;一等药材的总得分为61.82~135.40;二等药材的总得分<61.82。按照此标准,样品S8、S9、S11、S12、S13、S19、S21、S23被划分为特等;样品S2、S3、S4、S6、S10、S14、S17、S22被划分为一等;样品S1、S5、S7、S15、S16、S18、S20、S24被划分为二等。
3 基于HPLC-ELSD指纹图谱的西洋参药材质量评价
3.1 色谱条件
除梯度洗脱时增加了1个时段(70~100 min,40%A→100%A)外,其余色谱条件均与“2.3.3”项下相同。
3.2 方法学考察
依据2020版《中国药典》(四部)分析方法验证指导原则进行方法学考察[1]。因17号峰(人参皂苷Rb1)的对称性和分离度均良好,故将其作为参照峰(S)计算各共有峰的相对保留时间和相对峰面积。结果显示,精密度试验中各共有峰相对保留时间和相对峰面积的RSD分别小于1.95%、2.38%(n=6),重复性试验中各共有峰相对保留时间和相对峰面积的RSD分别小于1.05%、2.31%(n=6),稳定性试验中各共有峰相对保留时间和相对峰面积的RSD分别小于1.33%、2.92%(n=6)。
3.3 西洋参药材HPLC-ELSD指纹图谱的建立
取24批西洋参药材,按“2.3.1”项下方法制备样品溶液,然后按“2.3.3”项下色谱条件进样测定,记录色谱图。将24批西洋参药材的色谱图导入《中药色谱指纹图谱相似度评价系统(2012版)》中,以样品S1的色谱图为参照图谱,设置时间窗宽度为0.1 min,采用多点校正的方式生成24批西洋参药材的HPLC-ELSD叠加指纹图谱,并采用中位数法生成24批西洋参药材的对照指纹图谱(R)。结果,在24批西洋药材中共标定出25个共有峰。通过与混合对照品溶液图谱(图1B)比对,指认出了其中的7种成分,分别为峰6(人参皂苷Rg1)、峰7(人参皂苷Re)、峰16(拟人参皂苷F11)、峰17(人参皂苷Rb1)、峰18(人参皂苷Rc)、峰19(人参皂苷Rb2)和峰22(人参皂苷Rd)。24批西洋参药材的HPLC-ELSD叠加指纹图谱及对照指纹图谱R见图5。
3.4 相似度评价
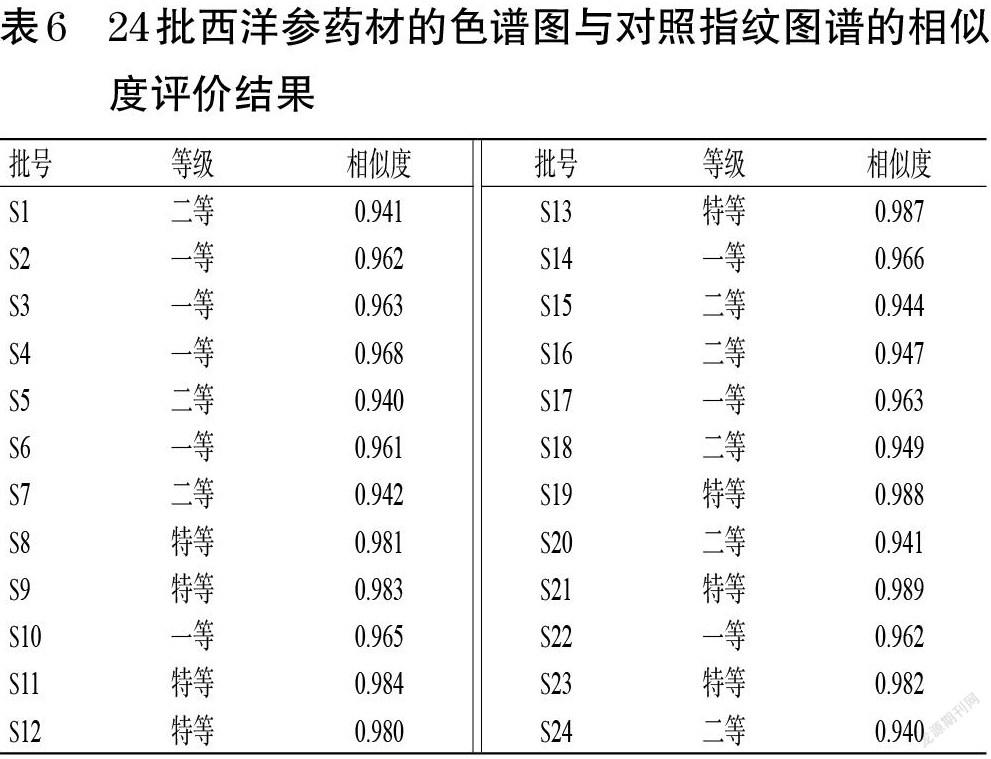
以对照指纹图谱为参考,通过《中药色谱指紋图谱相似度评价系统(2012版)》计算各批次西洋参药材色谱图与对照指纹图谱的相似度,结果见表6。结果显示,24批西洋参药材的色谱图与对照指纹图谱的相似度为0.940~0.989。其中,特等、一等、二等西洋参药材的色谱图与对照指纹图谱的相似度分别为0.980~0.989、0.962~0.968、0.940~0.949。
3.5 聚类分析
以24批西洋参药材中25个共有峰的相对峰面积为变量,利用SPSS 23.0软件进行聚类分析,结果见图6。结果显示,当判别距离为10时,24批西洋参药材被分为3类:特等西洋参药材(S8、S9、S11、S12、S13、S19、S21、S23)为第1类;一等西洋参药材(S2、S3、S4、S6、S10、S14、S17、S22)为第2类;二等西洋参药材(S1、S5、S7、S15、S16、S18、S20、S24)为第3类。聚类分析结果与前文等级划分结果一致,再结合相似度评价结果,提示本研究建立的HPLC-ELSD指纹图谱可用于评价西洋参药材的质量。
4 讨论
李嘉欣等[22]通过对不同生长年限西洋参中皂苷类成分进行测定,发现生长年份1~4年的西洋参中皂苷类成分含量随着生长年限的增加而增加,因此本研究选取相同生长年限(4年生)的西洋参样品进行研究。西洋参药材按主根类型不同分为原丛、短粒、圆粒以及枝这几种规格[8]。因西洋参的主要成分——人参皂苷分布在韧皮部,主根类型的不同可能会导致内在成分与外观性状之间的关系出现差异。因此,在制定西洋参药材等级时,需先区分药材的规格,采用相同规格的西洋参样品进行等级评价研究。本研究前期从 33批西洋参药材中选取24批相同规格(短粒)的西洋参药材进行研究,从源头上保证了研究的合理性。在标准建立后,笔者又利用剩余9批圆粒西洋参样品进行验证实验,发现本研究建立的标准同样适用于圆粒西洋参样品,可为不同规格西洋参等级标准的建立提供参考。
2020版《中国药典》(一部)对西洋参的主根长度、主根直径以及表面颜色、纵皱纹、断面、形成层环纹等外观性状进行了规定。2018年颁布的《中药材商品规格等级(226种)》从表面颜色、蘆头是否修剪、断面颜色、有无疤痕等方面对不同等级西洋参的特征进行了文字描述,并根据单根药材质量进行了规格划分[8]。因此,本研究选取主根直径、主根长度、单根药材质量作为外观性状指标。
前期,笔者通过实地考察发现,不同市场、不同药材售卖点实行的西洋参等级标准并不统一,大多是根据主根直径、主根长度进行主观分等;且西洋参药材的来源广泛,市场上掺假、以次充好的现象频繁发生。一些种植商家为了追求更高的经济利益,甚至会使用植物激素(如膨大剂)来促进西洋参根茎在短时间内变得粗大,虽然从外观性状来看可将上述药材划分为等级较高的一类,但是其所含的有效成分含量却可能较低。这提示,仅仅以单根质量、根茎粗壮等外观性状来判定西洋参的品质优劣缺乏一定的科学依据[11]。因此,本研究在外观性状的基础上,通过HPLC-ELSD法测定了西洋参中7种人参皂苷类活性成分的含量,并通过探究外观性状与内在成分的相关性,建立了一个结合了药材内、外多指标的等级划分标准,完善了西洋参药材品质的评价体系。同时,本研究建立的西洋参HPLC-ELSD指纹图谱可以指认西洋参药材中的特征性成分——拟人参皂苷F11,可应用于西洋参药材的专属鉴别;并且根据相似度评价结果来看,也可明显区分不同等级的西洋参药材。
综上所述,本研究建立了西洋参药材的等级划分标准,可为西洋参药材的质量控制及等级划分提供一定的参考。在此研究的基础上,今后笔者将增加样本量以及增加总皂苷、总黄酮等评价指标,进一步验证和优化西洋参药材的等级标准。
参考文献
[ 1 ] 国家药典委员会.中华人民共和国药典:一部[S]. 2020年版.北京:中国医药科技出版社,2020:136.
[ 2 ] 国家市场监督管理总局,国家标准化管理委员会.西洋参分等质量:GB/T 36397-2018[S].北京:中国标准出版社,2018.
[ 3 ] 钟运香,袁娇,刘丰惠,等.西洋参化学成分、药理作用及质量控制研究进展[J].中国中医药现代远程教育,2020,18(7):130-133.
[ 4 ] 于现花,刘军玲,金传山,等.西洋参破壁饮片中8种人参皂苷类成分双标多测法的建立[J].中国药房,2021,32(11):1345-1350.
[ 5 ] 李嘉欣,李梦瑶,张单丽,等. HPLC法同时测定不同生长年限、部位西洋参中2类成分[J].中成药,2020,42(10):2670-2674.
[ 6 ] 吕婧,高燕,李晨,等.基于斑马鱼模式生物的西洋参皂苷类成分增强免疫作用研究[J].中草药,2020,51(14):3728-3733.
[ 7 ] 李俊飞,焦晓林,毕艳孟,等.基于药材品质的山东西洋参主产区栽培地土壤肥力质量评价[J].中国中药杂志,2020,45(19):4598-4605.
[ 8 ] 赵方杰,廉喜红,胡小平,等.不同产地西洋参氨基酸种类及含量分析[J].西北农业学报,2020,29(7):1051-1058.
[ 9 ] 宋茜,孔祥词,陈树东,等.人参和西洋参的HPLC指纹图谱及化学模式识别研究[J].中国口岸科学技术,2021,3(5):56-63.
[10] 曹雪,蔡广知,赵凌,等.基于复合质量常数的北柴胡饮片等级评价[J].中国实验方剂学杂志,2018,24(18):36-41.
[11] 魏可欣,郭云龙,史娜文,等.人参药材等级标准[J].中国实验方剂学杂志,2019,25(11):145-153.
[12] 刘战,侯晓琳,宿莹,等.龙胆药材中龙胆苦苷、马钱酸含量测定与其外观性状的相关性及质量等级标准研究[J].中国药房,2019,30(16):2237-2242.
[13] 邓哲,焦梦姣,章军,等.相对质量常数用于甘草饮片等级评价研究[J].中国中药杂志,2017,42(13):2492-2496.
[14] 严华,张慧秀,白宗利,等.基于特征图谱的人参属药材西洋参、人参、三七的比较[J].世界中医药,2021,16(6):887-895.
[15] 顾承真,曾碧雪,张钰佳,等.人参属植物高温蒸制前后人参皂苷含量的变化和细胞毒活性研究[J].中草药,2021,52(11):3391-3397.
[16] 杨洋,赵大庆,李佳奇,等.基于指纹图谱结合化学计量法对不同干燥方式下西洋参皂苷类成分的分析[J].中华中医药学刊,2021,39(10):21-25,262.
[17] 高晖富,姜丽萍,姜志辉,等.不同方法测定不同产地西洋参中人参皂苷含量[J].人参研究,2017,29(4):6-8.
[18] 张丹,吴兰芳,王乾,等.不同产地西洋参药材中8种人参皂苷类成分含量测定及指纹图谱研究[J].中药材,2016,39(10):2276-2280.
[19] 张丹,郑开颜,吴兰芳,等.西洋参药材的质量特征与商品规格的相关性分析[J].中国中药杂志,2016,41(18):3329-3335.
[20] 刘璐,于双雨,刘艳华. HPLC-ELSD法测定胃康颗粒中人参皂苷Rb1和黄芪甲苷的含量[J].药学实践杂志,2020,38(4):359-363.
[21] 周昱杉,梁洁,黄光强,等.基于化学模式识别方法分析止得咳颗粒的抗炎谱效关系[J].中国实验方剂学杂志,2020,26(22):156-163.
[22] 李嘉欣,李梦瑶,张单丽,等. HPLC法同时测定不同生长年限、部位西洋参中2类成分[J].中成药,2020,42(10):2670-2674.
(收稿日期:2021-08-19 修回日期:2021-11-19)
(编辑:林 静)
