急性与慢性运动调控自噬水平机制研究进展
2022-01-12靳宝铭王岑依
靳宝铭 王岑依
(苏州大学体育学院 江苏苏州 215301)
长期久坐的生活方式会显著增加心肺疾病、2型糖尿病、癌症等疾病的患病风险[1]。体育运动可以增强免疫系统功能,有效预防慢性病的发生。过往研究已经指出,适当强度的运动锻炼,不仅能减轻压力,还能维持生理稳定,显著改善能量代谢、神经功能和心肺功能[2]。运动激活自噬是维持肌细胞代谢和能量稳定的重要机制。运动锻炼可以由多种信号传导通路以调控自噬水平,不同类型的运动方式对肌细胞自噬活性影响亦存在差异。然而,适度的运动可促进细胞自噬,而过度运动则可能导致细胞自噬破坏,严重时甚至会引起程序性细胞损伤或死亡。根据运动锻炼时间和锻炼频率,运动可以分为慢性运动和急性运动两种类型。慢性运动可定义为一定时间内反复进行一定量的运动,急性运动可定义为一次性运动。两种运动方式对自噬的影响会因运动时长和运动干预方式的不同而改变自噬活性水平。因此,该综述将回顾急性运动与慢性运动调控细胞自噬激活相关机制,希望为进一步探讨运动调控自噬活性机制提供参考依据。
1 运动对肌细胞自噬能力的影响
肌肉是人体最丰富的组织,也是人体中主要的氨基酸储存库。过度或受损的细胞自噬不利于肌肉健康和功能,甚至可能导致肌肉萎缩,而最佳的自噬激活电位或能力可以维持肌肉的完整性。运动对肌细胞自噬的作用机制主要包括骨骼肌细胞自噬和心肌细胞自噬调节作用。
1.1 运动对骨骼肌自噬的影响
适度的自噬在维持骨骼肌质量和功能调节方面发挥着重要作用。高强度运动可引起骨骼肌纤维退化,导致的骨骼肌萎缩或肌肉无力,当骨骼肌过度自噬时,可能会导致自噬性肌肉萎缩或质量维持下降。因此,运动方式和运动强度对于维持自噬调节、骨骼肌内部环境的稳定平衡以及提高骨骼肌运动能力都具有特别重要意义。细胞自噬在骨骼肌质量控制中的作用至关重要,其降解主要通过泛素蛋白酶体和自噬溶酶体降解途径调控。虽然目前其机制尚不明确,但过度自噬可导致骨骼肌萎缩[3]。运动训练可以增加骨骼肌细胞的自噬活性。虽然运动训练加快了细胞更新的速度,有利于机体的稳定,但过度训练会改变细胞自噬的敏感性,从而导致骨骼肌质量紊乱。因为肌肉萎缩相关基因Atrogin-1 和MuRF1 以及自噬相关基因如Atg7、Beclin1、LC3 和FoxO3 的活性会因过度运动而增加,从而导致骨骼肌细胞中蛋白质含量的过度降解,引起细胞抵抗降低,出现肌肉萎缩[4]。
1.2 运动对心肌自噬的影响
心肌细胞中含有丰富的肌原纤维以执行长时间持续收缩功能,具有高度分化的特点,激活细胞自噬可降解损伤的蛋白质分子,为心肌细胞提供能量。心肌肥大是心肌对各种心肌疾病的适应性反应,心肌肥大往往伴随着自噬水平的降低,也常出现心肌细胞中LC3蛋白表达的下降,而Atg5 和Atg7 蛋白水平的下降可导致心脏的心室扩张和收缩功能障碍[5]。自噬可降解变性蛋白并产生氨基酸,在心肌细胞质量、心肌形态结构和功能以及维持内环境的稳定扮演着关键角色。心肌自噬活性的适度激活,可防止肌细胞由于超载的血流动力导致心脏受损,但当心肌自噬被过度调节或抑制时,会发生异常的心脏功能[6]。
适度运动可增加心肌细胞自噬水平,降解细胞内代谢废物,从而维持心肌细胞稳态[7]。有研究表明,运动可以通过改变心肌自噬水平来改善受损的心脏功能。一定时间的运动可显著增加衰老心肌细胞膜双分子层的自噬体,提高自噬相关蛋白水平,从而改善心脏功能[8]。此外,运动还可以通过提高心肌BNIP3、LC3-II/LC3-I等关键蛋白的表达,降低p62蛋白的表达以提高心肌细胞自噬水平,减轻心肌细胞损伤[9]。
2 急性运动诱导自噬
2.1 急性运动对骨骼肌自噬影响的机制
研究表明,以12.3m/min 进行一次50min 的跑台训练后,小鼠的LC3-II、Beclinl、Atg7和AMP2表达水平降低,自噬活性降低[10]。相反,一次训练90min 后55%VO2max,LC3-II 表达明显增加,LC3-II/LC3-I 比值也显著增加[11]。这种看似矛盾的结果,应考虑是否与运动干预的时长和强度差异引起能量消耗水平出现差异有关。此外,有研究发现,急性运动后,LC3-II/LC3-I 比值降低,而将VO2max运动强度增加到70%时,LC3-II/LC3-I 比值则表现为显著升高,p62 蛋白表达显著降低[12]。这表明,低强度运动可能降低了能量消耗,从而导致自噬过程的启动失败。
急性运动结束收集肌细胞样本的时间差异,也可能成为影响自噬活性的因素之一,运动后自噬活性的变化具有较高的时间敏感性。一项急性跑台运动研究发现,小鼠骨骼肌的LC3-II蛋白表达在运动15min后降低,随后在30~80min逐渐升高。相反,p62蛋白在急性运动后,立刻出现了表达升高,在30~60min表达又逐渐下降;同样,骨骼肌细胞中Bcl2-Beclinl复合物的表达在停止运动初期(15min)出现降低,而到30min 后几乎检测不到[13]。此外,骨骼肌糖原水平的高低亦对自噬活性有重要影响。研究显示,骨骼肌中自噬小体的数量会在小鼠中禁食24h 后出现增加,而在一次速度12 m/min,时长为2h 的运动干预后,肌细胞中LC3-II/LC3-I比值表现出下降趋势,表明小鼠在禁食情况进行运动锻炼会抑制其骨骼肌细胞自噬活性[14]。运动可以在肌糖原缺乏的情况下抑制自噬活性,这可能是由于机体为预防骨骼肌受到过度降解而形成的一种保护机制。
2.2 急性运动影响心肌自噬的机制
在细胞内参与细胞自噬的蛋白中,Atg8 和Atg6 在哺乳动物中也被称为LC-3 和Beclin1,mTOR 信号通路和泛素样蛋白系统都参与了细胞自噬的调控过程[15]。由于炎症反应、蛋白质合成与降解、细胞凋亡等多种因素可能在一定程度上参与骨骼肌的能量代谢或衰老过程,自噬对维持机体的运动能力,保持健康状态扮演着重要角色。心肌细胞凋亡与维持心脏稳态和参与心脏病理过程密切相关[16]。急性运动降低了Bcl-2 蛋白的表达,特别是当急性运动持续时间超过1.5h时,凋亡相关的Bcl-2表达明显减少[17]。由此可推断,急性运动可能同时激活自噬与凋亡信号通路,在急性运动时突然受到大强度的运动刺激诱导肌细胞迅速凋亡,而机体无法在短时间内迅速激活相关调节机制抑制凋亡[18]。
急性运动可促进自噬相关蛋白Beclin1 的表达。不同形式的运动可以不同程度地增加心肌组织中细胞自噬相关蛋白Beclin1的水平,从而增强组织细胞的自噬活性,并有助于维持细胞内稳态,合理消除自由基和衰老蛋白,为细胞代谢提供能量。有研究表明,跑台运动和游泳运动比自由转轮运动自噬相关蛋白Beclin1的增幅更大,说明跑台运动和游泳运动更能提高细胞自噬相关蛋白Beclin1 的水平,增强细胞自噬活性[19]。已有大量的文献报道,由于心肌细胞分化再生能力很低,而细胞自噬可促进心肌保护有效对抗损伤,因此,心肌细胞自噬在保护心脏功能上发挥着显著作用。
3 慢性运动诱导自噬
3.1 慢性运动影响骨骼肌自噬的机制
慢性运动中运动的时长和选取的肌肉类型对研究骨骼肌自噬活性有着显著影响。在一项研究中,对小鼠进行速度30m/min,每天60min,为期5天的跑台干预后,骨骼肌纤维中Beclinl、Atg4、Atg7、Atg12与LC3蛋白水平均未发现变化[20]。相比之下,另一些研究结果则表明,运动干预4周后,小鼠比目鱼肌中的LC3II蛋白以及LC3II/LC3I 比值均出现了明显升高,Beclin1、线粒体自噬蛋白BNIP3、Atg6和Atg7等也表现出上升趋势,p62 蛋白则表达明显下降[21]。而不同骨骼肌纤维组织在面对自噬的刺激则会产生不同的反应。研究显示,运动干预4周后,比目鱼肌和跖骨肌肉中自噬相关蛋白Atg6、Atg7、BNIP3、COX-4、PGC-1α 均会出现明显上调,但比目鱼肌自噬相关蛋白水平明显高于跖骨肌,这提示不同类型肌纤维组织对运动干预诱导自噬活性水平影响并不相同[22]。尽管不同类型的锻炼形式都能增加肌细胞的自噬活性,但过度延长锻炼时长可能又会引起骨骼肌发生适应性改变。研究显示,大鼠经过36周的长时间运动干预后,其骨骼肌Beclinl、LC3 II/LC3 I、P62 等蛋白表达水平均无明显变化[23]。这项结果表明,持续延长运动干预周期可能使骨骼肌组织对运动刺激出现适应,而引起自噬活性不再进一步改变。
3.2 慢性运动影响心肌自噬的机制
适度的运动可以刺激细胞自噬水平的增加,从而预防或减轻各种心脏病的发展。运动可有效诱导自噬,长时间的锻炼可增加正常心肌细胞中自噬相关蛋白的表达。研究发现,慢性运动能够通过上调LC3-I、LC3-II和Beclin1的表达,降低p62蛋白水平的表达,增加心肌细胞自噬水平,进而进一步增强个体机能对运动锻炼的适应性[24]。与此同时,慢性运动还可以可刺激信号通路的代偿激活增加自噬水平,消除心肌细胞中损伤的蛋白和代谢物,减少心肌细胞损伤从而维持心脏代谢平衡。自噬降解受损细胞器和蛋白质后产生的生物分子也可成为合成代谢所需的底物,为维持心肌细胞的结构和正常生理功能提供物质基础[25]。与急性运动不同,慢性运动可诱导自噬并抑制细胞凋亡,这表明慢性运动能更好地维持细胞稳态。心脏重量和血流动力能够刺激心肌中自噬相关蛋白Beclinl 增长,但值得注意的是,在心肌特异性Beclinl表达剂量不足时,心脏重量和血流动力学外渗应激并未发现有明显变化,这可能是心肌细胞通过抑制自噬来调节应激诱导的心肌肥厚[26]。另一方面,心肌细胞通过线粒体的自噬也可以明显促进心肌细胞的内环境的稳定。研究发现,在经过跑步、游泳等不同运动方式的长期运动锻炼后,小鼠心肌细胞内线粒体的数量和体积明显增加,这表明长期坚持中等强度的运动锻炼,可提升肌细胞中线粒体的数量和质量[27]。
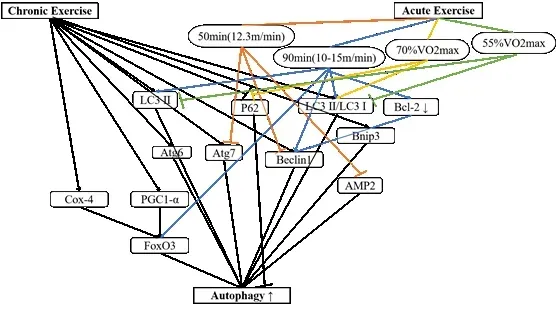
图1 急性与慢性运动诱导自噬信号通路可能机制
4 结语
综上所述,运动锻炼具有双重调节作用。适当的运动强度可上调细胞自噬水平,降解细胞内残基和破坏细胞器,维持细胞内稳定。大强度运动可能会使细胞自噬过度激活,导致细胞质和细胞器过度下降,造成细胞损伤和疲劳。同时,长期的运动锻炼可增强细胞自噬激活的可塑性,进一步改善细胞内环境的稳定性和能量代谢的平衡,对提高肌肉运动适应性和运动能力具有重要作用。当前,有关运动与自噬活性的研究仍处于初步探索阶段,不同运动对自噬的具体激活机制尚需进一步研究。未来的实验研究可以从运动能量代谢途径和因子变化的来源来探讨运动对自噬的影响,以为进一步探讨运动促进健康提供坚实的基础依据。
