黄芩苷壳寡糖纳米粒的体外释放与模型
2022-01-07吕凤娇蔡菊虹陈西林吴幼兰
吕凤娇,蔡菊虹,陈西林,吴幼兰
(泉州师范学院 化工与材料学院,福建 泉州 362000)
黄芩苷是唇形科植物黄芩的干燥根茎中提取分离出的一种黄酮类化合物,具有抗菌、抗病毒、抗氧化等多种药理作用[1-5],但黄芩苷亲水性较差,生物利用度低,限制了其临床应用[6].纳米粒为固态胶体,粒径在10~100 nm,药物可以溶解、包裹于高分子材料形成载体纳米粒[7].纳米粒可控制药物的释放,有较长的体内循环时间,可减少药物被网状内皮吞噬系统吞噬,从而增加疗效[8-9].纳米药物更具一些独特的性质,比如药物溶解速率加快,药物穿透能力增加,药效稳定,药物体内释放可控,难溶性药物的口服吸收改善等[10-12].本研究应用透析法研究黄芩苷壳寡糖纳米粒的体外释放,探究黄芩苷壳寡糖纳米粒的缓释特性,采用零级动力学方程、一级动力学方程、Higuchi方程、双相动力学方程、Ritger-Peppas方程和Hixson-Crowell方程拟合其释放行为[13-15],对其释放机制进行预报,以期为后黄芩苷壳寡糖纳米粒的临床试验研究和临床使用提供一定的参考价值.
1 实验方法
1.1 仪器与试剂
粒度分析仪(Nano-ZS90,英国马尔文公司);集热式恒温加热磁力搅拌器(DF-101S,巩义市予华仪器有限责任公司);紫外可见分光光度计(UV-1800,上海美谱达仪器有限公司);高速冷冻离心机(H2100R,湖南湘仪实验室仪器开发有限公司);电子分析天平(AR124CN,奥豪斯仪器(常州)有限公司);真空冷冻干燥机(Freezone 6plus,美国LABCONCO公司);超声波清洗机(KQ-500DB型,昆山市超声仪器有限公司);GL-802A型微型台式真空泵(GL-802A,海门市其林贝尔仪器制造有限公司);透射电子显微镜 (TECNAI G2 Spirit TWIN,捷克共和国FEI公司);黄芩苷标准品(110715-201016,上海金穗生物科技有限公司);壳寡糖(脱乙酰度>90%)(171010,青岛云宙生物科技有限公司);三聚磷酸钠(TPP,160820,天津市致远化学试剂有限公司).
1.2 黄芩苷壳寡糖纳米粒的制备
称取适量壳寡糖溶解于10 mL超纯水中,调节pH,配制成壳寡糖溶液(14 mg/mL).称取1.4 mg黄芩苷加入4 mL 0.4 mg/mL三聚磷酸钠溶液中,置于50 ℃恒温水浴中保温5 min.将上述配好的黄芩苷溶液以每秒一滴的速度逐滴加入,30 ℃搅拌10 min,即得负载黄芩苷的壳寡糖纳米粒混悬液.不加黄芩苷,同法制得空白纳米粒.
1.3 黄芩苷壳寡糖纳米粒体外释放度的测定
1.3.1 释放介质中黄芩苷的检测方法 (1)标准曲线的绘制.称取12.5 mg的黄芩苷,用PBS溶解,配制成浓度为2 mg/mL黄芩苷溶液.精密移取溶液0.1、0.2、0.3、0.4、0.5、0.6、0.7、0.8、0.9、1.0 mL,用pH=7.4 的磷酸盐缓冲溶液(PBS)稀释,分别稀释成浓度为5、10、15、20、25、30、35、40、45、50 μg/mL的黄芩苷溶液.空白对照为PBS,分别测其在276 nm的吸光度.以浓度为横坐标,吸光度为纵坐标,绘制黄芩苷的标准曲线.
(2)精密度试验.称取30 mg黄芩苷,用PBS溶解,配制成0.6 mg/mL黄芩苷储备液.从储备液中取出三份,用PBS稀释,制备成浓度分别为6、12、18 μg/mL的黄芩苷溶液.并分别在0、2、4 h测定其在276 nm波长下的吸光度,每种浓度在一个时间点下测定3次,计算出日内精密度.连续3 d,在同一时间点测定276 nm波长下的吸光度,同样每天每个样品测定3次,计算出日间精密度.
(3)回收率试验.从储备液中取出3份,每份都加入100 μL空白纳米粒,用PBS稀释,制备成浓度分别为6、12、18 μg/mL的黄芩苷溶液,测定每个浓度在276 nm波长下的吸光度,代入标准曲线,计算回收率.
1.3.2 黄芩苷壳寡糖纳米粒体外释放的测定 将制备好的黄芩苷壳寡糖纳米粒置于预处理过的透析袋中,取150 mL释放介质,保持恒定温度为37 ℃,分别于 0.5、1、2、4、8、12、24、36 h时间点取样 2 mL,同时补加2 mL的释放介质.将取出的样品用释放介质稀释至10 mL装入针筒中,用0.22 μm的微孔滤膜过滤,在276 nm波长处下测定续滤液的吸光度值,将其代入标准曲线计算各个时间点释放的黄芩苷的浓度,黄芩苷的累积释放率Q按式(1)[16]计算,从而得出累积释放率曲线.
(1)
其中:Ci为第i次取样时释放介质中黄芩苷的浓度,V为释放介质的体积,V1为取样的体积,M为黄芩苷初始的质量.
1.3.3 模型拟合分析 采用Origin Pro 8软件对体外释放情况进行模型拟合分析.
2 结果与讨论
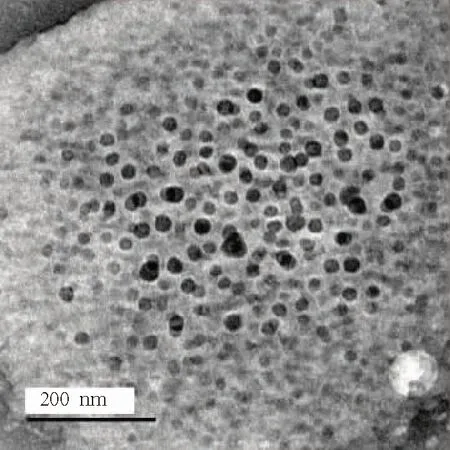
图1 黄芩苷壳寡糖纳米粒的透射电镜照片Fig.1 TEM image of Baicalin chitosan oligosaccharide nanoparticles
2.1 黄芩苷壳寡糖纳米粒形态观察
取适量黄芩苷壳寡糖纳米粒混悬液,稀释至一定倍数后滴在铜网上,静置5 min后,用滤纸吸干,滴加磷钨酸染色.常温下自然晾干,采用透射电镜观察纳米粒形态[17].纳米粒的透射电镜照片(图1)显示,黄芩苷壳寡糖纳米粒形态为均一、圆整球形,分散性好,平均粒径约为50 nm.
2.2 黄芩苷壳寡糖纳米粒的粒径及Zeta电位
用激光粒度分析仪测定黄芩苷壳寡糖纳米粒的粒径及Zeta电位,结果见图2和图3.黄芩苷壳寡糖纳米粒平均粒径测定为(63.2±2.7) nm,测得的粒径比透射电镜观察结果大,原因是测定条件为湿态.Zeta电位测定结果为(+19.6±0.6) mV,说明黄芩苷壳寡糖纳米粒分散性和稳定性较好.
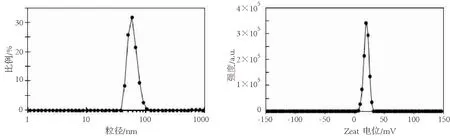
图2 黄芩苷壳寡糖纳米粒粒径分布图 图3 黄芩苷壳寡糖纳米粒Zeta电位Fig.2 Size distribution of Baicalin chitosan oligosaccharide nanoparticles Fig.3 Zeta potential of Baicalin chitosan oligosaccharide nanoparticles
2.3 释放介质中黄芩苷含量的测定
2.3.1 检测波长的确定 制备空白纳米粒及黄芩苷壳寡糖纳米粒,用紫外分光光度计扫描二者在200~400 nm的波长下的吸光度,结果如图4所示.由图中可知,黄芩苷在276 nm处有最大吸收波长,与空白纳米粒对比,在此波长下二者的吸光度相差较大,说明在此波长下,其他干扰物质对黄芩苷测定的影响小,所以选用276 nm为黄芩苷的测定波长.
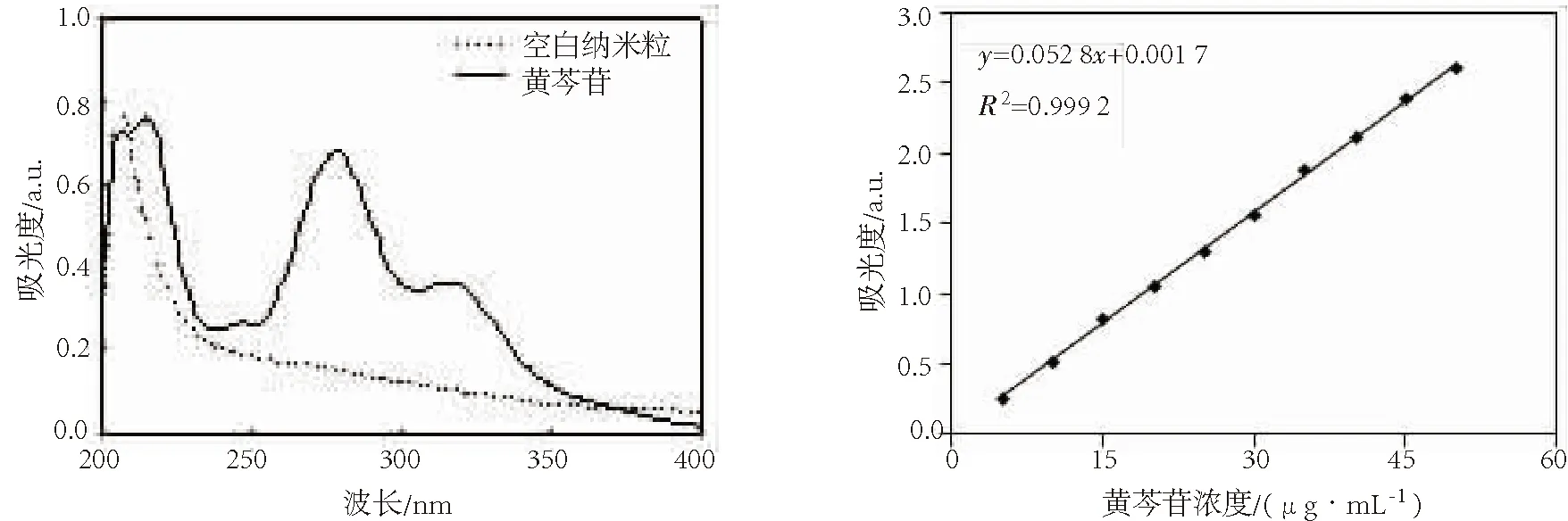
图4 黄芩苷壳寡糖纳米粒和空白纳米粒的波长扫描图 图5 黄芩苷的标准曲线 Fig.4 Ultraviolet scanning figure of Baicalin chitosan oligosaccharide nanoparticles and blank nanoparticles Fig.5 Standard curve of Baicalin
2.3.2 黄芩苷含量测定 按照“1.3.1(1)”项,以吸光度为纵坐标,以浓度为横坐标,绘制黄芩苷标准曲线为y=0.052 8x+0.001 7,R2=0.999 2,如图5所示.由图中可知,黄芩苷在5~50 μg/mL内浓度与吸光度的线性关系良好.精密度试验测得6、12、18 μg/mL黄芩苷溶液的日内精密度相对标准偏差(RSD)分别为1.90%、1.49%、1.79%,日间精密度RSD分别为3.09%、1.02%、0.66%.回收率的测定结果表明,6、12、18 μg/mL黄芩苷溶液回收率的平均值分别为102.81%、106.12%、108.74%,RSD分别为3.07%、0.66%、1.24%.说明用紫外分光光度法测定壳寡糖纳米体系中黄芩苷浓度的精密度和回收率符合要求.

图6 黄芩苷溶液和黄芩苷壳寡糖纳米粒的释放情况Fig.6 Release of Baicalin solution and Baicalin oligosaccharide nanoparticles
2.4 体外释放情况
采用透析法对比黄芩苷溶液与黄芩苷壳寡糖纳米粒的释放情况,结果如图6所示.由图中可知,黄芩苷溶液呈现较快的释放速度,6 h时黄芩苷溶液的累积释放率就达到了97.34 %,而8 h时黄芩苷壳寡糖纳米粒的累积释放率为74.09%,到36 h时才达到92.81%.可见黄芩苷壳寡糖纳米粒相对于黄芩苷溶液释放慢,具有明显的缓释效果.
2.5 模型拟合分析
为了进一步阐明黄芩苷溶液和黄芩苷壳寡糖纳米粒的体外释药特性,探讨其药物释放机理,在上述结果的基础上通过 Origin 2018对体外释药结果进行数据分析,采用零级动力学方程、一级动力学方程、Higuchi方程、双相动力学方程、Ritger-Peppas方程和Hixson-Crowell方程对黄芩苷溶液和黄芩苷壳寡糖纳米粒的体外释放情况进行模型拟合[18],结果见表1,拟合效果如图7和图8.药物释放曲线拟合的效果用相关系数R2表示,R2越接近于1,拟合程度越高,药物释放曲线与对应方程的拟合效果越好[19].
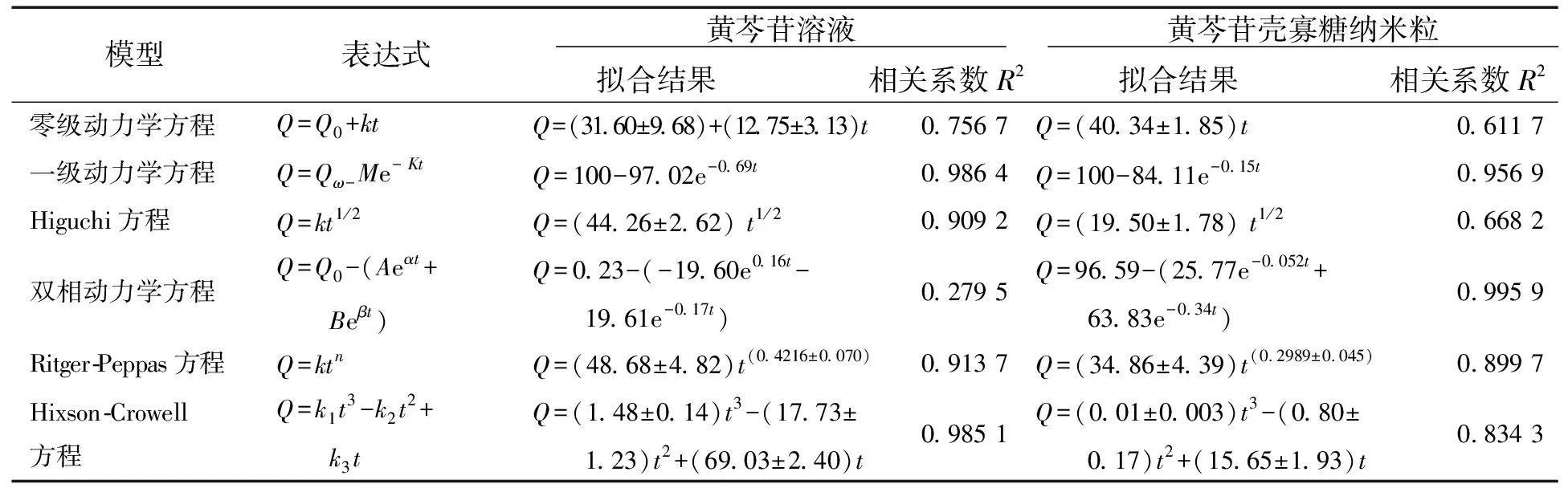
表1 黄芩苷溶液与黄芩苷壳寡糖纳米粒体外释放的拟合结果Tab.1 Fitting results of in vitro release of Baicalin solution and Baicalin chitosan oligosaccharide nanoparticles
由表1拟合结果显示,黄芩苷溶液的药物释放更接近一级动力学方程,相关系数R2为0.986 4.表明黄芩苷溶液在释放过程中以扩散为主.而双相动力学方程的相关系数仅为0.279 5;说明黄芩苷溶液释放快,而不存在突释效应,没有缓释相.
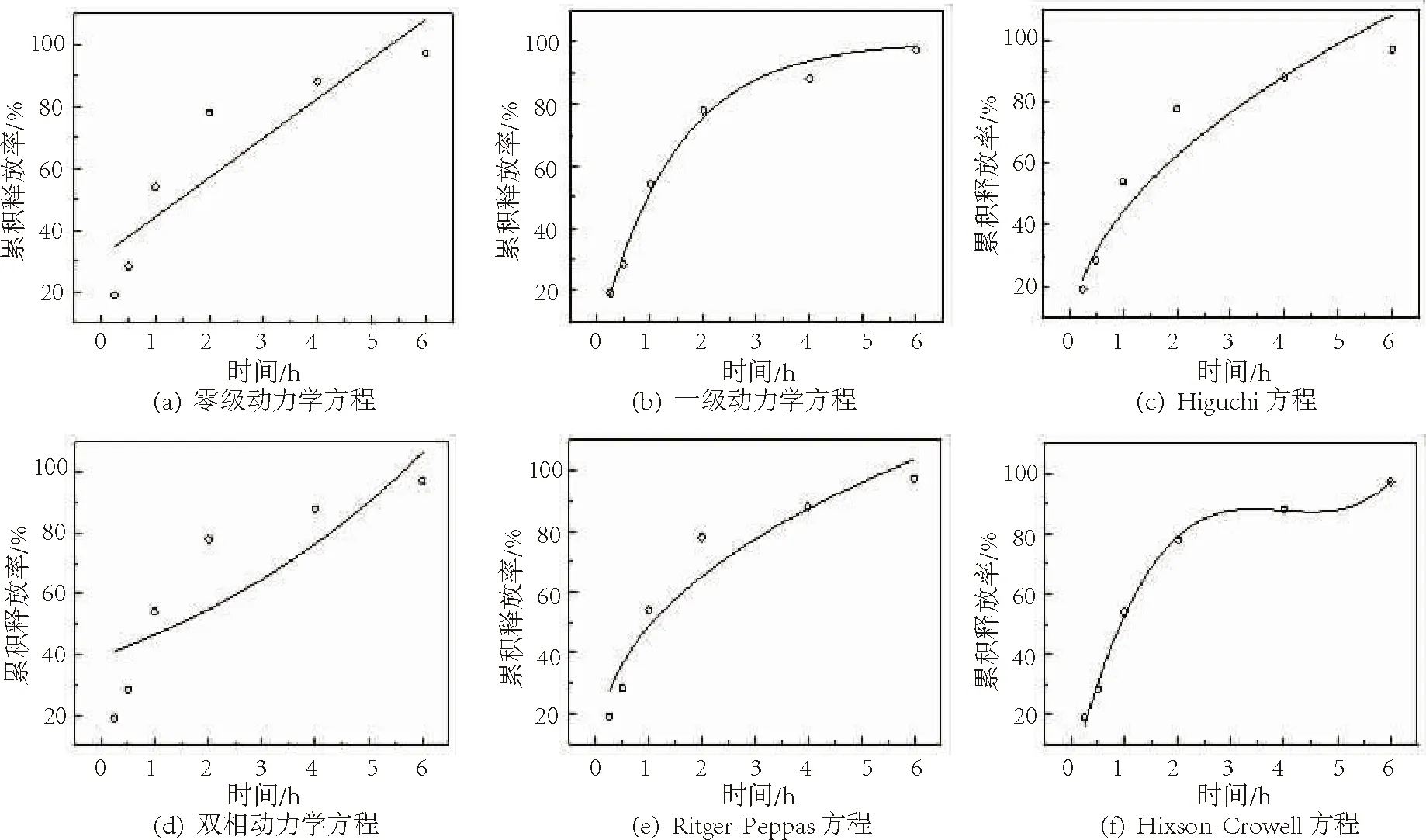
图7 黄芩苷溶液体外释放的拟合情况Fig.7 Fitting of in vitro release of Baicalin solution
黄芩苷壳寡糖纳米粒的体外释放更接近双相动力学方程,相关系数达到0.995 9,表明黄芩苷壳寡糖纳米粒的释放先快后慢,一开始释放纳米粒表面吸附的黄芩苷,后黄芩苷通过纳米粒表面孔道或载体开始溶解慢慢释放[20];一级动力学方程的相关系数为0.956 9,说明纳米粒的释放以扩散为主;Ritger-Peppas方程拟合的相关系数为0.899 7,且n=0.298 9±0.045,n<0.45说明纳米粒的释放为Fick’s扩散,其释放机制以扩散为主[21-22],但相关系数仅为0.899 7,表明可能还有一部分以溶蚀释放;Hixson-Crowell方程拟合的纳米粒的相关系数为0.834 3,说明药物释放过程中,扩散速度是药物释放的限速步骤,但也存在其他的限制过程,这与前面的分析相吻合.
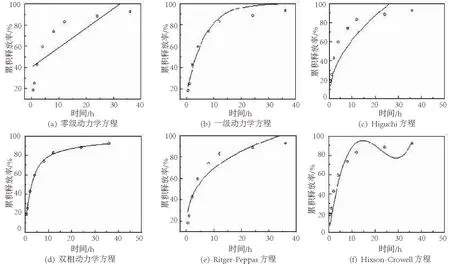
图8 黄芩苷壳寡糖纳米粒体外释放的拟合情况Fig.8 Fitting of in vitro release of Baicalin chitosan oligosaccharide nanoparticles
3 讨论
本研究所得黄芩苷壳寡糖纳米粒形态较规整,粒径均一,激光粒度仪所测的是纳米粒的水合粒径,故比透射电镜所得的粒径稍大.从体外释放结果可知,纳米粒药物释放持续而稳定,具有明显的缓释作用.本文采用其中6种经典模型[23-24]对黄芩苷溶液和黄芩苷壳寡糖纳米粒的释放数据进行拟合.释放模型拟合结果(双相动力学方程拟合的相关系数达到0.995 9)表明黄芩苷壳寡糖纳米粒的释放机理:前期由于纳米粒表面有黄芩苷吸附,释药快,之后从纳米粒表面小孔释放,同时载体溶解从表面孔道扩散释放,溶解缓慢将黄芩苷释放出来.
