含铂双药化疗EGFR-TKI耐药及未突变晚期肺腺癌临床观察
2021-12-30齐彦宇张军蒋莎莎周从明
齐彦宇 张军 蒋莎莎 周从明
近年我国肺癌发病率总体呈上升趋势,因其早期表现症状特异性差,发现时大多已是晚期,治疗效果差,使其成为恶性肿瘤中发病率和死亡率第一位的疾病[1]。随着肺癌分子分型研究的深入和靶向药物的广泛应用,使得部分对靶向药物敏感的非小细胞肺癌患者生存期和生活质量得以大幅提高。表皮生长因子受体(epidermal growth factor receptor,EGFR)基因突变阳性晚期非小细胞肺癌(NSCLC)患者一线治疗的多个随机对照研究显示,一代EGFR-TKI(吉非替尼、厄洛替尼、埃克替尼)及二代TKI(阿法替尼、达克替尼)对比单纯化疗均可提高患者总生存时间,且毒副反应低于单纯化疗[2-4]。FLAURA研究显示三代奥希替尼疗效优于一代EGFR-TKI,奠定了奥希替尼在EGFR突变阳性晚期NSCLC一线治疗的地位[5],但经酪氨酸激酶抑制剂治疗10~18个月后不可避免会出现病情进展,靶向耐药[6]。目前EGFR-TKI获得性耐药后的晚期NSCLC尚无标准的治疗方案,CSCO指南推荐二线首选培美曲塞联合铂类双药化疗方案[7-8]。同时培美曲塞联合铂类化疗也被推荐用于EGFR野生型腺癌患者一线治疗[9]。因此,本研究采用回顾性分析方法,探讨培美曲塞联合卡铂治疗EGFR-TKI耐药及未突变晚期肺腺癌的效果及不良反应,现报道如下。
1 资料与方法
1.1 一般资料
回顾性分析2017年10月-2019年12月成都市第三人民医院治疗确诊的晚期肺腺癌(ⅢB/Ⅳ期)的患者35例,纳入标准:卡氏评分(KPS)≥70分;有1个或多个可测量病灶;预计生存期>3个月。排除标准:化疗及靶向治疗绝对禁忌证。其中男19例,女16例,年龄30~80岁,平均61岁。根据EGFR基因检测突变情况分组,其中突变耐药组(EGFR 19Del、21L858R位点突变阳性)20例,未突变组(EGFR未突变)15例。两组患者年龄、性别、肿瘤分期比较,差异均无统计学意义(P>0.05),见表1。
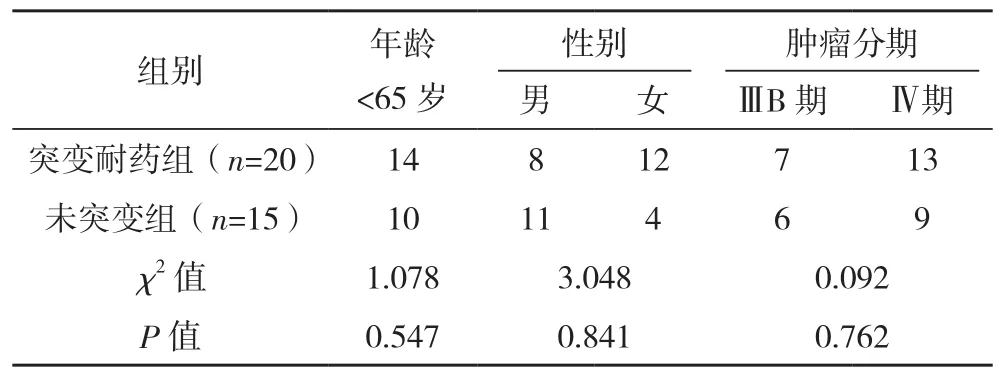
表1 两组一般资料比较(例)
1.2 方法
未突变组患者直接给予化疗。化疗药物为培美曲塞联合卡铂治疗,用药方法如下:培美曲塞(江苏豪森公司,国药准字H20051288;200 mg/支),500 mg/m2,每3周使用1次。卡铂(齐鲁制药有限公司,国药准字H20020180,100 mg/支)AUC=5,300~400 mg/m2,3周使用1次。3周(21 d) 为1个化疗周期。化疗前用药:化疗前1周口服多维元素片(善存,惠氏制药有限公司,国药准字H10950026)含叶酸400 μg/d,直至治疗结束;维生素B12(哈药集团三精制药有限公司,国药准字H23021687)1 000 μg/次,提前1周肌注,每3个化疗周期重复1次;地塞米松(广州华南药业集团有限公司,国药准字H44024469)4 mg,口服,2次/d,连续服用3 d。化疗的常规不良反应为胃肠道恶心、呕吐及骨髓抑制反应,根据临床指南可常规考虑给予5-羟色胺受体阻断剂(5-HTI)及重组人粒细胞集落刺激因子(rhG-CSF)预防治疗。
突变耐药组患者给予奥希替尼治疗,耐药进展后给予化疗。每日予以口服甲磺酸奥希替尼片(英国阿斯利康公司,进口药品注册证号H20170166)80 mg治疗,直到疾病进展或出现不可耐受的毒副反应为止,再给予培美曲塞联合卡铂化疗,化疗药物剂量和治疗周期时间同未突变组一致。
1.3 观察指标及评价标准
(1)疗效评定按最新实体瘤疗效反应评价标准(response evaluation criteria in solid tumor,RECIST)1.1版,完全缓解(complete response,CR):除结节性疾病外,所有目标病灶完全消失。部分缓解(partial response,PR):所有可测量目标病灶的直径总和低于基线≥30%。稳定(stable disease,SD):靶病灶减小的程度没达到PR,增加的程度也没达到PD水平,介于两者之间。进展(progressive disease,PD):以所有测量的靶病灶直径和相对增加至少20%,出现新的病灶。患者总有效率(overall response rate,ORR)=(CR+PR)/总例数×100%;疾病控制率(disease control rate,DCR)=(CR+PR+SD)/总例数×100%。(2)中位无进展生存 期(media progression-free survival,mPFS): 从开始化疗后,疾病进展或者发生任何原因的死亡之间的平均时间。并分析对PFS有影响的因素,计算总生存率。(3)不良反应:治疗期间患者所出现的不良反应,按照美国国家癌症研究所(National Cancer Institute,NCI)制定的毒性评价标准进行评价。
1.4 统计学处理
本研究数据采用SPSS 22.0统计学软件进行分析和处理,计量资料以(±s)表示,采用t检验,计数资料以率(%)表示,采用χ2检验,等级资料采用秩和检验,使用Kaplan-Meier法描绘生存曲线,Log-rank单因素和Cox回归多因素比较生存差异,P<0.05为差异有统计学意义。
2 结果
EGFR基因突变阳性患者按计划给予奥希替尼靶向治疗,治疗中未出现明显的毒副反应,基本可以耐受。两组患者均完成4个周期化疗。因出现KPS评分小于60分,一般情况差患者4例:突变组2例,未突变组2例;以及出现Ⅳ度骨髓抑制患者3例:突变组2例,未突变组1例,下一周期化疗给予20%~25%减量治疗。
2.1 临床疗效
35例患者中,CR 0例,PR 13例,SD 12例,PD 10例。ORR为 37.1%(13/35),DCR为 71.4%(25/35);不同年龄、性别、ⅢB/Ⅳ期的疗效比较,差异无统计学意义(P>0.05),见表2。未突变组ORR及DCR均高于突变耐药组(40.0% vs 35.0%、73.3% vs 70.0%),但两组比较差异无统计学意义(P>0.05),见表 3。
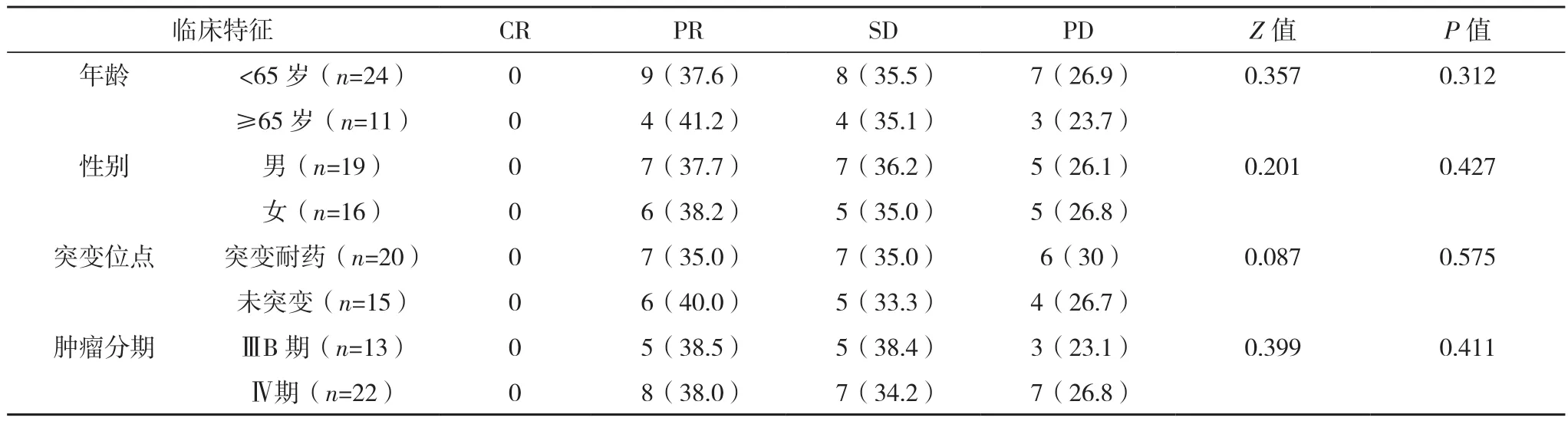
表2 不同临床特征患者的临床疗效比较[例(%)]
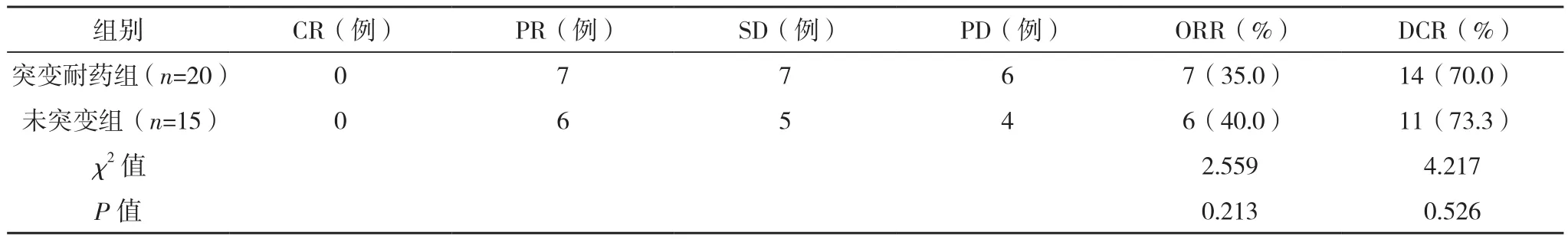
表3 两组临床近期疗效比较
2.2 两组中位无进展生存期比较
35例患者中,未突变组患者mPFS(8.9个月)长于突变耐药组患者(6.1个月),但差异无统计学意义(χ2=0.215,P=0.087),见图1。Cox回归多因素生存分析显示,对PFS有影响的因素为突变位点(P=0.038),其余年龄、性别、分期等指标比较差异无统计学意义(P>0.05),见表4。
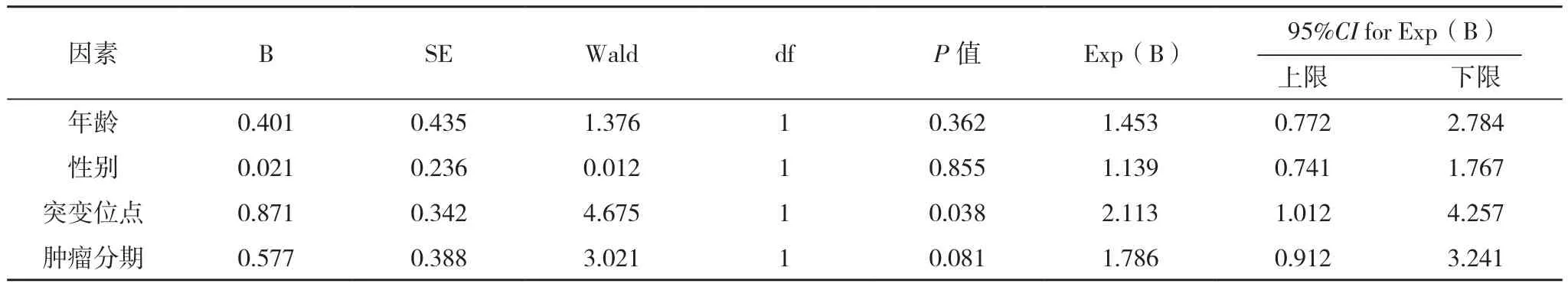
表4 Cox回归生存分析
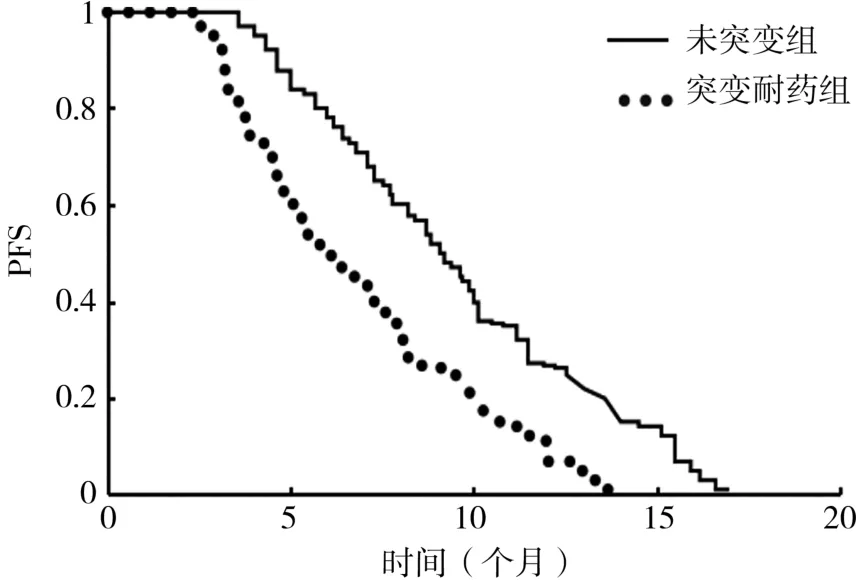
图1 Kaplan-Meier mPFS生存曲线分析
2.3 两组不良反应比较
35例患者的常见不良反应为胃肠道反应、骨髓抑制和皮疹等,不良反应多为Ⅰ~Ⅱ度,其中Ⅲ~Ⅳ度不良反应病例如下,骨髓抑制:白细胞减少6例(17.1%)、贫血3例(8.6%)、血小板减少3例(8.6%);消化道不良反应:恶心呕吐5例(14.3%);口腔炎1例(2.9%);发热1例(2.9%);乏力3例(8.6%);皮疹1例(2.9%);肝肾功能异常1例(2.9%);脱发1例(2.9%)。突变耐药组Ⅲ~Ⅳ度皮疹、口腔炎、脱发和骨髓抑制高于未突变组,未突变组乏力、恶心呕吐高于突变组,但比较差异均无统计学意义(P>0.05),见表5。
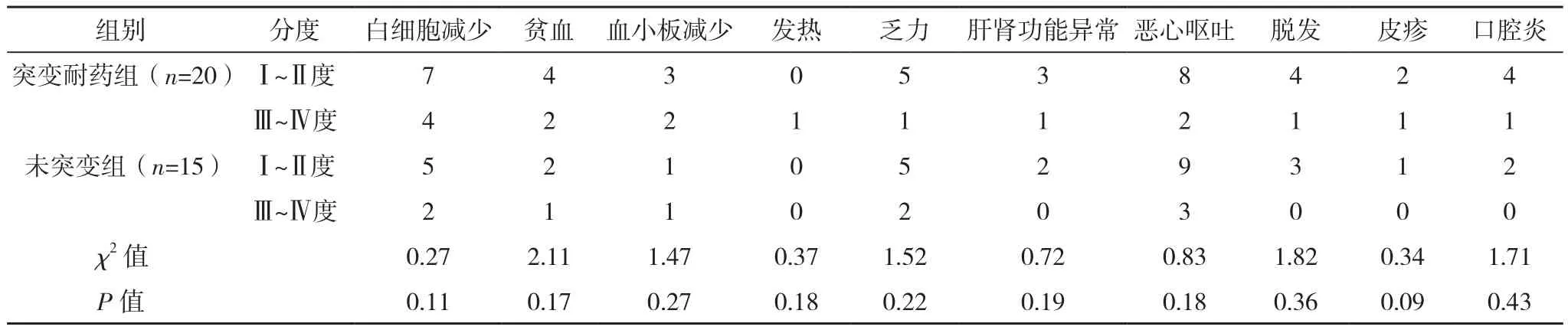
表5 两组不良反应比较(例)
2.4 随访1年总生存率
患者随访满1年后评估,死亡8例,其中突变组5例,未突变组3例,故1年总生存率为77.1%(27/35)。
3 讨论
在晚期非小细胞肺癌治疗中,中国抗癌协会临床肿瘤协作专业委员会(CSCO)指南早已经将EGFR基因突变靶点对应靶向药纳入临床治疗实践中,但患者经EGFR-TKI治疗后都会出现获得性耐药[10-11]。当EGFR-TKI治疗出现的耐药时,指南推荐后续治疗选择可采用培美曲塞联合铂类或含铂双药方案联合抗血管抑制药物或免疫药物治疗[12-13]。TORCH研究(Ⅲ期RCT)进一步说明靶向治疗应考虑人群的EGFR突变的构成比,对于可选择靶向和化疗的晚期NSCLC患者必须要检测EGFR突变实行个体化治疗,对于非选择人群一线治疗仍以化疗为主[14]。Ⅲ期临床研究(JMDB研究)不仅表明培美曲塞联合顺铂(AP方案)不劣于吉西他滨联合顺铂(10.3个月vs 10.3个月),而且表明AP方案对于非鳞非小细胞肺癌具有更好的疗效和安全性[15]。
本研究对肺腺癌EGFR突变人群根据基因突变类型进行了选择性的精准个体化治疗。FLAURA研究解决了对EGFR基因突变阳性的NSCLC临床选择最佳靶向用药的模式的问题:“1+3”(一代TKI+三代TKI)还是“3+X”(三代TKI+其他治疗)。根据其研究结果,总生存时间(OS)显示:三代靶向药(奥希替尼)一线使用对比一代序贯三代有明显生存获益(中位OS为41.4个月vs 30.6个月),因此,CSCO及NCCN指南推荐奥希替尼一线治疗[16]。本研究根据基因检测EGFR19、21位点突变的优势人群一线给予EGFR-TKI三代奥希替尼靶向治疗,而后续治疗出现耐药后,首选培美曲塞联合卡铂作为二线化疗的“3+X”模式。另一方面,对EGFR未突变人群,EGFR-TKI治疗效果较差,首选培美曲塞模式联合卡铂作为一线治疗。研究结果显示:培美曲塞治疗肺腺癌的效果与患者一般临床特征的年龄、性别及肿瘤分期无相关性,其中未突变组患者总有效率及疾病控制率均高于突变耐药组患者;未突变组患者mPFS优于突变耐药组患者。进一步研究表明:Cox回归分析显示,对PFS有影响的因子为突变位点。上述表明,其不同结果可能与EGFRTKI耐药机制有关,或可能直接与突变位点不同相关。由于样本数量较少和相关研究文献未见报告,需进一步深入临床和基础研究。本研究中非鳞非小细胞肺癌患者严格检测EGFR基因并一线给予三代TKI奥希替尼靶向治疗,耐药后给予含铂双药化疗,其1年生存率达77.1%,优于相关临床文献[17]报道效果,其可能因“3+X”模式的优化,但病例数较少,需进一步深入大样本多中心随机对照研究。研究中的常见不良反应骨髓抑制、胃肠道反应、皮疹等基本可以耐受,主要为含铂双药的化疗常规反应。其中突变耐药组Ⅲ~Ⅳ度皮疹、口腔炎、脱发高于未突变组,未突变组乏力、恶心呕吐高于突变组,基本可以耐受,但两组差异均无统计学意义(P>0.05)。笔者正在对全组患者进行总生存期的随访,对后期患者培美曲塞联合铂类化疗出现耐药后部分继续接受治疗,如抗血管抑制剂或免疫检查点抑制剂治疗,以进一步了解化疗联合治疗在晚期肺腺癌治疗中的优势,改善疾病预后。
