恶性胆道梗阻塑料支架植入后阻塞的介入治疗
2021-12-16任建庄陈鹏飞张文广李方正邝东林王家兴韩新巍
唐 凡, 任建庄, 陈鹏飞, 张文广, 李方正, 邝东林, 万 里, 王家兴, 韩新巍
经皮经肝胆道引流(percutaneous transhepatic cholangial drainage,PTCD)与经纤维十二指肠镜逆行胆胰管造影(endoscopic retrograde cholangiopanc reatography,ERCP)途径置入胆道支架是治疗已失去外科手术机会的恶性胆道梗阻的首选方式[1-4]。胆道塑料支架植入后阻塞是最常见的并发症之一,国内外指南建议塑料支架一旦发生阻塞,应及时内镜下更换或定期(3 个月)更换支架[5-7]。 由于内镜下选择性胆道插管困难,存在取出阻塞胆道塑料支架失败或重新置入新支架失败的可能性[7-13]。 本文探讨DSA 下(非内镜)恶性胆道梗阻塑料支架植入后阻塞的取出联合经皮肝穿途径胆道金属支架植入的安全性、可行性及临床疗效。
1 材料与方法
1.1 材料
回顾性分析郑州大学第一附属医院介入科2016 年 11 月至 2020 年 3 月收治的经 ERCP 置入胆道塑料支架治疗恶性胆道梗阻后支架阻塞的13 例患者的临床资料、实验室数据与影像学资料。 13 例患者中,男 6 例,女 7 例,年龄为(70.2±9.1)岁,范围为51~81 岁。所有患者均有不同程度厌食恶心、皮肤与巩膜黄染、皮肤瘙痒等梗阻性黄疸症状,其中6 例因一般情况差不能耐受内镜治疗(3 例合并急性梗阻性化脓性胆管炎,2 例合并脓毒血症,1 例合并重型急性胰腺炎)[13],2 例曾于当地医院内镜下取出阻塞塑料支架失败,5 例患者胆道塑料支架植入后2 周内因塑料支架早期阻塞不愿再接受内镜下治疗。所有患者经病理活检确诊为恶性肿瘤(胆管癌10 例,胰头癌2 例,肝癌1 例),均因肿瘤进展与转移已失去手术切除机会,于内镜下经ERCP 植入胆道塑料支架。 13 例患者术前行MRCP 或增强MRI 或增强CT 检查,实验室检查及其他临床资料提示胆道塑料支架堵塞。
1.2 方法
1.2.1 手术操作 根据患者临床症状、 实验室检查、影像学检查及术前评估讨论,制定2 种(A 与B)介入手术方案。
A 方案为一期胆道支架更换术,适用于无发热、无急性梗阻性化脓性胆管炎或其他严重感染、无严重肝功能损伤等一般情况稳定的恶性胆道梗阻的患者(图 1)。 首先在 DSA 下使用 5 F 导管与 0.035 英寸导丝相互配合经口进入食管,经胃腔并将其置于十二指肠乳头区域,后交换8 F 导引导管与“鹅颈”式抓捕器套件(Amplatz Goose Neck,ev3,美国)至十二指肠乳头区域,反复调整抓捕器接近阻塞胆道塑料支架肠道端后轻轻推进抓捕器杆直至完全打开圆环, 推进抓捕圆环圈住塑料支架肠道端2~3 cm处并缓慢推进抓捕器导管,收拢圆环固定塑料支架后,保持抓捕器套件相对固定一起缓慢逆行经消化道从口取出。 然后在局麻下行经皮经肝胆道穿刺造影,确认恶性胆道梗阻的部位、范围、狭窄程度,选择合适规格的胆道金属裸支架(Niti-S Biliary Uncovered Stent,Taewoong Medical,太雄,韩国),交换加硬导丝引导并引入胆道金属支架释放装置跨越胆道狭窄段,以狭窄段为中心释放。 造影证实胆道支架释放满意后沿导丝通过支架留置8.5 F 胆道内外引流管于肠道内,可酌情选择开放或关闭外引流。术后7~10 d 胆道造影复查, 胆道金属裸支架膨胀满意,对比剂通过顺畅,无移位或阻塞,拔除内外引流管。
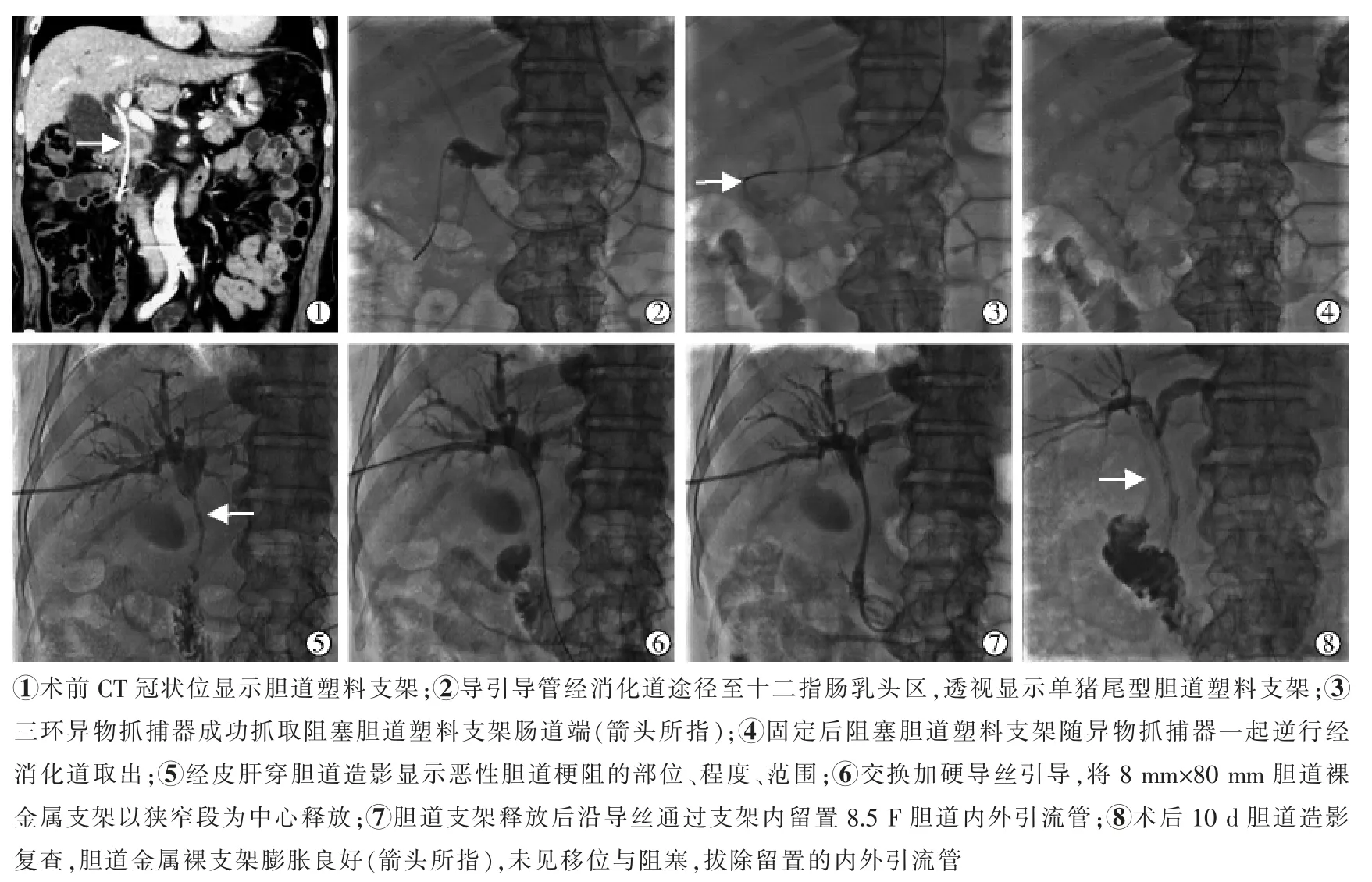
图1 A 方案的影像资料
B 方案为二期胆道支架更换术, 适用于合并反复发热、急性梗阻性化脓性胆管炎、重型急性胰腺炎或其他严重感染、肝功能严重损伤等一般情况差的患者(图2)。首先,经消化道逆行取出阻塞胆道塑料支架,具体取出操作同A 方案。 然后在局麻下行经PTCD 留置8.5 F 胆道外引流管。经过3~10 d 的胆道持续外引流与对症治疗后,再经原胆道引流途径置入胆道金属裸支架,具体释放金属支架操作同A 方案。 造影证实胆道支架释放满意后,留置8.5 F胆道外引流管于胆管扩张区,可酌情选择开放或关闭外引流管。术后7~10 d 胆道造影复查,胆道金属裸支架内对比剂通过顺畅,无移位或阻塞,拔除外引流管。

图2 B 方案的影像资料
1.2.2 疗效评估标准
DSA 下阻塞胆道塑料支架取出联合经PTCD途径金属支架植入技术操作成功定义为:阻塞胆道塑料支架取出与胆道金属裸支架植入均成功。
DSA 下阻塞胆道塑料支架取出联合经PTCD途径金属支架植入临床治疗成功定义为:①患者术后厌食恶心、皮肤与巩膜黄染、皮肤瘙痒等临床症状逐渐好转至消失,未出现如胆道出血、胆漏、肠穿孔等严重并发症;②术后患者白细胞、血淀粉酶及肝功能指标逐渐恢复正常范围或较阻塞胆道塑料支架取出术前下降50%以上;③胆道金属裸支架保持通畅,无移位、阻塞。
1.2.3 术后随访 对所有患者均定期随访(术后1、3、6 和12 个月),采用电话随访及门诊随访方式,随访包括询问患者相关临床症状,复查血常规、肝肾功、肿瘤标记物、凝血功能等,复查MRCP 或增强MRI 或增强CT 或胆道造影。 随访期间患者若出现不适,及时就诊。
1.3 统计学分析
使用SPSS21.0 软件进行统计学分析。正态分布数据以表达,非正态分布数据以中位数表达,术前术后实验室指标数据使用卡方检验及配对t 检验分析,以P<0.05 为差异有统计意义。
2 结果
所有患者阻塞胆道塑料支架DSA 下取出与经PTCD 途径胆道金属裸支架植入手术顺利, 技术和临床治疗均获成功, 其中 A 方案 7 例,B 方案 6 例(3 例术前合并急性梗阻性化脓性胆管炎,2 例合并脓毒血症,1 例合并重型急性胰腺炎)。 所有患者的厌食恶心、皮肤与巩膜黄染、皮肤瘙痒等临床症状逐渐好转至消失。 6 例B 方案患者于阻塞胆道塑料支架取出后,经过3~10 d 胆道外引流与抗感染等对症治疗均好转,白细胞计数恢复正常。
所有患者PTCD 术后穿刺区有轻微疼痛, 于术后2~7 d 逐渐缓解。 1 例A 方案患者在术后24 h出现急性轻型胰腺炎,对症治疗5 d 后好转,血淀粉酶、脂肪酶指标恢复正常。 未见胆道出血、胆瘘、肝脓肿、肠穿孔等严重并发症发生。
胆道金属支架植入术后所有患者的丙氨酸转氨酶、天冬氨酸转氨酶、碱性磷酸酶、谷氨酸转肽酶、总胆红素、直接胆红素等指标恢复正常或较阻塞胆道塑料支架取出前下降50%以上(表1)。
表1 13 例患者取出胆道塑料支架术前与更换胆道金属支架术后实验室检查结果

表1 13 例患者取出胆道塑料支架术前与更换胆道金属支架术后实验室检查结果
参数 塑料支架取出术前(3±1)/d 金属支架植入术后(7±2)/d t 值 P 值丙氨酸转氨酶 ALT/(U/L) 215.46±107.04 26.92±19.38 4.252 0.001天冬氨酸转氨酶 AST/(U/L) 211.92±186.14 24.00±9.72 3.692 0.003碱性磷酸酶 ALP/(U/L) 554.92±335.15 224.23±140.15 4.316 0.001谷氨酸转肽酶 GGT/(U/L) 585.15±403.76 157.15±114.69 4.505 0.001总胆红素/(μmol/L) 188.54±126.39 51.84±36.88 4.287 0.001直接胆红素/(μmol/L) 156.96±89.41 43.58±32.16 5.201 <0.001
13 例患者共取出13 枚胆道塑料支架:6 枚单猪尾型塑料支架,4 枚双猪尾型塑料支架,3 枚普通塑料支架共置入13 枚胆道金属裸支架,直径8 mm 的共8 枚,直径 10 mm 的共 5 枚。
随访发现, 术后 1、3、6 和 12 个月时患者胆道裸金属支架通畅率分别有 13 例、12 例、11 例、9 例,胆道金属支架保持通畅的中位时间为(8.4±3.2)个月。 随访期间,共4 例患者先后出现胆道金属裸支架阻塞(3~12 个月)。 1 例因胆汁淤积与胆泥形成导致胆道金属支架植入后3 个月阻塞,经再次持续胆道外引流12 d 后拔管并保持长期通畅;1 例因慢性炎性增生与肉芽组织形成导致胆道金属支架植入后6 个月阻塞,经再次胆道持续内引流后长期带管生存保持通畅;2 例因肿瘤进展导致胆道金属支架阻塞,经在原支架内再置入胆道金属裸支架解除阻塞。 随访期间,3 例患者死亡,其中1 例于术后8 个月死于电解质紊乱导致心律失常,2 例于胆道金属裸支架植入术后11、12 个月死于肿瘤进展与转移。
3 讨论
内镜下胆道内塑料支架引流术是治疗恶性胆道梗阻的常用方式,胆道塑料支架植入后平均通畅期仅为3~6 个月[6]。胆道塑料支架植入后阻塞是多因素共同作用的结果,主要原因有:①微生物聚集与生物膜形成。 微生物主要包括大肠杆菌、肠球菌、梭形杆菌、真菌等[14]。 同时,微生物的代谢产物与胶原蛋白、纤维蛋白、层粘连蛋白等不仅共同参与了生物膜的形成和支架阻塞进程,同时又促进了微生物聚集[15-17]。②胆汁淤积:胆汁淤积可造成自发性或细菌性胆盐沉淀,淤积胆汁的黏度增加还致使支架内胆汁流速减慢,影响胆盐的肠肝循环与胆固醇的代谢,形成易于沉淀的胆固醇结晶并聚集[18-19]。③十二指肠反流:随着肠内容物从十二指肠反流,食物纤维、 蛋白等可进入胆道塑料支架内参与阻塞形成,同时肠道菌群易位也促进微生物聚集与生物膜形成[16,18]。 此外,塑料支架直径、恶性胆道梗阻部位、支架植入位置、肿瘤进展以及患者个体差异性等因素均是塑料支架阻塞的影响因素[20]。
内镜下胆道塑料支架植入后一旦发生阻塞,在排除其他原因导致黄疸与胆管炎后,必须及时更换支架改善胆道引流,控制胆道感染,降低胆道内压,减轻胆管扩张,同时减退黄疸与恢复肝功能[4-6]。 通常在十二指肠镜下经ERCP 逆行使用Soehendra 支架回收器、取石网篮、圈套器、鼠齿钳、球囊等器械取出阻塞塑料支架并再次置入新的塑料或金属支架,必要时行括约肌切开术[8]。欧洲胃肠内镜学会指南于2018 版更新中表明经ERCP 途径取出胆道塑料支架并置入新支架的失败率为10%~20%,其中基于7 项有关ERCP 失败的研究中报道了约29%的ERCP 治疗失败的患者不愿再次尝试ERCP,而尝试再次ERCP 的失败率仍高达18%,证实了少数患者的阻塞胆道塑料支架在内镜下取出困难或更换失败的事实客观存在[7]。 尽管在本研究中, DSA下取出阻塞胆道塑料支架与胆道金属裸支架植入的技术与临床治疗均获成功,可能是经治的病例数较少或阻塞的塑料支架植入时间较短所致。
与胆道塑料支架相比, 金属支架在远期通畅率、 提高生活质量及延长生存期等方面占据优势,胆道金属支架的平均通畅时间为 6~12 月[6,21-23]。 有文献报道覆膜胆道金属支架和(非覆膜)胆道金属裸支架在长期通畅率以及生存期方面无明显统计学差异[7,24]。 覆膜胆道金属支架可有效阻止肿瘤向支架内生长且易取出,但存在易移位、易阻塞胆管分支及胰管造成胆管炎、胰腺炎等并发症的缺点[3]。胆道金属裸支架植入后不易移位且不易阻塞胆管分支及胰管开口,但同时也存在不易取出的缺点,近年来有胆道金属裸支架成功取出的文献报道[25-26]。在本研究中,若不及时取出就植入胆道金属支架可能会增加金属支架阻塞风险:一方面由于塑料支架本身管径可能会影响胆道金属支架的自膨,另一方面失去引流功能的塑料支架作为异物存在,不仅增加微生物聚集与生物膜形成、胆汁淤积与胆盐沉淀的可能,也能增加刺激胆道慢性炎性增生与肉芽组织的风险。 此外,失功的塑料支架是否有增加恶性胆道梗阻肿瘤进展的风险目前尚无确切定论,但不排除此可能[6,14-20]。 本研究中,胆道金属支架保持通畅的时间明显长于塑料胆道支架的通畅时间。
本研究中,DSA 下阻塞的胆道塑料支架取出后,无论A 方案还是B 方案植入胆道金属裸支架治疗恶性胆道梗阻都同样安全和有效, 这与Chatzis等[27]的报道基本一致。 A 方案适用于无发热、无急性梗阻性化脓性胆管炎或其他严重感染、无严重肝功能损伤等一般情况稳定的恶性胆道梗阻的患者。对于此类患者,内镜下更换塑料支架依然是首选治疗方式,但DSA 下取出阻塞胆道塑料支架联合经PTCD 途径置入胆道金属裸支架可作为内镜下更换支架失败或不愿接受内镜下再治疗的替代治疗或补充手段。B 方案适用于合并反复发热、急性梗阻性化脓性胆管炎、重型急性胰腺炎或其他严重感染、 肝功能严重损伤等一般情况差的患者[3,21,28]。对于此类患者,DSA 下取出阻塞的胆道塑料支架联合PTCD 引流, 二期置入胆道金属支架是首选方式,尤其是不愿接受或不能耐受内镜下再治疗的患者。同时,此项技术所需局部麻醉的门槛远低于内镜下治疗所需麻醉类型也是其独特的优势[29-30]。
对于不能外科切除的恶性胆道梗阻,除了早期胆道引流快速退黄、改善肝功能及胆道支架植入解除梗阻外,必须联合(全身或局部)放化疗、靶向治疗、免疫治疗等肿瘤多学科个体化治疗,最终达到治疗恶性肿瘤、提高胆道支架通畅率、改善生活质量与延长患者生存期的目标。 胆道金属支架植入后远期阻塞的可能性客观存在,一旦发生可在阻塞的金属支架内进行持续胆道外引流、球囊扩张联合胆道持续引流、再置入胆道支架或射频消融等治疗方式解除阻塞[6,31]。
目前阻塞胆道塑料支架在DSA 下的取出技术仅是初步探讨,经治的病例数较少,缺乏对照研究,故本研究存在一定的局限性, 需要进一步多中心、大样本、前瞻性的临床对照研究深入探讨。
综上所述,对于内镜下置入胆道塑料支架治疗恶性胆道梗阻后发生支架阻塞,尤其是不愿接受或不能耐受内镜下再治疗的患者,DSA 下取出阻塞的胆道塑料支架联合经皮经肝穿刺植入胆道金属支架的介入治疗是一种可行、安全、有效的微创手术,值得临床探讨和应用。
