氨溶-蒸发结晶制取仲钨酸铵和三氧化钨试验研究
2021-11-30杨娜
杨 娜
(山东工业职业学院,山东 淄博 256414)
黑钨精矿经酸解作业后获得两种产物:酸解液和粗钨酸。酸解液用于提钪,粗钨酸为提钨物料。酸解作业使得铁、锰、钪、铀、钍等酸溶物质大部分溶解入酸解液,粗钨酸实质上是经初步除杂提纯的产物,酸解后的WO3含量从70%左右提高到89%左右,酸难溶物钽、铌、锡等及少量溶解的铁、锰等残留于其中,其比放射性活度低于国家排放标准[1-2]。
目前,制取仲钨酸铵(APT)和三氧化钨(WO3)常采用方法有不纯的仲钨酸铵热离解-氨溶法、钨酸钠溶液(粗钨酸碱溶法制取)离子交换法、钨酸钠溶液(粗钨酸碱溶法制取)溶剂萃取法等。热离解-氨溶法条件:热离解在250~350 ℃下进行,或者在真空中50~150 ℃下进行;氨溶在95 ℃左右溶解4~6 h。该方法虽然流程短,但是能耗高,仅适用于生产小批量的高纯APT 和WO3或回收处理不合格的APT 产品。离子交换法APT 纯度高,但树脂空洞Na 等杂质不利于清洗,废水排放量大。溶剂萃取法产出的氨氮废水需要治理,而且萃取过程去除P、As、Si、Ta 和Mo 的效果不佳[3-5]。
针对目前APT 和WO3生产方法存在的问题,本文对粗钨酸进行了氨溶、氨渣碱溶、蒸发结晶等工序的试验,考查了所得仲钨酸铵及灼烧后的WO3是否合格,并分析了主要技术指标和铌、钽、锡有价元素的走向及富集情况等[6-7]。先采用工业氨水按工序进行了条件试验,考查WO3纯度;然后在条件试验的较优条件下,分别采用分析纯氨水和工业氨水进行了综合试验,对比考查WO3纯度和主要杂质及主要有价元素的分布情况。
1 试料成分及工艺流程
1.1 原料
试验用粗钨酸主要成分列于表1。从表1中看出WO3含量比扩试平均值略低,原因是该试料是包括扩试预备试验所产粗钨酸在内的全部粗钨酸的综合试料。主要杂质除铁、硅较高外,Mo、P 等含量都很低,对提钨极为有利。

表1 粗钨酸主要成分
1.2 主要试剂及设备
1)主要试剂:分析纯氨水(含NH325%~28%)、工业氨水(NH318%~20%,比重0.9)、1∶2工业氨水、分析纯NaOH。
2)主要设备:玻璃三口瓶(3 000 mL)、电动搅拌器(60 W)、电炉(1 500 W)、分液漏斗(500~1 000 mL)等。
1.3 试验工艺流程
试验工艺流程如图1所示。

图1 粗钨酸提取纯三氧化钨流程
2 条件试验
2.1 一次氨溶
2.1.1 试验原理
氨水将粗钨酸溶解使之与未分解的矿粒及其中未洗除的某些不溶性杂质进一步分离除去,从而获得较纯的钨酸铵溶液。主要化学反应见式(1)~(5)。

铁、锰等杂质的氢氧化物沉淀条件pH 值为Fe(OH)32.5~3、Fe(OH)25.5、Mn(OH)28.5、Ca(OH)2>10,一次氨溶磨矿粒度-300 目以下,在pH 值为11~12 氨溶条件下,铁、锰等杂质的氢氧化物都以沉淀除去(前期做过实验),因而可以获得铁、锰、钙、硅等杂质含量很低的钨酸铵溶液。
2.1.2 试验条件及方法
试验在3 L 三口玻璃瓶中进行,水浴保温,温度用水银触点温度计配6301 型电子继电器控制。
试验主要考查了氨水量和搅拌时间对溶解过程的影响。
每次称取100 ℃下干燥的粗钨酸200 g,用200 mL蒸馏水在1 L 烧杯中调浆,并在搅拌下将浆液温度加热至80~85 ℃。将计量的工业氨水(NH318%)倒入三口瓶内,在强搅拌下徐徐加入热钨酸浆,加完后用100 mL 热蒸馏水洗烧杯,洗液入三口瓶。至规定搅拌时间后取下三口瓶,将料液倒入贮液瓶内,用1∶2工业氨水50 mL 冲洗三口瓶,洗液合并入贮瓶内,加盖静置12 h 以上。然后用倾析法取出上清液,浓泥在布氏漏斗中抽滤,用1∶2工业氨水90 mL 分三次洗涤滤渣,洗液、滤液及上清液合并计量取样,分析WO3溶出率。滤渣烘干后称量,磨细后取样分析WO3含量。
2.1.3 试验分析
1)氨水量的影响。分别固定搅拌时间30 min、45 min、60 min,对氨水量做了理论量、过量50%、过量100%、过量150%的试验,结果见表2、图2。
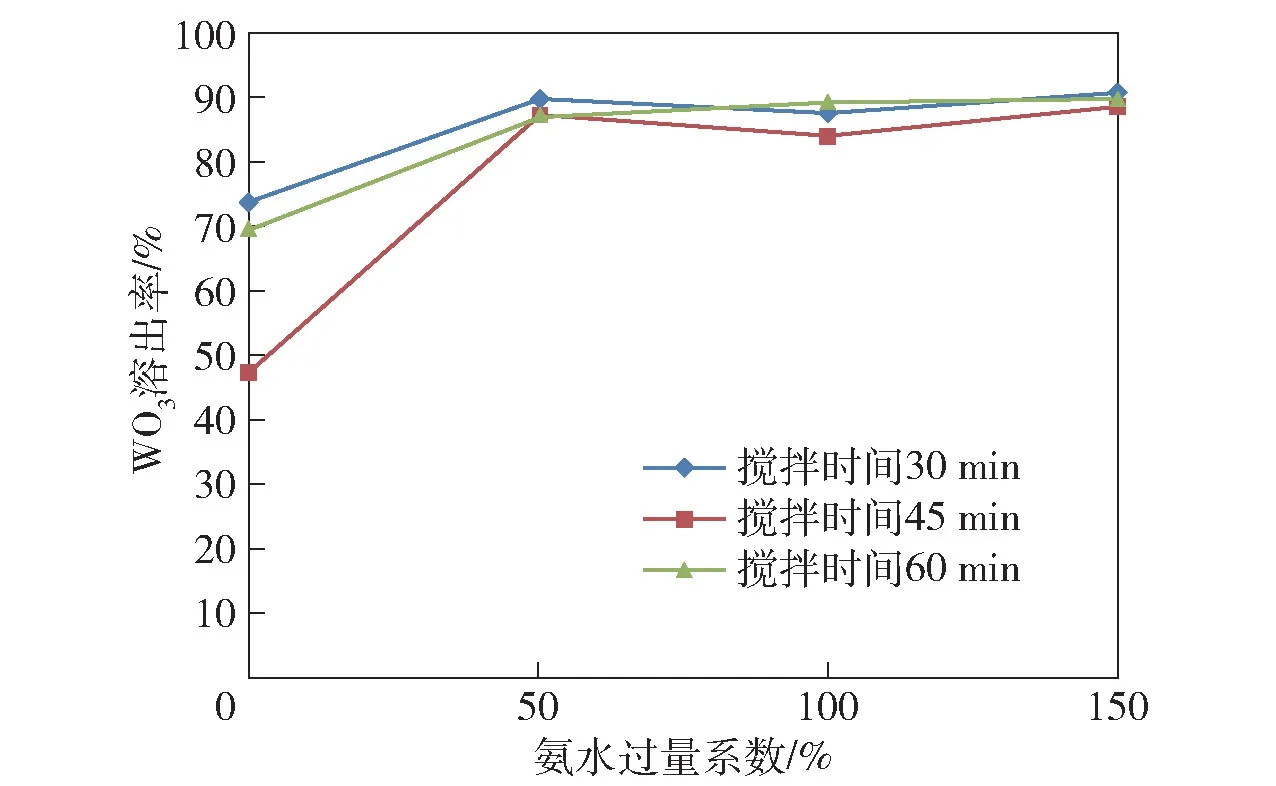
图2 一次氨溶条件试验结果
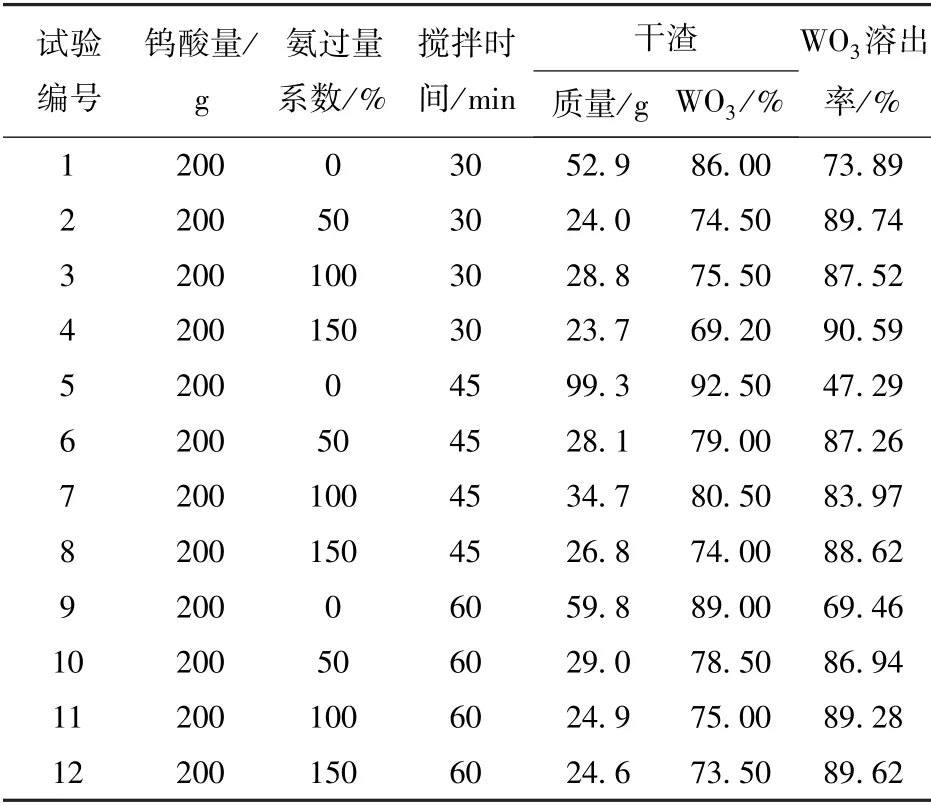
表2 一次氨溶条件试验结果
从表2可以看出,在相同的时间条件下,采用溶解钨酸所必须的理论氨量(氨过量系数为0)时,WO3溶出率只能维持在70%左右。当氨过量系数增大至50%时,WO3溶出率急剧提高90%左右。氨过量系数从50%再进一步增大时,WO3溶出率提高不明显。因此,在试验条件下,氨过量系数取50%为宜。
2)搅拌时间的影响。将表2中氨过量系数相同的试验分组进行对比可以看出,氨过量系数相同的情况下,无论搅拌时间为30 min、45 min 还是60 min,WO3溶出率影响不大。从生产能力考虑,取30 min是适宜的(前期做过实验,搅拌时间低于30 min,WO3溶出率受到影响)。
综上所述,一次氨溶最适宜的条件为氨过量50%,搅拌30 min,调浆固液比1∶5(包括洗水),浆液温度80~85 ℃。
2.2 二次氨溶
一次氨溶渣WO3含量达到70%以上,为了提高WO3的直收率,进行了二次氨溶试验。试验原料由一次氨溶条件试验获得的一次氨溶渣经混合、烘干、磨细后制得,含WO377.5%。每次取试料100 g,主要考查氨水量、温度、搅拌时间对WO3溶出率的影响。试验条件、装置、操作及试剂与一次氨溶相同。
采用正交方法安排试验。试验选择的因素及其相应水平列于表3。
从表3可以看出,本试验是三因素三水平试验,选用三水平正交表,该表共可安排九次试验。由表3和L9(34)正交表排出各组的试验条件列成试验方案表,并进行分组试验,试验结果见表4。
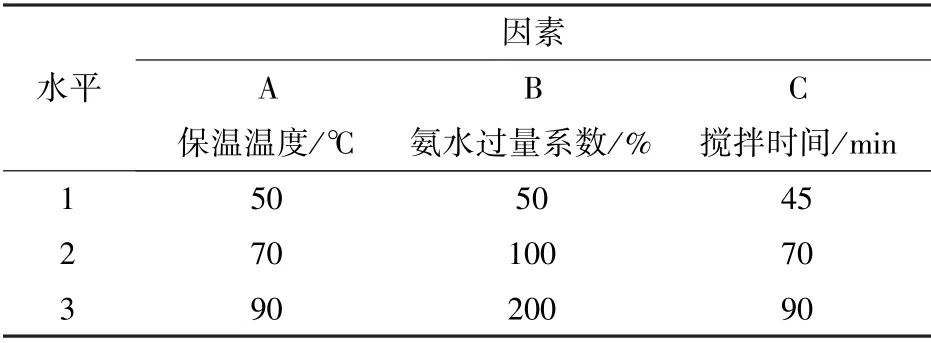
表3 二次氨溶正交试验
从表4可以看出,A 因素的极差远比其他因素大,是影响WO3溶出率的主要因素。B、C 因素的极差与空列极差相近,视为非主要因素。从而得出因素主次顺序为A→B→C。较好的工艺条件组合为A3B3C2,即保温温度90 ℃、氨水过量200%、搅拌70 min。

表4 试验方案和极差分析表
2.3 蒸发结晶制取仲钨酸铵
从钨酸铵溶液中析出仲钨酸铵,生产上常用中和法和蒸发法,本试验采用蒸发法析出仲钨酸铵。该方法实质上是用蒸发的办法除去部分NH3,使溶解度大的钨酸铵转变成溶解度小的仲钨酸铵结晶从溶液中析出,具体化学反应见式(6)。
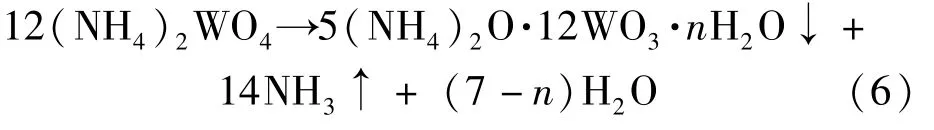
式(6)中的n随温度、晶形而变。温度高,片状结晶,n=5;温度低,针状结晶,n=11。
为了得到所需粒度的晶体,必须控制好影响粒度的各种因素,例如溶液的过饱和度、原始浓度、温度、时间、杂质种类及含量等。由于本试验主要考查产物的化学纯度,因此未对上述诸因素作详细探讨,只考查了不同蒸发程度下仲钨酸铵化学质量。
试液为二次氨溶试验所得钨酸铵溶液合并液,WO3浓度为212.8 g/L。将1 000 mL 试液倒入2 L烧杯内进行搅拌蒸发;采用水浴加温,温度70~80 ℃,用触点水银温度计配电子继电器控制;蒸发至规定体积后取下,自然冷却结晶约24 h;用布氏漏斗抽滤,并用300 mL 蒸馏水分三次洗涤仲钨酸铵,于80 ℃下烘干取样称重;洗水与滤液合并后取样分析,计算WO3结晶率。试验结果见表5、图3、图4。

表5 蒸发结晶试验结果
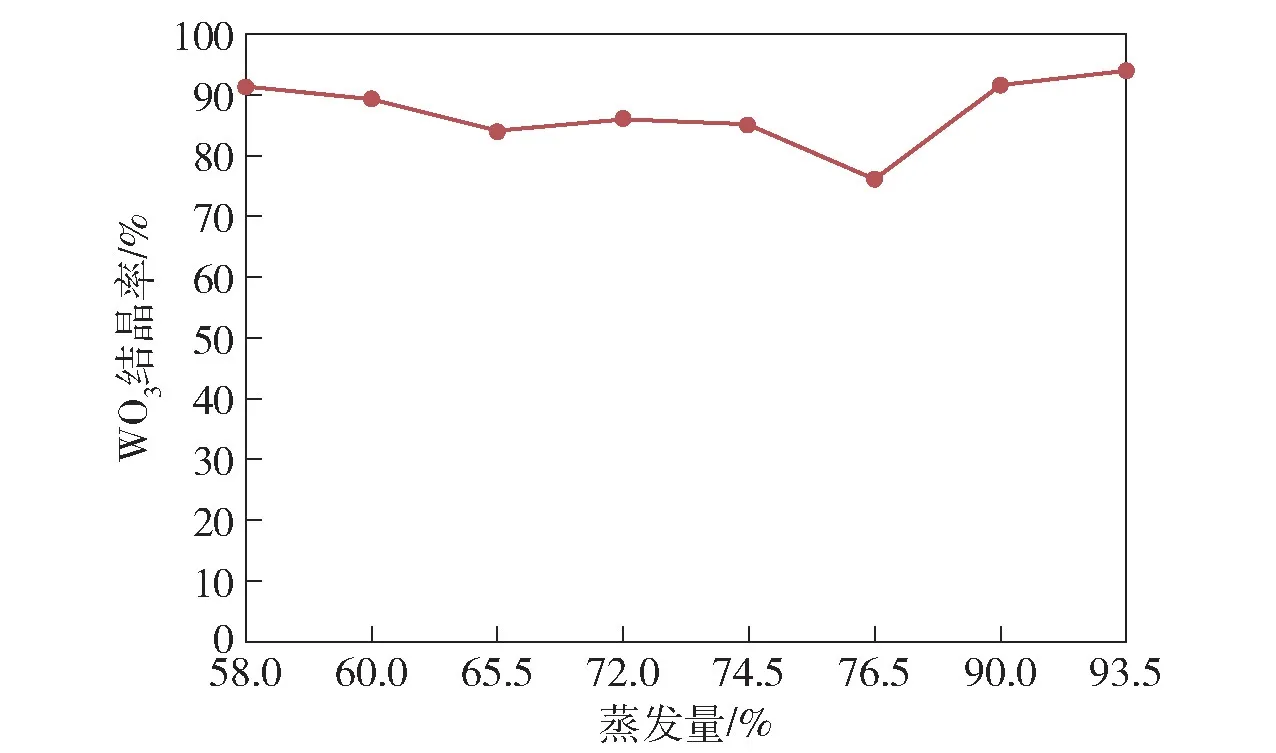
图3 蒸发量与WO3结晶率
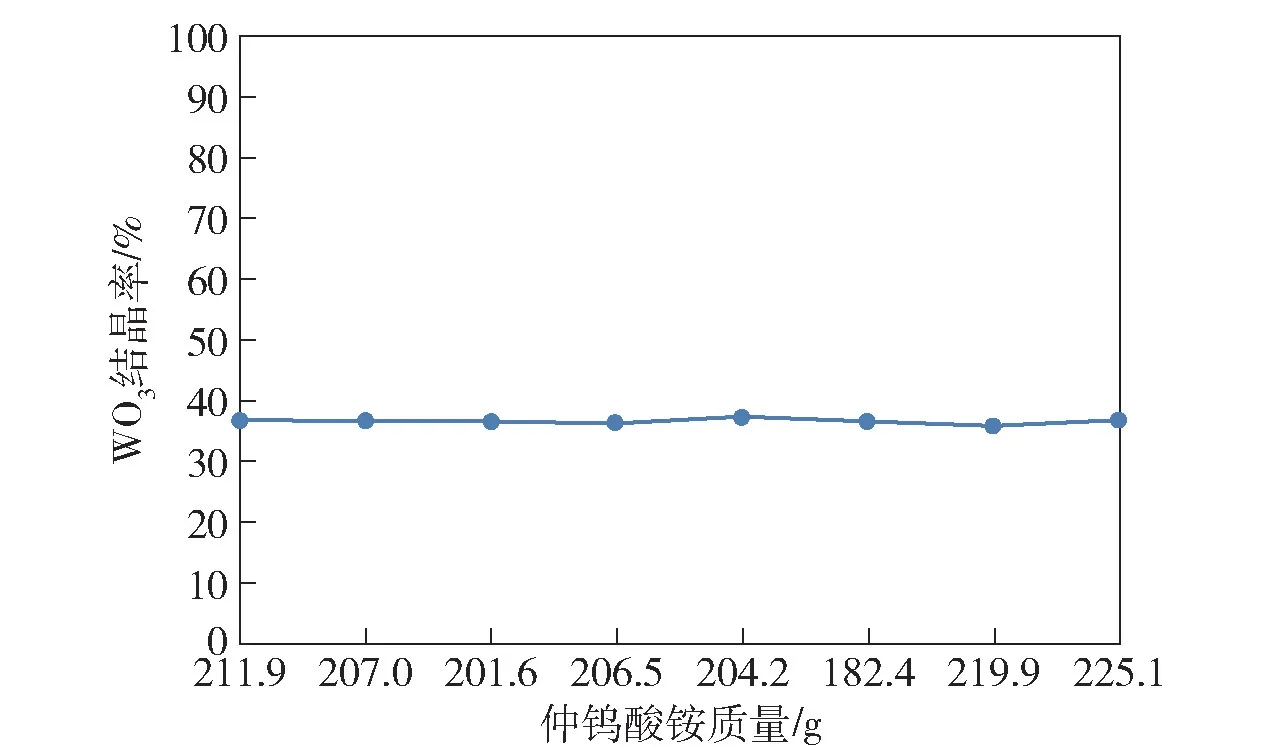
图4 仲钨酸铵结晶量与WO3 结晶率
从表5看出,蒸发量从58%升至93.5%,WO3结晶率变化范围为75.94%~93.78%。仲钨酸铵结晶中WO3含量为88.46%~88.75%,按五水仲钨酸铵折合,纯度为99.59%~99.92%。在粗钨酸成分基本相似情况下,此结果与王承友[8]研究钨酸铵蒸发结晶数据(蒸发量变化范围60%~93.5%,WO3结晶率为88.55%~88.75%)相比,钨酸铵蒸发范围和仲钨酸铵结晶范围更广,WO3纯度和结晶率更高,说明此试验工艺可行。
2.4 铵渣碱溶
二次氨溶渣仍含有60%左右的WO3,采用碱溶法加以回收,同时使有价元素钽、铌、锡在碱渣中得到进一步富集。本试验只做了常压浸出试验,所以碱渣含WO3还很高。为了提高回收率,可采用加压碱浸作业,该方法有待进一步试验验证。
二次氨渣经烘干磨碎后得碱溶试料,WO3含量为57.8%。试验每次取100 g 试料,在1 L 烧杯中进行。水浴加温,温度控制同前。溶剂用分析纯NaOH 配制而成。试验主要考查了碱量、碱浓度、温度和时间对WO3溶出率的影响。
先将计量的NaOH 和水在烧杯中搅拌溶解,加热升温至规定的水平,将称好的100 g 试样在搅拌下缓缓加入烧杯中,维持规定温度到反应规定时间后冷却过滤。浆液用布氏漏斗抽滤,然后用2%NaOH 溶液50 mL 分三次淋洗滤渣,制样分析WO3含量。所得碱液可制成钨酸返回氨浸,碱渣回收钽、铌、锡。
用正交法安排试验,试验因素水平见表6。
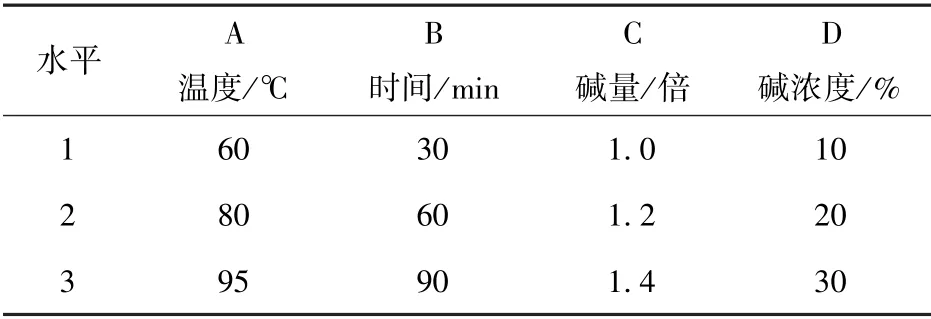
表6 试验因素水平
从表6看出,试验为四因素三水平试验,选用L9 (34)正交表。按正交表的编排进行分组试验。将试验结果WO3溶出率数据填入表的右侧;极差计算结果计入表下方。实验结果见表7。
从表7可得出较优工艺条件:温度95 ℃,碱浓度20%,NaOH 用量为理论量的1.4 倍,时间90 min。

表7 L9 (34)正交试验、结果和极差计算表
3 综合试验
为了进行对比,用分析纯氨水按与工业氨水相同的试验条件进行了对比试验,以便进行氨溶液杂质和随后所得产物的纯度进行对比。试验结果列于表8~10。
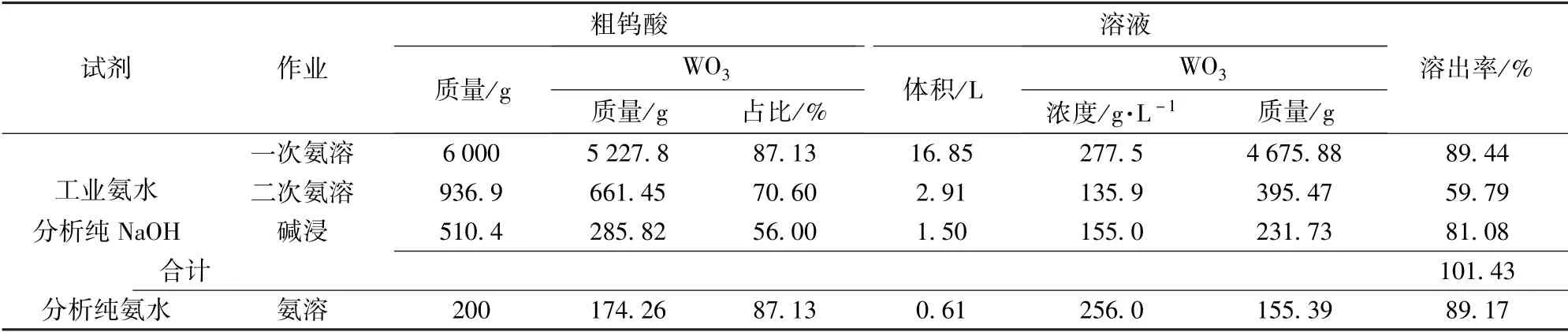
表8 粗钨酸处理综合串接试验结果-溶液
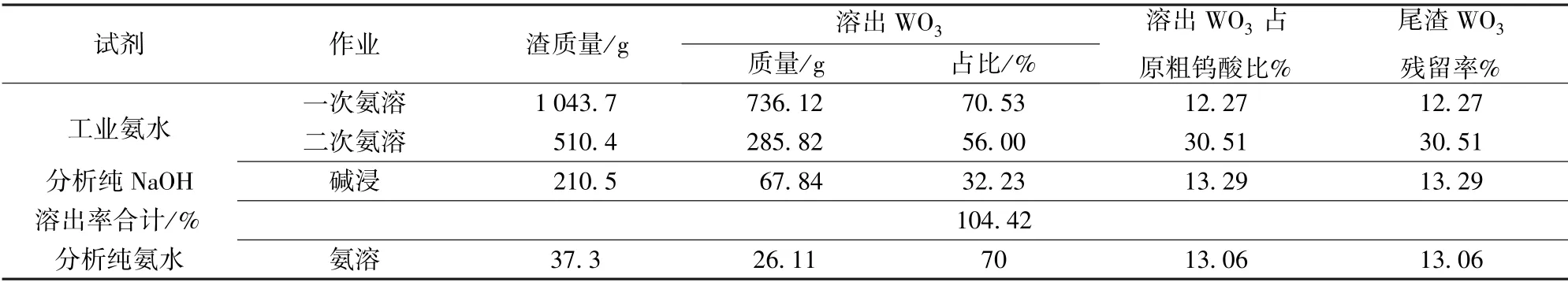
表9 粗钨酸处理综合串接试验结果-渣
两次氨溶时WO3溶出率(按液计):89.44% +6.31% +3.45% =99.20%。
从表10看出,用分析纯氨水所得的钨酸铵溶液除As 略高外,其余主要杂质均达到高纯溶液杂质含量要求。用工业氨水所获得的钨酸铵溶液,As、P 较高,但P 可达到工业纯溶液要求,其中二次液比一次液As、P 含量高,需进行除杂。因此本试验分别用工业氨水和分析纯氨水的一次氨浸出液进行蒸发结晶仲钨酸铵;在80 ℃左右蒸发至原体积的25%左右静置。经过滤洗净的仲钨酸铵在700 ℃下煅烧获得WO3产品,用光谱定量分析的杂质含量列于表11,差减法得到WO3纯度为:工业氨水一次氨液制得的WO3品位>99.94%,分析纯氨水制得WO3品位>99.96%。两种方法制得WO3纯度相近,均达到国家标准要求,但采用分析纯氨水尾渣中WO3残留量高,成本比工业氨水高,设备腐蚀性大,环境污染大。因此,工业生产上推荐使用工业氨水进行氨浸、蒸发结晶、煅烧仲钨酸铵制取三氧化钨。

表10 氨浸液和氨渣主要成分 %
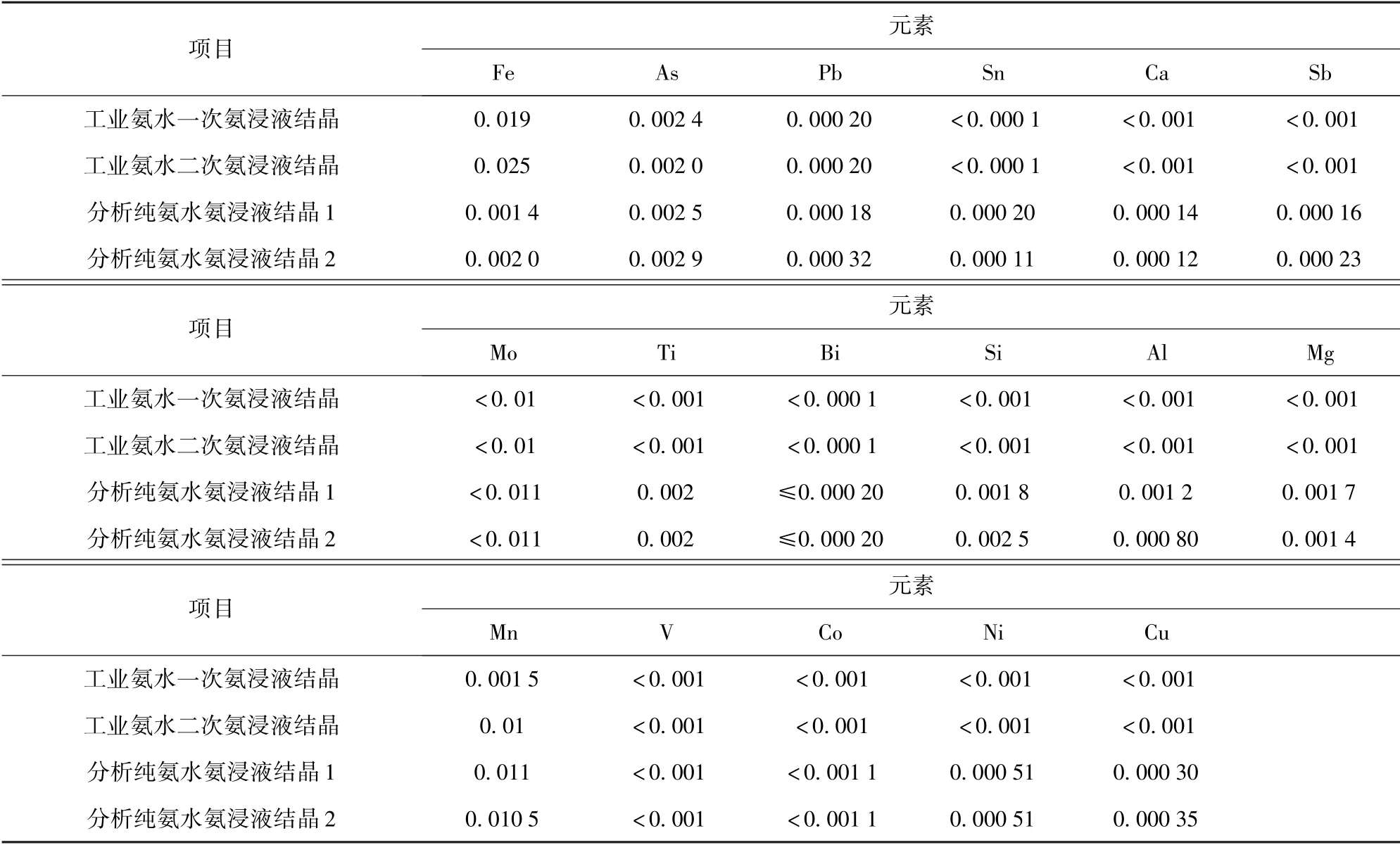
表11 三氧化钨产品主要杂质光谱定量分析结果 %
一次氨浸时,Nb2O3+Ta2O3有22.42%被溶解进入溶液,碱渣含Nb2O3+Ta2O32.55%,富集倍数为10 倍左右,入渣直收率72.49%;含Sn4.27%,富集倍数20 倍左右,直收率75%左右。该渣可作回收钽、铌、锡的原料,以年产20 000 t 钨冶炼产品厂家为例,预计每年有价金属回收价值将超过1 000万元。
结晶母液可制成钨酸、人造白钨或用萃取法回收其中的钨。碱溶液杂质情况可采取离子交换法提钨或制成钨酸或人造白钨返回主流程,该方法金属回收率高、生产环境友好、废渣和废水处理工作量少,对环境的污染小;使用白钨矿做原料时此法对矿源的适应性差,副流程长,金属实收率低,而且腐蚀性大,工作环境差,环境污染严重,效果不理想。
4 结论
本文针对目前APT 和WO3生产方法存在的问题,对粗钨酸进行了氨溶、氨渣碱溶、蒸发结晶等工序的条件试验,分别采用分析纯氨水和工业氨水进行了综合试验,试验数据说明粗钨酸采用氨溶法制得钨酸铵溶液,经蒸发浓缩或中和结晶析出仲钨酸铵,灼烧后的产物为三氧化钨的工艺流程是可行的。
1)试验结果表明,第二次氨溶液杂质含量高不宜直接结晶。因此推荐流程只采用一次氨溶,氨渣中残留的钨用碱浸回收。工业生产上推荐使用工业氨水进行氨浸、蒸发结晶、煅烧仲钨酸铵制取三氧化钨。
2)黑钨精矿经盐酸分解后获得的粗钨酸直接采用氨溶-蒸发结晶流程处理可获得含WO388.46%~88.75%的仲钨酸铵,经煅烧后的WO3纯度>99.9%。氨渣经碱溶后可充分回收钨。WO3的氨溶率可达到89% 以上,碱溶率可达10% 以上,WO3的总收率达99%以上,进入产品WO3的直收率75%以上。
3)结晶母液和碱溶液的处理有待进一步探讨,以便回收其中的钨或直接制取钨的产品。
4)粗钨酸经氨溶、碱浸出后,钽、铌、锡富集于碱渣中,Nb2O3+Ta2O3富集倍数10 倍以上,锡大于20 倍,可作回收钽、铌的原料。约有20%多的钽、铌进入氨溶液,可在提钨过程中分离提取。
