地理分布与乌药药材品质“道地性”的相关性分析
2021-11-16求鑫瑜楼招欢
求鑫瑜 楼招欢
1.浙江中医药大学药学院 杭州 311402 2.宁波市妇女儿童医院
乌药(Linderae Radix)系樟科植物乌药(Lindera aggregata(Sims) Kosterm.)的干燥根,现主要分布于浙江天台、衢州,江西景德镇、抚州、新余,湖南怀化、邵阳和四川巴中等地区。现代药理研究显示,乌药具有调节胃肠道功能的作用[1]。天台被认为是乌药的道地产区,天台乌药的药材品质和疗效与其他产地乌药相比有着显著的优势,这种优势或称为“道地性”是否与其生长的地理环境及由此产生的活性成分差异相关,目前尚未得知。研究表明,产地不同、生长的环境存在差异,可引起药材性状及所含有效成分的改变,进而影响药材的有效性[2-3]。特征性、指标性成分含量的高低是评价药材品质好坏的重要标准;而药材的显微特征观察示例可用于中药真伪鉴定和药材优劣评价,是道地药材鉴别的有效方法[4-5]。乌药醚内酯与去甲异波尔定是乌药的法定检测指标[6],其中乌药醚内酯亦是其特征性成分[7]。本研究采用高效液相色谱法(high performance liquid chromatography,HPLC) 法检测道地与非道地产区乌药去甲异波尔定、乌药醚内酯2个主要成分的含量并观察药材显微特征,探讨地理分布与乌药药材“道地性”的相关性,寻找道地产区乌药的独特综合性指标,拟阐释乌药“道地性”的科学内涵[8],为乌药进一步开发利用提供参考。
1 仪器和材料
1.1 材料 去甲异波尔定对照品、乌药醚内酯对照品均购于上海源叶生物科技有限公司 (批号:P10M9L61140、ZJ0630BA14);乙腈(色谱纯)、甲醇(色谱纯)均购于O-ceanpak公司(批号:20111102G108、20111027G108);甲醇(分析纯)、甲酸(分析纯)、盐酸(分析纯)均购于国药集团化学试剂有限公司(批号:20200928、20160516、20191216);甲酸(色谱纯)购于Aladdin公司(批号:E2022005)。浙江天台、湖南怀化产地乌药药材由浙江中医药大学中药饮片厂提供,浙江衢州、江西景德镇、湖北恩施产地乌药药材由宁波市鄞州医药药材有限公司提供,云南楚雄产地乌药药材由云南螺蛳湾药材批发市场采购,天台乌药样品在产地经刮皮处理,余产地样品为原药材干燥后所切饮片。
1.2 主要仪器 LC-20A型岛津高效液相色谱仪购于日本岛津公司;BSA224S型Sartorius电子天平为德国Sartorius公司产品;XS105DU型电子天平购于瑞士Mettler Toledo公司;SB-5200D超声波清洗机购于宁波东南仪器有限公司;DHG-9070A型电热恒温鼓风干燥箱购于上海精宏实验设备有限公司;DM500正置显微镜为徕卡仪器(德国)有限公司产品。
1.3 乌药醚内酯、去甲异波尔定含量测定
1.3.1 色谱条件
1.3.1.1 乌药醚内酯含量测定 Silversil C18柱(4.6nm×250nm,5μm),流动相乙腈:水(56:44),柱温30℃;流速1.0mL·min-1,检测波长235nm,进样量10μL,理论塔板数不低于2 000。
1.3.1.2 去甲异波尔定含量测定 Silversil C18柱(4.6nm×250nm,5μm),流动相为乙腈(A):含0.5%甲酸、0.1%三乙胺溶液(B),梯度洗脱(0~13min,10%~22%A,13~22min,22%A),柱温30℃,流速1.0mL·min-1,检测波长280nm,进样量10μL,理论塔板数不低于5 000。
1.3.2 对照品溶液的制备
1.3.2.1 乌药醚内酯对照品溶液的制备 精密称取乌药醚内酯对照品7mg,称定质量,置于50mL容量瓶中,以甲醇溶解并定容,得0.144mg·mL-1的乌药醚内酯对照品溶液。
1.3.2.2 去甲异波尔定对照品溶液的制备 精密称取去甲异波尔定对照品11mg,称定质量,置于50mL容量瓶中,以甲醇溶解并定容,得0.220mg·mL-1的去甲异波尔定对照品溶液。
1.3.3 供试品溶液的制备
1.3.3.1 乌药醚内酯含量测定供试品溶液制备 精密称取乌药粉末0.250g,过3号筛,置于25mL具塞锥形瓶中,加甲醇至刻度,超声1h,冷却,以甲醇补足至刻度线,过0.45μm微孔滤膜,即得乌药醚内酯供试品溶液。
1.3.3.2 去甲异波尔定含量测定供试品溶液制备 精密称取乌药粉末0.100g,过3号筛,置于具塞锥形瓶中,以移液管移取甲醇-盐酸(0.5→100)(2:1)25mL,称定质量,加热回流并保持微沸1h,冷却,再称定并补足质量,摇匀,取续滤液,过0.45μm微孔滤膜,即得去甲异波尔定供试品溶液。
1.3.4 精密度考察
1.3.4.1 乌药醚内酯精密度考察 精密称取同一批次乌药粉末,按照1.3.3.1项条件提取,1.3.1.1项色谱条件进样,连续进样6次,记录各峰面积(mAU×min),计算6次进样峰面积的相对标准偏差(relative standard deviation,RSD)值。
1.3.4.2 去甲异波尔定精密度考察 精密称取同一批次乌药粉末,按照1.3.3.2项条件提取,1.3.1.2项色谱条件进样,连续进样6次,记录各峰面积(mAU×min),计算6次进样峰面积的RSD值。
1.3.5 稳定性考察
1.3.5.1 乌药醚内酯稳定性考察 精密称取同一批次乌药粉末,按照1.3.3.1项条件提取,1.3.1.1项色谱条件进样,分别在0、4、8、12、16、20、24h检测并记录各峰面积(mAU×min),计算7次进样峰面积的RSD值。
1.3.5.2 去甲异波尔定稳定性考察 精密称取同一批次乌药粉末,按照1.3.3.2项条件提取,1.3.1.2项色谱条件进样,分别在0、4、8、12、16、20、24h检测并记录各峰面积(mAU×min),计算7次进样峰面积的RSD值。
1.3.6 重复性考察
1.3.6.1 乌药醚内酯重复性考察 精密称取同一批次乌药样品6份,按照1.3.3.1项条件提取,1.3.1.1项色谱条件进样,记录各峰面积(mAU×min),计算含量及其RSD值。
1.3.6.2 去甲异波尔定重复性考察 精密称取同一批次乌药样品6份,按照1.3.3.2项条件提取,1.3.1.2项色谱条件进样,记录各峰面积(mAU×min),计算含量及其RSD值。
1.3.7 线性方程考察
1.3.7.1 乌药醚内酯线性方程考察 精密吸取原浓度的乌药醚内酯对照品溶液1、2、4、6、10mL至10mL容量瓶中,加甲醇至刻度,摇匀,分别制成浓度为0.0144、0.0288、0.0576、0.0864、0.1440mg·mL-1的对照品溶液,准确吸取上述对照品溶液10μL,按1.3.1.1项色谱条件进行测定。以浓度为横坐标(x,单位mg·mL-1),峰面积为纵坐标(y,单位mAU×min),绘制标准曲线,得到回归方程。
1.3.7.2 去甲异波尔定线性方程考察 精密吸取原浓度去甲异波尔定对照品溶液1、2、4、5、10mL至10mL容量瓶中,加甲醇-盐酸(0.5→100)(2:1)至刻度,摇匀,超声至完全溶解,分别制成浓度为0.0220、0.0440、0.0880、0.1100、0.2200mg·mL-1的对照品溶液,准确吸取上述对照品溶液10μL,按1.3.1.2项色谱条件进行测定。 以浓度为横坐标(x,单位mg·mL-1),峰面积为纵坐标(y,单位mAU×min),绘制标准曲线,得到回归方程。
1.3.8 加样回收率考察
1.3.8.1 乌药醚内酯加样回收率考察 精密称取已知含量的天台乌药0.125g,加入一定量的乌药醚内酯对照品,按照1.3.3.1项的方法制备溶液,进样10μL,以1.3.1.1项色谱条件进行测定,测定峰面积,计算回收率,实验重复6次。
1.3.8.2 去甲异波尔定加样回收率考察 精密称取已知含量的天台乌药0.050g,加入一定量的去甲异波尔定对照品,按照1.3.3.2项的方法制备溶液,进样10μL,以1.3.1.2项色谱条件进行测定,测定峰面积,计算回收率,实验重复6次。
1.3.9 含量测定
1.3.9.1 乌药醚内酯含量测定 精密称取6个不同产地的乌药0.250g,分别按1.3.3.1项的方法制备供试品溶液,进样10μL,以1.3.1.1项色谱条件进行测定,记录色谱峰面积,计算乌药醚内酯含量,重复2次。
1.3.9.2 去甲异波尔定含量测定 精密称取6个不同产地的乌药0.100g,分别按1.3.3.2项的方法制备供试品溶液,进样10μL,以1.3.1.2项色谱条件进行测定,记录色谱峰面积,计算去甲异波尔定含量,重复2次。
1.4 不同产地乌药与天台乌药主成分含量差异比较 对比5个产地的乌药中的主成分乌药醚内酯、去甲异波尔定含量,分别按下式计算相对天台乌药的含量差异比。含量差异比(%)=(天台乌药主成分含量-其他产地乌药主成分含量)/天台乌药主成分含量×100%。
1.5 不同产地经纬度查询 通过百度网站查询,拾取坐标系统检索不同产地的经纬度。
1.6 显微观察性状特征 取6个不同产地的乌药,打粉过3号筛,取粉末适量,滴加甘油醋酸进行显微观察。
2 结果
2.1 精密度考察结果 计算得出,乌药醚内酯、去甲异波尔定RSD值分别为0.68%、0.03%,说明该测定方法的精密度良好。
2.2 稳定性考察结果 计算得出,乌药醚内酯、去甲异波尔定RSD值分别为0.36%、0.64%,说明样品至少在24h内稳定。
2.3 重复性考察结果 计算得出,乌药醚内酯、去甲异波尔定RSD值分别为0.52%、2.22%,说明该测定方法的稳定性良好。
2.4 线性方程考察结果 乌药醚内酯在0.0144~0.1440mg·mL-1浓度范围内线性拟合的标准曲线回归方程为y=906 471.4612x-1 150.7671(r2=1),去甲异波尔定在0.0220~0.2200mg·mL-1浓度范围内线性拟合的标准曲线回归方程为y=12 958 444.1900x+5 552.8778(r2=0.9997),说明该测定方法线性关系良好。
2.5 加样回收率考察结果 乌药醚内酯回收率RSD值为0.57%,加样回收率98.70%~100.30%;去甲异波尔定回收率RSD值为2.22%,加样回收率97.20%~103.90%,说明该方法的加样回收率符合要求。见表1、2。
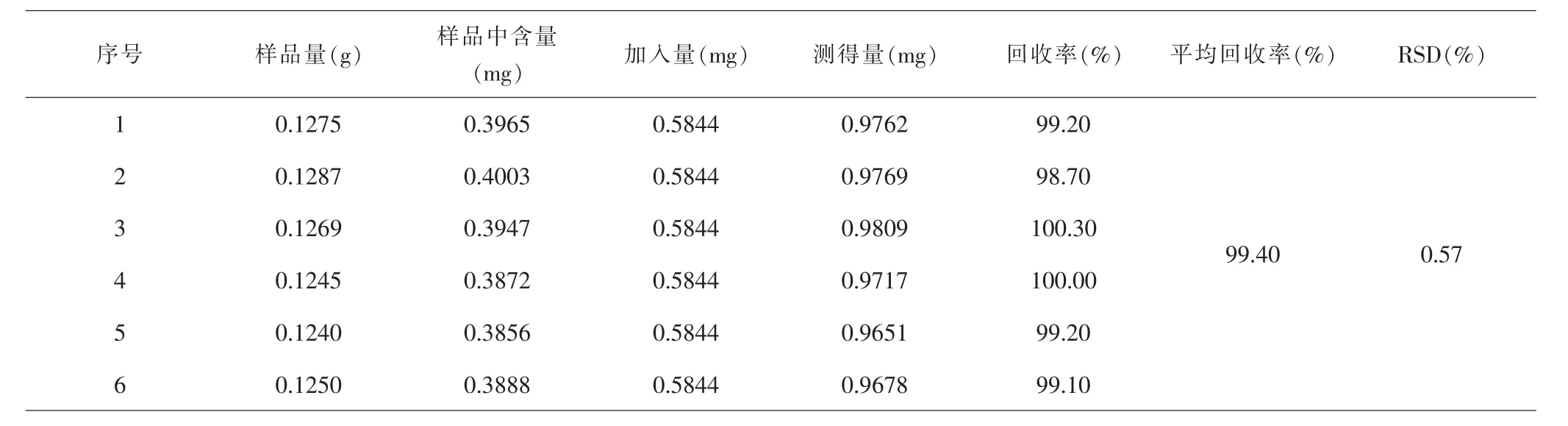
表1 乌药醚内酯加样回收试验结果Tab.1 Determination results of the recovery rate of linderane
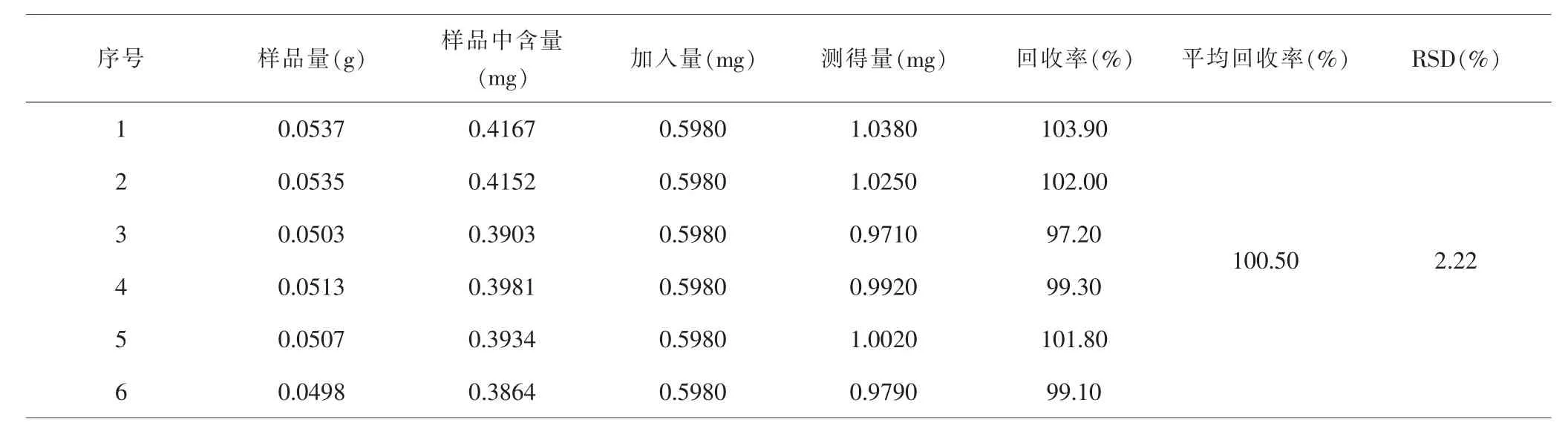
表2 去甲异波尔定加样回收试验结果Tab.2 Determination results of the recovery rate of norisoboldine
2.6 含量测定结果 计算得出6个不同产地乌药中乌药醚内酯、去甲异波尔定的含量,并换算成质量分数。见表3。浙江天台乌药中所含乌药醚内酯明显高于其他产地。各产地乌药醚内酯含量比例为浙江天台∶浙江衢州∶湖北恩施∶江西景德镇∶湖南怀化∶云南楚雄=67∶45∶40∶25∶20∶1, 去甲异波尔定含量比例为浙江天台:浙江衢州:湖北恩施:江西景德镇:湖南怀化:云南楚雄=62:75:84:65:59:1。
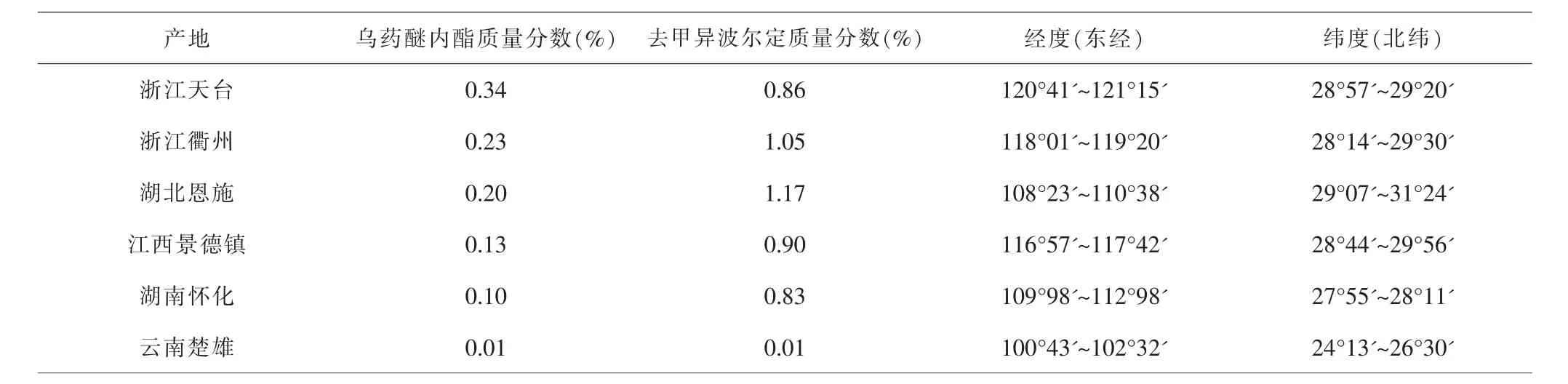
表3 不同产地乌药主要成分含量测定及地理分布Tab.3 Assay of main components and geographical distribution of Linderae Radix from different regions
2.7 不同产地乌药与天台乌药主成分含量差异比较 计算得出,其他产地相对天台产地的乌药醚内酯含量差异比,浙江衢州、湖北恩施、江西景德镇、湖南怀化、云南楚雄分别为32.80%、41.50%、62.70%、70.70%、98.50%;而其他产地相对天台产地的去甲异波尔定含量差异比,浙江衢州、湖北恩施、江西景德镇、湖南怀化、云南楚雄分别为22.00%、35.70%、4.90%、3.60%、98.40%。说明与天台比较,各产地所产乌药的去甲异波尔定含量相对接近,而乌药醚内酯含量差异比较大,适合作为不同产地品质的评价指标。
2.8 不同产地经纬度查询结果 浙江天台与浙江衢州、江西景德镇三个产地经度、纬度相近;湖北恩施与湖南怀化两者经度相近;云南楚雄与其他5个产地经度、纬度存在显著差异。见表3。
2.9 不同产地乌药性状特征显微观察 显微观察各个产地乌药粉末颗粒性状特征提示,浙江天台、浙江衢州、江西景德镇三者显微特征较相似,淀粉粒、油细胞常见,浙江天台、江西景德镇未见糊化淀粉粒;湖北恩施与湖南怀化两者显微特征较相似,均含有大量糊化淀粉粒,少量石细胞,较少的油细胞和淀粉粒,木纤维中淀粉粒较少;云南楚雄与其他5个产地乌药显微差异显著,其淀粉粒极多,多呈团簇状,木纤维中淀粉粒常见并且颗粒较大,油细胞较少。见表4及图1~7。

表4 不同产地乌药粉末显微性状特征Tab.4 Characteristics of microscopic properties of Linderae Radix powder from different regions

图1 不同产地乌药淀粉显微特征(40×)Fig.1 Microstructure of starch granules Linderae Radix from different regions

图2 不同产地乌药导管显微特征(40×)Fig.2 Microstructure of starch catheters of Linderae Radix from different regions

图3 不同产地乌药韧皮纤维显微特征(40×)Fig.3 Microstructure of bast fiber of Linderae Radix from different regions

图4 不同产地乌药木纤维显微特征(40×)Fig.4 Microstructure of wood fibers of Linderae Radix from different regions

图5 不同产地乌药油细胞显微特征(40×)Fig.5 Microstructure of eleocyte of Linderae Radix from different regions

图6 不同产地乌药石细胞显微特征(40×)Fig.6 Microstructure of sciereid of Linderae Radix from different regions
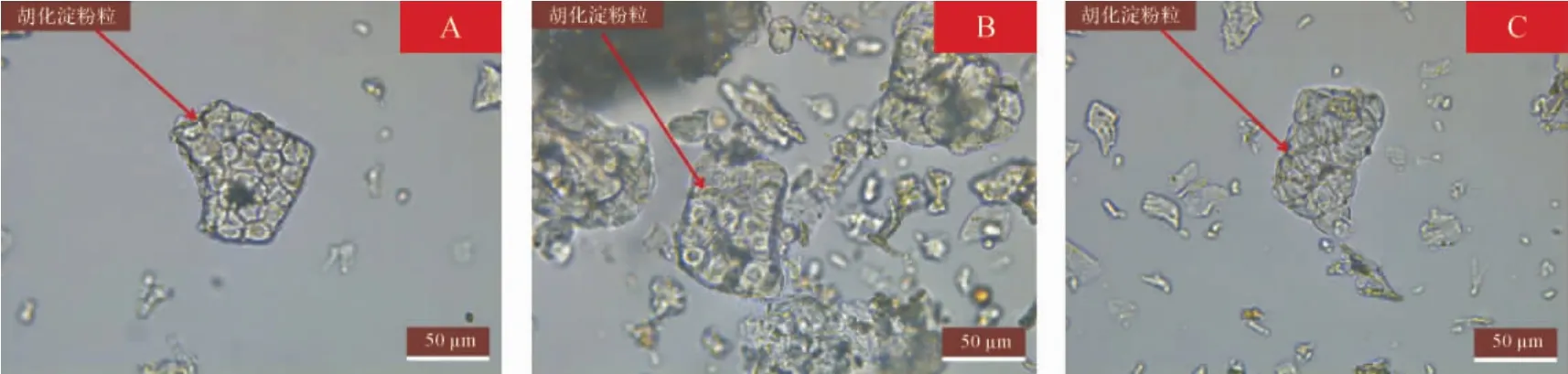
图7 不同产地乌药糊化淀粉粒显微特征(40×)Fig.7 Microstructure of Gelatinized starch granules of Linderae Radix from different regions
3 讨论
从主要成分含量检测结果看,本研究提示乌药地理分布与其“道地性”显著相关。浙江天台乌药中乌药醚内酯含量最高质量分数为0.34%,去甲异波尔定含量中等。浙江天台与浙江衢州、江西景德镇三个产地经度、纬度相近,三者主成分含量较相近,其中乌药醚内酯的含量随着经度减小而减少;湖北恩施与湖南怀化两者虽经度相近,但因为纬度差异,湖南怀化的乌药醚内酯含量仅为湖北恩施的一半;云南楚雄与其他5个产地经度、纬度差异均较明显,成分含量存在明显的差距。上述结果提示,产地的纬度、经度都能显著影响药物主成分的含量,产地经纬度与天台越接近,乌药醚内酯等主成分含量越道地。黄林芳等[9]对肉苁蓉进行了生态研究,发现不同经纬度肉苁蓉主成分含量存在明显差异,亦说明地理分布确实能影响药材的“道地性”。
从显微性状特征看,地理位置分布与乌药“道地性”亦存在显著相关性,产地经纬度与天台越接近,乌药显微特征越道地。浙江天台乌药淀粉粒、油细胞较多,木纤维中亦含有丰富的淀粉粒,但不含石细胞;浙江天台、浙江衢州、江西景德镇三个产地经度、纬度明显相近,三者显微特征皆较相似,其中淀粉粒个数随着经度减小而减少;湖北恩施与湖南怀化两者经度相近,显微特征比较相似,均含有大量糊化淀粉粒,少量石细胞,较少的油细胞和淀粉粒,且木纤维中淀粉粒较少;云南楚雄与其他5个产地经度、纬度相差较大,其所产乌药显微差异显著,其淀粉粒极多,多呈团簇状,木纤维中淀粉粒常见,而且颗粒较大,油细胞较少,偶见石细胞。王旭红等[10]研究认为乌药块根、直根中无石细胞;但笔者观察到了少量石细胞,与房志坚等[11]研究结论一致。综上所述,产地经纬度对药物显微特征的影响较大,经纬度相似的产地所产乌药的显微特征相近,经度越小淀粉粒越少,石细胞越多(云南楚雄除外);另外,淀粉粒、糊化淀粉粒和石细胞可作为不同产地乌药药材的显微鉴别特征指标。
研究表明,气候相似是保障药材品质的基本条件[12]。经度、纬度不同直接导致太阳辐射和海陆分布不同,造成不同地段气候条件的主要因子——光照、温度、水分等的差异,形成了不同的纬度地带性和经度地带性气候环境,这可能是造成不同产地药材主成分含量与显微性状差异的关键原因,也是造成药材“道地性”的根本原因。本研究也证实,不同产地经纬度不同,所产乌药主成分含量不同,显微性状也存在显著差异;乌药品质差异与地理分布明显相关,天台特殊的气候条件造就了天台乌药独特的生理生化特征。
综上所述,本研究结果提示可将乌药醚内酯含量高,淀粉粒较多、油细胞较多,不含石细胞,作为道地乌药独特的综合性指标。另外,依据《中华人民共和国药典》规定的标准:乌药醚内酯不少于0.03%,去甲异波尔定不少于0.40%[6],本研究中云南乌药所含乌药醚内酯为0.01%,去甲异波尔定为0.01%,不能应用于临床。
