米卡芬净联合伏立康唑治疗血液肿瘤侵袭性真菌病患者的临床分析*
2021-11-03谢晶郭智王强刘玄勇王月乔陈丽娜张弋慧智李旭绵韦丽娅陈晓
谢晶,郭智,王强,刘玄勇,王月乔,陈丽娜,张弋慧智,李旭绵,韦丽娅,陈晓
430065 武汉,武汉科技大学 医学院(谢晶、郭智、王强、刘玄勇);518116 广东 深圳,国家癌症中心/国家肿瘤临床医学研究中心/中国医学科学院北京协和医学院肿瘤医院深圳医院 血液肿瘤科(谢晶、郭智、刘玄勇、王月乔、陈丽娜、张弋慧智、李旭绵、韦丽娅、陈晓)
侵袭性真菌病(invasive fungal disease,IFD)是指真菌侵入人体,在组织、器官或血液中生长、繁殖,导致炎症反应及组织损伤的疾病。血液肿瘤的患者往往存在自身免疫功能低下、长期使用类固醇激素、化疗后中性粒细胞减少、经常使用大剂量广谱抗菌药物、中心静脉插管及长时间住院等情况,以上均是IFD的高危宿主因素,使得此类患者更容易出现真菌感染。近年来血液肿瘤患者IFD的发生率呈现上升趋势[1],有研究统计在接受化疗的血液肿瘤患者中,确诊和临床诊断IFD的总发生率为2.1%[2],是导致患者死亡的主要原因之一。米卡芬净是新型棘白菌素类抗真菌药物,对念珠菌和曲霉菌具有广谱的抗菌活性,不良反应少,已广泛应用于临床。伏立康唑是三唑类抗真菌药,对青霉菌、曲霉菌、念珠菌及新型隐球菌等均有效,常见的不良反应为肝功能损伤,被推荐作为侵袭性真菌感染的主要治疗药物之一。近年来双药联合抗真菌方案也逐渐形成趋势,尤其是针对单药治疗失败或无法耐受、多部位或耐药真菌感染的高危病例效果显著。本研究旨在探索米卡芬净联合伏立康唑治疗侵袭性真菌感染的疗效及不良反应。
1 资料与方法
1.1 资料来源
回顾性分析2019年6月至2020年6月在中国医学科学院肿瘤医院深圳医院血液肿瘤科诊断为IFD并接受抗真菌治疗的60例血液肿瘤患者,其中给予米卡芬净联合伏立康唑抗真菌治疗的30例患者设为观察组,包括男17例 ,女13例,年龄21~79岁,中位年龄46.5岁,其中非霍奇金淋巴瘤14例,霍奇金淋巴瘤2例,急性髓系白血病5例,急性淋巴细胞白血病3例,多发性骨髓瘤3例,骨髓增生异常综合征2例,慢性髓系白血病1例。选择同期单药伏立康唑抗真菌治疗的30例IFD患者设为对照组,包括男18例,女12例,年龄23~84岁,中位年龄48.0岁,其中非霍奇金淋巴瘤11例,霍奇金淋巴瘤1例,急性髓系白血病5例,急性淋巴细胞白血病4例,多发性骨髓瘤4例,骨髓增生异常综合征3例,慢性髓系白血病2例(表1)。观察组和对照组病例基数水平相当,具有可比性。
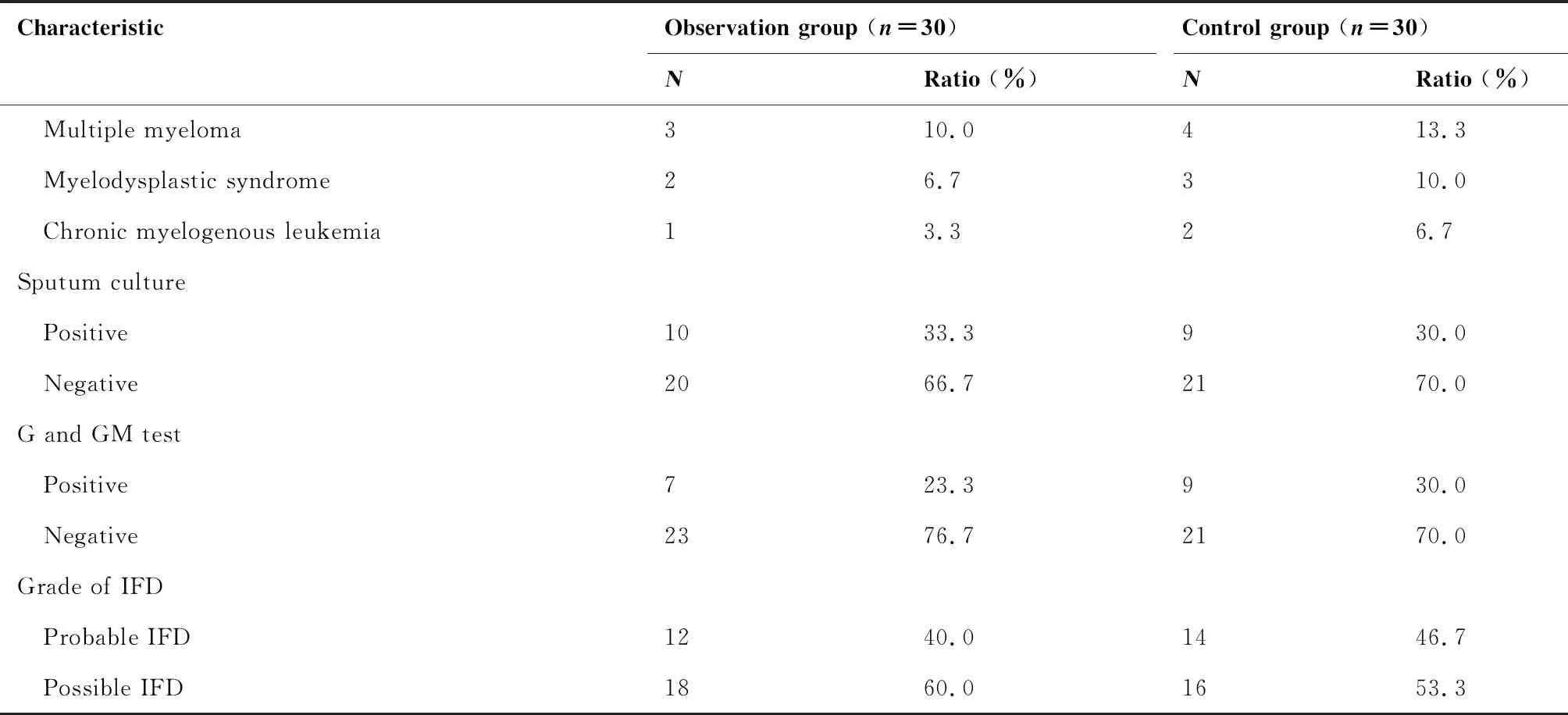
(Table 1 continues on next page)
IFD诊断标准依照《血液病/恶性肿瘤患者侵袭性真菌病的诊断标准与治疗原则(第五次修订版)》[3],观察患者的临床症状(如发热、咳嗽、咳痰、胸闷)、体征(如肺部啰音等)、一般情况(如血氧饱和度等)等,实验室检查包括血常规、肝肾功能、电解质、G试验(1,3-β-D葡聚糖检测)/GM试验(半乳糖甘露醇聚糖抗原检测),以及痰液、血培养等标本相关真菌感染培养结果,影像学检查包括胸部X线片、CT等,诊断IFD分为确诊、临床诊断、拟诊3个诊断级别(表2)。

表2 IFD诊断标准及级别
1.2 治疗方法
观察组:注射用米卡芬净钠100~150 mg,1次/天,静脉滴注时间大于1 h。联合注射用伏立康唑,首日负荷剂量6 mg/kg,1次/12 h,随后4 mg/kg,1次/12 h,静脉滴注。对照组:单药注射用伏立康唑,首日负荷剂量6 mg/kg,1次/12 h,随后4 mg/kg,1次/12 h,静脉滴注。观察组和对照组抗真菌治疗的用药时间至少1周以上,一般治疗周期为2~4周,抗真菌总疗程时间根据患者病情调整,至少需应用至体温正常、临床状况稳定,IFD相关微生物学和/或影像学指标恢复正常。当患者因初始抗真菌治疗药物毒性无法耐受,或初始抗真菌治疗2周临床症状加重、微生物学和影像学指标无好转时,应考虑调整抗真菌药物[3]。治疗结束后评估疗效。
1.3 疗效标准
监测患者体温、G试验、GM试验、肝肾功能以及真菌培养、胸部CT指标变化以及治疗时间。对治疗后患者疗效的评估从临床症状、体征、肺部影像学、病原学检查等方面来进行疗效评判。分为完全缓解:IFD相关症状和体征、影像学异常全部消失,微生物学证据提示真菌清除;部分缓解:IFD相关症状和体征、影像学异常有所改善,微生物学证据提示真菌清除;稳定:IFD相关症状和体征无改善,且临床、影像学和微生物综合评估未提示疾病进展;疾病进展:临床、影像学和微生物综合评估提示疾病进展;死亡:与IFD直接或间接相关的各种原因导致的死亡。总有效率=(完全缓解+部分缓解)/总例数×100%。
1.4 疗效评价
两组患者治疗开始后一般每周复查胸部CT进行疗效评价,观察患者治疗前后体温、呼吸道症状及体征改善情况,评价临床疗效及观察不良反应。治疗过程中定期进行血常规、肝肾功能、电解质、心电图、G/GM试验、痰培养等检查,使用抗真菌药物后观察患者有无视觉障碍、皮疹、恶心、呕吐和腹泻等不适,记录不良反应发生及其表现、严重程度、持续时间、针对不良反应的处理方法,最终评价观察组和对照组疗效和安全性。采用SPSS 25.0统计学软件对数据进行处理,分析观察组和对照组在治疗中位时间、有效率、发生不良反应率等有无差异,计数资料采用t检验,计量资料采用χ2检验进行比较,P<0.05为差异有统计学意义。
2 结 果
2.1 感染情况
根据指南诊断标准,观察组中临床诊断12例,拟诊18例。痰培养病原学检查阳性10例,其中4例为曲霉菌,4例为白假丝酵母菌,1例为近平滑假丝酵母菌,1例为克柔假丝酵母菌。实验室检查真菌G/GM试验阳性7例。对照组中临床诊断14例,拟诊16例。痰培养病原学检查阳性9例,其中5例为曲霉菌,2例为白假丝酵母菌,2例为近平滑假丝酵母菌。实验室检查真菌G/GM试验阳性9例。全部患者均有肺部特征性影像学改变,胸部CT主要表现为结节斑片影,有时可见晕轮征、新月征等相对较为特征性的表现,但发生率不高。疾病早期可呈现非特征性改变,如支气管周围实变影、树芽征和毛玻璃样改变等(图1)。
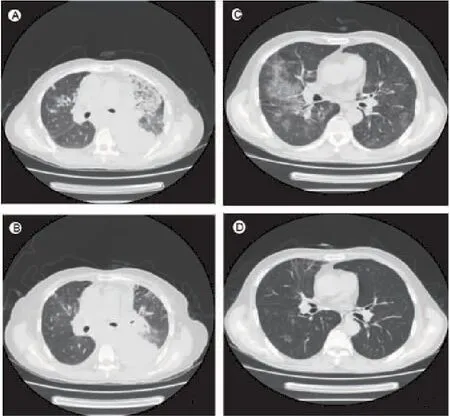
图1 IFD患者抗真菌治疗后复查胸部CT磨玻璃影消失(A、C治疗前,B、D治疗后)
2.2 疗效比较
观察组治疗中位时间是16.5天(7~52天),对照组治疗中位时间是22天(7~56天)。2组治疗中位时间比较存在统计学差异(P<0.05,表3)。观察组完全缓解11例,部分缓解15例,稳定3例,疾病进展1例,死亡0例,有效率为86.7%;对照组完全缓解8例,部分缓解11例,稳定6例,疾病进展4例,死亡1例,有效率为63.3%。两组有效率差异有统计学意义(P<0.05,表4)。
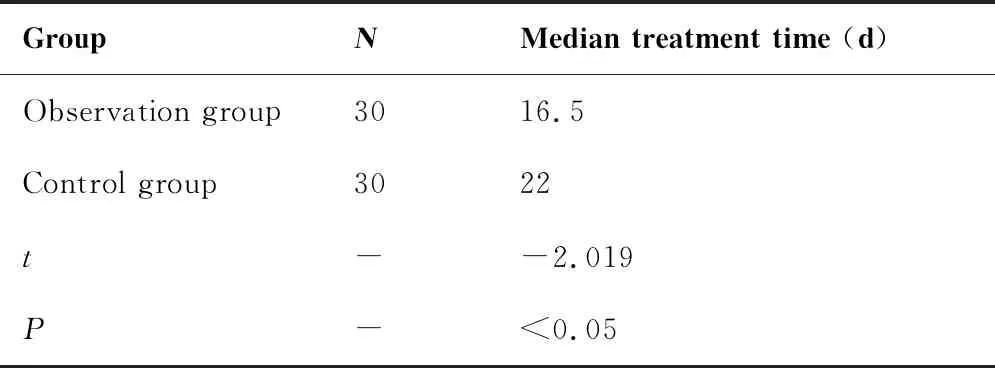
表3 观察组与对照组的治疗中位时间比较
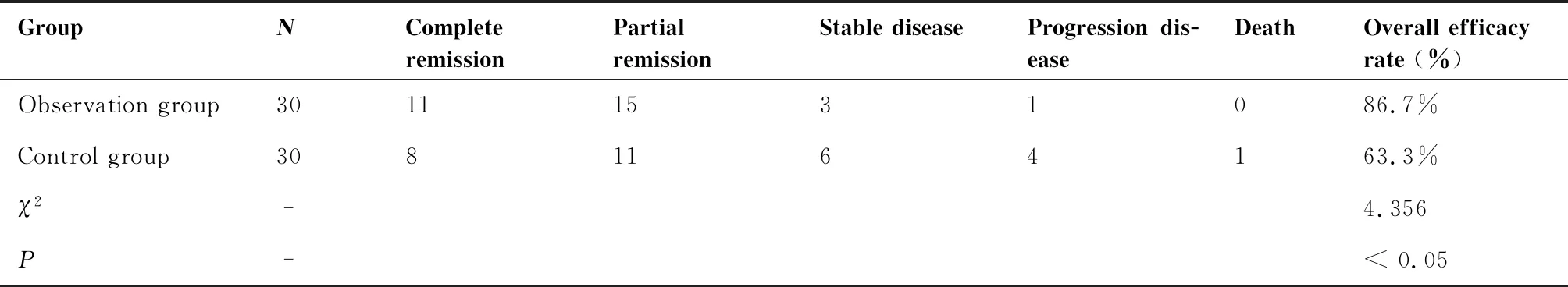
表4 观察组与对照组的总有效率比较例(%)
2.3 不良反应比较
观察组有5例不良反应,包括视觉改变(主要为幻视、色觉异常等)3例,肝功能异常1例,经保肝治疗好转,消化道反应(主要为恶心、呕吐等)1例。对照组有6例不良反应,包括视觉改变1例,肝功能异常3例,经保肝治疗后1例好转,2例出现重度肝功能异常更换抗真菌药物,消化道反应2例。观察组不良反应发生率为16.7%,低于对照组20%,两组比较差异无统计学意义(P>0.05,表5)。
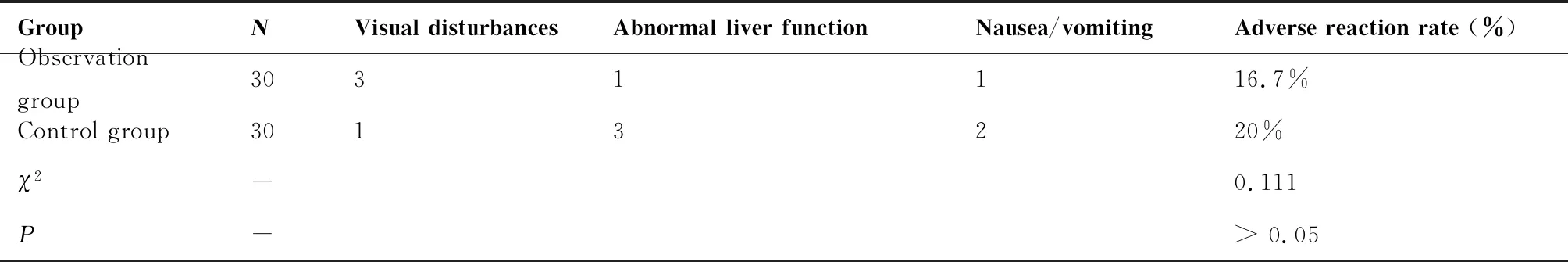
表5 观察组与对照组的不良反应比较
3 讨 论
IFD常发生于器官移植、血液病或恶性肿瘤患者免疫系统功能低下时,造成机体炎症并影响肺等组织器官的功能,致死率较高[4]。随着肿瘤发病率上升及细胞毒性治疗、造血干细胞移植普遍应用等,IFD发病率逐年攀升,尤其在血液肿瘤患者中[5]。因此,对于血液肿瘤IFD患者选择合适的抗感染药物和治疗方案具有十分重要的临床意义。IFD主要病原体是念珠菌属和曲霉菌属[3],临床上应用较多的抗真菌药主要有三大类,包括以两性霉素及其脂质体为主的多烯类药,以伊曲康唑、氟康唑和伏立康唑为代表的三唑类药,以及以卡泊芬净和米卡芬净为代表的棘白菌类药物。两性霉素B是既往治疗IFD的金标准用药,主要作用在真菌的细胞膜,可用于念珠菌、曲霉菌、隐球菌、荚膜组织胞浆菌、球孢子菌、芽生菌、孢子丝菌等引起的感染[6],抗菌谱较广,但具有严重的肾脏毒性,应用时需要频繁监测肾功能,适用人群存在局限性,随着多种新型抗真菌药的问世多烯类不再被指南推荐作为IFD一线抗真菌治疗的首选药物。近年来,三唑类及棘白菌类药物得到了广泛的应用。三唑类药物是通过竞争性抑制真菌羊毛甾醇去甲基化,促使细胞膜的流动性与通透性变差,从而影响膜表面酶的活性来发挥抗真菌的作用。不同的三唑类药物抗菌谱不同,伊曲康唑抗真菌谱覆盖念珠菌属、曲霉菌属、组织胞浆菌及隐球菌属,但对镰刀霉活性较低;氟康唑抗菌谱较窄,主要为白色念珠菌和隐球菌,对曲霉菌无活性;伏立康唑作为第二代氟康唑衍生物,对于念珠菌(包括氟康唑耐药的克柔念珠菌和光滑念珠菌)、新生隐球菌、和白吉利毛孢子菌都有良好的抑制活性作用;对一些霉菌如曲霉、尖端塞多孢子菌、镰刀菌、皮炎芽生菌和荚膜组织胞浆菌都有抑制作用。常见的不良反应主要有视觉异常、肝肾功能损伤、胃肠道反应(恶心、呕吐、腹泻)、皮疹等。被推荐作为侵袭性真菌感染的主要治疗药物和免疫功能低下患者的抗真菌预防药物[7]。棘白菌素类抗真菌药,作用机制不同于多烯类和三唑类,主要作用于真菌的细胞壁,通过抑制p(1,3)-D葡聚糖的合成,从而破坏真菌细胞壁的完整性,进而影响细胞形态和渗透压,最终导致细胞溶解死亡。因哺乳类细胞无细胞壁,故这类药物对宿主机体的不良反应明显降低。对念珠菌和曲霉菌具有广谱的抗菌活性,对新生隐球菌、镰刀霉属、毛霉等无活性[8-9]。主要的不良反应包括血细胞减少、溶血性贫血、过敏、休克、肝功能异常或黄疸、肾功能异常,总体不良反应发生率较低,且大多数是轻度和可逆的。有可能与多烯类和偶氮类药物起添加或协同作用。米卡芬净是新型棘白菌素类抗真菌药物,与另一种棘白菌素类抗真菌药物卡泊芬净相比较,治疗IFD具有较好的有效性、安全性和经济性[10],也是重症监护患者及器官移植患者合并IFD的循证医学证据指南推荐药物,欧洲及中国实体器官移植受者IFD临床诊治指南均有提及[11]。米卡芬净其它适应症包括推荐用于儿童IFD抗真菌治疗,同样具有较高的安全性及有效性[12-13]。
米卡芬净独特的抗真菌机制与多烯类、三唑类抗真菌药之间不存在交叉耐药性,以及不良反应轻的特点,对于致命性侵袭性真菌感染, 提供了与其他药物联合治疗的机会。指南也提出,对于单药治疗失败或无法耐受、多部位或耐药真菌感染的高危病例,为扩大抗真菌谱覆盖范围并增强疗效,可采用两种药物进行联合治疗。但由于多烯类的毒副作用较大,联合用药很可能会增加不良反应的发生率,故在临床工作中,多选择棘白菌素类联合三唑类药物的方案。目前有关米卡芬净联合伏立康唑治疗IFD的研究不多,有研究[14]分析了米卡芬净序贯伏立康唑疗法对比单独应用米卡芬净在IFD中的疗效,与米卡芬净单药相比,联合用药更具有疗效优势,且安全性好,不良反应少。同样,也有研究显示米卡芬净联合伏立康唑对儿童恶性血液病化疗后合并IFD具有良好的疗效及安全性[15]。还有一些研究也表明了米卡芬净联合伏立康唑在抗真菌治疗方面的优势,生存率有一定程度的提高[16-18]。本研究结果显示,米卡芬净和伏立康唑联合治疗与伏立康唑单独治疗的治疗中位时间分别为16.5天和22.0天,临床有效率分别为86.7%和63.3%,差异有统计学意义,表明米卡芬净和伏立康唑联合用药在治疗IFD方面较伏立康唑单药有更强的抗真菌作用,缩短了治疗周期。联合用药的不良反应率为16.7%,略小于伏立康唑单药的20%,表明米卡芬净和伏立康唑联合用药或可降低治疗副反应。分析这可能与米卡芬净和伏立康唑联合用药提高了抗感染治疗效果,从而缩短了病程有关,导致不良反应发生率减少。差异不具有统计学意义,可能是样本量偏小所致。在本研究中还观察到一个有意思的现象,两例IFD患者因使用伏立康唑单药时出现不可耐受的不良反应,后续更换为米卡芬净单药继续抗真菌治疗,最终疗效完全缓解出院。有研究[19-20]比较米卡芬净与伏立康唑的疗效和安全性,结果显示两者效果相当,而米卡芬净副作用更轻。米卡芬净肝肾损害小、安全性好,在肝肾功能不全患者使用时不需调整剂量,但米卡芬净联合伏立康唑相关毒副作用及疗效是否最佳仍需临床多中心进一步观察研究。
总之,本研究尚且存在一些局限性,采用回顾性分析方法可能导致选择性偏倚,我们纳入研究范围的样本量较小且均筛选自中国医学科学院肿瘤医院深圳医院,因此研究结果可能无法反映不同地域的流行病学差异。开展多中心、大样本、前瞻性临床研究以及深入挖掘两种治疗方案在不同原发病类型中的疗效与安全方面的表现,及不同种类的真菌菌种甚至真菌寄生的部位会否影响机体对药物的反应等将是我们下一步探索方向。
作者声明:本文全部作者对于研究和撰写的论文出现的不端行为承担相应责任;并承诺论文中涉及的原始图片、数据资料等已按照有关规定保存,可接受核查。
学术不端:本文在初审、返修及出版前均通过中国知网(CNKI)科技期刊学术不端文献检测系统的学术不端检测。
同行评议:经同行专家双盲外审,达到刊发要求。
利益冲突:所有作者均声明不存在利益冲突。
文章版权:本文出版前已与全体作者签署了论文授权书等协议。
