聚焦物质的分类、离子反应考点
2021-10-09马亚楼
■马亚楼
物质的分类及离子反应是高中化学学习的基础,也是考试的热点。重点考查混合物与纯净物的分类、强弱电解质的分类、酸碱盐及氧化物的分类、胶体的性质和丁达尔现象、离子方程式的正误判断、离子共存的判断等知识,与以前所学的混合物、纯净物、酸碱盐、氧化物等概念紧密相连。现将常见的考点进行分类例析。
考点一:物质的分类
考点点击:物质的分类贯穿于化学的始终,主要考查中学阶段常见的物质分类标准(单一分类、树状分类、交叉分类等),其中,纯净物与混合物、单质与化合物、氧化物的分类、酸碱盐的分类为考查的重点,也是该部分内容的难点及易错点。纯净物与混合物的本质区别是含有几种物质,含一种物质的为纯净物,含两种或两种以上物质的为混合物;单质与化合物的区别是物质中含有几种元素,含一种元素的为单质,含两种及以上元素的为化合物;氧化物为由两种元素组成,其中一种元素为氧元素的纯净物。
例1(2021 年江苏小高考题)2018 年中国火箭发射次数世界第一,肼(N2H4)常用作火箭燃料。肼属于( )。
A.单质 B.氢化物
C.有机物 D.氧化物
解析
由一种元素组成的纯净物属于单质,则N2H4不是单质,而是化合物,故A 项错误;由H 元素和其他元素构成的化合物属于氢化物,即N2H4属于氢化物,故B 项正确;N2H4不含C 元素,不是有机物,故C 项错误;含有两种元素,其中一种是氧元素的化合物属于氧化物,N2H4不含有O 元素,不是氧化物,故D 项错误。
答案:B
例2(2021年江苏小高考题)下列属于纯净物的是( )。
A.氢氧化铝胶体
B.汽油
C.液氨
D.深岩层饮用水
解析
纯净物是由一种物质组成的,混合物是由两种或两种以上物质组成的。氢氧化铝胶体属于混合物,故A 项错误;汽油是由C5~C11的烃组成的混合物,故B项错误;液氨是液态氨气,属于纯净物,故C项正确;深岩层饮用水含有水和溶于水的矿物质,属于混合物,故D 项错误。
答案:C
例3(2019年浙江高考题)下列属于碱的是( )。
A.C2H5OH B .N a2CO3
C.Ca(OH)2D .Cu2(OH)2CO3
解析
C2H5OH 属于有机物,故A项错误;Na2CO3是由金属阳离子和酸根阴离子组成的化合物,属于盐,故B 项错误;Ca(OH)2溶于水电离出的阴离子全部是OH-,属于碱,故C 项正确;Cu2(OH)2CO3属于碱式盐,故D 项错误。
答案:C
例4(2021年浙江高考题)下列物质属于纯净物的是( )。
A.汽油 B.食醋
C.漂白粉 D.小苏打
解析
由题给选项的物质可知,汽油、食醋、漂白粉均是混合物,而小苏打是纯净物。
答案:D
评注:本类题目主要考查物质的分类,明确有关概念与含义是解题的关键。此类题给出几种物质,判断是单质还是化合物、是纯净物还是混合物、是电解质还是非电解质等。注意含有不同状态的物质不一定是混合物,如误将混合的冰和水认为是混合物;含有同种状态的物质不一定是纯净物,如将纯净的空气误认为是纯净物等。弄清楚基本概念和物质的组成是解这类题的关键。
考点二:胶体的丁达尔效应
考点点击:胶体的本质特征是胶体的微粒直径介于1~100nm 之间。胶体的性质有布朗运动、丁达尔效应、电泳、胶体的聚沉等,重点考查利用丁达尔效应这种胶体特有的性质来区别胶体与溶液。胶体、溶液、浊液都是把一种(或多种)物质分散在另一种(或多种)物质中所得到的体系,按照分散质粒子的大小可分为溶液、胶体和浊液,溶质粒子(分子或离子)直径小于1nm 的为溶液;分散质离子直径在1~100nm 之间的为胶体;分散质粒子直径大于100nm 的为浊液。胶体和溶液都属于稳定的分散系,而浊液是不稳定的分散系。胶体能产生丁达尔效应、电泳现象,而溶液不能。
例5关于胶体和溶液的区别,下列叙述中正确的是( )。
A.溶液呈电中性,胶体带有电荷
B.溶液中溶质微粒一定不带电,胶体中分散质微粒带有电荷
C.溶液中溶质粒子的运动是有规律的,胶体中分散质微粒的运动是无规律的,即布朗运动
D.溶液中通过一束光线没有特殊现象,胶体中通过一束光线出现明亮的光带
解析
胶体本身不带电,只是其表面积较大,吸附了溶液中的离子而带了电荷,故A 项错;电解质溶液中阳离子带正电,阴离子带负电,所以溶液中的溶质微粒可能带电,B项错;溶液中溶质粒子的运动也是无规律的,C项错;丁达尔效应可以用来区分溶液和胶体,D 项正确。
答案:D
评注:本题主要考查了胶体和溶液性质的比较。此题容易错选B,由于对溶液中溶质理解受非电解质的干扰,实质上溶液中的溶质是非电解质时,溶液不导电,是电解质时,则导电。
考点三:电解质和非电解质
考点点击:电解质(包括酸、碱、盐、水等)和非电解质(包括非金属氧化物、NH3、大多数有机物等)的判断,强电解质和弱电解质(包括弱酸、弱碱、少数盐、水等)的判断。判断化合物所属的类型是高考的热点之一。
例6(2021年浙江高考题)下列物质属于弱电解质的是( )。
A.CO2B.H2O
C.HNO3D.NaOH
解析
CO2属于非电解质,故A 项错误;H2O 属于弱电解质,故B项正确;HNO3在水中完全电离,属于强电解质,故C 项错误;NaOH 在水中完全电离,属于强电解质,故D 项错误。
答案:B
例7(2019年浙江高考题)下列属于强电解质的是( )。
A.硫酸钡 B.食盐水
C.二氧化硅 D.醋酸
解析
硫酸钡虽然溶解度小,但其溶于水后完全电离,属于强电解质,故A 项正确;食盐水属于氯化钠的水溶液,属于混合物而不属于化合物,因此不属于强电解质,故B 项错误;二氧化硅不溶于水,且熔融的二氧化硅不导电,因此二氧化硅不属于电解质,故C 项错误;醋酸属于弱电解质,故D 项错误。
答案:A
评注:解析这类试题时必须对强弱电解质的含义及其外延理解清楚。如强电解质部分是离子化合物,部分是共价化合物,强弱电解质与其易溶还是难溶没有直接关系,溶液的导电性是由溶液中的离子浓度大小及离子所带的电荷所决定的,强电解质的导电性不一定就强于弱电解质的导电性等。
考点四:离子反应发生的条件
考点点击:对于复分解反应,若生成难溶物质、难电离或易挥发的物质中的一种,均可发生;对于氧化还原反应,通常遵循“强制弱”的规律,即强氧化剂可以制取弱氧化剂,强还原剂可以制取弱还原剂;金属活动性顺序表前面的金属单质(K、Ca、Na除外)可以把后面的金属元素从其化合物中置换出来;金属活动顺序表排在氢前面的金属单质可以把酸中的氢元素从其化合物中置换出来。
例8下列变化能够实现的是( )。
①弱酸与盐溶液反应生成强酸
②两种氧化物发生反应有气体生成
③两种酸的溶液充分反应后溶液呈中性
④复分解反应中既没有生成水,也没有生成沉淀和气体
A.①③B.②④
C.①②④ D.①②③④
解析
本题主要考查离子反应发生的条件。弱酸与盐溶液反应符合复分解反应发生的条件可以生成强酸,如氢硫酸与硫酸铜反应生成硫化铜沉淀与硫酸,故①正确;过氧化钠与二氧化碳反应生成氧气,故②正确;氢硫酸与亚硫酸恰好完全反应,所得溶液呈中性,故③正确;复分解反应发生的条件是生成难溶物、难电离物和易挥发性物质,醋酸钠与盐酸反应生成醋酸和氯化钠,既没有生成水,也没有生成沉淀和气体,故④正确。
答案:D
评注:该题主要考查离子反应发生的条件,此题容易漏选④,主要是对复分解反应发生的条件中难电离物质忽略了,所以在运用复分解反应条件时必须在初中所学基础上,加上难电离的物质。
例9在下列实验中能发生离子反应的是( )。
A.NaCl溶液与KOH 溶液混合
B.点燃H2和Cl2的混合气体
C.NaOH 溶液和CuSO4溶液混合
D.大理石与盐酸的反应
解析
A 项中尽管有自由移动的离子,但离子间不反应;B 项中反应物为两种气体,无离子;C 项中OH-与Cu2+反应生成Cu(OH)2沉淀;D 项中CaCO3与H+反应生成CO2气体。
答案:CD
评注:该题主要考查离子反应,判断一个化学反应是不是离子反应,关键看有没有离子参加反应或生成。解题时首先看反应物(或生成物)中有无离子,然后再根据离子反应发生的条件进行判断。
考点五:离子反应的书写与正误判断
考点点击:离子反应的实质是离子的重新组合,可以用离子方程式表示反应的实质。一般情况下会在选择题中考查离子方程式的正误判断,在填空题中考查离子方程式的书写。在书写与判断时要注意两个守恒、物质是否可拆、物质的用量、是否漏掉某种离子等。
离子方程式书写时必须注意:①要遵循反应事实,不能臆造化学反应,如Cu+2H+Cu2++H2↑(错)。②要遵循元素原子守恒及电荷守恒,若是氧化还原反应还要遵循电子守恒。③要遵循拆写原则(反应物和生成物都一样)。④不能违背约简原则,如稀硫酸和氢氧化钡溶液反应:H+++Ba2++OH-BaSO4↓+H2O(错),即不能局部约去H+、OH-、H2O 前面的计量数,正确的书写为2H+++Ba2++2OH-BaSO4↓+2H2O。⑤要注意题中有关量的关系(如过量、足量、少量等),如用氨水吸收少量的SO2:NH3·H2O+SO2+(错),正确的书写为2NH3·H2O+(要注意过量的CO2、SO2、H2S等气体分别与碱溶液或某些盐反应时生成这些气体对应的酸式根离子)。⑥关于酸式盐与量有关的离子反应方程式,一般书写时量不足的物质参加反应的离子的物质的量之比一定要与它的化学式相符合,而足量的物质参加反应的离子的物质的量之比不一定与化学式相符合。如果没有明确的用量,写成恰好完全反应的情况。
例10 (2021 年浙江高考题)不能正确表示下列变化的离子方程式是( )。
C.锌溶于氢氧化钠溶液:Zn+2OH-+2H2O[Zn(OH)4]2-+H2↑
解析
碳酸镁微溶于水,在离子反应中不能拆开书写,正确的离子方程式为MgCO3+2H+Mg2++H2O+CO2↑,故A 项错误。
答案:A
例11 (2020 年江苏高考题)下列指定反应的离子方程式正确的是( )。

解析
HClO 是弱酸,在离子方程式中不能拆成离子形式,故A 项错误;B项的配平错误,正确的离子方程式 为3NO2+H2O2H++2+NO;NaAlO2溶液中通入CO2,CO2过量时产物是NaHCO3,且方程式已配平,故C 项正确;AgNO3溶液中加入过量浓氨水最终生成[Ag(NH3)2]+,离子方程式为Ag++2NH3·H2O[Ag(NH3)2]++2H2O,故D 项错误。
答案:C
评注:该题考查离子方程式的书写,涉及氧化还原反应、复分解反应和多步反应。此题容易出错的是C 项,错在没有看清“过量”二字,因CO2过量,因而最终生成的是,所以在书写离子方程式时特别要注意题目中的“适量”“过量”等。
考点六:离子共存
考点点击:离子共存知识是高考的热点、重点,该部分考查的内容包括离子反应发生的条件、氧化还原反应、物质的电离与水解、溶液酸碱性的计算、电极反应式的正误判断、离子的推断等。解此类题时要注意看清题干中的要求和题目中的隐含条件。此类试题题干中一般会出现“能大量共存”或“不能大量共存”的字样,同时还隐含有无色溶液、酸性溶液、碱性溶液或pH 等,所以解题时必须看清题目的要求,方可正确解答。
例12 (2021 年湖南省新高考题)对下列粒子组在溶液中能否大量共存的判断和分析均正确的是( )。
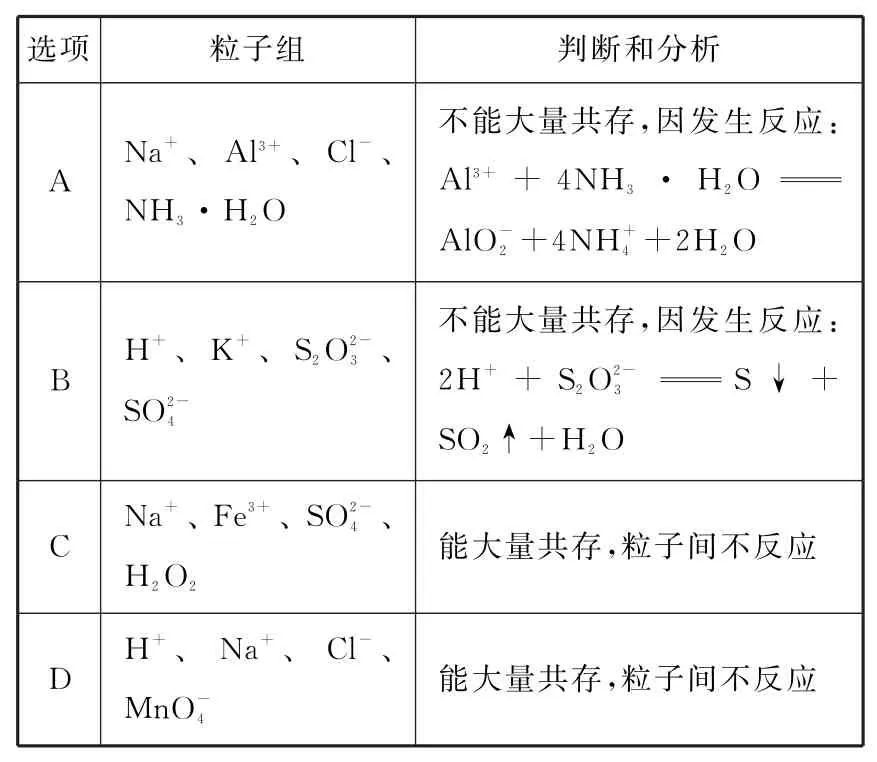
解析
Na+、Al3+、Cl-、NH3·H2O不能大量共存,因为发生反应Al3++3NH3·H2OAl(OH)3↓+,A 项分析错误;不能大量共存,因发生反应SO2↑+H2O,B项判断和分析均正确;Na+、粒子中,Fe3+可以作为H2O2分解的催化剂,C 项判断错误;酸性条件下,具有强氧化性,可以氧化Cl-,D项判断错误。
答案:B
例13 (2020年江苏高考题)常温下,下列各组离子在指定溶液中能大量共存的是( )。


解析
A 选项中氨水与各离子以及各离子之间均不发生反应,能大量共存,故A 项正确;由于H+和可以结合生成H2SiO4沉淀,不能大量共存,故B项错误;MnO2具有氧化性,与I-发生氧化还原反应,不能大量共存,故C 项错误;Ag+与因生成沉淀而不能大量共存,故D 项错误。
答案:A

感悟与提高
1.2017年1月26 日哈佛大学的科学家发布了成功获取金属氢的报告。金属氢属于( )。
A.单质 B.化合物
C.氧化物 D.混合物
2.下列属于酸的是( )。
A.H2SO4B.CO2
C.NaCl D.NaOH
3.下列属于盐的是( )。
A.NaCl B.KOH
C.HNO3D.CO2
4.下列物质的水溶液都能导电,但属于非电解质的是( )。
A.HClO B.Cl2
C.NH4HCO3D.SO2
5.下列说法正确的是( )。
A.强电解质的水溶液中不存在溶质分子,弱电解质的水溶液中存在溶质分子和离子
B.强电解质的水溶液的导电性强于弱电解质的水溶液的导电性
C.强电解质都是离子化合物,弱电解质都是共价化合物
D.强电解质易溶于水,弱电解质难溶于水
6.下列表示对应化学反应的离子方程式正确的是( )。

参考答案:1.A 2.A 3.A 4.D 5.A 6.D 7.A 8.C 9.C
