新辅助化疗联合内分泌治疗乳腺癌的临床研究
2021-09-29石鑫
石 鑫
(山西省中医院乳腺科,山西太原 030012)
乳腺癌是女性常见恶性肿瘤,占全球女性癌症总数的23%[1]。随着人们生活方式、饮食习惯、生活环境等的改变,我国乳腺癌的患病率不断升高,且呈年轻化趋势。乳腺癌是一种化疗敏感性的恶性肿瘤,新辅助化疗主要利用相关抗肿瘤药物来抑制肿瘤细胞代谢的特性,能缩小乳腺癌肿块,并杀灭亚临床病灶,减少远处传播发生的概率,提高乳腺癌的治疗效果,但单独应用此治疗措施对雌激素受体(ER)或(和)孕激素受体(PR)阳性的乳腺癌患者治疗效果不佳[2]。研究显示,雌激素高水平表达和乳腺癌病发率存在相关性,而采用芳香化酶抑制类药物药治疗乳腺癌患者能减少乳腺癌复发率,降低乳腺癌转移风险[3]。阿那曲唑作为第3代芳香化酶抑制药,能使血清雌激素水平降低超过90%,具有显著的辅助抗肿瘤效果[4]。基于此,本研究重点探讨了新辅助化疗联合内分泌治疗乳腺癌的临床疗效,现将研究结果作如下报道。
1 资料与方法
1.1 一般资料 按照随机数字表法将山西省中医院2018年1月至2020年1月收治的80例乳腺癌患者分为对照组和观察组,每组40例。对照组患者年龄32~70 岁,平均(42.69±5.36)岁;TNM 分期[5]:Ⅰ期15例,Ⅱ期13例,Ⅲ期7例,Ⅳ期5例;ER阳性15例,PR阳性20例,ER与PR均阳性5例。观察组患者年龄33~71岁,平均(42.03±5.71)岁;TNM分期:Ⅰ期16例,Ⅱ期12例,Ⅲ期6例,Ⅳ期6例;ER阳性16例,PR阳性18例,ER与PR均阳性6例。两组患者一般资料比较,差异无统计学意义(P>0.05),组间可进行对比。诊断标准:参照《中华妇产科学》[6]中关于乳腺癌的诊断标准。纳入标准:符合上述诊断标准,且行组织病理学检查确诊者;可行化疗者;可测得肿块大小者;无远端转移者;ER和(或)PR受体阳性者。排除标准:接受过相关抗癌治疗者;存在相应药物服用禁忌证者;妊娠、哺乳期患者。本研究在山西省中医院医学伦理委员会审核批准下实施,且患者及家属签署知情同意书。
1.2 方法 对照组患者接受新辅助化疗,给予地塞米松片(三才石岐制药股份有限公司,国药准字H44024276,规格:0.75 mg/片)进行化疗预处理,7.5 mg/次,2次/d,每个化疗疗程的第1~2天口服。采用TE化疗方案(多西他赛+表柔比星):多西他赛注射液(扬子江药业集团有限公司,国药准字H20174009,规格:2 mL∶80 mg)75 mg/m2,于第1天对患者进行静脉滴注;注射用盐酸表柔比星(山东新时代药业有限公司,国药准字H20184161,规格:50 mg)75 mg/m2,于第 1 天对患者进行静脉滴注。21 d为1个疗程,化疗6个疗程。化疗期间需密切监测患者的肝、肾功能、心电图,对症处理不良反应。观察组患者接受新辅助化疗联合内分泌治疗,化疗方案同对照组,内分泌治疗:阿那曲唑片(浙江海正药业股份有限公司,国药准字H20133110,规格:1 mg/片)1 mg/次,1次/d,口服,30 d为1个疗程,治疗3个疗程。
1.3 观察指标 ①比较两组患者治疗结束后近期疗效,其中完全缓解(CR):目标病灶完全消失,且1个月内未出现新病灶;部分缓解(PR):目标病灶缩小≥ 30%,且1个月内未出现新病灶;疾病稳定(SD):目标病灶缩小 <30%或扩大 <20%,且1个月内未出现新病灶。疾病进展(PD):新病灶出现和(或)原病灶扩大≥20%[6]。客观有效率(ORR)=(CR+PR)例数/总例数×100%;疾病控制率(DCR)=(CR+PR+SD)例数/总例数×100%。②比较两组患者治疗前、治疗结束后血清糖类抗原153(CA153)、糖类抗原125(CA125)、人表皮生长因子受体 -2胞外段(HER2-ECD)水平,分别抽取两组患者空腹静脉血5 mL,进行离心操作(3 000 r/min,10 min),取血清,采用电化学发光技术检测血清CA153、CA125、HER2-ECD水平。③观察两组患者不良反应,包括白细胞减少、肝功能异常、心脏毒性、恶心呕吐等。
1.4 统计学分析 采用SPSS 25.0统计软件分析处理数据,血清CA153、CA125、HER2-ECD含量为计量资料,用()表示,行t检验;近期疗效、不良反应发生率为计数资料,用[ 例(%)]表示,行χ2检验。以P<0.05表示差异有统计学意义。
2 结果
2.1 近期疗效 治疗结束后观察组患者ORR较对照组显著升高,差异有统计学意义(P<0.05),两组患者DCR比较,差异无统计学意义(P>0.05),见表1。

表1 两组患者近期疗效比较[ 例(%)]
2.2 血清CA153、CA125、HER2-ECD水平 治疗结束后两组患者血清CA153、CA125、HER2-ECD水平均较治疗前显著下降,且观察组下降幅度较对照组显著增大,差异均有统计学意义(均P<0.05),见表2。
表2 两组患者血清CA153、CA125、HER2-ECD水平比较()
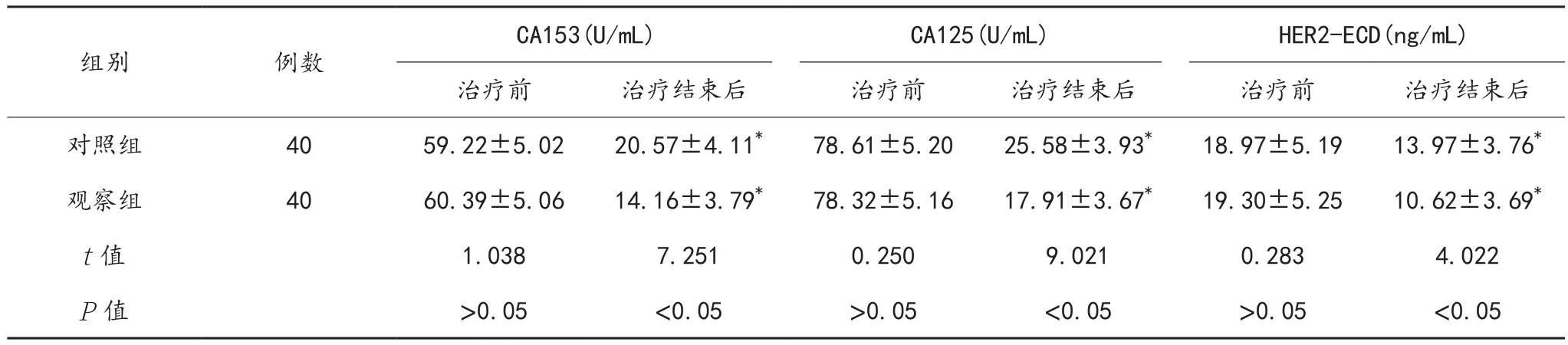
表2 两组患者血清CA153、CA125、HER2-ECD水平比较()
注:与治疗前比,*P<0.05。CA153:糖类抗原153;CA125:糖类抗原125;HER2-ECD:人表皮生长因子受体-2胞外段。
CA153(U/mL) CA125(U/mL) HER2-ECD(ng/mL)治疗前 治疗结束后 治疗前 治疗结束后 治疗前 治疗结束后对照组 40 59.22±5.02 20.57±4.11* 78.61±5.20 25.58±3.93* 18.97±5.19 13.97±3.76*观察组 40 60.39±5.06 14.16±3.79* 78.32±5.16 17.91±3.67* 19.30±5.25 10.62±3.69*t值 1.038 7.251 0.250 9.021 0.283 4.022 P值 >0.05 <0.05 >0.05 <0.05 >0.05 <0.05组别 例数
2.3 不良反应 两组患者白细胞减少、肝功能异常、心脏毒性、恶心呕吐发生率比较,差异均无统计学意义(均P>0.05),见表 3。

表3 两组患者不良反应发生率比较[ 例(%)]
3 讨论
2017年中国肿瘤登记年报显示,乳腺癌占我国大城市肿瘤致死率的12.78%,及时诊治是改善患者预后的关键[7]。TE方案是常用的新辅助化疗方案,能够抑制肿瘤细胞增殖,缩小肿块,并杀灭经血转移的亚临床病灶,减少肿瘤细胞播散,但部分患者采用该治疗方案治疗耐受性较差,对于改善患者生存质量、延长患者生存期的作用不理想[8]。
乳腺癌是一种激素依赖性肿瘤,其发生、发展受体内多种激素的影响。经CYP1B1催化生成的雌二醇(E2)是细胞发生癌变的主要原因,女性绝经前,E2主要来自卵巢,而绝经后则由雄激素通过芳香化酶的催化转化而成。阿那曲唑是内分泌治疗的常用药物,能够抑制体内E2合成,调节体内激素水平,起到抗肿瘤的作用[9]。本研究结果显示,治疗结束后观察组患者ORR较对照组显著升高,原因应为新辅助化疗联合内分泌治疗可发挥协同增效的作用,从而控制病情进展。
CA153是乳腺癌上皮细胞表面的糖蛋白变异体,细胞癌变时会导致CA153释放入血,使血清CA153水平升高。CA125是上皮性卵巢癌的标记物,在乳腺癌中呈高表达,常联合CA153检测诊断乳腺癌。HER2-ECD是新发现的一种血清标志物,相关研究显示,乳腺癌治疗中,血清HER2-ECD阴性患者的ORR(94.7%)高于HER2-ECD阳性患者(60.0%)[10]。新辅助化疗联合内分泌治疗能降低肿瘤负荷,可使肿瘤降期,消除肿瘤微小病灶,抑制肿瘤转移,减少CA153、CA125、HER2-ECD释放入血,从而降低血清肿瘤标志物水平,对乳腺癌的临床治疗效果突出[11]。本研究结果显示,治疗结束后,观察组患者血清CA153、CA125、HER2-ECD水平下降幅度显著大于对照组;两组患者白细胞减少、肝功能异常、心脏毒性、恶心呕吐发生率比较,差异均无统计学意义。提示新辅助化疗联合内分泌治疗可通过降低血清肿瘤标志物水平,提高乳腺癌患者的临床疗效,改善患者生活质量,且联合内分泌治疗未显著增加患者不良反应,安全性较好。
综上,新辅助化疗联合内分泌治疗乳腺癌能提高化疗效果,降低血清CA153、CA125、HER2-ECD水平,且安全性良好,值得推广。但本研究样本量较少,需扩大样本量进一步深入研究。
