粪菌移植治疗克罗恩病的Meta分析
2021-09-26吴凯妮刘少松周晓东
吴凯妮,张 蔓,刘少松,钟 嫦,周晓东
(南昌大学第一附属医院消化内科,南昌 330006)
克罗恩病(CD)是由多种病因引起的,遗传和环境相互作用的慢性复发性炎症性疾病。随着对儿童和成人克罗恩病的深入研究,人们发现该病的发病率逐年上升[1-2],社会成本负担加重[3]。尽管克罗恩病的发病机制尚未完全确定,但有研究[4-5]发现肠道菌群紊乱起着至关重要的作用。目前免疫抑制治疗仍然是克罗恩病常规治疗的主要手段[6],但不难发现免疫疗法并不完全有效。部分患者常常由于不良反应,如过敏和不耐受药物,从而导致停药和病情恶化[7]。
粪菌移植是将健康人粪便中的功能性细菌转移到患者的胃肠道,重建新的肠道菌群并实现肠外疾病的治疗。目前,粪菌移植在国内外引起了越来越多的关注。近年来,一些研究已经阐明了粪菌移植治疗艰难梭状芽胞杆菌感染(CDI)[8-15]和溃疡性结肠炎(UC)[16-19]的功效,带动了研究其他肠道菌群相关疾病的治疗,如克罗恩病。因此,本文通过对前瞻性队列研究的证据进行Meta分析,以评估粪菌移植治疗克罗恩病的有效性和安全性。
1 方法
1.1 检索策略
首先仔细阅读用于系统回顾和荟萃分析(PRISMA)[20]声明的首选报告项目。检索2020年5月20日之前收录于Pubmed、Embase、Cochrane图书馆、万方、维普和知网数据库的文献。初步筛选的英文关键词为inflammatory bowel disease、IBD、crohn disease、CD和fecal、faecal、stool、microbiota、microbiome、transPlant、transPlantation、transfusion、bacteriotheraP、FMT。中文关键词为粪菌移植、粪便微生物群移植、粪便移植、肠微生态移植、肠菌移植和粪菌治疗。试验对象限定为人类,但没有语言或地域的限制。该策略不仅适用于医学主题词、自由词检索,而且可以组合使用。两名调查人员分别审查了所有合格文献的标题和摘要。
1.2 资料选择
纳入符合条件的前瞻性研究,包括旨在缓解儿童或成人克罗恩病患者的随机对照研究(RCT)和队列研究。排除没有明显缓解或临床终点不合格的研究。同时,排除病例报告、病例系列、合并感染和少于5名参与者的研究。
1.3 质量评价
采用纽卡斯尔-渥太华量表(NOS)[21]评估前瞻性单臂研究的方法学质量。两名研究人员根据暴露组的代表性、暴露组的可比性等对每个报告进行分级。在每个主要类别中评估偏倚风险。高风险偏差得1分,低风险偏差不得分,最高分是8分。
1.4 统计学方法
使用ComPrehensive Meta-Analysis software V.2.0软件进行统计分析。Meta分析仅包括前瞻性队列研究,最终效应指标是合并临床缓解率和临床反应率。因此,使用随机效应模型计算效应指标的总值及其95%置信区间(CIs)。Cochran’s Q用于讨论异质性。当P<0.1时,存在异质性。同时,采用Higgins检验(I2)进行异质性分析。当I2<25%、介于25%~75%和>75%时,异质性分别为低、中、高[22]。
亚组分析包括患者类型[儿童vs成人]、实验国家[中国vs美国]、给药途径[上消化道vs下消化道]、粪便制备[新鲜vs冷冻]、预防性使用抗生素[是vs否]和肠道灌洗[是vs否]。敏感性分析评估数据稳定性并使用Egger’s回归检验评估发表偏倚。
2 结果
2.1 文献检索的结果
共检索到1327篇文献。过滤标题和摘要之后,筛选到33篇文献。然后通过全文回顾剔除25篇原始文章,最终纳入的文献只包括7个队列研究和1个试点随机对照研究(图1)。
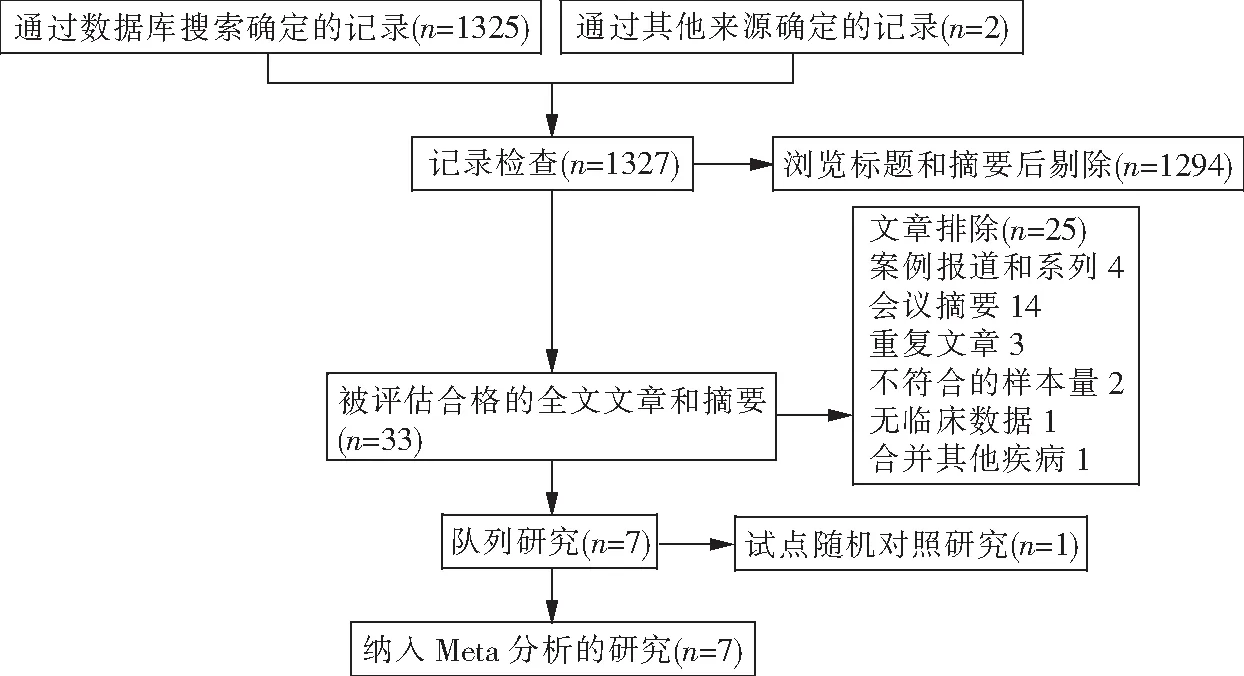
图1 研究流程图
2.2 纳入研究的结果和基本特征
7个队列研究[23-29]都是单臂前瞻性研究。在这7个样本量>5的研究中,共有217例克罗恩病患者。纳入的1项试验性随机对照研究[30]中,8例接受粪菌移植的患者作为试验组,9例未接受粪菌移植的患者作为对照组。
这些研究于2015—2020年分别在美国、中国、比利时和法国进行。两项研究调查了16名儿童患者,五项研究调查了79名成人患者,一项研究调查了139名儿童和成人患者。不同研究中,粪菌移植的路径也不同,包括鼻十二指肠管、结肠镜和胃镜检查。参与者在2次试验中得到冷冻粪便,在5次试验中得到新鲜粪便,在1次试验中得到冷冻和新鲜粪便。总结这些研究的特点见表1。
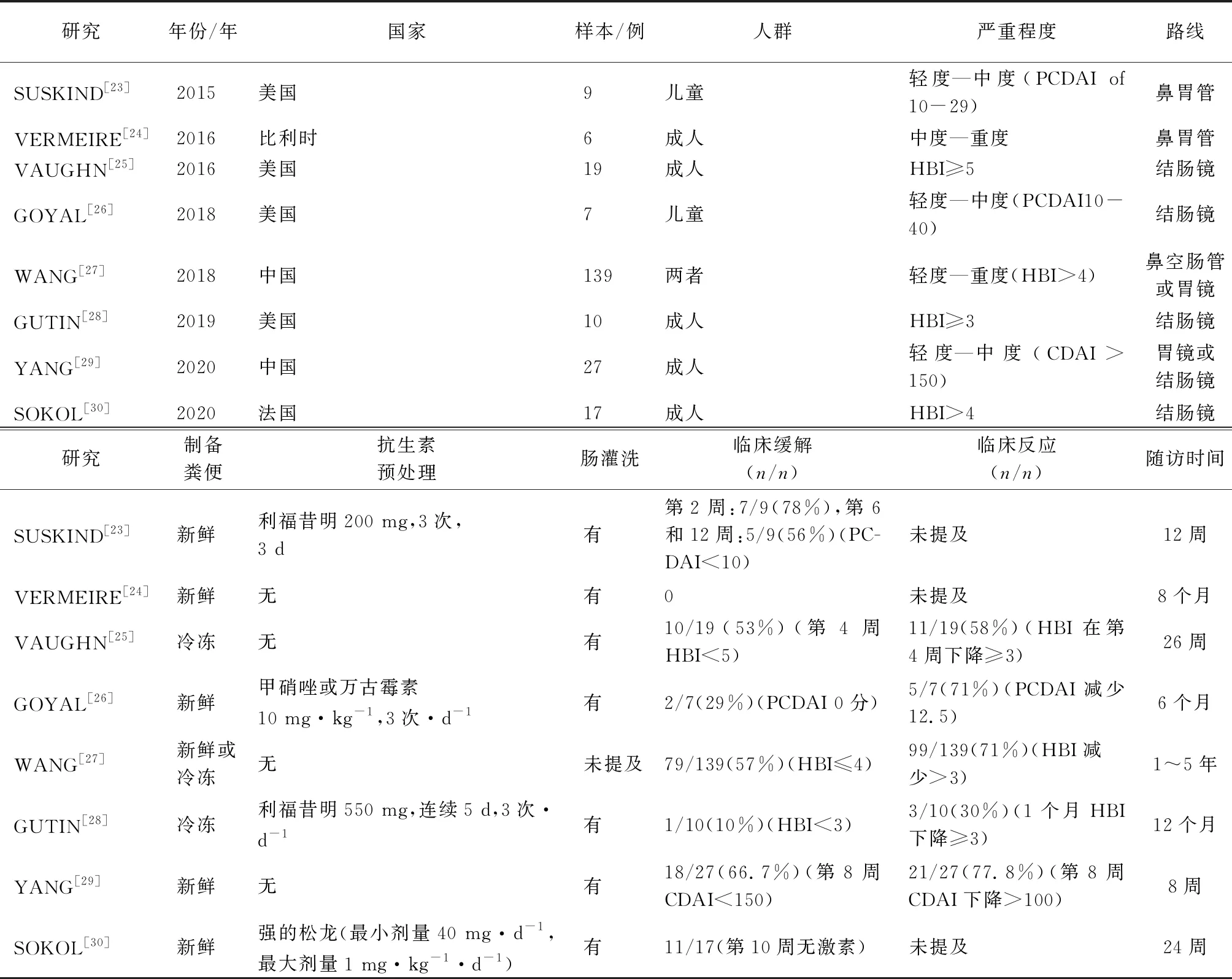
表1 纳入研究的特点
2.3 文献质量
采用标准NOS项目对纳入队列研究的质量进行评估(表2)。根据该表,4个研究被认为是6分,3个研究被认为是5分。可以发现,所有文献都表现出良好的质量。然而,每个试验都缺少对照组,因而与队列的可比性这一项都缺失。
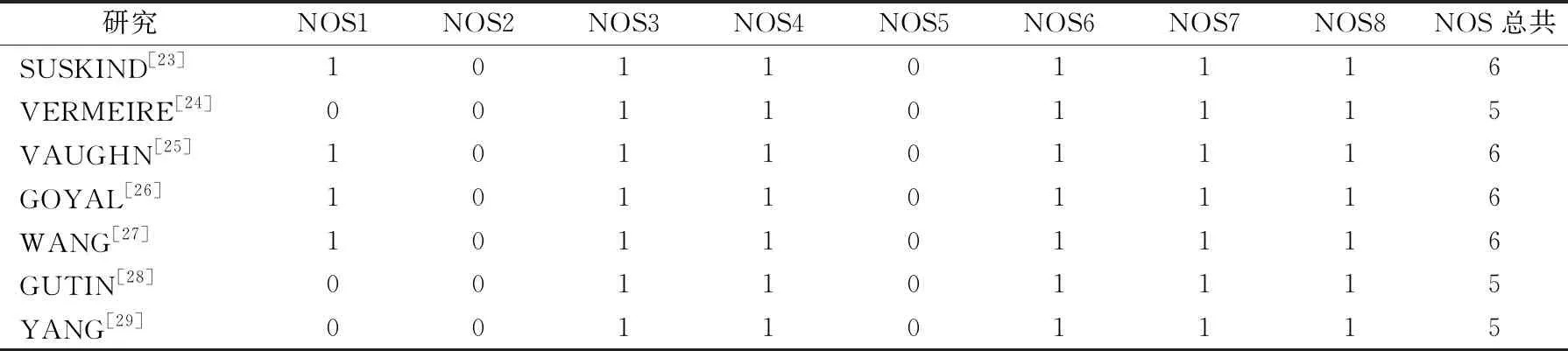
表2 纳入队列研究的偏倚评估风险 分
2.4 治疗的有效性
8项不同研究中,临床缓解及临床反应有着不同的定义,但相似的是采用了Harvey-Bradshaw指数评分(HBI)和成人或儿童克罗恩病活动度指数评分(CDAI或PCDAI)来进行定义(表1)。总的来说,54.7%(128/234)的克罗恩病患者获得临床缓解,68.8%(139/202)的患者获得临床反应。7个队列研究显示,217例患者中,50.3%(95%CI,35.4%~65.6%)的患者获得临床缓解(图2),异质性中等(P=0.031,I2=56.718%)(表3),不存在发表偏倚(表4)。获得临床反应的患者202例,综合比例为71.7%(95%CI,57.2%~82.7%)(图3),异质性中等(P=0.197,I2=33.723%)(表3),未发现发表偏倚(表4)。
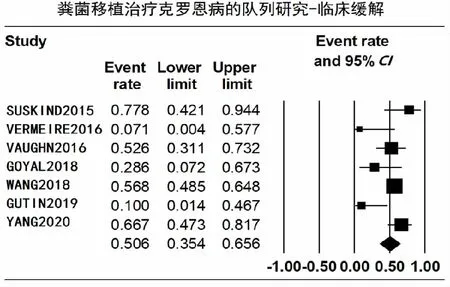
采用随机效应模型计算95%置信区间(CI)的合并比例。
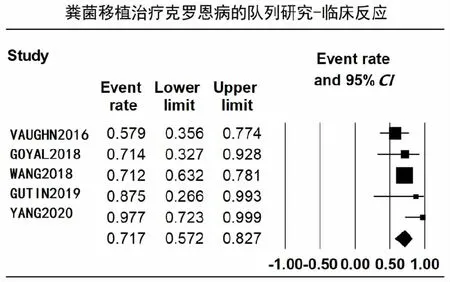
采用随机效应模型计算95%置信区间(CI)的合并比例。

表3 纳入队列研究的Meta分析总结

表4 纳入队列研究的Meta分析发表偏倚
2.5 亚组分析
1)试验国(美国vs中国):两国的合并临床缓解率在亚组分析中显示出差异。美国为42.9%(95%CI,18.4%~71.5%;P=0.047;I2=62.296%)。中国为58.4%(95%CI,50.7%~65.6%;P=0.345;I2=0%)。见表5。
2)群体年龄(儿童vs成人):亚组分析显示获得临床缓解的儿童患者合并比例54.5%(95%CI,12.5%~90.9%;P=0.061;I2=71.458%),成人患者38.4%(95%CI,15.2%~68.4%;P=0.017;I2=70.448%)。见表5。
3)药物途径(上消化道vs下消化道):不同的给药途径显现出不同的临床效果。上消化道粪便输注合并临床缓解率为38.7%(95%CI,1.5%~96.3%);P=0.022;I2=80.812%,而下消化道输注粪便率为32.2%(95%CI,1.16%~63.2%);P=0.106;I2=55.529%)。见表5。
4)制备粪便(新鲜vs冷冻):输注新鲜粪便的临床缓解率为50.0%(95%CI,21.8%~78.2%);P=0.045;I2=75.061%,而冷冻粪便输注率为29.9%(95%CI,4.4%~79.8%);P=0.042;I2=63.416%)。见表5。
5)抗生素预处理(否vs是):亚组分析中,试验前是否进行抗生素预处理也有不同的结果。使用抗生素预处理的综合临床缓解率估计为36.8%(95%CI,7.6%~80.5%;Cochran’s Q,P=0.023;I2=73.422%,未进行抗生素预处理为56.4%(95%CI,4.37%~80.5%);Cochran’s Q,P=0.177;I2=39.107%)。见表5。
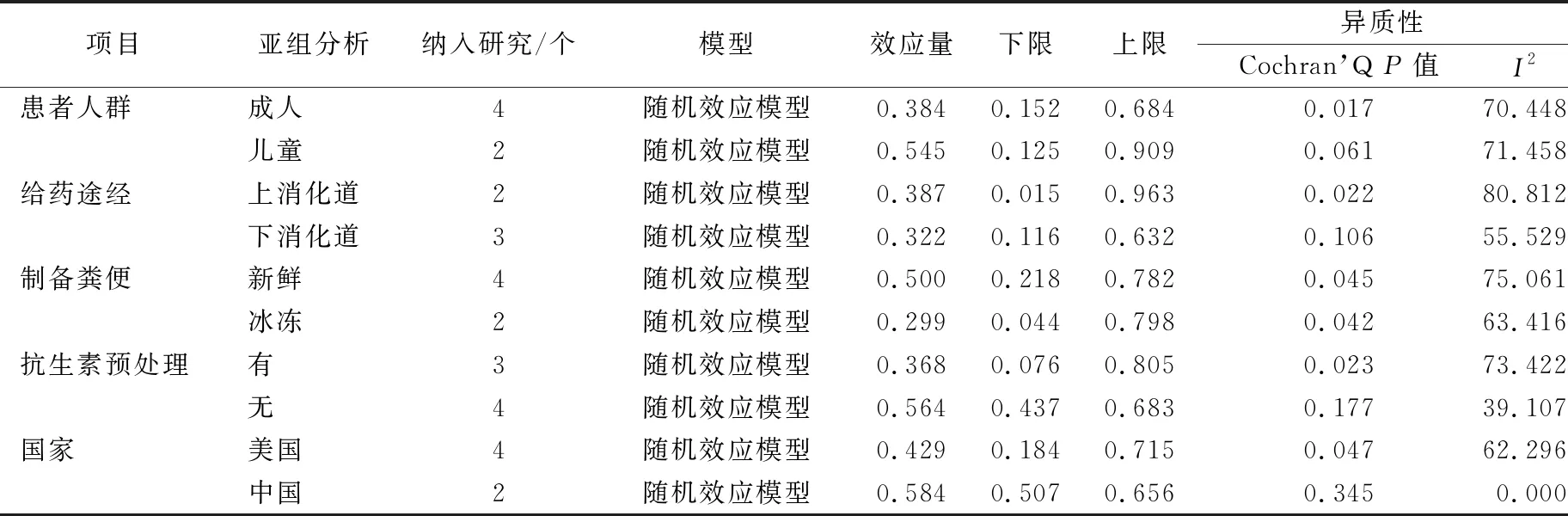
表5 临床缓解的亚组分析
6)不良事件:所有的研究均报道了不良事件,这些研究发现粪菌移植具有良好的整体耐受性。4项研究[23,25,28,30]报道了胃肠道不适,如腹痛、腹胀、腹泻,而这些不良反应大部分在短时间内可得到改善。3项研究[24,26,28]显示,在粪菌移植后会出现发热,这可能与细菌的暂时移位有关。2项研究[28,30]中的11例患者粪菌移植后出现克罗恩病恶化的严重不良反应,有2例患者因此退出了试验。总的来说,不良反应是自限性和预后良好的。
3 讨论
本文包括一系列完整的前瞻性非对照研究和1篇RCT,是关于粪菌移植治疗克罗恩病安全性和有效性的独立Meta分析,显示出良好的创新性。然而,由于缺乏完整的RCT,本文没有有关RCT的Meta分析,导致研究质量水平不高。此外,样本量不足和研究设计差距较大等也可能导致结果发生显著变化。
评价克罗恩病患者使用粪菌移植治疗后的疗效,可以发现54.7%(128/234)的克罗恩病患者达到临床缓解。由于许多原始研究[31-32]同时涵盖溃疡性结肠炎和克罗恩病,这导致了Meta分析中克罗恩病的样本量较小,偏倚较大。PARAMSOTHY等[33]发表了一篇评价溃疡性结肠炎和克罗恩病研究的综述,发现6项克罗恩病研究的综合临床缓解率为52%(95%CI,31%~72%),有着中等风险的异质性(P=0.063,I2=52%)。因此,本研究排除了样本量<5的文献,结果显示临床缓解患者人数过半,异质性显示中等风险,效果良好,结果较为理想。本研究治疗克罗恩病的临床缓解综合比例(50.3%)略低于以前同时报道溃疡性结肠炎和克罗恩病的Meta分析[(P=60.5%,95%CI:28.4%~85.6%)[32](P=52%,95%CI:31%~72%)[34]]。这可能是由于数据的局限性和研究方法的差异造成的。目前样本量仍然不足,但显著大于之前的荟萃分析。这与之前的研究[31-32]存在发表偏倚的事实是一致的,而本研究没有检测到发表偏倚。
亚组分析显示中国地区临床试验的综合缓解率(58.4%)高于美国(42.9%)。虽然美国参与了更多的试验,但中国有更大的样本量,这可能是产生这些结果的最大原因。从已经有试验经验的地区招募更多的患者,并且积极鼓励还未进行此研究的国家,可能会减少不同地区的偏见。不同年龄的患者对粪菌移植的反应似乎也不同。儿童临床缓解的比例明显高于成年人。目前研究[35]表明,虽然人类肠道微生态是动态发展的,但成人肠道微生态相对稳定。而儿童肠道微生物群则处于不断适应和发展的过程中,这可能是儿童对粪菌移植治疗反应较好的一个原因。令人担忧的是,粪便捐赠者大多是成年人,而且儿童的肠道系统更加脆弱。肠道微生物移植可能对儿童的免疫系统和其他非免疫系统产生重大影响,甚至可能产生不良后果。
鼻胃管、胃镜等均为上消化道输注方法,结肠镜是下消化道输注的方法。上消化道给药的比例高于下消化道给药。然而,在FANG等[36]的分析中,结肠镜输注的比例更高。粪菌移植粪便灌注方式对克罗恩病患者的治疗至关重要,现有文献中的试验设计差异较大,导致结果存在偏差。本研究发现,4项研究注入新鲜粪便,2项注入冷冻粪便,但不同的粪便制备方法对临床缓解结果没有显著影响。不同粪便储存方式可能会引起肠道菌群的活性和组成发生变化,但这种变化的具体机制尚不清楚。为了更准确地比较两者,有必要设计规范的粪便处理程序和完善的粪便处理设施。在粪菌移植前使用抗生素是否有利于患者的临床缓解,目前仍是一个有争议的话题。本研究发现是否抗生素预处理没有显著差异。IANIRO等[37]认为,抗生素是治疗某些疾病的可靠手段,可以增加有益菌群的数量,对肠道菌群紊乱有积极作用,而且一次就能使人体实现共生。尽管如此,BECATTINI等[38]认为,抗生素通过改变肠道微生物群的成员和功能,对肠道微生态产生了有害影响。这需要进一步的研究和更多的试验验证。
对大多数患者来说,粪菌移植治疗克罗恩病是安全且可接受的。最常见的不良反应是胃肠道不适,这是自限性的或服用药物可迅速缓解。移植后出现胃肠道反应可能与肠道微生态的突然变化有关。部分患者出现发热,这可能与细菌移位相关。大多数研究只报道了短期随访结果,但粪菌移植的长期安全性需要更长的随访观察。因此,建议延长随访时间,选择依从性合适的患者。
4 结论
粪菌移植是治疗克罗恩病一种有效而安全的方法,有望成为克罗恩病的补充治疗和抢救治疗。然而,目前发表的研究质量参差不齐,长期安全性的随访结果尚不清楚。未来需要更多标准粪菌移植工艺用于缓解克罗恩病的对照研究和随机对照试验。
