6F血管鞘在细径静脉的自体标准动静脉内瘘术中的应用研究▲
2021-09-24曾莹晖吴潮清韦俏宇彭小梅
曾莹晖 吴潮清 唐 盛 韦俏宇 姚 璐 彭小梅
(广西壮族自治区人民医院肾内科,广西南宁市 530021)
血透通路是尿毒症患者的生命线。长期血液透析的血管通路有自体动静脉内瘘 (arteriovenous fistula,AVF)、移植物内瘘和带隧道的双腔中心静脉留置导管。自体AVF通畅率最好,栓塞和感染等并发症发生率最低,需要干预及维护的成本最低,因此它是目前建立长期血管通路的首选。《中国血液透析用血管通路专家共识(第2版)》指出,目前尚无绝对理想的血管通路类型,专家组认为长期性血管通路应首选AVF[1]。临床上很多患者自身血管条件差,血管细、分支多,或有局部狭窄,致使AVF建立困难或手术成功率降低。因此,在AVF术中如何通过改进手术技巧来提高手术的成功率、AVF的通畅率及内瘘自然血流量,促进内瘘成熟,是肾内科医师需要考虑的问题。本研究选择细径静脉患者,在自体标准AVF术中采用6F血管鞘直接机械扩张及间接液压扩张头静脉,并与术中不使用6F血管鞘的常规手术方法进行对比,探讨6F血管鞘在细径静脉的自体标准AVF术中的应用价值。
1 资料和方法
1.1 临床资料 选取2019年3月至2020年3月在我院肾内科行自体标准AVF术的慢性肾衰竭细径静脉患者共100例,随机分为血管鞘手术组50例及常规手术组50例。手术由固定的两位有5年以上AVF术经验的医生完成,血管鞘手术组既往糖尿病史16例,术前头静脉内径(1.76±0.16)mm,术前桡动脉内径(1.85±0.47)mm;常规手术组既往糖尿病史15例,术前头静脉内径(1.72±0.16)mm,术前桡动脉内径(1.85±0.26)mm。两组患者的一般资料比较,差异无统计学意义(均P>0.05),具有可比性。
1.2 纳入与排除标准 纳入标准:(1)年龄≥14岁;(2)诊断为慢性肾衰竭,根据慢性肾脏病流行病合作组公式估算肾小球滤过率<20 mL/(min·1.73 m2),选择血液透析作为长期肾脏替代治疗方式;(3)未在术肢做过自体AVF或人造血管内瘘;(4)术前评估Allen试验阳性;(5)术前彩色多普勒超声评估桡动脉内径1.5~2.5 mm,自然状态下(非束臂状态下)头静脉内径1.5~2.0 mm,延续性良好,血流通畅;(6)签署书面知情同意书。排除标准:(1)严重心脑血管疾病急性期;(2)术肢局部皮肤感染;(3)严重心功能不全;(4)恶性肿瘤;(5)术肢严重的血管钙化;(6)严重的高血糖或难以控制的高血压;(7)中心静脉(术侧锁骨下静脉或无名静脉或上腔静脉)狭窄或闭塞;(8)严重低蛋白血症;(9)预期生存时间<6个月。
1.3 方法
1.3.1 术前准备 (1)术前常规查血常规、肝功能、肾功能、电解质、血糖、血脂、凝血功能、甲状旁腺激素、术前五项、心电图、胸片、心脏彩超等;(2)Allen试验评估桡动脉及尺动脉供血情况;(3)彩色多普勒超声检查评估术肢桡动脉、尺动脉供血情况及前臂头静脉向近心端回流是否通畅,测量自然状态下(非束臂状态)头静脉、桡动脉内径,并标记头静脉走行及分支;(4)术前控制收缩压在120~160 mmHg;(5)已进入透析的患者术前充分透析达到干体重。
1.3.2 手术过程
1.3.2.1 常规手术组 自体标准AVF手术方法:(1)患者取仰卧位,术侧上肢外展外旋,常规消毒、铺巾,1%利多卡因局部浸润麻醉,在桡动脉与头静脉之间做一3~4 cm的纵向切口。(2)钝性分离皮下组织,在浅筋膜里寻找并游离出一小段头静脉,从静脉下方穿过一条血管牵引条适度提拉头静脉,向静脉近端和远端分别游离至长度2~4 cm,结扎静脉属支。(3)在肱桡肌腱及桡侧腕屈肌腱之间触及桡动脉搏动,分离浅筋膜,暴露并剪开深筋膜,显露桡动脉,然后剪开血管鞘,游离一小段桡动脉(约1.5 cm),并从后方穿过一条血管牵引条,提拉牵引条,小心分离与之伴行的桡静脉,结扎桡动脉两侧小分支(必要时离断)。(4)尽量靠远端结扎头静脉,靠近结扎线近端离断头静脉,由离断处向头静脉管腔注射稀肝素盐水(肝素500 U+生理盐水100 mL配制),驱血并感受注射阻力以判断血管通畅情况,退出针头后立即用血管夹阻断头静脉近心端,修剪静脉断端开口成斜形,长约1 cm。(5)在桡动脉游离段的近端和远端各用一血管夹阻断血流,用手术刀尖以反挑方式切开桡动脉前壁,用Potts剪刀从破口探入血管腔内,纵向剪开桡动脉前壁约1 cm,用稀肝素盐水冲洗血管腔。(6)使用7-0双针无创伤血管缝合线(聚丙烯缝线)以连续缝合的方法行头静脉及桡动脉血管端侧吻合,缝合的针距约1 mm,缝合的边距约0.5 mm。(7)先松开静脉血管夹,再松开桡动脉远心端血管夹,观察吻合口出血情况,若无喷射状出血,松开桡动脉近心端血管夹(若针距间有喷射状出血,则在出血处缝合修补),观察AVF血流情况。如果AVF吻合口血流通畅,用手可以触摸到血管震颤。(8)再次检查确认手术范围无活动性出血后,缝合皮下组织和皮肤。
1.3.2.2 血管鞘手术组 自体标准AVF手术方法:除上述步骤(4)外,其余手术步骤同常规手术组。步骤(4)手术不同点:打开一次性6F血管鞘鞘包(北京天地和协科技有限公司,MMQG 06160),稀肝素盐水(肝素500 U+生理盐水100 mL配制)冲洗鞘芯、外鞘管,生理盐水纱布湿润导丝后把导丝送入头静脉,先后缓慢、轻柔地送入血管鞘鞘芯及外鞘管,在头静脉内留置10~15 s,直接机械扩张头静脉(为避免损伤头静脉,若放入外鞘有阻力,则只放入内芯),注意导丝末端要始终保持露出鞘芯尾部,然后拔掉导丝及鞘芯,助手按压鞘管近心端头静脉阻断血流,通过外鞘管快速注入稀肝素盐水冲洗并间接液压扩张头静脉管腔,然后缓慢向远心端退外鞘管,边退边继续快速注入稀肝素盐水冲洗及间接液压扩张头静脉管腔,外鞘管完全退出后立即用血管夹阻断头静脉近心端,修剪静脉断端开口成斜形,长约1 cm。
1.4 观察指标 (1)记录两组患者术后当天、3个月、6个月、12个月内瘘通畅情况;(2)分别于术后第2天、1个月、2个月、3个月行彩色多普勒超声检查,测量头静脉流出道内径(距离吻合口1 cm测量),记录术后1个月、2个月、3个月的内瘘自然血流量,并参照文献[1]标准判断内瘘是否成熟;(3)随访12个月,统计内瘘相关并发症(狭窄、闭塞)发生情况。

2 结 果
2.1 术后内瘘通畅率比较 术后当天、3个月、6个月、12个月,两组患者的内瘘通畅率差异无统计学意义(均P>0.05)。见表1。

表1 两组患者术后内瘘通畅率比较 [n(%)]
2.2 术后头静脉流出道内径比较 术后第2天、1个月、2个月、3个月时,血管鞘手术组患者的头静脉流出道内径大于常规手术组,差异有统计学意义(均P<0.05)。见表2。

表2 两组患者术后头静脉流出道内径比较 (,mm)
2.3 术后内瘘自然血流量比较 术后1个月、2个月、3个月,血管鞘手术组患者内瘘自然血流量大于常规手术组,差异有统计学意义(均P<0.05)。见表3。

表3 两组患者术后内瘘自然血流量比较 (,mL/min)
2.4 术后内瘘成熟率比较 术后1个月,两组患者的内瘘成熟率差异无统计学意义(P>0.05);术后2个月、3个月,血管鞘手术组的内瘘成熟率高于常规手术组,差异有统计学意义(均P<0.05)。见表4。

表4 两组患者术后内瘘成熟率比较 [n(%)]
2.5 术后12个月内瘘相关并发症情况比较 术后12个月,两组患者的内瘘相关总并发症发生率比较,差异有统计学意义(P<0.05)。见表5。
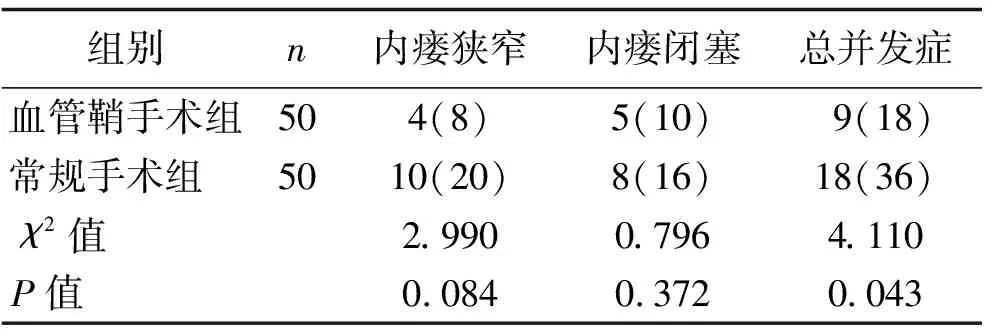
表5 两组患者术后12个月内瘘相关并发症情况比较 [n(%)]
3 讨 论
血透通路是尿毒症患者的生命线,而自体标准AVF即前臂腕部桡动脉-头静脉动静脉内瘘一直是建立长期血透通路的首选术式,也是目前临床上最常见的AVF[2]。由于慢性肾衰竭患者中有许多高龄或合并糖尿病、高血压和周围血管病变的患者,这些患者血管条件差,多表现为血管细、分支多,甚至有局限性的狭窄,可能导致自体标准AVF建立困难或者AVF失功,因而只能建立高位内瘘或移植物内瘘,甚至不得不行中心静脉留置导管[3-4]。因此,在AVF术中如何通过改进手术技巧来扩大静脉直径,提高手术的成功率、AVF的通畅率和成熟率,是肾内科医师需要考虑的问题。
很多学者通过各种尝试以扩大静脉直径,徐大宇等[5]通过向6F导尿管尖端球囊注入生理盐水的方式扩张小口径头静脉(直径小于2.5 mm),陈健等[6]在小口径头静脉(直径1.5~2.5 mm)的AVF成形术中应用F5输尿管导管辅助液压扩张头静脉,两者均能够促进内瘘成熟,提高内瘘短中期通畅率。唐卫刚等[7]予中心静脉导管分段液压扩张头静脉后再行功能性端侧吻合,提高了AVF首次手术成功率和远期通畅率,但未测量内瘘血流量,也未评估内瘘成熟情况。
近几年,血管鞘在外周血管通路介入操作中应用广泛。常用的鞘管大小为5~7F(1F=0.33 mm),其中6F血管鞘的内径约2.0 mm,与自体标准AVF术需要的静脉内径相当。但目前关于6F血管鞘应用于AVF术的研究报道极少,刘乃全等[8]在AVF手术中应用血管鞘技术,可以显著提高患者术后内瘘血流量、内瘘通畅率和透析时的血流量,但纳入研究的患者头静脉直径约3 mm,不是细径静脉,也未对术后并发症进行统计。本研究探讨自体标准AVF术中采用6F血管鞘直接机械扩张及间接液压扩张细径头静脉后,患者术后的内瘘自然血流量、通畅率、成熟率及术后并发症情况。《中国血液透析用血管通路专家共识(第2版)》[1]建议自体AVF成形术的最小动脉内径应≥1.5 mm、静脉内径≥2 mm(束臂后)。Silva等[9]认为满意的静脉流出道所需的标准是AVF的静脉管腔直径≥2.5 mm。一项荟萃分析[10]数据显示,吻合静脉直径小于2.5 mm是影响内瘘成熟的独立危险因素,可导致内瘘成熟率下降、早期失功率明显上升。余文洪等[11]结合临床经验认为,行AVF的静脉全程通畅、弹性好,动脉搏动有力,动静脉直径>1.5 mm是可行的。基于上述文献基础,本研究拟纳入前臂细径头静脉(1.5~2.5 mm)患者作为研究对象,但是我们在实际临床工作中却发现前臂头静脉内径大于2.0 mm的患者较少,绝大部分患者前臂头静脉内径小于2.0 mm,因此把头静脉内径入组条件调整为1.5~2.0 mm。
本研究结果显示,术后当天、3个月、6个月、12个月,两组患者的内瘘通畅率差异无统计学意义(均P>0.05),这可能与观察时间不够长、样本量小有关,需要扩大样本量和更长时间的随机对照研究。另外,与常规手术组相比,血管鞘手术组术后1个月、2个月、3个月的头静脉流出道内径及内瘘自然血流量均较大,术后2个月、3个月的内瘘成熟率也较高,术后12个月发生内瘘相关总并发症较少(均P<0.05)。这说明血管鞘手术组的内瘘更能满足有效透析的需要,内瘘成熟率高、并发症发生率低。因此在AVF术中使用6F血管鞘,能充分利用患者有限而宝贵的血管资源,使细径血管的使用达到极限,可使患者获益更多。
AVF术中使用6F血管鞘的优势:(1)价格较便宜(约150元);(2)6F血管鞘的内径约2.0 mm,对于细小静脉可轻松送入;(3)6F血管鞘比较光滑,送入过程中对静脉内膜损伤小;(4)6F血管鞘扩张血管技术难度不大,操作简单、安全,容易掌握;(5)通过直接机械扩张和间接液压扩张可解除轻度血管狭窄(如静脉穿刺或留置套管针导致的静脉狭窄),还可使静脉内径适度扩大,更方便术者缝合,降低了手术难度,提高了手术成功的可能性;(6)充分利用了前臂的血管资源,尤其是使细径血管的使用达到了极限,明显降低了中心静脉血透导管的使用率。我院血液净化中心2018年中心静脉导管的使用比例为18.6%,从2018年底开始在AVF手术时充分利用细径血管及使用6F血管鞘后,2019年中心静脉导管使用比例下降至15.2%,2020年下降至13.3%。
在AVF术中使用6F血管鞘时需要注意:送鞘入血管时动作需缓慢、轻柔,不宜反复多次扩张血管,以免损伤血管内膜导致血栓形成;在送鞘过程中若发现有阻力,提示可能有血管分支或严重狭窄,不可强行送鞘,可只予鞘芯扩张血管,以防鞘尖端戳破血管;由于6F血管鞘鞘管长度有限(本研究使用的鞘管长度为16 cm),本研究术中只能扩张前臂静脉,对肘窝部及上臂的静脉无扩张作用,若该部位头静脉内径细小或有局部狭窄,使用6F血管鞘并不能改善。
综上所述,在细径头静脉的自体标准AVF术中使用6F血管鞘扩张静脉技术的难度不大,操作简单、安全,可充分合理利用患者宝贵的血管资源,提高内瘘的短中期通畅率,增大内瘘的血流量,促进内瘘成熟,减少内瘘狭窄和闭塞,能有效解决一些细径静脉患者的血管通路问题,但本研究观察时间较短、样本数量较少、未纳入内瘘其他并发症(假性动脉瘤、窃血综合征等)的统计,可能会影响研究结果的准确性,需要扩大样本量和更长时间的研究。
