基于美国FDA不良事件数据库的利伐沙班不良反应信号挖掘
2021-08-10吴圆圆郑淑芬钟诗龙
吴圆圆 郑淑芬 钟诗龙

中圖分类号 R973+.2;R969.3 文献标志码 A 文章编号 1001-0408(2021)14-1764-06
DOI 10.6039/j.issn.1001-0408.2021.14.17
摘 要 目的:挖掘利伐沙班的药品不良反应(ADR)信号,为其临床安全合理使用提供参考。方法:基于美国FDA不良事件报告系统,采用报告比值比法和比例报告比法对FDA公共数据开放项目中于2008年9月-2020年12月上报的利伐沙班ADR报告进行数据挖掘,分析相关ADR报告并映射得到对应的系统器官分类(SOC);同时,统计报告病例的性别、年龄、适应证等基本信息。结果与结论:共提取到相关ADR报告9 373 236例,其中以利伐沙班为伴随和怀疑药物的ADR报告有102 027例;共挖掘得到ADR信号883个,涉及系统器官27个。102 027例ADR报告中,女性(41 294例,占40.47%)与男性(41 071例,占40.26%)比例相当;年龄主要在>50~75岁(29 261例,占28.68%)和>75岁(21 470例,占21.04%);上报年份主要集中在2018年(18 446例,占18.08%);主要上报国家为美国(75 390例,占73.89%);严重的ADR报告有35 046例(占34.35%),以住院或住院时间延长为主。利伐沙班ADR信号的SOC主要集中在血液和淋巴系统疾病、血管疾病、各类检查及神经系统疾病。在ADR报告数排序前20位的ADR首选术语中,除肺栓塞、急性肾损伤和心房颤动外,其余主要为出血相关的ADR,其中颅内出血是较为严重的ADR。当利伐沙班应用于房颤和预防脑血管意外时易引发颅内出血,当应用于肺栓塞、(深)静脉血栓和血栓形成预防时易引发肺栓塞,临床应密切关注。
关键词 利伐沙班;美国FDA不良事件报告系统;药品不良反应;信号挖掘;比例报告比法;报告比值比法
ADR Signal Mining of Rivaroxaban Based on FDA Adverse Event Reporting Database
WU Yuanyuan1,2,3,ZHENG Shufen2,3,ZHONG Shilong1,2,3(1. School of Biology and Biological Engineering, South China University of Technology, Guangzhou 510006, China; 2. Dept. of Pharmacy, Guangdong Provincial Peoples Hospital, Guangzhou 510080, China; 3. Guangdong Provincial Key Laboratory of Coronary Heart Disease Prevention and Treatment, Guangdong Provincial Peoples Hospital, Guangzhou 510080, China)
ABSTRACT OBJECTIVE: To excavate the ADR signals of rivaroxaban and provide reference for its safe and rational use in clinic. METHODS: Based on FDA adverse event reporting system (FAERS), the ADRs of rivaroxaban reported from September 2008 to December 2020 in FDAs Open Data Program were mined using ratio of reports to odds (ROR) and proportional report ratio (PRR). The related ADRs were analyzed, and the corresponding system organ classification (SOC) was mapped. At the same time, the basic information such as gender, age and indications of the patients were statistically reported. RESULTS & CONCLUSIONS: Among 9 373 236 ADR reports extracted, 102 027 ADR reports with rivaroxaban as concomitant and suspected drug were obtained; 883 ADR signals were mined, involving 27 systems. Among 102 027 reports, the proportion of female patients (41 294 cases, 40.47%) was similar to that of male patients (41 071 cases, 40.26%). The patients were mainly >50 to 75 years old (29 261 cases, 28.68%) and >75 years old (21 470 cases, 21.04%). The reporting year was mainly in 2018 (18 446 cases, 18.08%); main reporting country was the United States (75 390 cases, 73.89%); there were 35 046 cases (34.35%) of severe ADR reports, mainly involving hospital or prolonged hospital stay. The SOC of rivaroxaban ADR singal mainly focused on diseases of the blood and lymphatic system, vascular diseases, various types of examination and nervous system diseases. Among top 20 preferred terms of ADRs with the highest frequency, except for pulmonary embolism, acute kidney injury and atrial fibrillation, the rest were mainly bleeding related ADRs, of which intracranial hemorrhage was the more serious ADR. Intracranial hemorrhage may occur when rivaroxaban is used for the prevention of atrial fibrillation and cerebrovascular accidents, and pulmonary embolism may occur when rivaroxaban is used for the prevention of pulmonary embolism, (deep) venous thrombosis and thrombosis. Great importance should be paid on it.
KEYWORDS Rivaroxaban; FDA adverse event reporting system; Adverse drug reactions; Signal mining; Ratio of reports to odds; Proportional report ratio
利伐沙班(rivaroxaban)是一种口服、直接的Ⅹa因子抑制剂,具有高度选择性,可竞争性地与Ⅹa因子的活性位点结合,是新型口服抗凝药物(NOACs)的代表药物[1]。利伐沙班于2008年9月在加拿大上市,并于2009年6月在国内上市,现已在全球90多个国家获得批准,被广泛用于骨科术后静脉血栓、非瓣膜性房颤、肺栓塞、深静脉血栓、急性冠脉综合征和外周动脉疾病等多种血栓栓塞性疾病的治疗和预防,是所有NOACs中适应证最多的一个[2-3]。有研究表明,利伐沙班具有与华法林同等或更高的疗效和安全性,并且其许多特性较华法林更优,如不易与其他药物及食物产生相互作用、起效迅速且安全性良好、服用更方便、无需实时监测药动学和药效学指标等[4-5]。
药物在上市前都要经过一系列疗效和安全的评估研究,但因用药疗程和观察时间较短,很难发现一些迟发的、罕见的不良反应(ADR)。随着利伐沙班的广泛应用,其ADR也日渐受到关注。与使用百年之久的华法林不同,利伐沙班在临床上的使用时间较短,其迟发的、严重的ADR尚不明确,国内安全性研究较少。目前,国际上对利伐沙班的ADR信号挖掘多集中在其出血方面[6-8],而对其引发的其他ADR尚未可知。为此,本研究通过提取和分析美国FDA不良事件报告系统(FAERS)的相关数据,对利伐沙班的ADR信号进行挖掘和分析,拟梳理、评价其安全性,为其临床合理使用提供参考。
1 资料与方法
1.1 数据来源
本研究数据来源于FDA公共数据开放项目(open-FDA),其ADR的原始数据由FAERS导入。本研究使用可以对药物警戒数据进行清洗和标准化的开放工具OpenVigil 2.1(http://openvigil.sourceforge.net/)来进行数据查询。
1.2 数据提取与处理
利伐沙班于2008年9、10月分别在加拿大和欧盟上市,故本研究提取open-FDA中2008年9月-2020年12月公布的利伐沙班的ADR资料。本研究通过检索药物通用名称“rivaroxaban”和商品名“Xarelto”,筛选利伐沙班相关ADR,排除重复、非此药物及名称不确定的报告。
1.3 信号挖掘方法
目前,国际上多采用报告比值比法(ROR)和比例报告比法(PRR)进行数据检测,两种方法均属于频率法,均能估计相对危险度,并可减少由于对照组选择所带来的偏倚,具有计算简单、结果一致性好等特点,二者的信号检测算法见表1[9-10]。基于此,本研究采用ROR法和PRR法对利伐沙班的ADR信号进行挖掘,并将ADR报告数≥3例、ROR及其95%置信区间(CI)下限以及PRR值>1作为有效信号生成的条件[7],若满足上述条件则提示药物与目标ADR具有统计学关联。经ROR法和PRR法计算出ROR值和PRR值,其数值越大,信号就越强,说明目标药物与目标ADR之间的统计学联系越强[11]。
1.4 国际医学用语词典(MedDRA)标准化查询
按MedDRA中的首选术语(PT)及系统器官分类(SOC)对用ROR法和PRR法筛选得到的利伐沙班ADR信号进行汇总和分析,并映射得到对应的SOC。同时,统计报告病例的人口学特征(性别、年龄等)、上报年份、上报国家或地区、严重ADR、适应证等信息。相关内容查询网址为http://bioportal.bioontology.org/、https://www.meddra.org/。
2 结果
2.1 纳入数据
在open-FDA中共提取得到相关ADR报告9 373 236例;删除无效数据后,以利伐沙班为伴随和怀疑药物的ADR报告共102 027例。
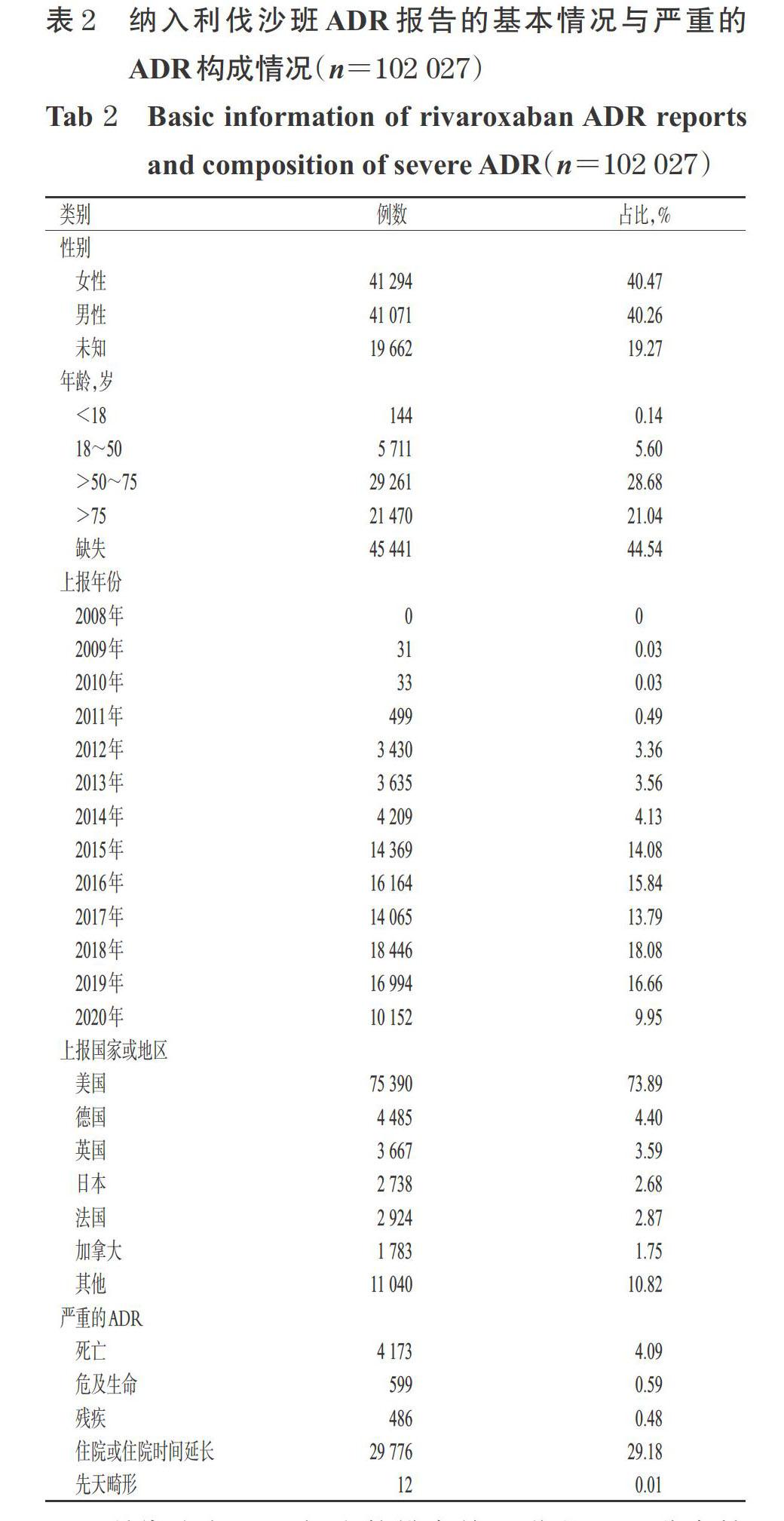
2.2 纳入ADR报告的基本情况与严重的ADR构成情况
在纳入的102 027例ADR报告中,女性(41 294例,占40.47%)与男性(41 071例,占40.26%)比例相当;年龄主要分布在>50~75岁(29 261例,占28.68%)和>75岁(21 470例,占21.04%);上报年份主要集中在2018年(18 446例,占18.08%);主要上報国家为美国(75 390例,占73.89%),其次为德国、英国等;严重的ADR报告有35 046例(占34.35%),以住院或住院时间延长为主,详见表2。
2.3 纳入ADR报告的信号分析
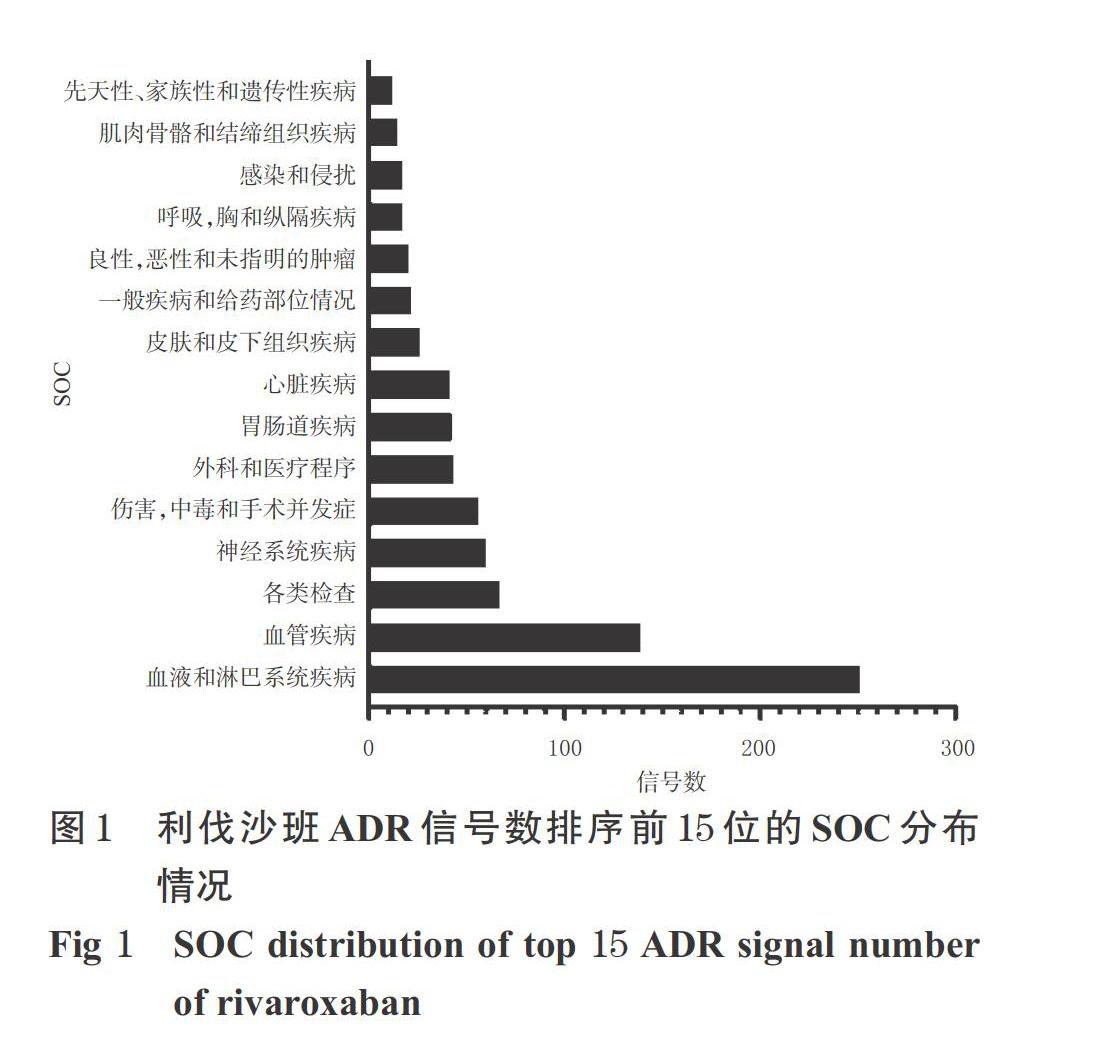
2.3.1 SOC 从纳入的102 027例ADR报告中挖掘得到利伐沙班ADR信号883个,并映射到27个系统器官,其中ADR信号数排序前15位的SOC分布情况见图1。由图1显示,利伐沙班ADR的SOC主要包括血液和淋巴系统疾病(251个信号)、血管疾病(139个信号)、各类检查(67个信号)、神经系统疾病(60个信号)等。
利伐沙班ADR报告数排序前15位的SOC分布情况见图2。由图2显示,利伐沙班ADR报告数较高的SOC包括血液和淋巴系统疾病(68 065例),血管疾病(22 187例),呼吸、胸和纵隔疾病(7 541例),神经系统疾病(5 939例)等。
信号数排序前4位的SOC是利伐沙班ADR的重点SOC,其相关PT分布见表3。由表3显示,在血液和淋巴系统疾病相关ADR中,胃肠道出血的ADR报告数最多,并且信号值较强。在血管疾病相关ADR中,鼻出血、肺栓塞和脑血管意外的ADR报告数较多。在各类检查相关ADR中,N端激素前体脑利钠肽异常的信号值最强。在神经系统疾病相关ADR中,脑血管意外和脑梗死的ADR报告数较多,且均为有效信号;而栓塞性脑梗死的信号值最强。脑血管意外、脑梗死、栓塞性脑梗死等均未在利伐沙班药品说明书中被提及,尤其值得关注。
2.3.2 PT 利伐沙班ADR报告数排序前20位的PT分布见表4。由表4显示,除肺栓塞、急性肾损伤和心房颤动外,其余ADR主要以出血相关的ADR为主,其中颅内出血是较为严重的ADR,其信号值也较高,药品说明书中也有提及。
2.3.3 患者适应证 为进一步评估不同适应证患者的ADR信号情况,本研究对ADR报告数最多的前5个适应证[依次为房颤、预防脑血管意外、血栓形成预防、(深)静脉血栓和肺栓塞]的PT进行统计,分布情况见表5。由表5显示,在上述5个适应证中,胃肠道出血为最常见的ADR,且在血栓形成预防中,胃肠道出血的ADR报告数占比甚至达到15.56%。另外,当利伐沙班应用于房颤和预防脑血管意外时,较为严重的ADR颅内出血出现在第10位,占比分别为1.05%和1.22%;而在血栓形成预防、(深)静脉血栓和肺栓塞患者报告数前10位的ADR中并没有出现颅内出血,但均可见肺栓塞。这说明当适应证为房颤和预防脑血管意外时,利伐沙班更容易使患者发生颅内出血;而当适应证为肺栓塞、(深)静脉血栓和血栓形成预防时,利伐沙班更容易使患者发生肺栓塞。
3 讨论
3.1 筛选出的ADR信号和重点SOC检测结果分析
根据药品说明书提示,利伐沙班最常见ADR为术后出血、头晕、恶心和转氨酶升高,本研究结果再次验证了利伐沙班的ADR主要表现为出血,与其他研究结果以及用药警戒信息基本一致[12-15]。颅内出血是一种非常严重的可累及中枢神经系统的疾病,可造成患者出现一系列危险症状(如昏迷、呼吸心跳骤停和瘫痪等),严重者还可危及生命。本研究结果提示,颅内出血的信号值较强,应为临床关注的重点。在本研究挖掘出的前20位的PT中,除出血相关的ADR外,还出现了急性肾损伤、肺栓塞和心房颤动。有研究显示,大约2/3的利伐沙班由肝脏代谢为非活性代谢物,然后通过肾和肝胆系统消除,可能会引起急性肾损伤[16],并且肾损伤对利伐沙班的药动学、药效学和安全性也有重要影响[17]。这提示临床在用利伐沙班时除需关注出血相关ADR外,还应当重视急性肾损伤等ADR。利伐沙班在临床上可以用于肺栓塞和心房颤动的血栓治疗,值得注意的是,本研究挖掘出利伐沙班也能引发这两个ADR,故临床上仍有必要开展大样本、多中心、随机对照、平行、前瞻性试验和临床经济学评价,以提高利伐沙班使用的规范性、安全性及药物经济性。此外,本研究在神经系统方面挖掘出了脑血管意外、栓塞性中风和栓塞性脑梗死等未被利伐沙班药品说明书收载的ADR阳性信号,考虑可能是其新的具有临床指导价值的潜在ADR,但这一结论仍需大量的临床研究予以验证。
3.2 不同适应证的信号检测结果分析
利伐沙班用于临床的适应证较其他Ⅹa因子抑制剂更为广泛,但是其在不同的适应证中的ADR并不完全相同[12]。因此,为具体了解利伐沙班在不同适应证患者中的ADR信号的差异性,本研究对其报告数排序前5位的适应证进行了ADR信号挖掘。结果显示,适应证为房颤的报告数最多(38 210例),其次为预防脑血管意外(31 667例)等。利伐沙班在治疗这些适应证最易引发的ADR为胃肠道出血。与其他NOACs比较,利伐沙班用于心房颤动和静脉血栓栓塞的治疗时只需每天给药1次[18],而达比加群酯和阿哌沙班都是每天2次。笔者推测利伐沙班较高的出血比例可能与其每天1次的剂量有关。值得注意的是,当利伐沙班应用于房颤(1.05%)和预防脑血管意外(1.22%)时发生颅内出血的报告数占比均高于其他适应证。这提示利伐沙班用于这2种适应证时显著增加了患者发生颅内出血的风险。尽管利伐沙班在临床上可用于肺栓塞的治疗,但本研究结果提示,在使用利伐沙班会一定程度上增加患者发生肺栓塞的风险,尤其当应用于肺栓塞、(深)静脉血栓和血栓形成预防时。但目前尚缺乏直接的文献证据,其相关性也并不明确,值得关注并有待进一步研究。因此,利伐沙班片用于治疗出血风险高的疾病时需密切关注患者的出血风险。
3.3 本研究的局限性
虽然本研究对利伐沙班的潜在ADR信号及其强度进行了新的描述,但仍存在一些局限性,包括FAERS数据库中的ADR低报、漏报和患者临床信息的缺失、偏倚等都会对数据挖掘结果造成影响[19-20],因此还需要更多的时间和更多的数据来确证这些ADR的发生概率。同时,本研究发现上报的患者年龄多为老年人,一方面可能是由于利伐沙班在临床中多用于老年患者,另一方面也可能是因为年龄较大的患者发生出血等ADR的风险更高[21]。故未来的研究应当针对更多的人群,包括青少年、孕妇和哺乳期人群。此外,本研究采用的PRR法和ROR法产生的风险信号不代表药物与ADR存在必然的因果联系,只能表明药物与ADR信号有统计学关联[22],故需要进一步对风险信号进行临床研究和評估加以确定。
4 结语
本研究通过对FAERS数据库的信号挖掘,分析和评价了利伐沙班重要的ADR信号,发现了可能造成严重损害且未被记录在药品说明书中但信号值较强的ADR,如肺栓塞、栓塞性脑梗死等。但是本次研究并未挖掘到药品说明书中列出的转氨酶升高的ADR,这可能是由于上报的患者自身没有肝损伤,所以不容易出现转氨酶升高。此外,对不同适应证的ADR信号进行分析发现,利伐沙班在应用于房颤和预防脑血管意外时引发颅内出血的风险较高,应用于肺栓塞、(深)静脉血栓和血栓形成预防时引发肺栓塞的风险较高。
参考文献
[ 1 ] VERMA A,HA A C T,RUTKA J T,et al. What surgeons should know about non-vitamin K oral anticoagulants:a review[J]. JAMA Surg,2018,153(6):577-585.
[ 2 ] STEFFEL J,VERHAMME P,POTPARA T S,et al. The 2018 European Heart Rhythm Association Practical Guide on the use of non-vitamin K antagonist oral anticoagulants in patients with atrial fibrillation[J]. Eur Heart J,2018,39(16):1330-1393.
[ 3 ] HOSNY N M. A review on:analysis of the first oral,direct factor Ⅹa inhibitor;rivaroxaban[J]. Microchem J,2020,159:105336.
[ 4 ] MAQSOOD M,IMRAN M,YAMEEN M,et al. Use of oral rivaroxaban in cerebral venous thrombosis[J]. J Drug Assess,2020,10(1):1-6.
[ 5 ] DALIA T,LAHAN S,RANKA S,et al. Warfarin versus direct oral anticoagulants for treating left ventricular thrombus:a systematic review and meta-analysis[J].Thromb J,2021,19(7):2-8.
[ 6 ] JIN M,SUSSMAN E,FENG A,et al. Hemorrhage risk of direct oral anticoagulants in real-world venous thromboembolism patients[J]. Thromb Res,2021,204:126-133.
[ 7 ] AKHTAR T,FRATTI J,MATTUMPURAM J,et al. Factors associated with bleeding events in patients on rivaro- xaban for non-valvular atrial fibrillation:a real-world experience[J]. Int J Cardiol,2020,320:78-82.
[ 8 ] SENNESAEL A L,LAROCK A S,DOUXFILS J,et al. Rivaroxaban plasma levels in patients admitted for bleeding events:insights from a prospective study[J]. Thromb J,2018,16(1):28.
[ 9 ] 江静,侯永芳,刘秀娟,等.药品不良反应信号检测方法概述[J].中国药物警戒,2010,7(2):78-80.
[10] 郑东妮,周后凤,任常谕,等.塞瑞替尼不良反应信号挖掘与分析[J].中国药房,2021,32(2):236-240.
[11] 周健,陈力.索拉非尼的不良反应信号挖掘[J].中国医药导报,2018,15(14):111-115.
[12] ASHTON V,KEROLUS-GEORGI S,MOORE K T. The pharmacology,efficacy,and safety of rivaroxaban in renally impaired patient populations[J/OL]. J Clin Pharmacol,2021:1-17(2021-02-18)[2021-03-19]. https://doi.org/10.1002/jcph.1838.
[13] INOUE K,HIRAO K,KUMAGAI K,et al. Long-term effi- cacy and safety of anticoagulation after atrial ?brillation ablation:data from the JACRE registry[J]. J Cardiol,2021,77(3):263-270.
[14] DELOUGHERY E P,SHATZEL J J. A comparative analysis of the safety profile of direct oral anticoagulants using the FDA adverse event reporting system[J]. Eur J Haematol,2019,103(1):43-46.
[15] NATHAN K T,CONN K M,VAN MANEN R P,et al. Signal detection for bleeding associated with the use of direct oral anticoagulants[J]. Am J Health Syst Pharm,2018,75(13):973-977.
[16] SCICCHITANO P,TUCCI M,BELLINO M C,et al. The impairment in kidney function in the oral anticoagulation era:a pathophysiological insight[J]. Cardiovasc Drug Ther,2020,35:505-519.
[17] KUBITZA D,BECKA M,MUECK W,et al. Effects of renal impairment on the pharmacokinetics,pharmacodyna- mics and safety of rivaroxaban,an oral,direct factor Ⅹa inhibitor[J]. Br J Clin Pharmacol,2010,70(5):703-712.
[18] BAUERSACHS R,BERKOWITZ S D,BRENNER B, et al. Oral rivaroxaban for symptomatic venous thromboembolism[J]. N Engl J Med,2010,363(26):2499-2510.
[19] 王郁薇,蒙龙,刘箫.基于美国FDA不良事件数据库的注射用紫杉醇(白蛋白结合型)不良反应信号挖掘[J].中国药房,2021,32(3):328-333.
[20] ALOMAR M,TAWFIQ A M,HASSAN N,et al. Post marketing surveillance of suspected adverse drug reactions through spontaneous reporting:current status,challenges and the future[J]. Ther Adv Drug Saf,2020,11:1-11.
[21] CIOS D,FANIKOS J. Rivaroxaban to prevent pulmonary embolism after hip or knee replacement[J]. Circulation,2012,125(14):E542-E544.
[22] FADINI G P,BONORA B M,AVOGARO A. SGLT2 inhibitors and diabetic ketoacidosis:data from the FDA adverse event reporting system[J]. Diabetologia,2017,60(8):1385-1389.
(收稿日期:2021-03-09 修回日期:2021-07-01)
(编辑:邹丽娟)
