湖北省部分医疗器械生产企业工艺用水水质状况调查
2021-07-21梅享林魏嫣湖北省医疗器械质量监督检验研究院湖北武汉430075
梅享林 魏嫣 湖北省医疗器械质量监督检验研究院 (湖北 武汉 430075)
内容提要: 目的:掌握湖北省内医疗器械生产企业工艺用水水质状况。方法:依据相关标准对湖北省内31家医疗器械生产企业的34批次生产工艺用水理化指标进行抽检并查看企业工艺用水管理情况。结果:共有6家生产企业的工艺用水超过参考限值,不合格的主要问题主要集中在电导率、易氧化物和酸碱度等三个项目。结论:本省生产企业的工艺用水存在一定的问题,企业应加强对工艺用水的管理。
水是医疗器械生产中广为使用的一种原料,其制备、检测、储存等影响工艺用水质量的过程,也直接或间接影响到产品的质量。水质的污染会给医疗器械生产环境及产品带来影响,如拉管成型生产、工位器具和洁净服使用了不符合标准的水进行清洗,将会增加其自身的菌落数,从而污染产品及其生产环境。一般情况下,生产工艺用水的制水系统需要定期监测水质,定期维护保养和消毒,必要时还应该进行再验证。因企业的技术能力的差距,可能存在部分企业工艺制水系统并未及时维护保养,同时水质监测工作也未做到位,水质已经污染仍然在继续使用的情况。
体外诊断试剂生产企业在本次抽检中占比较大,近年来体外诊断试剂行业发展迅速,纯化水在体外诊断试剂中既作为产品的组成成分,如样本稀释液、缓冲液,又作为生产过程中使用的工艺用水,水中的杂质可干扰检验结果,所以纯化水的质量可以直接影响诊断试剂结果的准确性,YY/T 1244-2014《体外诊断试剂用纯化水》[1]作为第一个专门针对体外诊断试剂制定的纯化水标准于2015年7月1日实施。目前本省体外诊断试剂生产企业的生产工艺用水都采用YY/T 1244-2014和中国药典2015版,两个标准的技术指标不同。
为了掌握湖北省医疗器械生产企业的生产工艺用水的质量,2019年湖北省医疗器械质量监督检验研究院对湖北省内部分地市的31家生产企业的生产工艺用水进行了检测,并对检测结果进行了分析和讨论,为有关部门的监管和风险预警提供依据。
1.材料与方法
1.1 一般材料
样品采集:每个取水点取水1000mL。因每个企业的取水点分布不一样,有的企业如输注器具生产车间的取水点分布较多,有的企业如纺织品敷料类企业的取水点较少,为了统一评价标准,本次检验只抽取工艺制水系统的总送水和总回水两个取水点进行评价。
仪器设备:S-700型电导率仪(梅特勒);S20P型酸度计(梅特勒);Sievers 860型TOC分析仪(GE)。
试剂:0.02mol/L高锰酸钾标准滴定液(国家标准物质中心);试验用水为超纯水(Millipore纯水系统制备)。
1.2 方法
水中需要去除的物质包括电解质、颗粒、有机物和微生物。其中,电解质以各类可溶性无机物、有机物离子状态存在于水中,具有导电性,可通过测量水的电导率反映这类电解质在水中的含量;颗粒杂质可以通过测量水的性状进行评价;有机酸、有机金属化合物等有机物在水中常以阴离子状态存在,分子量大,通常通过总有机碳来反映这类物质在水中的相对含量。本次重点对理化指标进行检测,微生物项目本次抽检没有涉及。抽检项目见表1。

表1. 生产工艺用水抽检项目
1.3 观察指标与判定标准
检测标准和评价指标:抽检的生产企业包括无菌医疗器械生产企业、普通无源医疗器械生产企业和体外诊断试剂生产企业。生产工艺用水的依据分别为《中华人民共和国药典》[2]2015版中纯化水和注射用水标准,YY/T 1244-2014《体外诊断试剂用纯化水》[3]和企业制定的工艺用水水质标准或检验规程。抽检采用相对应的方法进行检测。
本次结果判定参考《中华人民共和国药典》2015版中纯化水和注射用水标准,YY/T 1244-2014《体外诊断试剂用纯化水》和企业制定的工艺用水水质标准或检验规程进行判定。超过参考限值的判定为不合格样品。
2.结果
所检测的31家企业中有3家生产企业工艺用水为注射用水,按照《中华人民共和国药典》2015版进行检测和判定,注射用水合格率为100%。8家体外诊断试剂生产企业采用行业标准YY/T 1244《体外诊断试剂用纯化水》作为参考标准,3家企业出现电导率不符合情况,合格率为62.5%。20家其他医疗器械生产企业配备有符合《中华人民共和国药典》2015版中纯化水要求的制水设备,3家企业出现易氧化物、酸碱度和电导率等不符合现象,合格率为85%。3家企业使用的为自行制定的标准,经检测均合格,合格率为100%。理化指标检测结果见表2。
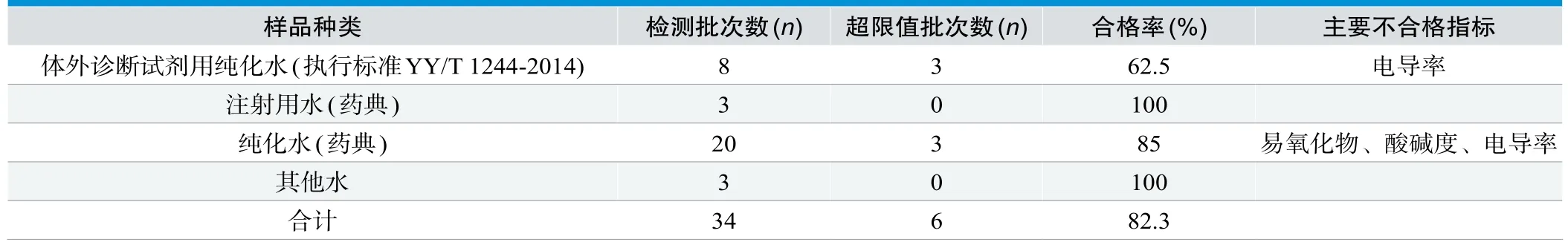
表2. 生产工艺用水理化指标检测结果
3.讨论
3.1 体外诊断试剂生产企业引用标准问题
在被检31家企业中,有13家属于体外诊断试剂生产企业,其中8家工艺用水采用YY/T 1244《体外诊断试剂用纯化水》作为参考标准,4家企业采用药典纯化水为参考标准,1家企业纯化水标准为自行制定的。此两种标准的技术指标要求不同,中国药典2015版中有10个技术指标,YY/T 1244-2014中有5个技术指标,对酸碱度、硝酸盐、亚硝酸盐和氮含量均未做要求。YY/T 1244标准中对电导率要求较高,为0.1mS/m(25°C),中国药典2015版明确了不同温度(0~100°C)时的电导率限值,其中药典纯化水在25°C电导率要求为5.1uS/cm(换算统一单位为0.51mS/m)[2]。YY/T 1244-2014电导率要求显著高于中国药典2015年版,两个标准之间差距较大,这次抽检的13家体外诊断试剂企业出现的3家不符合,其不符合项均为电导率值,且这三家企业均采用YY/T 1244《体外诊断试剂用纯化水》作为参考标准,要求限值相对较高,企业工艺用水质量标准选取应在保证产品质量和工艺用水质量保证可行性之间达到平衡。
有2家企业使用的工艺用水为软水,因软水无国家和行业标准,企业自行制定了操作规程和判定标准,其合理性有待验证。
3.2 企业工艺用水管理薄弱
水设备只有通过验证后进行标准程序(SOP)操作运行、有效监控,生产出来的工艺用水才是稳定可靠的,才可以有效地监测水质的偏移。纯化水系统作为生产的关键环节,其日常管理必须包括运行和维护、检测并根据水质变化调整设备的运行条件。如果产品对电导率有较高要求,如基因诊断试剂企业,应加强对纯化水电导率的监测力度。在抽检过程中发现,很多企业并不重视生产工艺用水的管理,有少部分企业缺少工艺用水检测的作业指导书,维护保养操作规程、监控维护记录等文件。
监督抽检的目的是提高产品质量,保障用械安全。在抽检中发现不同企业的制水设备布局差距较大,有的生产企业仅有总送水口,未设计总回水口,工艺用水未在车间内循环。通过本次抽检也希望生产企业能够更加重视生产工艺用水的管理,增强企业质量意识,使企业认识到产品质量与工艺用水息息相关。
3.3 监管建议
通过对以上问题的分析,生产工艺用水的监管还有待于法规的完善和行业的进一步规范。下一步亟需加强监管力度,包括体系核查和监督检验。在体系考核中重点关注制水系统的验证记录和文件、并结合企业的化学试剂(如甲基红、溴麝香草酚蓝等)购置使用情况、滴定液配制(如高锰酸钾标准滴定液)和使用等情况检查生产企业水质日常检测记录,关注涉及水质检验的仪器设备精度及需要计量和检定的器皿,如电子分析天平的精度应精确到0.1mg。同时,加大监督检验的力度,为加强监管提供数据支撑。
