基于砷形态的分离/富集加深学生对“分布分数”的理解
2021-07-14何蔓陈贝贝胡斌
何蔓,陈贝贝,胡斌
武汉大学化学与分子科学学院,武汉 430072
分析化学是化学专业本科生的四大基础课之一,涵盖的内容非常广泛。该课程的教学目的在于:要求学生掌握分析化学的基本理论,准确树立“量”的概念,了解定性、定量分析方法(包括化学分析和仪器分析),培养其分析问题和解决问题的能力。分析化学涉及的基本概念非常多,在讲授课本知识的同时,教师可结合基本概念在生活、科研工作中的应用实例,加深学生对其的理解和掌握。下面将以不同砷形态的“分布分数”为例,阐述分析化学教学过程中理论和实践相结合的教学实践。
1 分析化学教学中的“分布分数”
学生最初接触“分布分数”是在“酸碱滴定法”章节中:一元酸/碱或多元酸/碱在溶剂(通常为水溶液)中以不同形式存在,这些组分/型体的平衡浓度随溶液中H+浓度的变化而变化。“分布分数”被定义为“溶液中某酸碱组分的平衡浓度占其总浓度的分数”[1],通常采用代数法,基于一元酸/碱或多元酸/碱的解离平衡常数(pKa)和溶液的pH计算得到。除了计算之外,学生还应该掌握依据酸/碱性物质的pKa和溶液pH快速判断其在溶液中存在形式的技巧。如,对于一元弱酸HA而言,其解离平衡常数为pKa,那么当介质的pH < pKa− 2时,HA的分布分数接近100%,它主要以HA中性分子的形式存在;当介质的pH > pKa+ 2时,A−的分布分数接近100%,它主要以A−阴离子的形式存在。
2 不同砷形态的分布分数及其在砷形态分离/富集中的应用
砷以多种存在形式广泛分布于自然界中,表1列举了五种重要砷形态的pKa信息。在环境水体中,砷的主要存在形式是三价砷As(III)和五价砷As(V);在细菌、酵母等微生物的作用下,无机砷将转变为有机砷,通过食物链进入到人体中。无机砷的毒性大于有机砷,被认为是强毒性和致癌性化合物;因此,砷的形态分析已成为分析科学研究的热点之一。目前,进行砷形态分析最有效的手段是高效液相色谱(HPLC)-等离子体质谱(ICP-MS)联用技术;此外,为了避免复杂基体干扰、提高方法对目标砷形态的灵敏度,在砷形态分离检测之前通常需要辅以合适的样品前处理技术。需要强调的是,在针对目标砷形态构建分离和/或富集方法的过程中,其pKa和在不同pH介质中的分布分数是重要的参考信息。
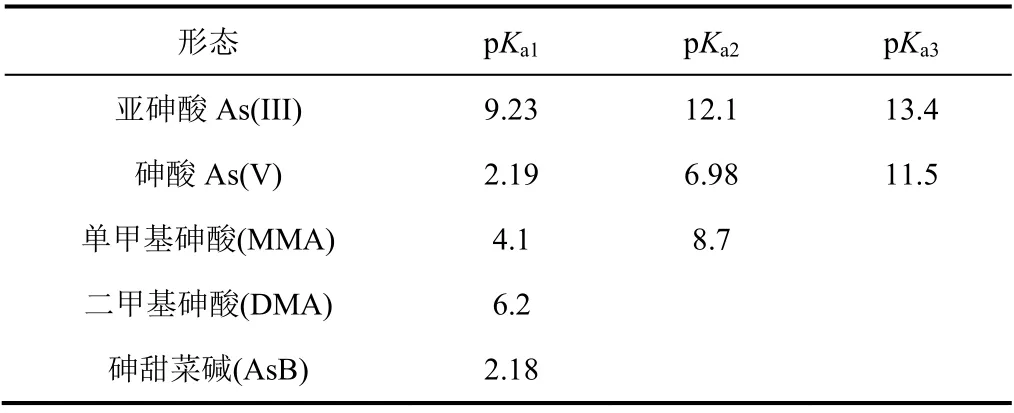
表1 几种重要砷形态的解离平衡常数(pKa) [2]
2.1 四种砷形态的色谱分离——以阴离子交换色谱为例
阴离子色谱柱是HPLC分离分析砷形态中最常用的色谱分离固定相,而流动相的pH通常选择为6左右;在此条件下,四种砷形态的色谱分离图如图1所示。
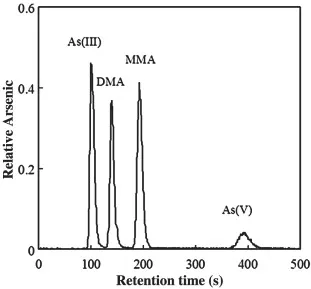
图1 四种砷形态的色谱分离图
基于各形态在pH = 6的分布分数,我们可以推测它们的存在形式,并依此解释它们的洗脱顺序:
在pH = 6的介质条件下,As(III)主要以不带电荷的H3AsO3形式存在,在阴离子色谱柱上无保留;
DMA以HA和A−各占一半的形式存在,在阴离子色谱柱上有一定保留;
MMA完全以HA−的形式存在,在阴离子色谱柱上的保留强于DMA;
部分As(V)已经以HA2−的形式存在,是这几种形态中保留最强的,所以最后流出。
可以看出,这几种砷的形态基于pKa的差异在色谱柱上实现了相互分离。
2.2 无机砷形态的非色谱分离——以氨基功能化硅胶材料为例
在介质pH 2–9范围内,As(III)和As(V)在氨基改性硅胶上的吸附行为如图2所示[4]。当pH在3–9范围内时,该材料对As(V)的吸附率大于90%,而在pH为2–9时对As(III)基本不吸附。基于分布分数对这一现象进行解释如下:
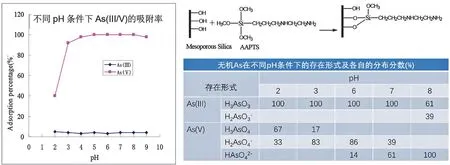
图2 As(III/V)在氨基改性硅胶吸附剂上的吸附行为(左)及其在pH 2–8范围内的分布分数(右) [4]
在pH 2–9范围内,改性硅胶中的氨基被质子化(带正电荷),而As(III)主要以H3AsO3的中性分子存在,所以吸附率很低;
当pH > 3以后,As(V)主要以带负电荷的H2AsO4−和HAsO42−形式存在,其与改性硅胶材料中质子化氨基之间的静电作用增强,吸附率增大。
因此,可以利用氨基功能化材料,在较宽pH范围内实现无机砷形态As(III/V)的分离。
2.3 多种砷形态的同时富集——以混合模式吸附剂为例
由表1可以看出,六种砷形态性质差别较大。在中性条件下,As(III)呈中性,As(V)和MMA带负电,DMA和AsB呈两性,AsC带正电;很难找到单一功能化的萃取材料对它们实现同时吸附/富集。陈贝贝等[5]实验发现,在pH = 6条件下,含巯基功能团的γ-巯丙基三甲氧基硅烷(γ-MPTS)在吸附材料中的加入明显改善As(III)的吸附,部分磺化聚苯乙烯(PSP)的添加对AsC的吸附有明显改善,而带负电的As(V)、MMA以及两性的DMA、AsB在氨基功能化涂层上均有恒定的吸附。基于此,制备了基于γ-MPTS、N-(β-氨乙基)-γ-氨丙基三甲氧基硅烷(AAPTS)和PSP的混合萃取材料,实现了六种砷形态的同时富集(图3)。
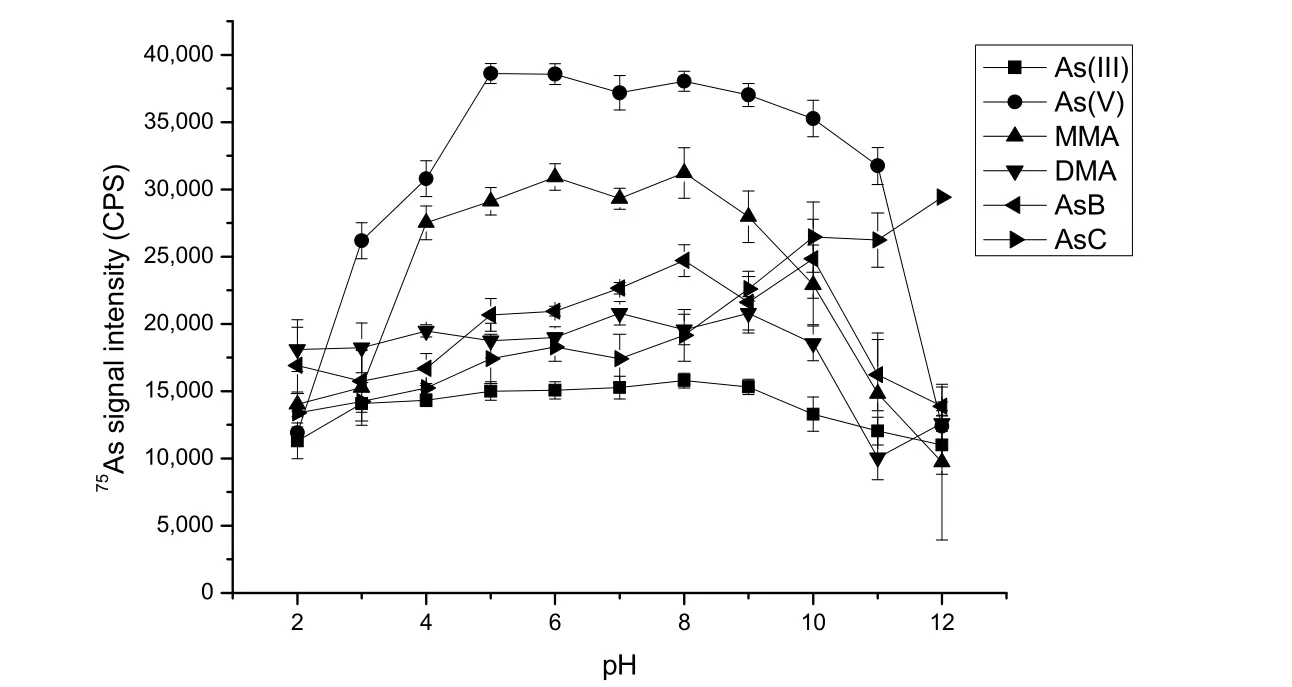
图3 pH 2–12范围内六种砷形态在混合模式吸附涂层上的保留行为[5]
对其可能的吸附机理进行讨论如下:
当pH > 4之后,As(V)和MMA主要以阴离子形式存在,与质子化的氨基产生静电作用;当pH >8后,氨基逐渐去质子化,对As(V)和MMA的作用力逐渐降低。因此,As(V)和MMA在该材料上的最佳吸附pH范围为5–8。
当pH < 6时,DMA以中性分子形式存在,与涂层之间的主要作用力为疏水作用;当pH > 6时,DMA主要以阴离子形式存在,与涂层之间存在静电作用。
以两性状态存在的AsB,与涂覆材料之间存在静电作用和疏水作用。
AsC在溶液中带正电,与PSP上的磺酸基之间存在阳离子交换作用。
另外,As(III)在pH 3–9的范围内有稳定的吸附主要基于其与γ-MPTS上巯基之间强亲和作用。
3 讨论及小结
酸性和碱性物质的解离平衡常数及其在不同pH条件下的分布分数信息,对于针对性地构建分离/富集和分析方法有着重要的作用。在教学过程中,应对学生进行适当引导,加深他们对这一概念的理解和掌握;同时,教学要遵循由浅入深和反复提及的原则。具体而言:
(1) 在酸碱滴定章节的授课过程中,重点放在阐述分布分数的定义、计算,以及基于此的不同类型溶液的pH的计算;不宜对分布分数的应用展开讨论。
(2) 在后续章节,寻找合适契机插入,如“酸碱指示剂”部分,可根据特定指示剂的解离平衡常数,让学生计算分布分数,学会有目的地调节介质pH,让指示剂以预想的形式存在;在“分离和富集方法”部分,让学生基于酸碱物质的解离平衡常数和分布分数,理解水相pH对两相液液萃取的影响,以及构建膜辅助三相液相萃取的基本原理;在仪器分析“液相色谱”部分,可以引导学生基于分布分数,思考某种分离模式下不同物质保留时间差异的根本原因。
(3) 在反复强化认知的过程中,大部分学生对“分布分数”这一概念会形成比较明晰的认识,对酸碱性物质的解离平衡常数更敏感,有助于培养其快速捕获信息、分析问题、解决问题的能力。
此外,常用教材上收录的解离平衡常数信息有限,在教学和科研过程中,对特定分析物的分布分数等相关参数,可以借助网络软件(如https://chemicalize.com/#/calculation)快速获取。
