不同溶剂中玉米醇溶蛋白的聚集状态和结构性质
2021-06-30赖婵娟吴磊燕胡林芳涂瑾董武辉
赖婵娟,吴磊燕,胡林芳,涂瑾,董武辉
(1.江西农业大学食品科学与工程学院,江西南昌 330000)(2.广东佳焙食品股份有限公司,广东东莞 523000)
玉米醇溶蛋白(zein)是玉米中的贮藏蛋白,非极性氨基酸含量高[1]。zein不溶于水,可溶于醇的水溶液、强酸(pH≤4)、强碱(pH≥11、高浓度的尿素或阴离子表面活性剂溶液中[2],温度高于溶剂的沸点时,玉米醇溶蛋白能溶于高浓度的乙醇甚至无水乙醇溶液[3]。这说明溶剂环境的物理和化学性质影响蛋白质的溶解性,同时,也会影响其折叠和动力学变化[4],促进蛋白质动态重排和必要的结构,使构象转变,进行纤维聚集或无定形聚集[5],最终在溶液中形成微球、纳米颗粒。这种蛋白质的聚集方式也是影响Pickering乳液稳定的关键因素。同样,zein在溶液中也经历聚集这个复杂过程,大部分情况是先自组装成β-sheet为主的二级结构,随着依靠各种化学键进行盘曲、折叠、螺旋,最终形成螺旋结构纤维聚集体[6]。当环境改变,pH处于中性或靠近蛋白质等电点,或在高离子强度条件下,蛋白质分子表面的电荷被中和或被屏蔽,疏水相互作用占主导地位,蛋白就趋于形成无定形聚集[7]。这种溶剂或蛋白环境改变,对蛋白质的构象、状态、聚集形貌有重要的影响最后决定了宏观的蛋白颗粒或膜的性质,如纳米颗粒的通透性和蛋白膜的机械性质[8]。
目前,国内外对zein的研究集中在蛋白改性、生物膜、微胶囊壁材、纳米粒子和Pickering乳液等方面的制备和应用[9-12]。通过改性去改变zein的溶解特性,为开发其应用潜力和应用领域[13]。特别地,zein因其独特的自组装特性广泛应用于生物活性物质的传递系统及Pickering乳液等体系,而其在溶液中的状态和性质影响这些体系的性能。
从上可知,研究蛋白在溶液中的性质至关重要,而溶液中溶剂决定了蛋白所处的环境和状态,对蛋白折叠和展开构象有重要影响。本文选用甲醇、乙醇、异丙醇、甲酸和丙酮五种不同极性的有机溶剂水溶液作为玉米醇溶蛋白的溶解环境,研究这些有机溶剂对玉米醇溶蛋白溶解、聚集特性和结构等性能的影响,以期为zein的后续研究及应用提供一定的理论依据。
1 材料与方法
1.1 原料及设备
1.1.1 原料
玉米醇溶蛋白粉(纯度≥98%),北京索莱宝科技有限公司;8-苯胺-1-萘磺酸(ANS),上海阿拉丁试剂有限公司;其他化学试剂(分析纯)均从西陇科学股份有限公司购买。
1.1.2 主要仪器设备
756PC UV紫外可见分光光度计,天津瑞普生物技术股份有限公司;ColorQuest XE色差分析仪,美国HunterLab公司;Nano-ZS纳米粒度仪,英国Malvern Panalytical公司;F-9700荧光分光光度计,日本Hitachi Corp公司;FTIR-7600傅里叶变换红外光谱仪,澳洲Lambda公司;JSM-6490LV扫描电子显微镜,日本JEOL公司;OSA 100界面分析仪,北京东方德菲仪器有限公司。
1.2 试验方法
1.2.1 溶液透光率的测定
当玉米醇溶蛋白溶解时,可通过测定其溶液的透光率来研究溶液浊度从而研究玉米醇溶蛋白在几种有机溶剂中的溶解及聚集状态。称取0.01 g zein,分别用甲醇、乙醇、异丙醇、乙酸和丙酮这五种不同浓度(70%、80%、90%、100%)的溶剂将zein溶解,zein浓度为1 mg/mL。利用紫外可见分光光度法在633 nm条件下测定溶液的透光率。以不加玉米醇溶蛋白的醇类溶液作空白。
1.2.2 溶液色差测定
称取0.01g zein,分别溶于80%浓度的甲醇、乙醇、异丙醇、乙酸和丙酮这五种不同极性溶剂中,zein浓度为1%,用色差分析仪测定每组样品的L*、a*、b*值。仪器用标准白板进行校正。总色差
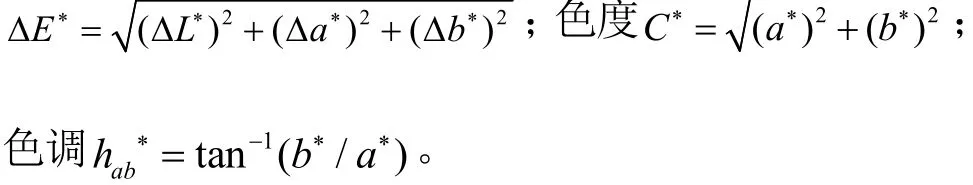
1.2.3 粒径测定分析
将zein分别充分溶解在不同浓度(70%、80%、90%、100%)的甲醇、乙醇、异丙醇、乙酸和丙酮这五种溶剂中,将zein稀释成1 mg/mL,过0.22 μm有机微孔滤膜。应用Malvern纳米粒度分析仪测定溶液的粒径大小及其分布。平衡时间为180 s,水的折射率为1.33,样品的折射率为1.53,测试温度为25 ℃。
1.2.4 内源性荧光光谱扫描
根据董世荣[14]的方法,测定不同处理条件下的玉米醇溶蛋白样品的内源性荧光光谱。内源性荧光光谱用于研究蛋白质溶液体系内部荧光基团的微环境,进而反映蛋白质的构象变化。激发波长为280 nm,发射波长为250~400 nm,激发波长和发射波长的狭缝宽度均为5 nm,扫描速度为10 nm/s,测定的吸光度值为玉米醇溶蛋白的内源性荧光光谱。
1.2.5 ANS荧光光谱分析测定
参照任晓锋[6]的方法,蛋白表面疏水性釆用8-苯胺-1-萘磺酸(ANS)作为荧光探针进行测定。用0.2 mol/L pH=7.0的磷酸缓冲液将ANS配制成2 mmol/L的溶液待用。将分别由不同浓度(70%、80%、90%、100%)、不同溶剂溶解得到的zein溶液稀释成蛋白浓度为1 mg/mL的待测液样品。同时取上述样液6 mL,加入50 μL ANS溶液,充分混匀后避光反应15 min。设置荧光分光光度计的激发波长为360 nm,发射波长为400~600 nm,激发波长和发射波长狭缝宽度均为5 nm,扫描速度为10 nm/s,测定反应后样品的吸光度值,获得不同处理条件下的玉米醇溶蛋白表面疏水性光谱。
1.2.6 紫外光谱分析测定
将zein充分溶解在80%浓度的几种有机溶剂中,zein浓度为1 mg/mL,紫外光谱扫描波长为245~445 nm,扫描速率为0.1 nm/s。
1.2.7 红外光谱分析测定
傅里叶红外变换光谱用来测定蛋白分子结构信息的变化。经不同处理后的蛋白冷冻干燥制成粉末,过100目的筛。精确称量蛋白粉末与KBr,蛋白粉末与KBr比例为1:100,研磨、制片。红外扫描范围为4000~400 cm-1,分辨率为4 cm-1,扫描次数为64。
1.2.8 光学显微镜观察
取200 μL 0.1 g/mL的zein溶液滴在载玻片上,盖上盖玻片,用光学显微镜观察溶液。
1.2.9 SEM分析测定
采用扫描电子显微镜观察溶解后玉米醇溶蛋白的表面微观结构。取1 mg/mL的少量样品溶液涂在双面导电胶上,自然干燥后进行喷金处理,喷金厚度约10 nm。离子溅射时间为3 min,真空度为0.05 Mbar;最后将样品转移置成像室,设置电镜在15 kV电压下扫描。测试温度为25 ℃。
1.2.10 接触角的测定
将zein分别溶解在80%的五种溶剂中,zein浓度为10%。然后将zein倒在聚四氟乙烯板上形成平整的zein膜。剪取2 mm×2 mm的膜片,固定在界面仪的载物台上,分别测定zein膜两面(膜液与聚四氟乙烯板的接触面和与空气的接触面)的接触角。
1.3 数据统计分析
试验中所有数据结果均为三次测定的平均值,采用IBM SPSS Statistic软件进行数据统计分析以及显著性差异(p<0.05)评价,并用平均值±标准差表示。用Origin 9.0软件作图。
2 结果与讨论
2.1 溶剂对zein溶液透光率和色差的影响
图1 是溶剂和浓度对zein溶液的透光率影响,收集瓶中液体对应为80%溶剂溶解的zein溶液。结果表明,不同有机溶剂中的zein溶液透光率的存在差异。随着甲醇的浓度增大,zein溶液的透光率也增大。在乙酸溶液中,zein溶液的透光率随浓度增加无明显变化;而在乙醇、异丙醇和丙酮溶液中,在高浓度溶剂中(90%以上),蛋白质透光率降低。根据光学原理,若溶液的混浊程度越小,表现出的光学效应强度就会相应增大,所测得的透光率值就大,即溶液溶解效果较好[15]。溶解度除受到溶质自身性质、溶剂极性及两者相互作用的影响外,还与溶液体系所处的环境有关,如浓度、温度、pH值和离子等[16]。从图1中看出,zein更易溶于100%的乙酸、80%~90%的乙醇。而在100%的乙醇、异丙醇和丙酮中zein蛋白溶液透光率显著下降,最低降至60.70%,此时,溶液呈悬浊液状态且出现聚集甚至成团现象。溶剂浓度和极性差异使zein复杂的多肽链展开程度不一,所以呈现的溶解状态也不同。在高浓度的有机溶剂中,zein疏水基团充分暴露,在疏水相互作用下主导zein分子自组装,形成更大的颗粒,透光率下降[17]。Chen Ye等在热处理对玉米醇溶蛋白颗粒在醇水溶液中的分散和聚集研究中也证实了这一结果[16]。
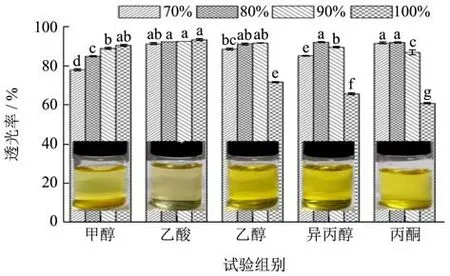
图1 溶剂和浓度对zein溶液透光率的影响Fig.1 Effect of different solvents on light transmittance of zein solution
色差在一定程度上反映zein蛋白分子在溶液中的状态。溶解时,蛋白展开,将与高度螺旋化的zein缠绕在一起的色素释放出来,使溶液颜色改变[18]。从直观上看,zein蛋白溶解在不同溶剂中都呈现黄色(见图1收集瓶中溶液颜色),但深浅不一,表明蛋白的展开程度不同。表1是用色差仪测得的zein溶液(80%溶剂)色差值,色差值越大,溶液颜色越深。乙酸环境的蛋白溶液颜色最浅,说明zein蛋白展开程度最小。
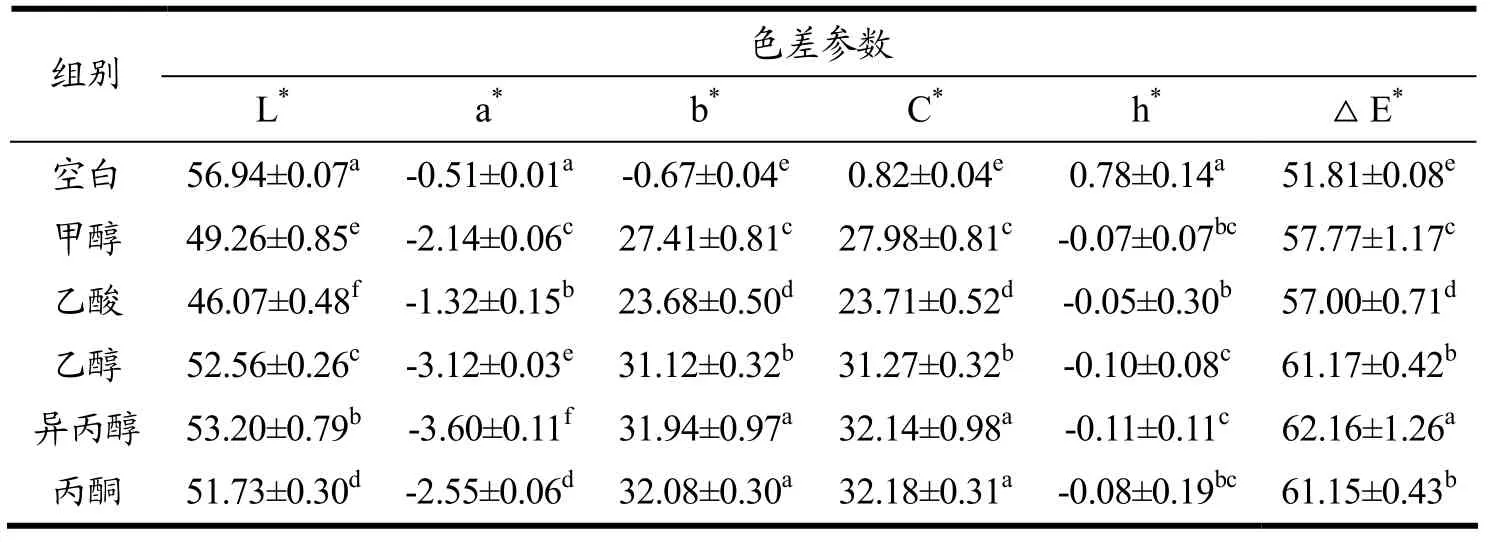
表1 不同溶剂对zein溶液色差的影响Table 1 Effect of different solvents on chromatic aberration of zein solution
2.2 溶剂对zein溶液粒径大小的影响
表2 是zein在不同溶液中的粒径变化情况,从表中可看出,zein溶液的粒径大小随着有机溶剂不同而变化。相同溶剂浓度下,在乙醇溶液中的粒径较小,而在乙酸中的粒径最大。蛋白在溶液粒径大小跟蛋白质的展开程度和蛋白聚集有关。乙酸溶液中,虽然其展开程度较低,但蛋白在该溶液中易聚集,形成了较大的颗粒,70%乙酸溶液中,zein粒径达到5230.16 nm。另外,同溶液中随着溶剂浓度的增加,粒径也发生变化。在甲醇和乙酸溶液,随着溶剂浓度的增加,zein粒径逐渐减小,而在乙醇、异丙醇和丙酮溶液,zein粒径先变小,后变大,80%的乙醇溶液中的zein粒径最小,为25.52 nm。粒径差异与溶剂极性也有关系,蛋白质溶液中不仅存在蛋白之间相互作用,也存在蛋白与溶剂之间的相互作用,溶剂浸入蛋白内部,使蛋白逐渐展开,暴露内部疏水基团,改变蛋白分子的亲水/疏水性[18]。Kim等[17]在研究玉米醇溶蛋白在乙醇水溶液中结构变化时提出:蛋白间疏水作用力不同,会直接导致蛋白质肽链断开与二硫键形成速度不一或者是溶剂极性差异导致了玉米醇溶蛋白极化程度不一样,蛋白亚基间通过非共价键形成大小不一的微聚体[19]。不同浓度的溶液,其亲水/疏水性不同,让蛋白展开的程度和聚集的程度也不同,形成粒子大小有差异。
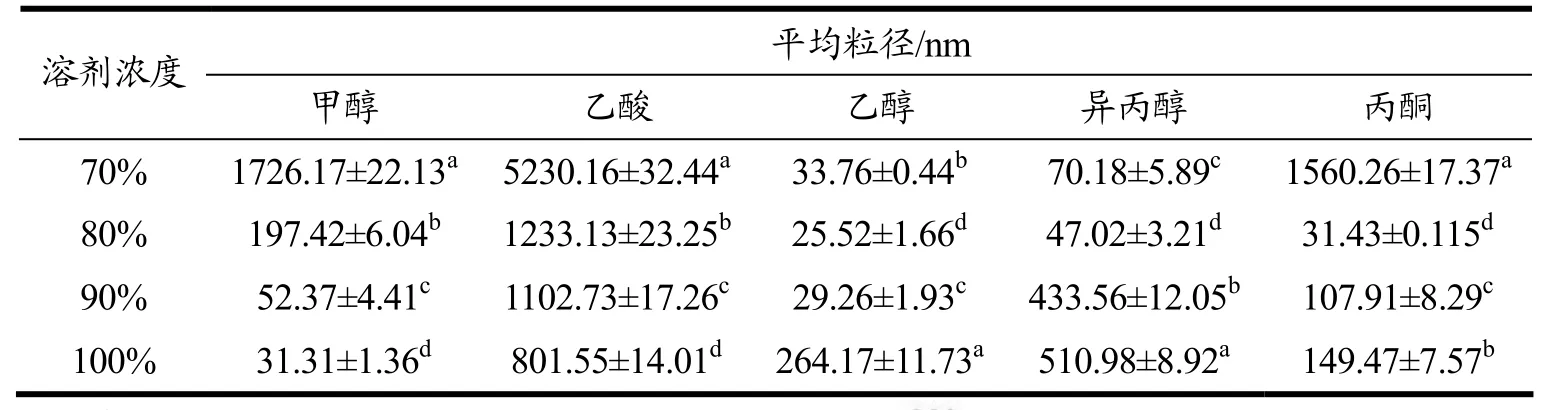
表2 不同溶剂对zein溶液粒径大小的影响Table 2 Effect of different solvents on particle size of zein solution
2.3 溶剂对zein表面疏水性的影响
维持蛋白质分子构象的化学键主要有氢键、范德华力、二硫键、离子键和疏水相互作用力等,而疏水相互作用力对蛋白质三级结构、四级结构的形成与稳定起很重要的作用。疏水相互作用力大小外在表现之一为蛋白的表面疏水性的强弱[6]。
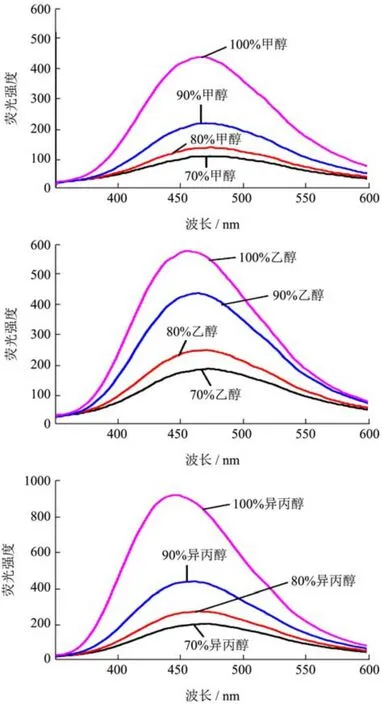
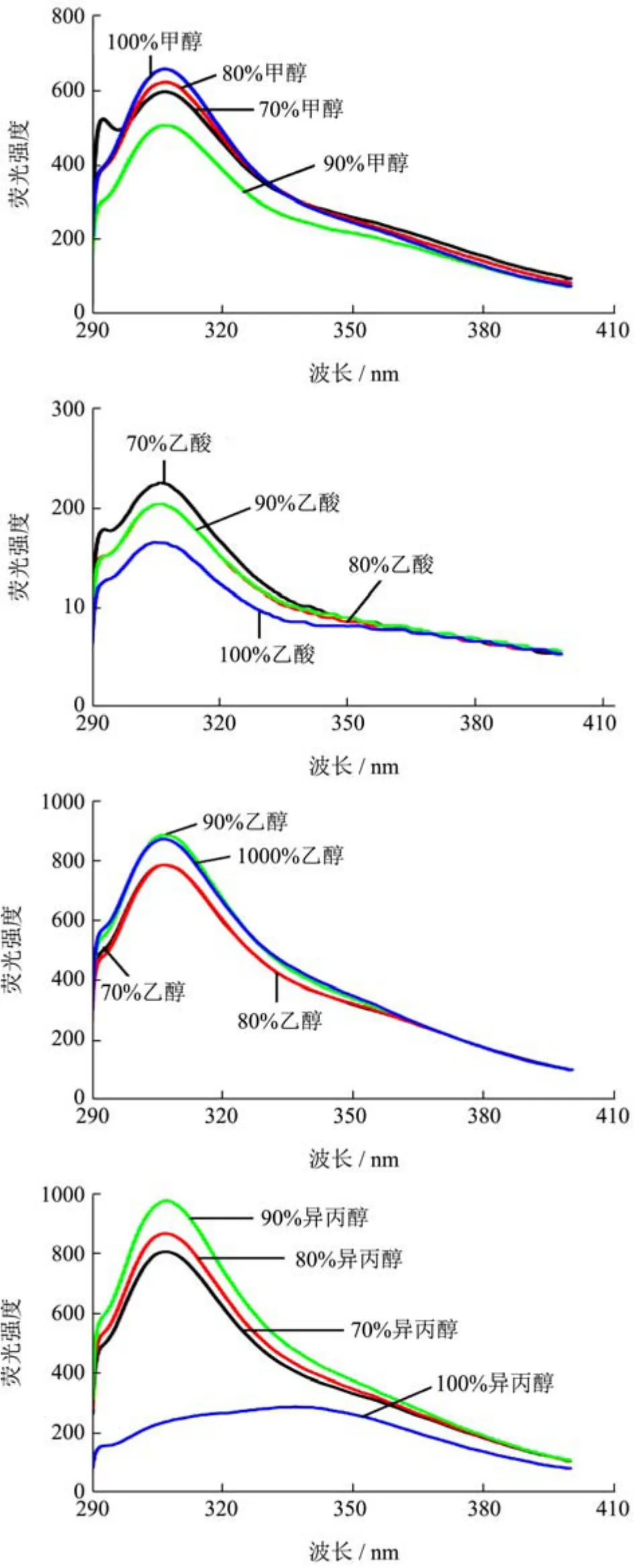
图2 显示zein溶液的内源性荧光吸收光谱最大峰位都在306 nm附近。蛋白质的吸收光谱主要是指色氨酸和酪氨酸吸收值,该值依赖发色团的微环境极性的变化。自然状态下的蛋白质暴露在溶剂中的残基和包裹的基团的吸附效应差异是很小的[20]。因此,不同的蛋白质溶液的吸收值变化不大,在图中表现为峰值位置相近。对于同一种溶剂,不同浓度zein溶液的内源性荧光强度有显著差异。因为当溶剂含量不同,溶液的极性也发生改变,蛋白质展开程度不同,造成荧光吸收值的差异。zein溶于丙酮溶液时,zein蛋白的内源性吸收荧光强度很小,这可能是zein在丙酮溶液中生色基团暴露后重新由于疏水作用聚集在一起,使外露疏水基团减少,引起蛋白溶液荧光强度变小[21]。加入ANS后,ANS与蛋白中的疏水基团结合表现出荧光强度,ANS与蛋白质结合的荧光强度与蛋白质的表面疏水性成正比[22]。图3表明加入荧光探针ANS后,溶液的荧光强度随着溶剂的浓度增大而增大,且不同溶剂处理的zein溶液 ANS荧光强度不同,zein蛋白在乙酸溶液中的荧光吸收最弱,在丙酮溶液中的荧光吸收最强。溶剂使溶液微环境极性发生变化,推测出蛋白质构象发生变化。原因是有机溶剂浓度增大,蛋白分子间疏水相互作用增强,zein结构变得更加松散,疏水长链暴露,有效地改变了zein的表面疏水性,这与Kelly等报道中的结果相符[23]。
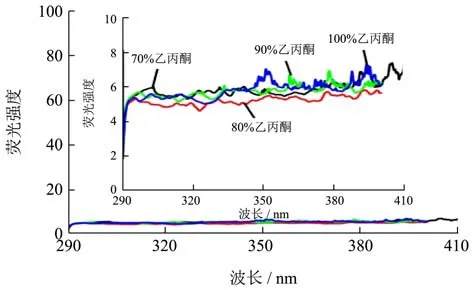
图2 不同溶剂对zein内源性荧光光谱的影响Fig.2 Effects of different solvents on the endogenous fluorescence spectra of zein
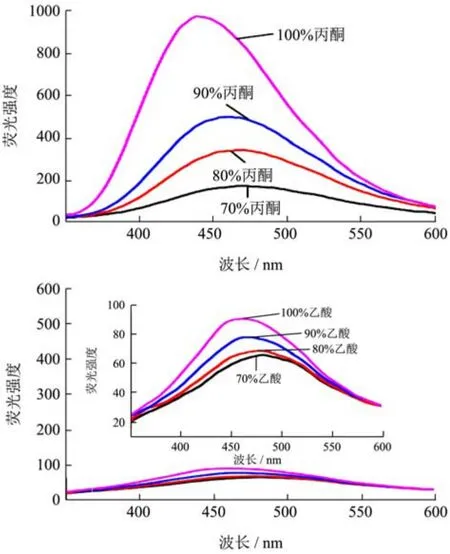
图3 不同溶剂对zein表面疏水性的影响Fig.3 Effect of different solvents on surface hydrophobicity of zein
2.4 溶剂对zein蛋白结构的影响
图4 的紫外光谱扫描结果反应了zein不同溶剂中溶解后化学结构的变化。Zein溶于有机溶剂中,蛋白间巯基形成二硫键以及氢键的作用使其次级结构被破坏,疏水基团去折叠,zein有序的紧密结构变松散无序[20]。图4中丙酮溶解的玉米醇溶蛋白在295 nm处有一吸收宽峰,而其他四种溶剂溶解的玉米醇溶蛋白在278 nm处都有明显的紫外吸收,这主要是紫外吸收峰波长分别为277 nm和285 nm酪氨酸和色氨酸残基的伸缩振动引起的[24]。丙酮、乙酸、异丙醇、乙醇和甲醇处理组的峰强度依次下降,原因可能是羰基和羧基比羟基更有利于zein生色基团的展开。丙酮溶解的zein很有可能还引起了部分苯丙氨酸和半胱氨酸残基向外翻转,暴露于微环境中。紫外光谱分析结果说明zein溶解、聚集状态的变化不仅有溶剂极性大小有关,还与溶剂自身化学结构息息相关,溶剂自身化学结构主要影响蛋白质二、三级结构作用位点[25]。
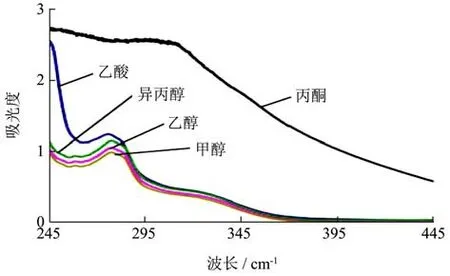
图4 不同溶剂溶解的zein的紫外光谱扫描Fig.4 UV scanning of zein dissolved in different solvents
根据图5中傅里叶红外光谱结果发现,天然zein在1233 nm、1660 nm、2954 nm和3315 nm处有明显的红外吸收峰,分别归因于C-N键、酰胺键、CH2键和N-H键的伸缩振动[6]。Zein溶解在有机溶剂,这些特征红外吸收峰显著降低甚至消失,这可能是溶剂通过氢键和疏水相互作用改变zein多肽链之间的空间构象,从而使蛋白质红外吸收强度降低或消失[26]。此外,处理组在1760~2750 nm范围内有一宽峰,这对应-SH的伸缩振动。说明蛋白质溶解在有机溶剂中,由于溶剂极性和电负性差异,蛋白基团吸附电子能力下降,引起键的断裂,从而溶液中-SH增加。
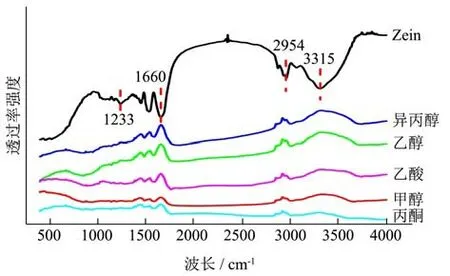
图5 不同溶剂对zein的傅里叶红外光谱分析Fig.5 Fourier infrared spectroscopy analysis of zein in different solvents
2.5 zein蛋白在溶液中表观形貌的研究
从图6-1中可看出,在50倍光学显微镜下,zein蛋白在几种溶液中以球形颗粒状态存在,且颗粒大小和形状略有差异。颗粒之间由“有机膜”链接,这说明蛋白在溶液中发生聚集。进一步用扫描电镜(SEM)观察(图6-2),溶剂诱导zein蛋白在溶液中聚集和自组装。zein蛋白在甲醇溶液中颗粒均匀分散,在异丙醇溶液中是密集分布状态,在乙酸溶液中,颗粒大小和间距最大,分散程度高,而在乙醇和丙酮溶液中颗粒很小。这现象与表2粒径大小的结果一致。这表明不同有机溶剂溶解分散zein的能力不同,这主要是因为不同溶剂极性不同,且它们的主要作用官能团分别是羟基、羧基和羰基,所带电负性不同,从而影响zein蛋白疏水长链的折叠与展开。
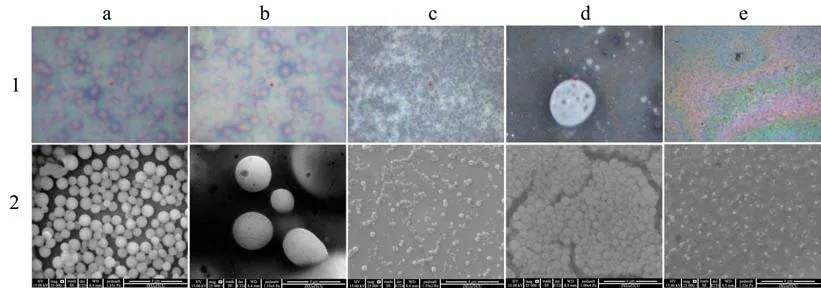
图6 zein在不同溶液的形貌Fig.6 Morphologies of zein in different solutions
2.6 溶剂对zein界面性质的影响
水在不同zein膜上的接触角信息一定程度上也可以反映出溶剂对zein膜的表面疏水性,这可以作为研究zein膜的界面性质[27]。10% zein蛋白(W/V)溶解在不同溶剂中,随着溶剂的蒸发,zein蛋白形成更大的聚集,通过化学键及分子间的相互作用形成薄膜。从图7可看出,从不同溶液中形成的蛋白膜的水接触角具有显著差异,表示形成的膜表面亲水性质差异较大。zein蛋白溶解在不同溶剂中,结构展开程度有差异,当溶剂蒸发时,蛋白分子之间聚集,溶剂分子蒸发速率也不同,形成的蛋白膜除表面形貌上的差异,还有膜表面的亲水性质的差异。溶剂极性差异导致蛋白极化程度和与水的相互作用不同,促使蛋白无定型聚集的过程趋于多元化。介质不同,蛋白分子内部二硫键、氢键和疏水相互作用之间的平衡水平不同,宏观表现为静态接触角和表面疏水性的差异[18]。80%乙酸和乙醇溶解的zein蛋白与容器接触一侧的接触角为88.90°和86.60°,表现出中性润湿性,适合稳定油水界面[28]。另一方面,蛋白膜的性质还跟溶液体系外的环境有关,如成膜时的温度、湿度[29]。特别有趣的是,跟膜接触面也相关。从图7中可以看出,跟容器接触侧的zein膜表面比跟空气侧接触的表面具有更大的水接触角。原因可能是容器侧比空气侧的疏水性更强,因而吸引蛋白疏水基团在该侧聚集,使该膜表面疏水性增加。再者,容器侧表面平整,水分从空气侧蒸发,形成容器侧表面光滑,空气侧表面粗糙的zein蛋白膜。当水滴在空气侧膜表面时,由于水分子的流动性,首先将凸凹不平的表面填平,因此,从滴形上看,其显得更扁平,计算出的接触角更小。图8可直观地看出空气侧和容器侧的zein蛋白膜表面的滴形。从甲醇溶液中形成的膜的空气侧接触角最大,为72.10°。
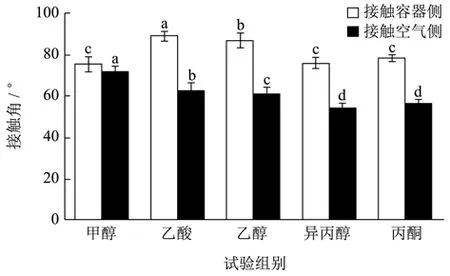
图7 不同溶剂对zein膜接触角的影响Fig.7 Effect of different solvents on the contact Angle of zein film
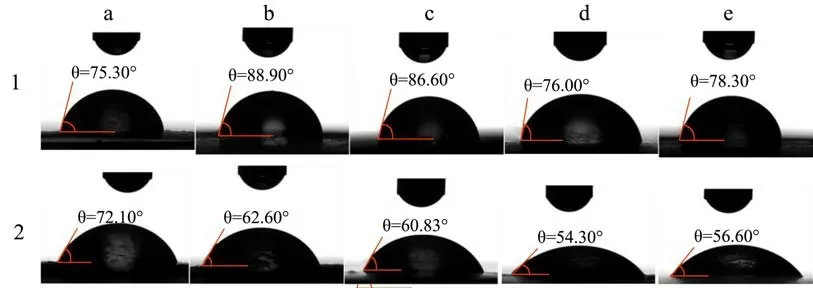
图8 不同zein膜的接触角图;Fig.8 Contact Angle diagram of different zein films
3 结论
玉米醇溶蛋白溶解在甲醇、乙醇、异丙醇、乙酸和丙酮有机溶液中,由于溶剂效应,蛋白质在溶液中折叠和展开程度存在差异,主要体现为蛋白在不同溶剂中的溶解、聚集状态和结构性质的不同。高浓度有机溶剂(>90%)中,蛋白质的水合作用减弱,zein分子趋于聚集,形成较大颗粒;另一方面,蛋白疏水相互作用增强,表面疏水性也增强。就溶剂而言,zein在异丙醇和丙酮溶液的表面疏水性较强,结构松散;而在甲醇和乙酸溶液中表面疏水性较弱,结构紧密。SEM结果表明溶剂诱导zein蛋白在溶液中聚集和自组装成球形颗粒,但颗粒大小和分布不一。Zein蛋白膜表面疏水性不仅跟其在溶液中的展开程度和聚集状态有关,也与成膜时的接触面有关,容器侧形成的膜表面的接触角比空气侧膜表面接触角大,疏水性更强。本文的研究为玉米醇溶蛋白颗粒的形成提供理论依据,对今后玉米醇溶蛋白在生物膜、纳米体系和生物活性物质递送系统方面的进一步研究和应用具有重要的意义。
