利巴韦林抗病毒治疗致重症新冠肺炎患者1例不良反应报道 *
2021-06-18雷贤英高晓岚
雷贤英,高晓岚,刘 勇,王 欢
(西南医科大学附属医院ICU,四川 泸州 646000)
自新型冠状病毒感染肺炎(简称新冠肺炎)疫情暴发以来,研究者就在筛选一些有效的抗病毒药物,有针对性地进行抗病毒治疗。到目前为止,尚无特效的针对新冠病毒的抗病毒药物。利巴韦林作为一种广谱抗病毒药,有报道显示,将其单用或联合其他抗病毒药治疗 SARS 和 MERS 均有一定疗效[1-2]。在国家卫生健康委员会出台的试行第五版《新型冠状病毒感染肺炎诊疗方案》中,首次将利巴韦林列为新冠肺炎的抗病毒治疗药物,接下来第五版《新型冠状病毒感染肺炎诊疗方案》(试行修正版)和第六版《新型冠状病毒感染肺炎诊疗方案》(试行)分别对利巴韦林的用法用量和疗程进行了修正和限定[3-5]。作为一种新的疾病,利巴韦林在新冠肺炎患者中的用药情况鲜有报道。由于重症新冠肺炎患者机体存在多系统、多器官病理生理改变,与轻型和普通型相比,重型/危重型新冠肺炎患者对药物的耐受性和反应存在极大差异,现将1例危重型新冠肺炎患者使用利巴韦林抗病毒致不良反应的临床观察和用药体会报道如下。
1 临床资料
患者,女,68岁,长居武汉,于2020年1月20日从武汉返回泸州,回泸州后因发热伴头昏3+d,于当地行胸部CT检查提示右肺上叶前、后段及右肺下叶基底段渗出改变,行咽拭子荧光逆转录-聚合酶链反应(RT-PCR)检测新型冠状病毒核酸阳性后于1月24日入院。既往有高血压病史10+年,否认糖尿病病史,但最近半年常感口干。查体:体温(T) 38.6 ℃,脉搏(P)128次/分,呼吸 20次/分,血压(BP):178/96 mm Hg(1 mm Hg=0.133 kPa),入院随机血糖14.6 mmol/L,糖化血红蛋白7.3%。诊断为新型冠状病毒肺炎;2型糖尿病;高血压病2级,很高危。
入院后予洛匹那韦利托那韦片、连花清瘟颗粒、血必净抗病毒,防治感染、控制血糖、保肝等对症处理。患者于入院第6天开始病情逐渐加重,体温最高39.8 ℃,脉搏血氧饱和度(SPO2)下降,第8天起呼吸困难明显,期间最低氧分压46 mm Hg,诊断为危重型新冠肺炎,予以呼吸机无创通气和高流量吸氧交替进行呼吸支持,加用甲强龙进行抗炎治疗,并升级抗感染方案,于第13天患者在无创通气和高流量吸氧(吸氧浓度60%)交替呼吸支持下各项体征波动于正常范围,T 37 ℃,P 78次/分,R 26次/分,BP 141/70 mm Hg,SPO299%,辅查各项指标(第13天,2月5日):谷丙转氨酶(ALT)41.9U/L,谷草转氨酶(AST)40.8 U/L,总胆红素14.8 μmol/L,肌酐49.4 μmol/L,血红蛋白(Hb)104 g/L(第16天,2月8日)。鉴于患者咽拭子RT-PCR检查提示新冠病毒载量仍高,遂于第16天(2月8日)加用利巴韦林每次0.5 g,每12小时1次静脉滴注,第17天(2月9日)复查发现患者转氨酶和肌酐水平均升高,ALT 145.2 U/L,AST 42.7 U/L,总胆红素36.6 μmol/L,肌酐88.6 μmol/L,遂于第19天(2月11日)停用利巴韦林,停药后第3天(2月14日)复查Hb较前下降,86 g/L(用利巴韦林前104 g/L),考虑患者目前仍处于肺康复阶段,高流量吸氧维持氧合(流速35 L/min,吸氧浓度30%),为提高红细胞携氧能力,于第23天(2月15日)输注悬浮红细胞2 U提升Hb水平,输血后复查(2月18日)Hb 95 g/L。用利巴韦林前后肝肾功能和Hb变化情况详见图1、2。经过积极的肺康复训练,营养支持,控制血糖,增强免疫等治疗,患者呼吸情况改善,CT示肺部渗出部分吸收(图3、4),连续3次咽试子和1次大便新冠肺炎核酸检测均呈阴性,于第32天(2月24日)好转出院。
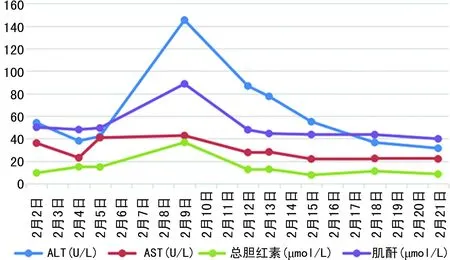
图1 使用利巴韦林(2月8-11日)前后患者相关生化指标的变化
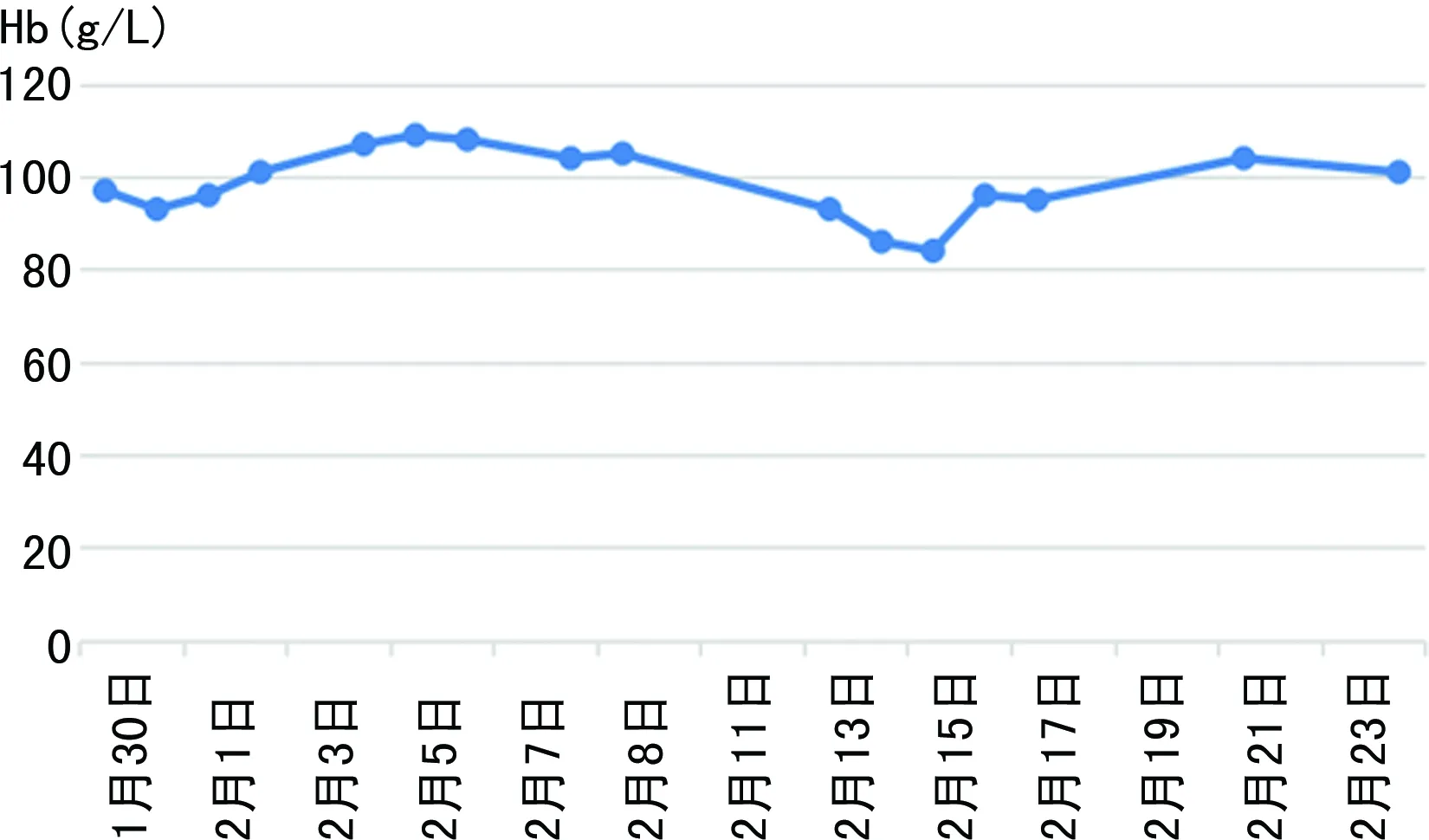
图2 使用利巴韦林(2月8-11日)前后患者Hb变化情况
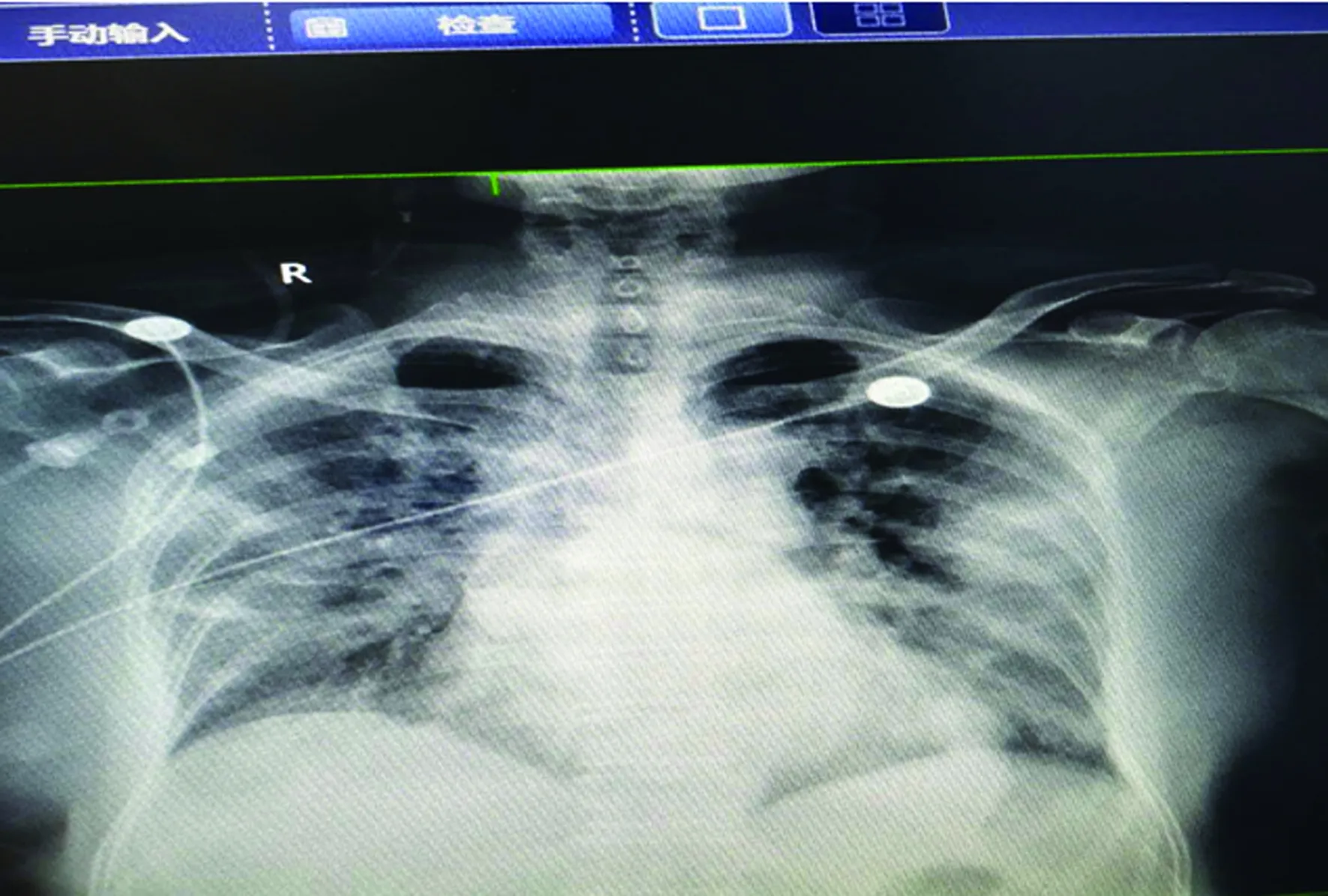
图3 入院第9天(2月1日)胸部X线片情况
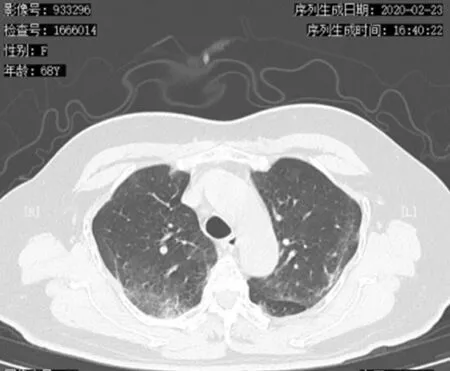
图4 入院第31天CT片情况
3 讨 论
利巴韦林是一种活性强、耐药率低、抗病毒谱广的治疗病毒性传染病的一线药物,其疗效确切、价格低廉[6]。但因其不良反应较多,在一定程度上该药的使用受到了限制。此次抗击新冠肺炎,作为“老药新用”的利巴韦林,成为研究者关注的一个热点。
利巴韦林是一种强效嘌呤核苷酸类似物,其药理机制是通过对肌苷酸-5-磷酸脱氢酶抑制,达到抑制多种 RNA、DNA 病毒复制的作用,干扰病毒的早期转录,如影响mRNA的加帽和延伸,阻碍核糖核蛋白的合成,从而使 RNA 基因发生致死性突变[7]。将SARS-CoV-2 分别与SARS-CoV和 MERS-CoV 的进行全基因组对比,结果显示,其序列相似性约分别为40%和70%,鉴于新型冠状病毒的病理特征同SARS 和 MERS 的冠状病毒基因序列存在相似性,故在临床治疗方面更多参考了 SARS 和 MERS 的治疗。在 2003 年 SARS 暴发期间,中国和加拿大等国家有应用大剂量利巴韦林治疗 SARS能明确降低插管率和死亡率的报道[8]。但利巴韦林用于 MERS 的抗病毒治疗的有效性存在争议。有研究结果显示,利巴韦林治疗MERS 有一定效果,但与利巴韦林组相比,使用洛匹那韦/利托那韦组的死亡率更低[9-10]。一项回顾性队列研究表明,加用利巴韦林辅以其他抗病毒药物治疗MERS,可以显著提高患者的生存率[11]。从以上利巴韦林在 SARS 和 MERS 的临床使用证据及治疗经验来看,将其用于新冠肺炎的抗病毒治疗具有一定的临床疗效。利巴韦林口服制剂不良反应较少、较轻[12],临床使用时可考虑以口服代替注射剂,大剂量利巴韦林的使用主要是口服制剂,但大剂量口服可能导致利巴韦林蓄积。考虑到使用利巴韦林的安全性和有效性,国家卫生健康委员会印发的《新型冠状病毒肺炎诊疗方案》从试行第五版、第五版修正版、试行第六版对利巴韦林的用法、用量、疗程进行了调整,于2020 年 3 月 3 日,国家卫生健康委员会出台了试行第七版)《新型冠状病毒肺炎诊疗方案》[13],将利巴韦林的使用剂量调整为:500 毫克/次(成人),每天 2 ~ 3 次静脉滴注,并限定疗程不超过 10 d,并强调要注意药物的不良反应、禁忌证及与其他药物的相互作用等。
由于利巴韦林有较高的不良反应发生率,在救治新冠肺炎患者的过程中,选用利巴韦林进行抗病毒治疗时,尤其应注意利巴韦林的临床应用,需要严格掌握适应证,用药时应进行严密观察,警惕药品不良反应。本例患者严格按照诊疗方案推荐剂量使用,用药前充分评估了患者各脏器功能良好,使用过程中严密监测肝肾功能、血色素等变化,警惕药物不良反应的发生。利巴韦林常见的不良反应是贫血,较少见的不良反应有头痛、疲倦、失眠、恶心、食欲减退、呕吐等。 利巴韦林几乎不与血浆蛋白结合,药物吸收后迅速分布到身体各部位,进入红细胞后在红细胞内蓄积量大,可在红细胞内蓄积数周。利巴韦林进入血液后,便在红细胞中发生磷酸化,形成 5-三磷酸,由于人红细胞磷酸酶的作用偏弱,因此红细胞内的磷酸化需要较长时间,从而导致大量的利巴韦林存留在红细胞内。利巴韦林发生溶血性贫血的概率与剂量呈正相关,尤其是日剂量超过1 000 mg时。因利巴韦林不会影响骨髓网织红细胞的增生,仅是延迟网织红细胞的成熟进程,故利巴韦林引起的贫血为可逆性,停药后会缓慢上升。据临床观察发现,使用利巴韦林的患者约有 10% 的比例会出现Hb下降到 10 g/dL 以下的情况,尤其是在初始用药的前2周,停药后需要4~8周时间才能逐渐恢复[14]。导致使用利巴韦林后出现严重贫血具有以下高风险因素,如女性、高龄、低体重、低Hb、肾功能损害和预处理使用血小板等。关于利巴韦林对脏器功能的影响,有研究者通过给猪饲喂食高剂量(0.1~0.2 g/kg体重)的利巴韦林,建立利巴韦林致实验猪急性中毒实验动物模型,病理观察显示实验猪的肝脏肿大,有明显淤血现象,色淡、质脆;肾脏明显肿大、有出血,色淡,包膜易剥离,质脆易碎[15]。一项关于利巴韦林在仔猪体内的药物代谢动力学与毒理学研究结果显示,中、高剂量组实验猪的肝、肾、心、骨髓、血液、消化道、胰腺、脑均有明显的组织学改变,肝细胞发生轻微的颗粒变性,见大量含铁血黄素巨噬细胞,肾小管上皮细胞变性坏死,见蛋白管型。该毒理学机制主要与利巴韦林对各组织器官的泛嗜毒性有关[16]。因此,临床上使用利巴韦林时应警惕不良反应的发生,尤其在本身存在肝肾功能异常时应慎用。
此例危重型新冠肺炎患者在使用利巴韦林后,迅速出现脏器损害表现,转氨酶、胆红素、肌酐水平短时间内迅速升高,并出现Hb水平下降。经停用该药后,肝肾功能逐渐恢复,经输血治疗后Hb水平稳定。探究重症新冠肺炎患者使用利巴韦林抗病毒后迅速出现溶血、肝肾功能损害等不良反应原因和机制,考虑与以下2个因素有关:(1)新冠病毒本身对机体多系统、多脏器有损害。感染新冠病毒后,病毒首先与细胞膜上的血管紧张素转换酶 2(ACE2)结合,导致机体局部或全身发生氧化应激、炎性反应,从而导致组织、细胞缺氧,这是新冠病毒感染机体后的基础病理生理机制。而病程的最终发生、发展和转归,则由机体的炎症和抗炎反应的斗争和抗衡结果而定,轻型患者可无明显的临床表现,重型/危重型患者则会进展为休克、难以纠正的代谢性酸中毒、凝血功能障碍、急性呼吸窘迫综合征(ARDS)和多器官功能衰竭等,甚至导致患者死亡[17]。该例患者经过前期的积极处理后,已度过炎症风暴期,经评估,患者肺功能尚未恢复,需要交替进行无创通气和高流量吸氧来维持氧合,在呼吸支持下,患者各项体征和肝肾功能等尚稳定,为促进体内病毒清除,在此阶段加用了利巴韦林,在使用利巴韦林后,患者迅速出现药物不良反应。患者在用药后短时间内即出现脏器的损害和Hb水平下降的不良反应,考虑同患者新冠病毒感染后机体本身的重症状态有关,即患者处于重型/危重型的阶段本身应作为纳入使用利巴韦林的高风险因素的评估条件之一。导致重症新冠肺炎患者使用利巴韦林抗病毒后迅速不良反应的因素二:重症新冠肺炎患者的低氧血症。新冠病毒感染机体的基本病理生理机制是病毒与人体细胞膜上的ACE2结合,ACE2在人体各个组织中均有表达,最丰富的是在肺泡上皮上表达[18]。但此次新冠肺炎患者的感染多以肺部为主要表现,重型/危重型患者临床上主要表现为低氧血症。从重症新冠肺炎患者的肺部病理解剖可以看出,由于肺泡腔内大量浆液渗出,肺泡形成透明膜,肺泡间隔血管充血、水肿伴灶性肺组织出血、坏死、机化和肺间质纤维化。因此,肺作为新冠病毒感染后受损害的首要靶器官,发生低氧血症是重症新冠肺炎的典型临床特征之一。此例患者在使用利巴韦林期间呼吸衰竭尚未纠正,持续在呼吸机和高流量氧疗仪交替使用进行呼吸支持下氧合指数为234(氧分压117 mm Hg,吸氧浓度50%),在机体的这种缺氧状态下,使用利巴韦林不良反应大的风险会大大增加,因此使用该药务必严密监测Hb和肝肾功能等相关指标,当发现该例患者出现不良反应后,即刻予以停药,并予以对症处理,为防止贫血和低氧血症给患者带来双重打击,影响预后,随即予以输注悬浮红细胞增加机体的携氧能力,以增加氧供。经一系列积极处理后,患者的Hb未再下降,肝肾功能也恢复正常。
综上所述,鉴于利巴韦林本身的药理学特点和不良反应的存在,将其用于轻型、普通型患者的适应证偏广,而用于重型、危重型新冠肺炎抗病毒治疗时,应充分评估重症患者使用该药的高风险因素,如患者的基础疾病、机体缺氧的程度和器官功能的状态等,充分考虑患者对药物的耐受性和反应性,评估用药的利与弊;同时,在用药的过程中,务必密切监测患者的血常规、肝肾功能等情况,及时发现药物的不良反应,一旦发现不良反应,及时停药并予以对症处理。新冠肺炎作为一个人类面临的新的疾病,也给研究者们带来了新的挑战,基于对利巴韦林药物不良反应的考虑,尤其是针对不同的COVID-19分型患者,结合其器官功能耐受性不一样,采用同一剂量、同一疗程也存在一定的争议。建议在真实世界环境下进一步明确利巴韦林对重型/危重型新冠肺炎患者用药的安全性和对长期预后影响的评估。
