CT造影剂对脑动静脉畸形VMAT计划剂量分布的影响
2021-06-03邓官华李少群周巧敏罗日顺张平戴鹏罗龙辉赖名耀山常国蔡林波
邓官华,李少群,周巧敏,罗日顺,张平,戴鹏,罗龙辉,赖名耀,山常国,蔡林波
广东三九脑科医院肿瘤综合治疗中心,广东广州510510
前言
脑动静脉畸形(Arteriovenous Malformation,AVM)是一种先天性局部脑血管发育异常的血管团[1],大体上AVM呈现为相互缠绕的血管,常有一个局限中心团以及引流静脉,并且在AVM中不含脑实质[2]。临床上为了更准确地勾画AVM病灶及危及器官(Organs-at-Risk,OAR),通常会在CT扫描过程中静脉注射造影剂。然而在实际治疗阶段,脑血管中的CT造影剂早已代谢清空,AVM病灶等血供丰富组织的CT值会有较大幅度下降,经过CT-电子密度曲线转化后计算放疗计划剂量分布时会产生一定误差。相关的研究发现静脉注射CT造影剂对放疗计划剂量分布的影响较小,临床上可忽略[3-5];但同时也有研究表明在增强CT图像上设计放疗计划会导致患者接受的实际剂量偏高[6-8]。针对目前静脉注射CT造影剂对AVM患者放疗计划剂量分布影响的系统研究国内报道较少,本研究将主要探讨在AVM容积旋转调强(Volumetric Modulated Arc Therapy,VMAT)计划中,因使用CT造影剂导致组织CT值增大所引起的剂量计算误差。
1 资料与方法
1.1 病例选取
选取广东三九脑科医院肿瘤综合治疗中心2017年1月至2020年1月收治确诊为AVM的15例患者为研究对象,其中,男9例,女6例,年龄8~48岁,肿瘤体积为0.4~32.0 cm3。
1.2 设备仪器
定位CT为SIMENS 64排大孔径螺旋放疗专用CT(SOMATOM Definition AS);放疗计划系统为VARIAN Eclipse 13.6;治疗机为VARIAN UNIQUE直线加速器,配备120片全自动独立多叶准直器(Multi-Leaf Collimator,MLC),中间80片MLC宽度为0.5 cm,其余MLC宽度为1.0 cm,射线能量为6 MV光子。
1.3 CT扫描
患者采取仰卧位,用Brainlab专用头架和热塑面膜固定(科来瑞迪,R408),扫描层厚1.5 mm,层间距0 mm,电压120 keV,电流350 mAs。扫描范围:上界至颅顶,下界至第二颈椎。先获取平扫CT图像(C-),通过计算机内置设定,在相同体位下行增强扫描(C+),最终将两次CT图像传输到放疗计划系统Eclipse 13.6。CT造影剂为碘克沙醇(威视派克,通用电气药业(上海)有限公司),采用高压注射器经手臂以2 mL/s注射速度静脉注射60 mL造影剂,延时35 s扫描。CT扫描过程中,嘱咐患者保持体位固定,并将耳环、假牙等摘除[9]。
1.4 靶区勾画和计划设计
通过VARIAN Eclipse工作站的图像配准功能对两组CT图像进行配准。放疗医生根据AVM介入治疗欧洲专家共识等的推荐[10],在增强CT图像上勾画计划靶区(Planning Target Volume,PTV)和OAR,其中OAR包括晶体、眼球、视神经、视交叉、脑干以及感兴趣区域(Region of Interest,ROI)。待医生勾画完PTV和OAR后,物理师将上述结构复制至平扫CT图像。
所有放疗计划均采用VMAT技术照射,5条非共面弧,如图1所示。为了避免叶片引起的凹凸论效应,适当调整MLC角度[11]。采用各向异性分析算法计算照射区域剂量,PTV处方剂量为16 Gy/次。正常组织约束条件为:晶体Dmax<3 Gy,视神经Dmax<10 Gy,延髓Dmax<10 Gy,脑干Dmax<10 Gy[12]。VMAT计划优化完后由医生评估确认,并以此治疗计划作为模板计划。打开平扫CT图像,插入先前保存的模板计划,不进行通量优化,重新计算剂量分布。模板计划使得平扫CT图像的弧条件、处方剂量以及计算方法与增强CT图像一致。所有生成VMAT计划仅限于实验参数比较。

图1 脑动静脉畸形(AVM)VMAT计划设计示意图Fig.1 Schematic diagram of volumetric modulated arc therapy plan for arteriovenous malformation(AVM)
1.5 剂量学评价
比较两组计划的PTV、OAR和正常组织的剂量分布。PTV的剂量评价包括D2%、D98%、Dmean以及剂量分布的适形度、均匀性和跌落速度。剂量分布的适形度、均匀性和跌落速度分别用适形度指数(Conformity Index,CI)、均匀性指数(Homogeneity Index,HI)以及梯度跌落指数(Gradient Index,GI)来表示。CI、HI及GI计算公式如下[13-15]:

其中,TVPV为接受处方剂量照射的PTV体积,TV为PTV体积,PV为处方剂量照射的体积,D2%为2%PTV体积的受照射剂量,D98%为98% PTV体积的受照射剂量,Dmean为PTV的平均剂量,V50%为50%处方剂量线包裹体积,V100%为处方剂量线包裹体积。
同时记录晶体、眼球、视神经、脑干的Dmax以及正常组织受照射体积(V2Gy、V10Gy、V12Gy)。
1.6 统计学方法
采用SPSS 21.0对数据进行统计学分析,计量资料采用均数±标准差表示,采用非参数配对Wilcoxon检验,P<0.05为差异有统计学意义。
2 结果
图2为AVM患者的增强和平扫CT图像,CT值的改变如表1所示。在ROI(粉红色区域,脑血管)处CT值增大明显,大约平均增加110 HU;PTV(绿色区域)CT值有所增大,大约平均增加50 HU。眼睛、脑干等造影剂尚未到达区域,CT值增大不明显。
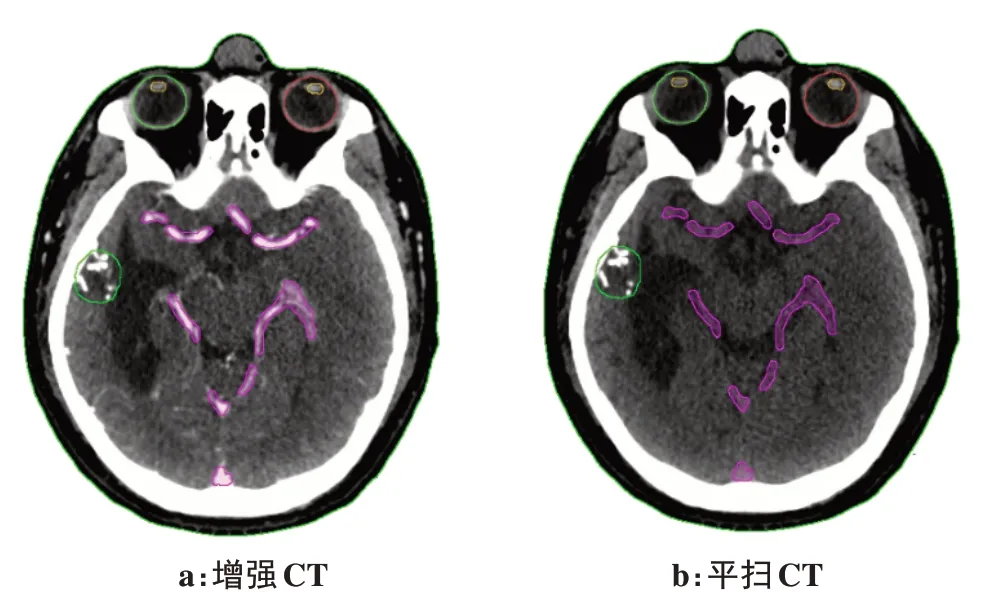
图2 AVM患者的增强和平扫CT图像Fig.2 Contrast enhanced CT image and non-enhanced CT image of AVM patient
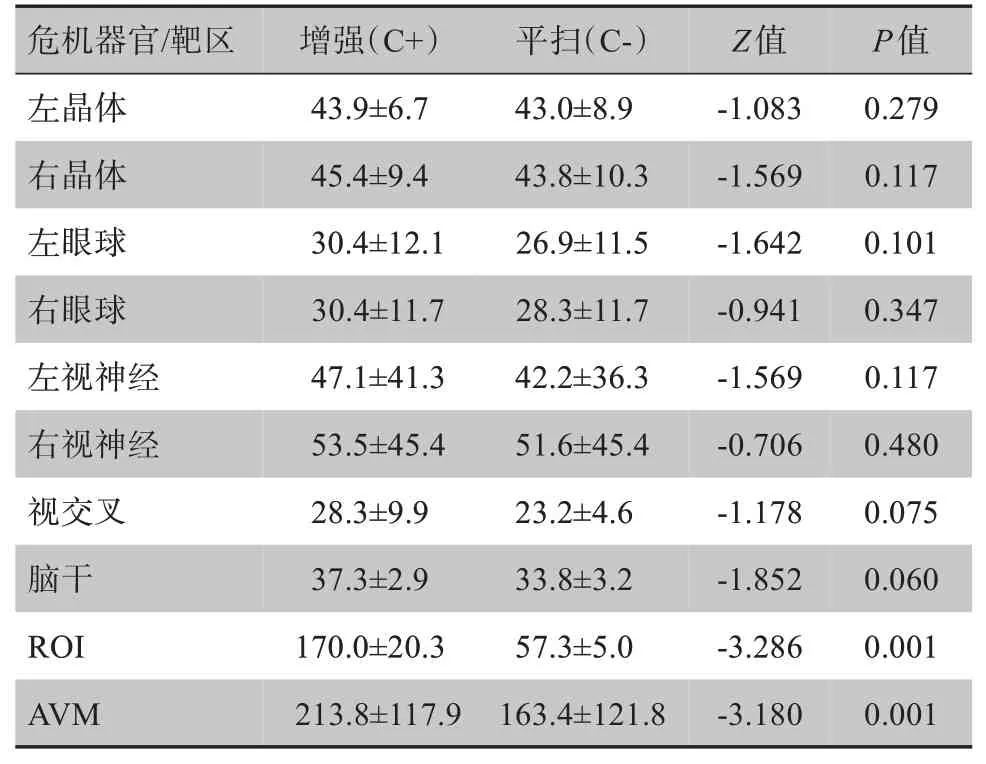
表1 增强和平扫图像的CT值比较(HU)Tab.1 Comparison of Hounsfield unit between contrast enhanced CT image and non-enhanced CT image(HU)
图3为增强和平扫CT图像的CI、HI及GI的箱线图。增强和平扫CT图像的CI分别为0.82±0.08和0.83±0.07;HI分别为7.88±2.25和8.33±1.07;GI分别为5.25±2.76和5.14±2.26。两组图像的CI、HI及GI差异均无统计学意义(P>0.05)。

图3 增强和平扫CT图像的CI、HI以及GI比较Fig.3 Comparison of conformity index,homogeneity index and gradient index between contrast enhanced CT image and non-enhanced CT image
表2为增强和平扫CT图像的PTV、OAR及正常组织剂量参数表,两组图像的PTV、OAR及正常组织间的剂量学参数差异小于2%,且无统计学意义(P>0.05)。
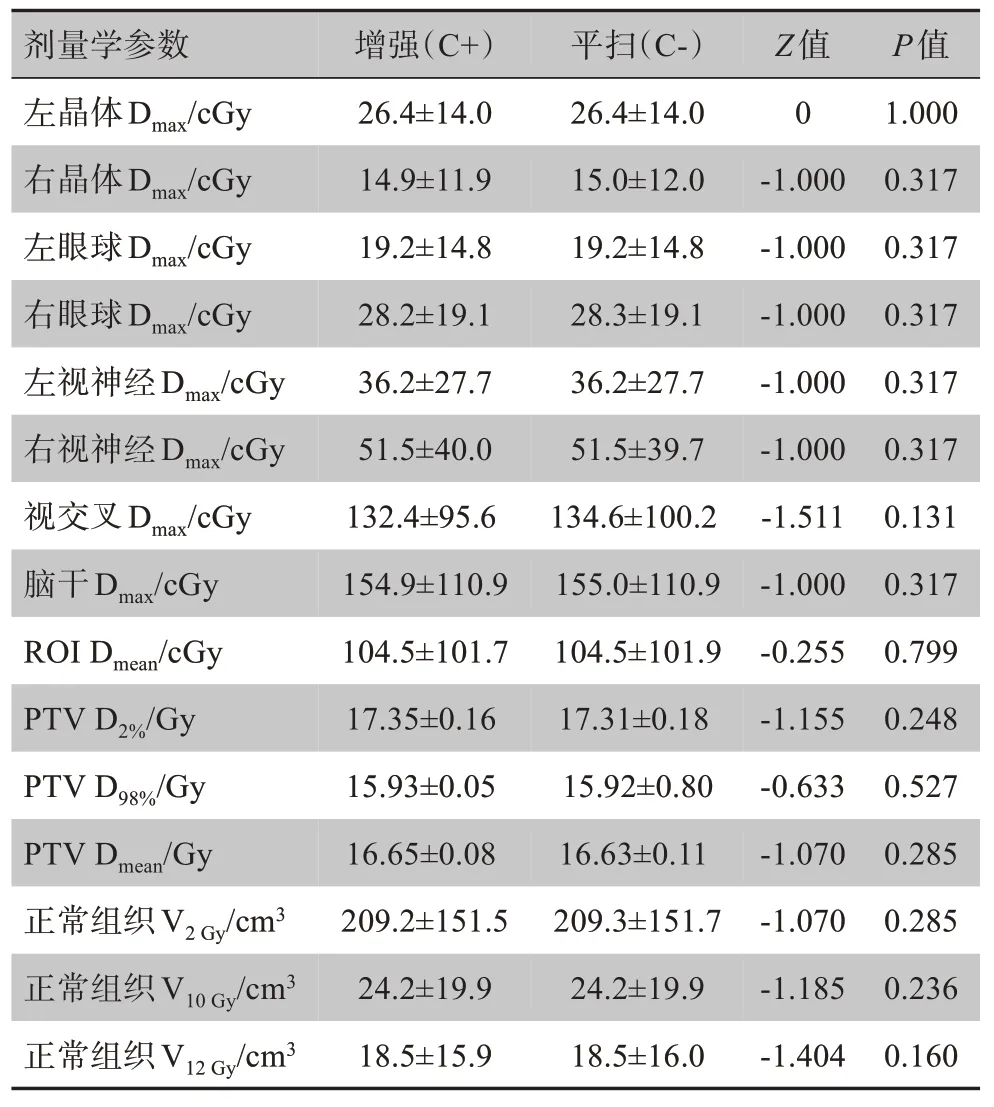
表2 增强和平扫图像的剂量学差异比较Tab.2 Dosimetric comparison between contrast enhanced CT image and non-enhanced CT image
3 讨论
AVM是指由脑血管先天发育障碍引发的脑局部血管数量和结构异常,常伴有供血动脉增粗迂曲,血流加快[16]。AVM最为常见和最为严重的并发症是颅内出血,病死率高达30%[17]。采取不开颅、无创伤的立体定向放疗可降低颅内出血率,改善临床症状,是一种较为理想的治疗方式。对AVM患者行大剂量的立体定向放疗的关键在于准确勾画PTV和OAR。因此,在CT扫描过程中需静脉注射造影剂,以提高脑血管与周围脑组织的对比度。
目前的放疗计划系统是建立在组织CT值基础之上,通过CT-电子密度转换曲线来进行剂量计算[18-21]。CT值的大小反映了X射线在人体内不同密度组织线性衰减的强弱。CT值越小,线性衰减系数越小,组织对X射线的衰减越弱,即相当于有更多的X射线穿过组织[22]。高原子序数的造影剂经静脉进入脑血管等血供丰富的组织中,使各组织的CT值增大,对X射线的衰减增强,但这种衰减在临床上是否具有意义,目前学术界尚未有统一结论。王艳霞等[6]的研究表明CT造影剂对中上段食管癌患者的调强放疗计划有影响,在设计动态调强放疗计划时,改变增强CT图像中大血管内的电子密度,能够有效降低肺等危机器官的受照射剂量。杨晓霞等[7]发现CT造影剂会影响胸腹部肿瘤患者三维适形计划的等中心点剂量。然而也有研究表明CT造影剂对放疗设计剂量分布的影响有限,临床上可忽略。林志安等[3]发现造影剂对食管癌调强放疗计划剂量分布的影响有限,可直接在增强CT图像上设计放疗计划。朱鹭超等[4]研究结果表明在食管癌三维适形放疗中使用CT造影剂对放疗剂量分布影响较小,均在临床接受范围内。Shibamoto等[23]发现CT造影对剂量分布的影响与解剖部位有关。
目前静脉注射CT造影剂是否对AVM的VMAT计划剂量分布产生影响的系统研究国内报道较少,因此本研究针对上述问题进行了系统的分析,结果发现,虽然增强和平扫图像在PTV和ROI的CT值上存在统计学差异(PTV约平均增加50 HU;ROI约平均增加110 HU),但是这种CT值差异并没有导致剂量学的差异。此外,本研究还发现两组计划的CI、HI、GI和OAR剂量等均无统计学差异。究其原因,有以下几方面:(1)相对于胸腹部肿瘤而言,脑组织血管虽然密集,但大血管数量较少,血流量相对没那么丰富,造影剂流经范围没这么大[23],所以增强和平扫图像OAR的CT值差异并没有统计学意义;(2)本研究中约有90%的AVM患者行过栓塞手术治疗,造影剂无法通过脑血管大量进入靶区内,使得PTV的CT值差异(50 HU)在经过CT-电子密度曲线转换后无法形成剂量学差异[24];(3)即使造影剂进入血流相对丰富的脑组织,导致增强图像的CT值高于平扫图像,但是只要VMAT计划的弧不经过或者较短时间内经过血管密集脑组织,那么这种由于注射造影剂带来的CT值差异也不会造成剂量学的影响。此外,相对于胸腹部因呼吸运动导致的OAR位移较大,AVM患者由于头部骨骼的存在,颅内OAR移动相对较小。加上患者采用热塑面膜固定,且平扫和增强两幅图像采集时间较短,避免了患者在CT扫描期间的不自主移动,因此本研究不考虑图像配准阶段引入误差的影响。综上所述,对于行过栓塞手术治疗的AVM患者,使用CT造影剂对VMAT计划的PTV及OAR剂量分布影响很小,临床上可忽略。
本研究只探讨了CT造影剂对行过栓塞手术治疗的AVM患者VMAT计划剂量分布的影响,考虑到三维适形放疗或调强放疗计划的射野角度是否穿过脑血管,穿过脑血管的射野在总剂量中的贡献度以及AVM患者是否行过栓塞手术等都有可能造成研究结果的差异,因此对于三维适形放疗及调强放疗计划是否具有相同的结论,还需作进一步研究。
4 结论
本研究探讨CT造影剂对AVM的VMAT计划剂量分布的影响,发现在PTV和ROI处,虽然增强图像的CT值显著高于平扫图像,但两组计划的剂量学参数并没有统计学差异。因此,临床上对行过栓塞治疗的AVM患者可用增强CT代替平扫CT进行PTV勾画和VMAT计划设计。
