儿童髓母细胞瘤合并Gorlin-Goltz综合征八例
2021-05-27张新颜李建康RaynaldLiu李亚农张冰克孙黎明邱晓光李春徳
张新颜 李建康 李 伟 Raynald Liu 杨 宝 李 苗 李亚农 张冰克 孙黎明 邱晓光 姜 涛 李春徳
髓母细胞瘤是一种病变位于后颅窝的高度恶性肿瘤,约占儿童期中枢神经系统肿瘤的20%[1]。2016年版世界卫生组织病理分型系统将其分为5个病理亚型:经典型(classic)、促纤维增生/结节型(desmoplastic/nodular)、广泛结节形成型(medulloblastoma with extensive nodularity,MBEN)、大细胞型(large cell)和间变型(anaplastic)。其中大细胞型和间变型因预后较差,统称为LC/A亚型[2-4]。国内外统计显示,髓母细胞瘤患者的5年存活率为50%~70%[5,6]。近年来髓母细胞瘤的研究方向已经深入基因层面,根据肿瘤细胞基因突变情况、甲基化情况对髓母细胞瘤进行分子分型,共分为4个亚型:WNT亚型、SHH亚型、Group 3亚型以及Group 4亚型。临床通过分子分型、患者年龄、病理类型、是否转移等将髓母细胞瘤分为不同危险等级,给予不同放化疗组合方案。
部分髓母细胞瘤患者存在基因胚系突变,可导致遗传性综合征,最常见为Gorlin-Goltz综合征(Gorlin-Goltz syndrome,GS综合征),又称之为痣样基底细胞癌综合征(nevoid basal cell carcinoma syndrome,NBCCS,MIM #109400),属于临床少见的常染色体显性遗传性疾病[7]。GS综合征相关髓母细胞瘤属于SHH亚型髓母细胞瘤首选化疗,多预后良好[8]。国内对于髓母细胞瘤相关的GS综合征认识及治疗方案尚不统一。本研究分析了2014年1月至2021年1月首都医科大学附属北京天坛医院收治的8例GS综合征临床资料,以提高对该病的认识。
材料与方法
一、一般资料
本研究获得首都医科大学附属北京天坛医院伦理委员会批准(KY2019-098-1)。8例中,男4例,女4例;7例年龄在3岁以下(9~36个月,平均19个月),1例9岁。临床表现:3例头围增大,7例呕吐,5例走路不稳。患者5及患者7被纳入本课题组既往研究中[8]。
二、手术情况及病理分型
8例均行肿瘤切除手术,其中2例首次手术为大部切除术,复发后行二次手术(病例7首次手术和病例5复发后再次手术为本院手术,其他均为外院手术)。根据病理报告,7例为促纤维增生/结节型,1例为广泛结节形成型。
三、分子分型
采用泛生子公司的分子分型平台,通过检测髓母细胞瘤相关的 39 个基因(APC/ARID1B/BCOR/CDH1/CDK6/CHD7/CREBBP/CSNK2B/CT-DNEP1/CTNNB1/DDX31/DDX3X/GABRG1/GFI1/GFI1B/GLI2/GPS2/KDM4C/KDM6A/KMT2B/LDB-1/MLL3/MYC/MYCN/NCOR2/OTX2/PIK3CA/PTC-H1/PTCH2/PTEN/SMARCA4/SMARCC2/SMARCD-2/SMO/SNCAIP/SUFU/TERT/TP53/ZMYM3)点突变、插入、缺失和5个基因(CDK6/GLI2/MYC/MYCN/OTX2)拷贝数变异情况,通过低深度全基因组测序检测大片段缺失/扩增结果(1p/2q/3q/4p/4q/13p/21q)预测髓母细胞瘤四种分子分型。
四、Gorlin-Goltz综合征诊断标准
采用2011年修订版Gorlin-Goltz综合征诊断标准,包括6个主要标准和6个次要标准。主要标准包括: ①超过2个基底细胞癌,或患者在20岁之前患有基底细胞癌; ②牙源性角化囊肿; ③3个及以上的掌跖坑状凹陷; ④大脑镰或小脑幕钙化; ⑤分叉肋或融合肋; ⑥家族中一级亲属患有痣样基底细胞癌综合征(Gorlin-Goltz syndrome,GS综合征)。次要标准包括: ①颅骨畸形:巨头畸形、眶距增宽; ②先天性面部畸形:唇裂或腭裂; ③其他骨骼畸形:高位肩胛、胸骨畸形和并指畸形; ④影像学表现:脊柱畸形、手脚畸形; ⑤卵巢纤维瘤; ⑥髓母细胞瘤。患者需满足两条主要标准,或者一条主要标准和两条次要标准,或者一条主要标准伴基因检测结果阳性,即可诊断为Gorlin-Goltz综合征。随访从手术切除肿瘤开始,至末次随访或者患者死亡时结束,随访方法为电话随访结合门诊复诊。
五、基因检测解读标准
使用4种数据库对已鉴定的变异进行频率过滤:1000 Genomes Project (http://browser.1000genomes.org/),dbSNP (http://www.ncbi.nlm.nih.gov/projects/SNP/),ESP6500(http://evs.gs.washington.edu/EVS/),ExAC (http://exac.broadinstitute.org)。潜在致病变异使用以下3种方法预测:Sorting Intolerant from Tolerant (SIFT,http://sift.jcvi.org/),Polymorphism Phenotyping v2 (PolyPhen-2,http://genetics.bwh.harvard.edu/pph2/),MutationTaster software (http://www.mutationtaster.org/)。最后,剩下的变异使用ClinVar (https://www.ncbi.nlm.nih.gov/clinvar/),HGMD(http://www.hgmd.cf.ac.uk/ac/index.php) 数据库,结合潜在的有害性影响、基因型-表型关系分析、文献报道以及“ACMG遗传变异分类标准与指南”,将相关变异分为“致病的”、“可能致病的”、“意义不明确的”、“可能良性的”和“良性的”5类。
结 果
一、临床预后
截至2021年2月,患者平均随访38个月(1~78个月),1例围手术期因肺部感染死亡,其余7例均存活。7例中,手术后单纯放疗2例,单纯化疗4例,放疗+化疗1例。2例肿瘤复发,目前化疗中。1例发病时3岁,因后颅窝肿瘤手术切除,给予全脑脊髓放疗(全脑脊髓轴放疗30.6 Gy,瘤床55.0 Gy),手术后5年因颌骨囊肿于外院口腔科手术治疗,其后发现头皮基底细胞癌行切除手术。
二、基因检测和Gorlin-Goltz综合征诊断结果
除病例2外,7例接受基因检测,其中SUFU基因胚系突变4例,PTCH1基因胚系突变2例,PTCH2基因胚系突变1例,均可明确诊断为Gorlin-Goltz综合征。2例无分子分型结果,其余均为SHH亚型。见表1。
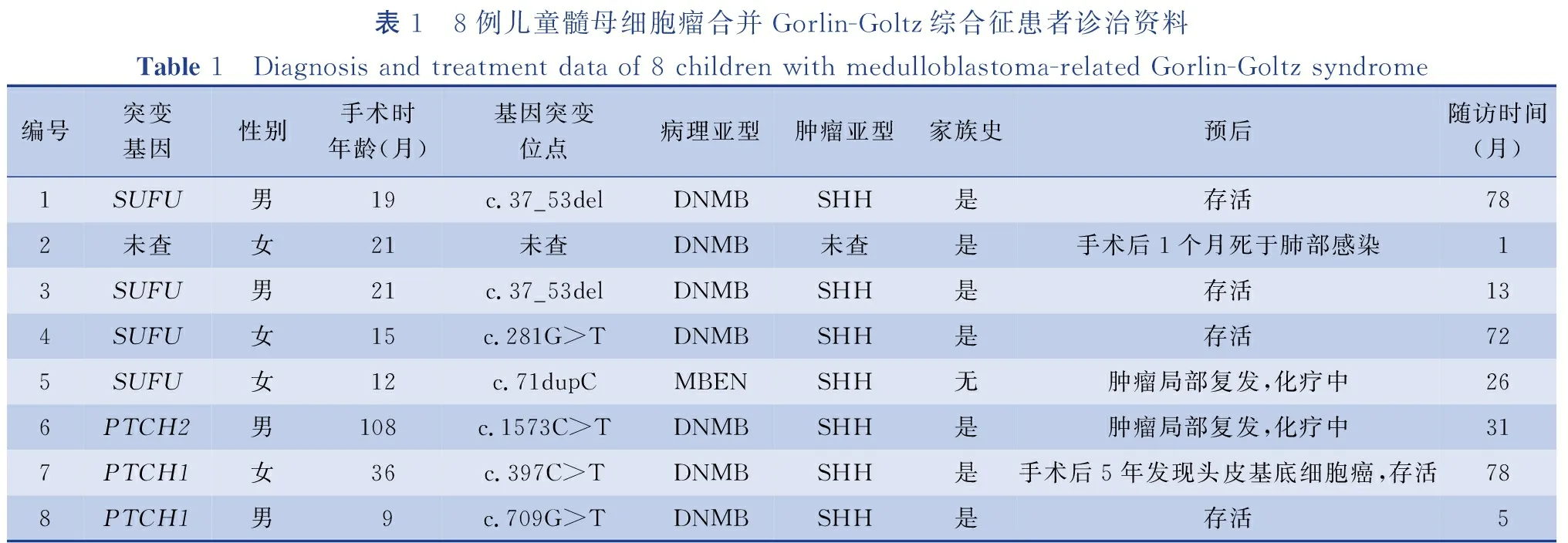
表1 8例儿童髓母细胞瘤合并Gorlin-Goltz综合征患者诊治资料Table 1 Diagnosis and treatment data of 8 children with medulloblastoma-related Gorlin-Goltz syndrome编号突变基因性别手术时年龄(月)基因突变位点病理亚型肿瘤亚型家族史预后随访时间(月)1SUFU男19c.37_53delDNMBSHH是存活782未查女21未查DNMB未查是手术后1个月死于肺部感染13SUFU男21c.37_53delDNMBSHH是存活134SUFU女15c.281G>TDNMBSHH是存活725SUFU女12c.71dupCMBENSHH无肿瘤局部复发,化疗中266PTCH2男108c.1573C>TDNMBSHH是肿瘤局部复发,化疗中317PTCH1女36c.397C>TDNMBSHH是手术后5年发现头皮基底细胞癌,存活788PTCH1男9c.709G>TDNMBSHH是存活5
三、典型病例
表1中病例1、病例2和病例3属于同一家族(图1至图3),手术时年龄分别为19个月、21个月、21个月,手术前均表现出“呕吐、进食差、行走不稳”等颅内压升高、小脑受压症状,行头颅CT/MRI等检查,发现后颅窝病变,合并梗阻性脑积水,于外院行肿瘤近全切除,病理结果均为促纤维增生/结节型髓母细胞瘤。病例2手术后出现肺部感染,于围手术期死亡。病例1和病例3于外院继续化疗,定期复查,随访过程中未见肿瘤复发。病例1、病例3于我院行基因检测,明确诊断为SUFU基因胚系突变,结合发病年龄、病理诊断和基因检测,明确诊断为GS综合征。病例2手术时未行基因检测,但结合其病理诊断和家属史可确诊GS综合征。我们对以上3例患者的部分家族成员行头颅CT检查,发现颅内大脑镰、小脑幕等异常钙化,可以明确诊断为Gorlin-Goltz综合征。
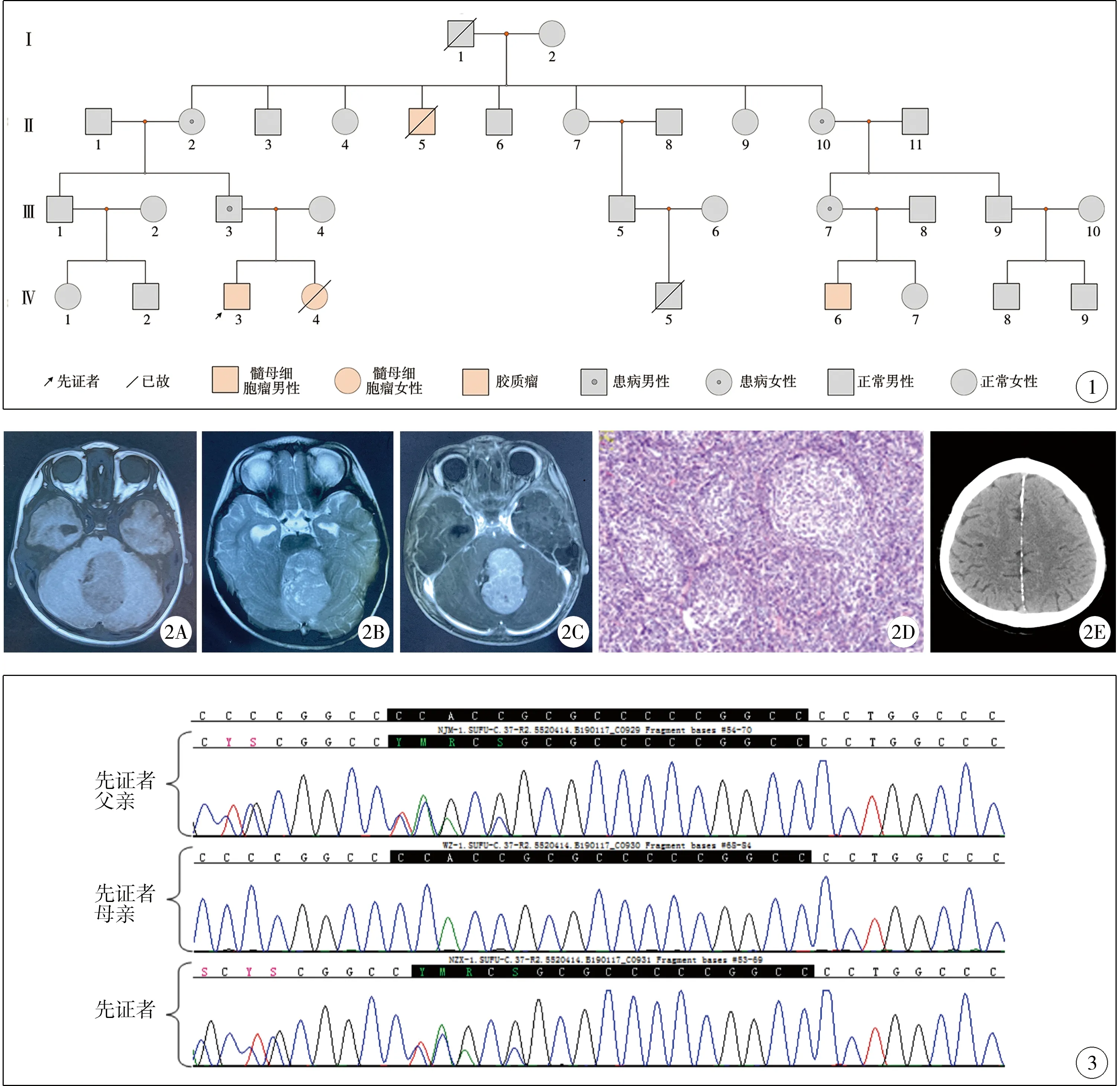
图1 髓母细胞瘤合并Gorlin-Goltz综合征患者家系图 图2 患者1的影像学和病理学检查图片 注 19月龄男性患者,肿瘤位于第四脑室,T1加权MRI可见病变位置呈低信号(A), T2加权MRI高信号,肿瘤强化明显(B、C);病理诊断为促纤维增生/结节型髓母细胞瘤(D);患者父亲头颅CT见大脑镰钙化明显(E) 图3 SUFU基因突变检测结果,先证者、先证者父亲可见突变,先证者母亲突变检测结果阴性
讨 论
GS综合征在婴幼儿髓母细胞瘤中主要见于SHH亚型髓母细胞瘤,和婴幼儿促纤维增生/广泛结节形成型髓母细胞瘤存在密切关联。Garre等[9]调查了82例14岁以下的髓母细胞瘤患者,共发现5例Gorlin-Goltz综合征,年龄均在3岁以下,病理结果为促纤维增生/结节型或者广泛结节形成型,预后良好。2018年,Waszak等[10]调查发现SUFU/PTCH1基因胚系突变约占婴幼儿SHH亚型髓母细胞瘤的21%。
GS综合征筛查在髓母细胞瘤诊断和治疗中有重要临床意义,对符合GS综合征的髓母细胞瘤患者以化疗为一线治疗方案多可获得良好预后;而采用放疗方案,二次肿瘤(基底细胞癌、脑膜瘤等)发生概率会明显增加,应尽量避免[9,10]。为降低二次肿瘤发生率,此类患者应尽可能减少放射学检查(X线、CT),建议采用超声或磁共振检查;在日常生活中,也要减少紫外线照射,外出应用遮阳伞、太阳镜等防止日光照射[9]。本组中病例7行全脑脊髓放疗后5年出现头皮基底细胞癌,佐证了该观点[8];既往我院曾报道1例患者放疗后出现胸腔淋巴瘤导致死亡,符合Gorlin-Goltz综合征诊断,但暂无基因诊断结果,故未纳入本研究[11]。
Gorlin-Goltz综合征的3种典型表现为多发基底细胞癌、颌骨囊肿(keratocysts)、颅内钙化(cerebral calcifications)[12]。研究发现,该综合征的疾病或体征表现具有年龄分布特点,髓母细胞瘤多发于3岁以下儿童,而大脑镰/小脑幕钙化70%~80%见于成年患者。本研究中的3例典型病例属于同一家族,我们对家族中部分成年人行头颅CT平扫,均可见小脑幕和大脑镰钙化,符合GS遗传性综合征的特点,有助于临床医生诊断。应当注意的是,即使钙化阴性也不能完全排除该诊断,需要进一步行基因检测后明确诊断。如前所述,合并Gorlin-Goltz综合征患者年龄大多在3岁以下,此时颅内钙化多不可见,本研究中病例均未见大脑镰/小脑幕钙化。因此对于该年龄段患者,由于多无其他症状辅助诊断,导致诊断困难,基因检测和密切随访往往是早期诊断的重要措施。
GS综合征为遗传性综合征,发生突变的基因包括PTCH1、SUFU、PTCH2等,PTCH1突变较为常见,占60%~75%,但SUFU突变后发生髓母细胞瘤的概率是PTCH1的20倍,因此靶向治疗成为目前研究的热点[5]。SMO抑制剂(sonidegib,vismodegib等)已开始应用于SHH亚型和复发髓母细胞瘤的治疗,SHH亚型患者无进展生存期明显延长,且和PTCH1突变相比,SUFU突变患者应用靶向治疗可获得更好的效果[13-15]。同时SMO抑制剂也应用于Gorlin-Goltz综合征患者皮肤基底细胞癌的治疗。
目前国内对于髓母细胞瘤患者尚未常规进行基因检测,有关遗传性髓母细胞瘤的报道极少。2019年Bagemann等[16]报道了GPR161基因胚系突变也可以导致类似Gorlin-Goltz综合征的症状,患者均为SHH亚型,发病年龄均在3岁以下,临床预后良好,但后期可以发生基底细胞癌和放疗相关的脑膜瘤等病变。本研究采用的基因检测方法多为PANEL靶向测序,未能包含GPR161基因,目前对于该基因和髓母细胞瘤的关注较少,有待进一步研究。
