乌梅提取物对草莓保鲜效果的影响
2021-05-21李肖均路飞李哲肖志刚
李肖均 路飞 李哲 肖志刚
(1.沈阳师范大学粮食学院,辽宁 沈阳 110034;2.河南工业大学粮油食品学院,河南 郑州 450001)
目前大多数的水果保鲜主要是低气压保鲜法、气调保鲜法[1]、低温冷藏法以及化学药剂保鲜法。近几年,人们对食品的安全卫生要求越来越严格,所以生物保鲜剂[2]的研究也得到很多专业人士的重视。Olivas 等[3]研究了由海藻酸盐制成的可食性涂层对最小加工的嘎拉苹果品质的保护作用,藻酸盐涂层可以保持苹果片的质量,而不会引起水果中的任何厌氧呼吸。乌梅是一味药食同源的中药,除了做药物使用外,还可制作果脯、饮料等,集医疗、保健、养生于一体,是一味很有研究前途的中药。有关乌梅提取液的抑菌研究,乌梅及其制剂在体外对大肠杆菌、金黄色葡萄球菌等有抑制作用。其中,乌梅对产生的氧自由基具有很强的清除能力,有很强的抗氧化作用。现代人们的食物大多趋向于精制食品,长期食用调味剂和动物性食物,会让人体体内血液中聚集大量毒素。乌梅具有清血功效,可以使血液的流动正常,从而排掉过量的毒素。同时乌梅也具有保护消化系统,减压消除疲劳,增进食欲等功效。乌梅提取物结合可食用性涂膜,在草莓外部以产生一种可改变的环境,从而减少腐烂、延缓成熟和变色,改善外观[4]。其中,壳聚糖被称为“人体的环保剂”,同时还具有抗氧化及杀菌抑菌的作用[5-6],也正是因为它的杀菌作用,本实验用它作为涂膜剂增强了保鲜的效果。
本实验主要对经过壳聚糖涂膜处理的不同浓度的乌梅总提取物对草莓的保鲜效果进行研究,探讨乌梅作为一种食品保鲜剂的应用效果,使乌梅作为一种保鲜剂的同时又可以发挥其保健药理功能,可以真正做到“一食多得”。同时,本实验也将乌梅提取物结合其他生物保鲜剂共同作用,来进一步研究更具有实用价值的复合生物保鲜剂。
1 材料与方法
1.1 材料与试剂
双流冬草莓(沈阳水果批发市场购得),四川省双流县特产,以其含糖量高、成熟期提前、采摘期提前等特点得到广大北方消费者的喜爱。实验所用的草莓,采集新鲜,果实完整,大小均一,色泽鲜红。
乌梅粉:西安汇林生物科技有限公司;鹿蹄草粉:西安汇林科技有限公司。
壳聚糖(脱乙酰度92.3%):国药集团化学试剂有限公司;纳米SiOX粉末(8000 目);2,6—二氯酚靛酚(分析纯):上海金穗生物科技有限公司;30%过氧化氢(分析纯):沈阳市东兴试剂厂;愈创木酚(分析纯):天津市大茂化学试剂厂;氯化硝基四氮唑蓝(分析纯):上海源叶生物科技有限公司;甲硫氨酸(分析纯):合肥博美生物科技有限责任公司;核黄素(分析纯):合肥博美生物科技有限责任公司。
1.2 主要实验仪器
RHB-080 型手持折射仪:上海光学仪器厂;UV-5100 型紫外可见分光光度计:上海元析仪器有限公司;CT3 4500 型质构仪:美国Brookfield 博勒飞公司;YP2000-2 型电子天平:上海佑科仪器仪表有限公司;DK-S26 型恒温水浴锅:上海精宏实验设备有限公司。
1.3 实验方法
1.3.1 涂膜剂的制备 实验所用的涂膜剂由两部分组成,首先是乌梅提取物水溶液,作为草莓表层的保鲜剂,外层为壳聚糖—纳米SiOX溶液作为保护膜,保护内部保鲜剂成分的同时也在一定程度上减少草莓果实所受到的机械损伤。
配制壳聚糖—纳米SiOX溶液:量取500 mL 的蒸馏水于烧杯中,加入冰醋酸3 mL,搅拌,再加入占溶液质量0.015%的纳米SiOX,手动搅拌5~10 min,待混合后,用超声振荡10 min,温度保持室温,分散均匀后再搅拌10 min,随后加入占溶液质量1%的壳聚糖,搅拌20 min 使其充分溶解,再超声振荡10 min,待无大颗粒状存在的情况下,调整其pH 值为5.6,然后超声振荡5 min,制得壳聚糖—纳米SiOX溶液[7-8]。
1.3.2 乌梅提取物的提取方法 乌梅的水提取法[9],取4 个烧杯,称取经粉碎(过40 目筛)的乌梅粉5 g、10 g、15 g 于3 个烧瓶中分别标号记作提取液A1、提取液A2,提取液A3,量取250 mL 蒸馏水,依次加入上述3 个烧杯中,将称取的10 g 乌梅粉和10 g 鹿蹄草粉1∶1 比例混合在烧杯中,记为提取液A4,同样量取250 mL蒸馏水于A4 中。在60 ℃的温度下,在水浴锅中进行浸提2 h,浸提过程中适当搅拌。浸提后,所得粗浸提液用纱布进行初过滤,将滤液于布氏漏斗中进行二次过滤,最后得到3 种乌梅提取水溶液,和乌梅与鹿蹄草1∶1 复配提取水溶液,所得滤液在4 ℃下保存备用。
1.3.3 草莓保鲜的处理 将新鲜的双流冬草莓果实每10 个为一组,分别在不同浓度的提取液中浸泡30 s,然后将捞出后的草莓置于干燥通风处,等其自然凉干。之后进行涂膜,将之前晾干的草莓在纳米SiOX壳聚糖涂膜液中浸泡2 min,捞出后重复之前的过程[8]。将晾干的凃膜草莓置于防压的一次性塑料保鲜盒中,其外部用保鲜膜包好后,轻放于冰箱的冷藏保鲜柜中,调整其温度为4℃。在整个冷藏保鲜期间,每隔一天从冰箱中任意取出一定数量的草莓样品进行测定[9-10]。
本实验将处理后的草莓分为A1、A2、A3、A4 四组作为实验组,实验组A1 为0.02 g/mL 浓度的乌梅提取水溶液,实验组A2为0.04 g/mL 浓度的乌梅提取水溶液,实验组A3 为0.06 g/mL 浓度的乌梅提取水溶液,实验组A4 为0.04 g/mL 乌梅提取水溶液与0.04 g/mL 鹿蹄草提取水溶液进行1∶1 复配的提取液,空白对照BK 为等量的蒸馏水。每个分组进行3 次重复实验。
1.3.4 草莓贮藏中主要成分的测定 每2 d 定时对草莓果实进行观察及进行酸度、可溶性固形物、维生素C 和硬度的测定,记录果实腐烂率,失重率,SOD 活性和POD 活性等品质的变化,比较不同浓度处理的差异。
(1)总酸度的测定
称取8 g 捣碎的草莓样品置于烧杯中,将蒸馏水煮沸,待其冷却后,用蒸馏水将捣碎的样品转移入250 mL 容量瓶中,随后加蒸馏水至刻度,充分混匀后,过滤。用移液管吸取样品稀释液10 mL,转移至三角瓶中,滴入酚酞指示液2 滴,用新配置的0.1 mol/L 氢氧化钠标准溶液滴定,滴至显红色半分钟不褪色为止,同时做试剂空白实验。每个样品重复滴定3 次,取平均值。
(2)可溶性固形物的测定
称取10 g 草莓果实样品,将其放入研钵中磨碎,得到的果汁经过滤后待用。打开手持折光仪的保护盖,在棱镜表面滴两滴蒸馏水,盖上保护盖。在水平状态下,从目镜处观察,检查视线中的明暗交界线是否处于零刻线上。若与零刻线不完全重合,则旋动刻度调节旋钮,使分界线与零刻线重合。用擦镜纸将水擦干,在玻璃棱镜上滴2 滴果汁,进行观测,读取视线中的明暗交界线上的刻度,所显刻度即为草莓中可溶性固形物含量(%)(糖的大致含量),进行3 次重复试验。
(3)维生素C 含量的测定
本实验采用2,6-二氯酚靛酚滴定法,取8 g 草莓样品与等量2%草酸,加入组织捣碎机中,匀浆5 min。取出匀浆物质10 g,用少量1%草酸将称取的匀浆物质倒入100 mL 容量瓶中,并用1%草酸反复洗涤烧杯,其洗涤液一并移入,用1%草酸定容到100 mL。盖上玻璃塞,将匀浆物质与1%草酸充分混合均匀,静置10 min 后,取上述溶液过滤。用量筒量取10 mL 滤液,将其倒入三角瓶中,同时加入10 mL 1%的草酸溶液;量取10 mL 蒸馏水置于三角瓶中,向其中加入10 mL 1%的草酸溶液(空白对照)。向上述溶液中加入1 mL 氯仿,将2,6-二氯酚靛酚染料滴定至终点记录染料的消耗量。
每100 g 样品中维生素C 的含量(mL)计算公式如下:
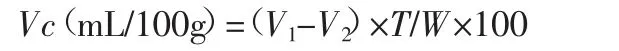
式中:
V1——滴定样品时耗去的染料溶液的量(mL)
V2——滴定空白时耗去的染料溶液的量(mL)
T——1 mL 染料溶液相当于坏血酸的毫克数
W——滴定时所取的滤液中,含样品的量(g)
Vc——每100 g 样品中Vc 的含量(mL/100g)
(4)失重率的测定
采用称重法测定,每天同一时间称量每组草莓的总重量。每个样品重复测3 次,取平均值。
(5)腐烂率的测定
选择100 个涂膜草莓,对照组与实验组共5 组,每组20 个,每隔一天分别对5 组的草莓的腐烂情况进行统计,腐烂个数以时间进行叠加,每个样品重复测3 次,取平均值。
(6)硬度的测定
草莓硬度用CT3 4500 型质构仪测定,实验选定圆柱形探针,设定测试类型为压缩,负载50 g,测试速度0.2 mm/s,形变目标值15%。每组每次测定用草莓果实3 个,每颗草莓只测一次,取平均值。
(7)超氧化物歧化酶(SOD)活性的测定
使用氮蓝四唑法测定草莓中超氧化物岐化酶活性,取草莓于研钵中,加入磷酸缓冲液,研磨成浆使终体积为4 mL,离心20 min,上清液为SOD 粗提取液。之后,进行显色反应,设置对照组与测定组。将其中一个对照管置暗处,剩下的试管置于日光下反应20 min。至反应结束后,全部移入暗处,以不光照的对照管作空白,在560 nm 波长下分别测定其他各管的吸光度。
计算公式如下:
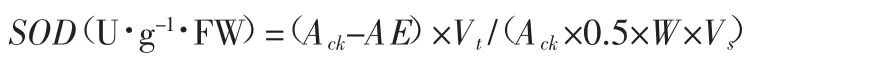
式中:
Vt——总酶液量(mL)
Vs——所用酶液量(50 uL)
W——叶片鲜重(N)
Ack——用缓冲液代替酶液的光照对照管吸光度
AE——样品管吸光度
(8)过氧化物酶(POD)活性的测定
称取草莓1 g,加入20 mmol/L KH2PO4溶液5 mL,于研钵中研磨成匀浆,离心5 min,将上清液移入25 mL 容量瓶中,剩余部分再用5 mL KH2PO4溶液提取一次,合并两次上清液,定容混匀,冷藏备用。
取若干只比色皿,向其中的一只加入反应混合液3 mL,KH2PO4溶液1 mL,作为参比液;向其余的各只中分别加入反应混合液3 mL,新提取的酶液1 mL,并立即记时同时置于分光光度计中。在470 nm 的波长下,测定其光密度值,测定过程中每隔1 min 读一次数据,连续测定10 min。
计算公式如下:
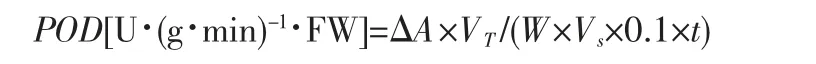
式中:
W——草莓果实鲜重(g)
ΔA——反应时间内吸光度值的变化
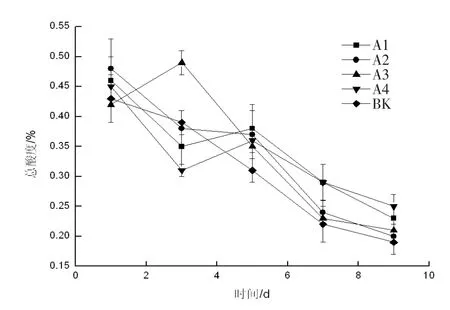
图1 不同浓度对草莓总酸度的影响
VT——提取粗酶液总体积(mL)
Vs——测定时所用的粗酶液体积(mL)
t——反应时间(min)
2 结果与分析
2.1 草莓总酸度的变化
草莓当中的有机酸,不仅可以作为细胞中许多生化过程所需中间代谢物的提供者,同样也是呼吸基质、合成ATP 的主要来源[11]。从图1 可以看出,对照草莓酸含量明显下降,冷藏条件下,0.02 g/mL、0.04 g/mL、0.06 g/mL 浓度的乌梅提取液和0.04 g/mL 乌梅提取水溶液与0.04 g/mL 的鹿蹄草进行1∶1 配比的复合液涂膜处理的草莓酸含量降低比较缓慢。对照草莓在第9 d 酸度降到0.19%,0.02 g/mL、0.04 g/mL、0.06 g/mL 浓度的乌梅提取液涂膜处理的草莓第9 d 最多才降到0.20%,下降速度缓慢。
2.2 草莓可溶性固形物的变化
草莓中的可溶性固形物主要是指可溶性糖,可溶性糖的含量变化可以直接反映草莓的成熟程度和品质变化状况[12]。由图2 可见,所有草莓从保存第1 d 开始可溶性固形物含量明显出现下降,下降速率开始较快,从第3 d 起下降的速率开始减慢。在整个贮藏期间,A2,A3 组乌梅提取液处理组可溶性固形物显然高于对照,空白对照组其可溶性固形物折线斜率高于A2 和A3 实验组,说明了0.04 g/mL、0.06 g/mL 浓度的乌梅提取液对样品可溶性固形物质的下降起到一定的抑制作用。其中,实验组A2 的草莓其可溶性固形物的含量变化率较低,所以可以得出结论,0.04 g/mL浓度的乌梅提取液对草莓的保鲜效果最佳。
2.3 草莓维C 含量的变化
维生素C 又称作抗坏血酸,草莓的Vc 含量高,在贮藏过程中Vc 含量会随着时间的变化而不断减少,所以通过Vc 的含量变化可以看出草莓腐烂变质的程度[13]。由图3 可见,草莓中的Vc 含量从第2 d 开始出现下降趋势。对照组折线斜率一直高于实验组,说明对照组的腐败变质速率较快,同时也说明了乌梅提取液对草莓Vc 含量的下降起到一定的抑制作用。实验组A1 组,其数值变化始终低于其余各组,这说明了0.02 g/mL 乌梅提取液涂膜的保鲜效果最佳。
2.4 草莓失重率的变化
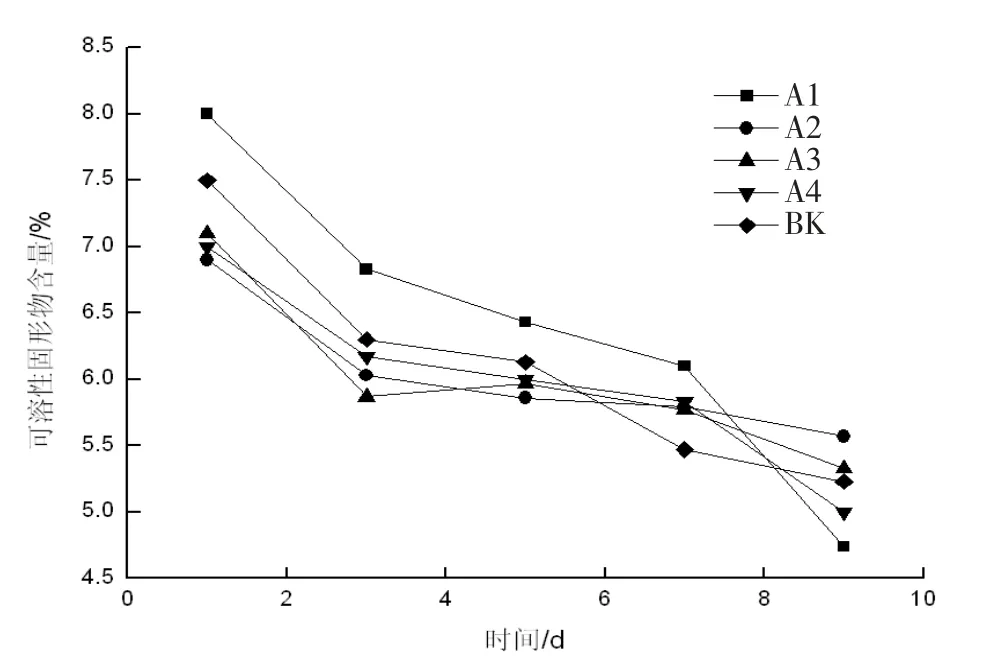
图2 不同浓度对草莓可溶性固形物含量的测定
由图4 可见,从第4 d 开始草莓失重率突然上升。整个冷藏期间,3 组乌梅提取液实验组及0.04 g/mL 乌梅提取水溶液与0.04 g/mL 的鹿蹄草提取液进行1∶1 配比的复合液涂膜的实验组,4 组的失重率明显低于对照组,这说明了不同浓度的乌梅提取液对草莓均有明显的保鲜作用。对照组折线斜率始终高于实验组,说明其腐败变质的速率较快,同时也说明了乌梅提取液对草莓的呼吸代谢起到一定的抑制作用。A2 组数值明显低于其余各组的数值,这也说明了0.04 g/mL 浓度的乌梅提取液对草莓的保鲜效果最佳。
2.5 草莓腐烂率的变化
腐烂率是衡量果蔬贮藏品质的重要性因素,采摘后的草莓,在冷藏贮藏中,草莓果实自身的呼吸作用依旧比较旺盛,会引起草莓衰老,从而导致腐烂[14]。从图5 可见,乌梅提取水溶液和0.04 g/mL 乌梅提取溶液与0.04 g/mL 的鹿蹄草提取液进行1∶1配比的复合液涂膜处理过的草莓腐烂率均低于对照。对照草莓在第3 d 出现腐烂,到第5 d 腐烂发展迅速,腐烂率达到40%,草莓表面开始出现褐色病斑。第9 d 几乎全部腐烂。经0.04 g/mL、0.06 g/mL 浓度的乌梅提取液涂膜处理的草莓,A2、A3 实验组在冷藏条件下第3 d 开始腐烂,但腐烂发展速度较慢,第9 d 腐烂率达到90%。根据折线图的走势,说明乌梅提取液涂膜对草莓保鲜贮藏有一定的效果,且A2、A3 实验组的效果最佳。
2.6 草莓硬度的变化
草莓在采摘过后,随着时间的增长,其硬度会出现先上升后下降的趋势。所以,可根据其硬度的变化情况,反映草莓的成熟及品质变化。如图6 所示,从折线图很明显可以看到,空白组从第3 d 出现了明显的下降趋势,而其余各组的下降趋势相对较缓慢,这说明乌梅提取液在一定程度上对草莓具有保鲜作用。不难发现,A3、A4 组的草莓硬度折线变化率始终低于其余各组,说明0.04 g/mL 浓度的乌梅提取液与0.04 g/mL 的鹿蹄草进行1∶1 配比的复合液涂膜处理过的草莓保鲜效果最好。
2.7 超氧化物歧化酶(SOD)活性的变化
SOD 广泛存在于生物体内,是生物体内重要的酶制剂,SOD可以清除人体内的氧自由基,抑制生物体的氧化衰老。所以,生物体内SOD 含量的高低是生物体衰老死亡的直观指标[15]。由图7 可以看出,在实验开始的第1 d 到第3 d,所有草莓的SOD 有一定的上升趋势,但从第3 d 开始出现下降趋势,说明草莓在刚开始贮藏时自身抗氧化能力上升,贮藏3 d 以后草莓的SOD 开始下降,自身抗氧化能力降低。第5 d 以后,SOD 值的变化更加明显,处理组和对照组的差距逐渐变大,同时也说明了乌梅提取液对草莓的腐烂变质起到一定的抑制作用。A2、A3 组乌梅提取液处理的草莓SOD 值始终处于较高的位置,说明0.04 g/mL、0.06 g/mL 浓度的乌梅提取液对草莓的保鲜效果最佳。
2.8 过氧化物酶(POD)活性的变化
POD 是由微生物或植物体所产生的一类活性较高的氧化还原酶,它是活性氧清除酶系的一员,可协同其他抗氧化酶一起清除过氧化氢,可作为考察植物衰老过程的一项指标[16]。如图8 所示,对照组和处理组果实的POD 活性在贮藏前期均不断增强,在5 d 左右达到最大值,且处理组果实POD 活性的增幅高于对照组,表明草莓在贮藏过程中会激活POD 活性来抑制自身的成熟衰老,而乌梅提取物涂膜处理能增强植物体的抗衰老机制。在整个贮藏期间,处理组A3 的POD 活性水平一直处于较高水平,且POD 活性的变化比较缓慢,表明0.06 g/mL 浓度的乌梅提取液对草莓的保鲜效果最佳。
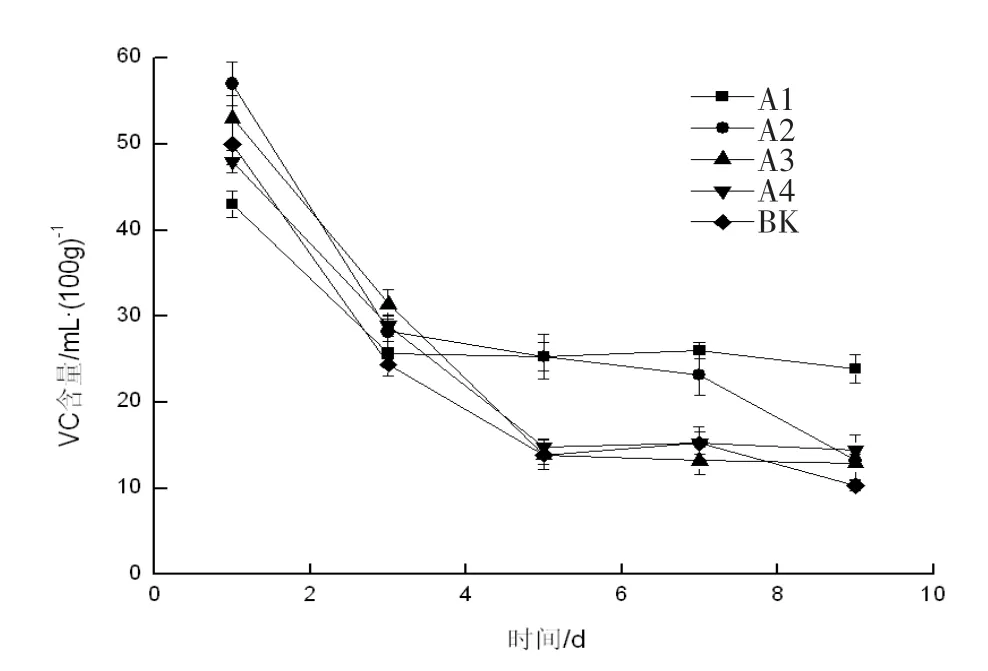
图3 不同浓度对草莓Vc 含量的影响
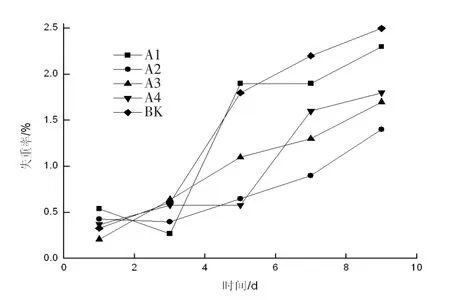
图4 不同浓度对草莓失重率的影响
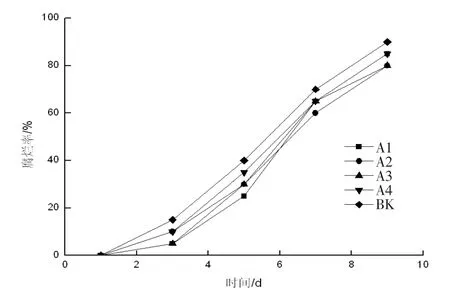
图5 不同浓度对草莓腐烂率的影响
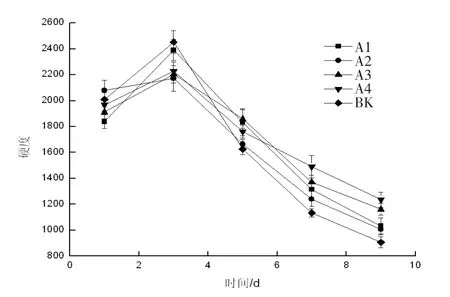
图6 不同浓度对草莓硬度的影响
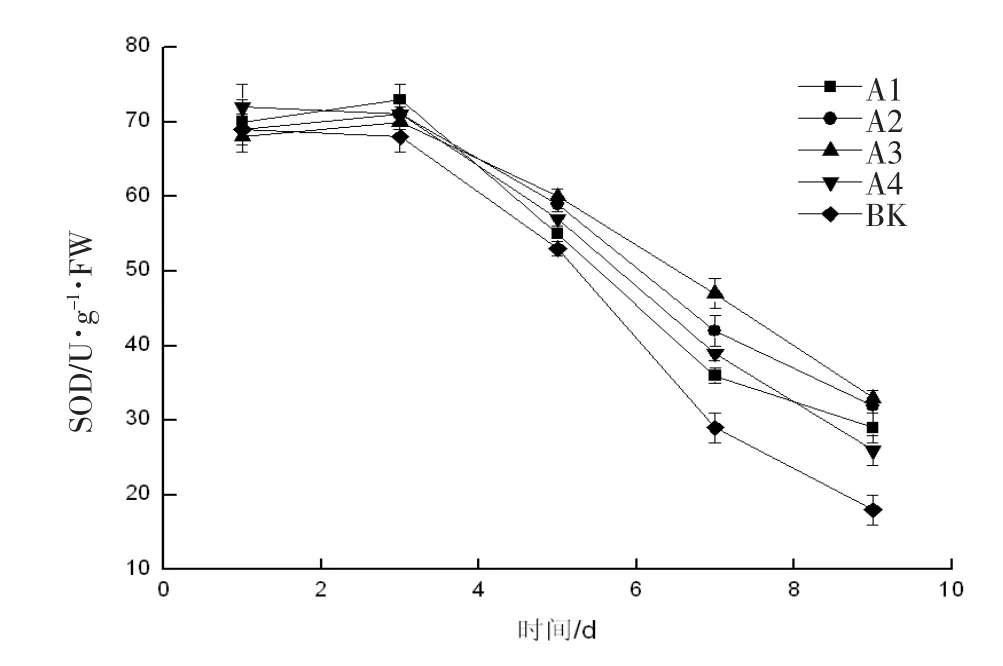
图7 不同浓度对草莓SOD 值的影响
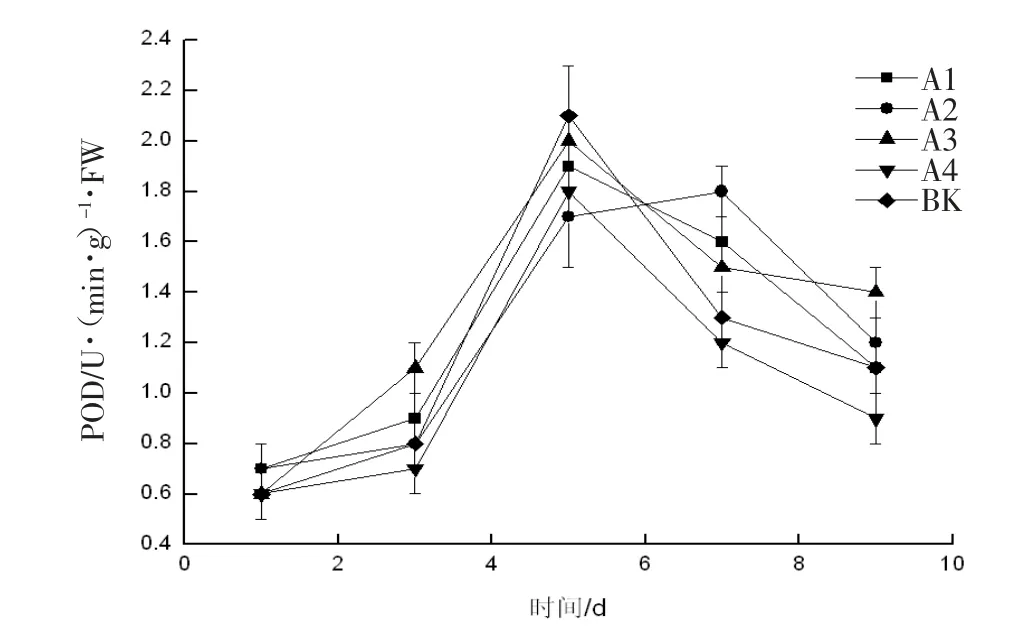
图8 不同浓度对草莓POD 值的影响
3 结论
在对草莓的各项指标测定结果中发现,0.04 g/mL 浓度的乌梅提取物对草莓的可溶性固形物的下降起到了明显的抑制作用,并且有效降低了草莓在储藏过程中的失重率。草莓腐烂率的测定结果显示,浓度为0.06 g/mL 乌梅提取液可以大大降低草莓在贮藏过程中的腐烂情况。草莓的SOD 值也在一定程度上反映了浓度为0.04 g/mL~0.06 g/mL 乌梅提取液用于草莓保鲜,可以延缓果实氧化衰老。结果表明,所有草莓在储存期间都会发生腐烂变质,储存时间越长腐烂情况越严重,不同浓度的乌梅提取液对草莓均有保鲜作用;草莓在储藏的前3 d,自身抗氧化能力较好,储藏3 d以后,其抗氧化能力明显降低,不同浓度的乌梅提取液对草莓抗氧化能力都有显著的协同作用。乌梅提取液对草莓的保鲜效果随浓度的增加而增强,在乌梅提取液的浓度为0.04~0.06 g/mL 时,对草莓保鲜有较好的辅助作用。同时,本实验从品质和抗氧化性能方面研究了乌梅提取物—壳聚糖复合保鲜液对草莓的保鲜效果,探索了乌梅提取液的最佳保鲜浓度,为健康无害高效的复合防腐保鲜液的发展提供理论依据。
