电解法制备低浓度次氯酸钠消毒水的参数优化及表观动力学探究
2021-05-12王晓晴鲁宁宁
王晓晴 鲁宁宁 肖 宁
(北京化工大学 化学工程学院, 北京 100029)
引 言
目前,新型冠状病毒在世界范围内大肆爆发,日常隔离与常态消毒是控制疫情传播最有效的手段。84消毒剂是一种高效、廉价的消毒剂,已经逐渐成为人们不可或缺的日常消毒用品,其有效成分为高浓度的次氯酸钠溶液,通过破坏微生物的细胞膜、体蛋白质、核酸而达到消毒的目的[1-2]。高浓度的次氯酸钠溶液在储存、稀释过程中会产生氯气中毒、腐蚀皮肤等危险[3-4],并且随着存放时间的延长,有效氯浓度会迅速降低[5]。因此找到一种更加安全、方便的消毒方法显得很有必要。
若采用连续式进水,通过电解低浓度食盐水制备浓度适宜、无需稀释的次氯酸钠溶液,则可将新鲜的次氯酸钠溶液直接喷洒在需要消毒的场所。这种低浓度消毒液不仅可以避免类似84消毒液在使用过程中可能发生的危险,并且新鲜的消毒液中氧化还原电位(ORP)和活性氧、活性氯等物质均保持在最佳状态,杀菌效果最好[6-8]。
一般电解法制备次氯酸钠所用盐的质量浓度为30~40 g/L[9-10],出水有效氯的质量浓度较高,在8 000 mg/L以上[11-12],而电解低浓度氯化钠溶液制备用于卫生消毒的次氯酸钠的报道较少。本文通过在无隔膜电解槽中电解低浓度的氯化钠溶液,制备了低质量浓度的次氯酸钠溶液,探究电解参数对电解效果的影响,确定了该反应的表观动力学级数,以及初始盐浓度、电流密度对反应速率常数的影响,可为电解法制备低浓度次氯酸钠溶液用于日常生活消毒提供数据支持。
1 实验部分
1.1 实验材料和仪器
1.1.1实验材料
氯化钠,分析纯,国药集团化学试剂有限公司;碘化钾,分析纯,福晨(天津)化学试剂有限公司;Na2S2O3·5H2O、硫酸、盐酸,分析纯,北京化工厂;可溶性淀粉,分析纯,陇西科学股份有限公司。RuO2- IrO2- TiO2/Ti钛网阳极和石墨阴极由宝鸡钛普锐斯钛阳极科技有限公司提供。
1.1.2仪器
SS- 3020KD- 30V/20A型直流稳压电源,东莞市不凡电子有限公司;BT100L- CE型蠕动泵,保定雷弗流体科技有限公司;FA2004型电子天平,力辰科技有限公司。
1.2 实验装置
电解装置由食盐水储罐、进水蠕动泵、自制立式电解槽(容积1.9 L)、直流稳压电源、消毒水储罐5个核心部分组成,如图1所示。电解槽中的电极对由3组面积相同的阴极、阳极板(1.3 dm2/片)并联组成,阴极为石墨板,阳极为涂覆催化剂的钛网电极,极板间距为2 cm。食盐水储罐1中的稀盐水通过进水蠕动泵2以一定流量进入电解槽3,经电解后从上方出水口流入消毒水储罐5,在规定时间从出水口取液测试。
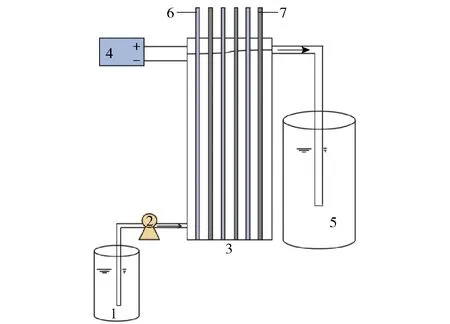
1—食盐水储罐;2—进水蠕动泵;3—电解槽;4—直流稳压电源;5—消毒水储罐;6—阳极板;7—阴极板。图1 电解装置示意图Fig.1 Schematic diagram of the electrolytic device
1.3 实验方法
1.3.1工艺参数优化
采用单因素实验法探究盐水流量、盐的质量浓度、电流密度和进水温度对电解效果的影响,以有效氯浓度、电流效率和运行费用为评价指标,选择最优工艺参数。
1.3.2有效氯浓度测定
溶液中有效氯的浓度采用碘量法[13]测定,有效氯的质量浓度ρ(mg/L)的计算公式为
(1)
式中,V1为滴定待测液时消耗的Na2S2O3·5H2O的体积,mL;c为Na2S2O3·5H2O的浓度,mol/L;M为氯原子的摩尔质量,g/mol;V2为待测液体积,mL。
1.3.3电流效率计算
电流效率为出水有效氯的浓度稳定后的值,其计算公式为
(2)
式中,η为电流效率;m1为实际有效氯的生成量,g;m2为理论有效氯的生成量,g。
1.3.4运行费用计算
运行费用为生产1 kg有效氯的电耗费用与盐耗费用的总和,运行费用X(元)的计算公式为
X=0.8×X1+1.0×X2
(3)
式中,X1为生产1 kg有效氯需要的电量,kW·h;X2为生产1 kg有效氯需要的盐量,kg;0.8为电费单价,元/(kW·h);1.0为食盐单价,元/kg。
1.3.5表观动力学探究
根据实验数据推导反应级数,确定反应动力学模型,并探究两个重要的反应影响因素(初始盐浓度和电流密度)与表观反应速率常数k的关系,最后得出动力学方程。电解氯化钠的过程中生成有效氯的反应如下[14]。
2NaCl+2H2O=2NaOH+Cl2+H2
(4)
Cl2=2Cl·
(5)
上面两个方程可简化为
Cl-→Cl·
(6)
初始浓度:a0
t时刻浓度:a-xx
其中,a为Cl-的初始浓度,x为t时刻的有效氯浓度。
假设有效氯的生成反应为表观一级反应过程,则该反应速率的微分表达式为:-d(a-x)/dt=k(a-x),由积分法可得:ln(a/(a-x))=kt。如果将实验数据带入积分表达式得到关于ln(a/(a-x))和t的线性方程,则上述假设成立。
2 结果与讨论
2.1 工艺参数优化结果
2.1.1盐水流量
电解开始后,电解槽的出水有效氯的质量浓度逐渐增加,此时电解过程处于暂态;随着电解时间的延长,在不同盐水流量条件下,出水有效氯的质量浓度分别稳定在某一数值后不再发生变化,此时电解过程处于稳态,理论上稳态时间为电解槽容积与盐水流量的比值。暂态时,在不同盐水流量下有效氯的质量浓度随时间的变化如图2所示。
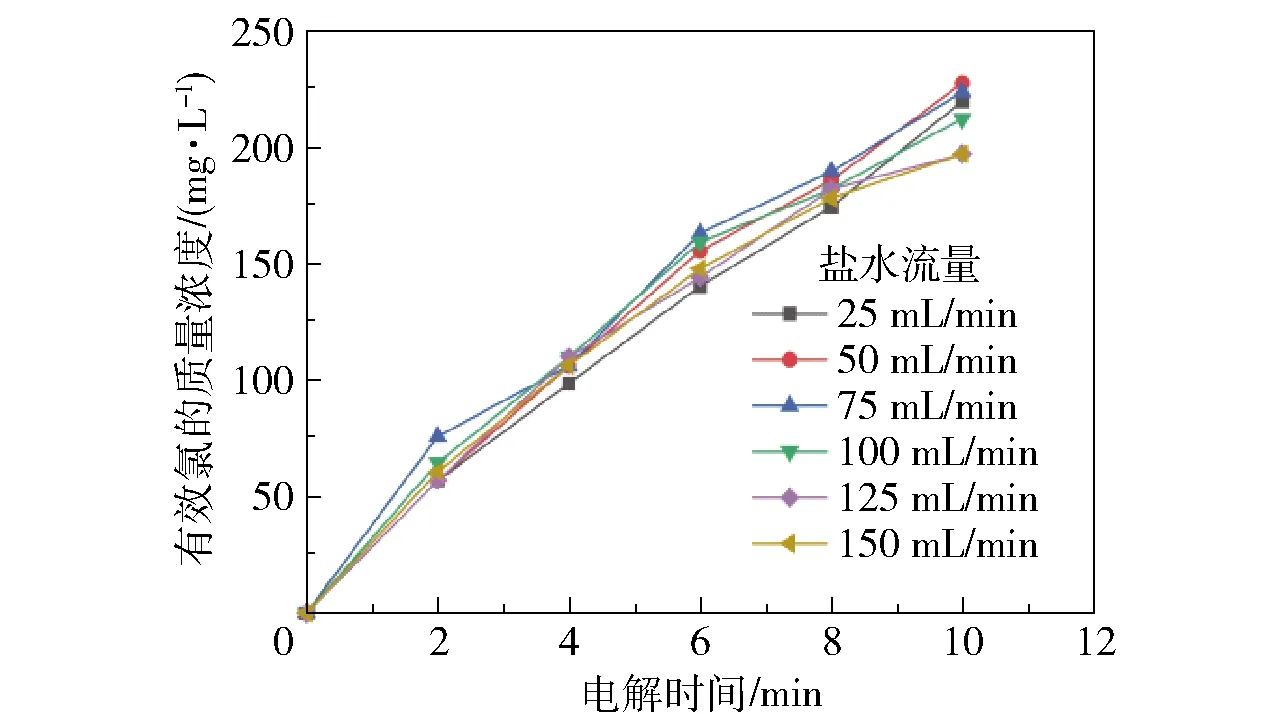
图2 暂态下有效氯的质量浓度随时间的变化曲线Fig.2 Relationship between the mass concentration of effective chlorine and time in the transient state
由图2可知,盐水流量的变化对出水有效氯的质量浓度几乎没有影响,说明在此实验条件下,由流量控制的传质过程对有效氯的生成影响很小,在该电解反应中传质过程并非反应速率控制步骤,界面电化学反应才是速率的控制步骤。
稳态下,出水有效氯的质量浓度和电流效率与盐水流量的关系如图3所示。
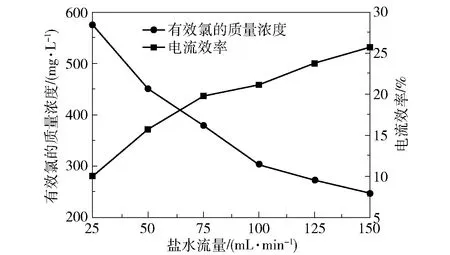
图3 盐水流量对电解效果的影响Fig.3 Effect of brine flow on electrolysis
由图3可以看出,稳态下随着盐水流量的增大,出水有效氯的质量浓度逐渐减小,这是因为盐水流量越大,盐水在电解槽中的停留时间越短,电化学反应时间越短,导致有效氯的质量浓度降低。随着盐水流量的增大,电流效率逐渐增大,说明虽然流量增大时出水有效氯的质量浓度降低,但单位时间内有效氯的生成总量增大,因此电流效率逐渐升高。
为了筛选出最佳的盐水流量,对不同盐水流量下的运行费用进行了对比,结果如图4所示。由图4可知,随着盐水流量的增加,运行费用先减少后增加,流量为75 mL/min时运行费用最低。结合电解效果考虑,选择盐水流量75 mL/min作为最佳实验参数。
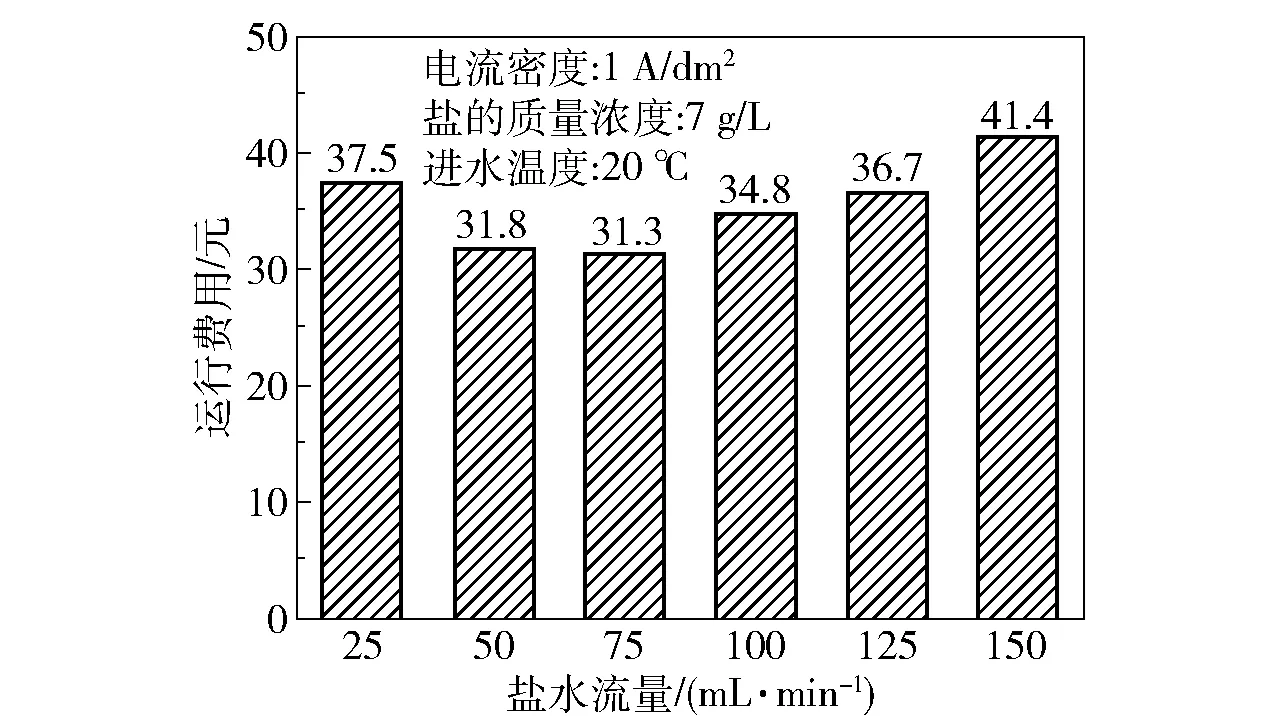
图4 运行费用随盐水流量的变化Fig.4 Variation in operating cost as a function of brine flow
2.1.2盐的质量浓度
在电解过程中盐的质量浓度对有效氯的生成起着至关重要的作用,本实验使用的盐的质量浓度为3~13 g/L,图5显示了盐的质量浓度与出水有效氯的质量浓度和电流效率的关系。
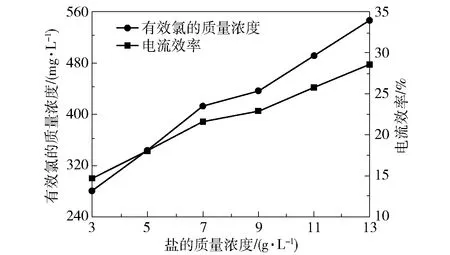
图5 盐的质量浓度对电解效果的影响Fig.5 Effect of salt mass concentration on electrolysis
由图5可知,随着盐的质量浓度的增大,出水有效氯的质量浓度和电流效率逐渐增大。溶液中Cl-浓度越高,越有利于析氯反应的发生,抑制析氧副反应的发生,减少电能的无效消耗,提高电流效率。
图6表明了运行费用与盐的质量浓度的关系,可以看出,当盐的质量浓度为7 g/L时运行费用最低。结合电解效果考虑,选择盐的质量浓度7 g/L作为最佳实验参数。
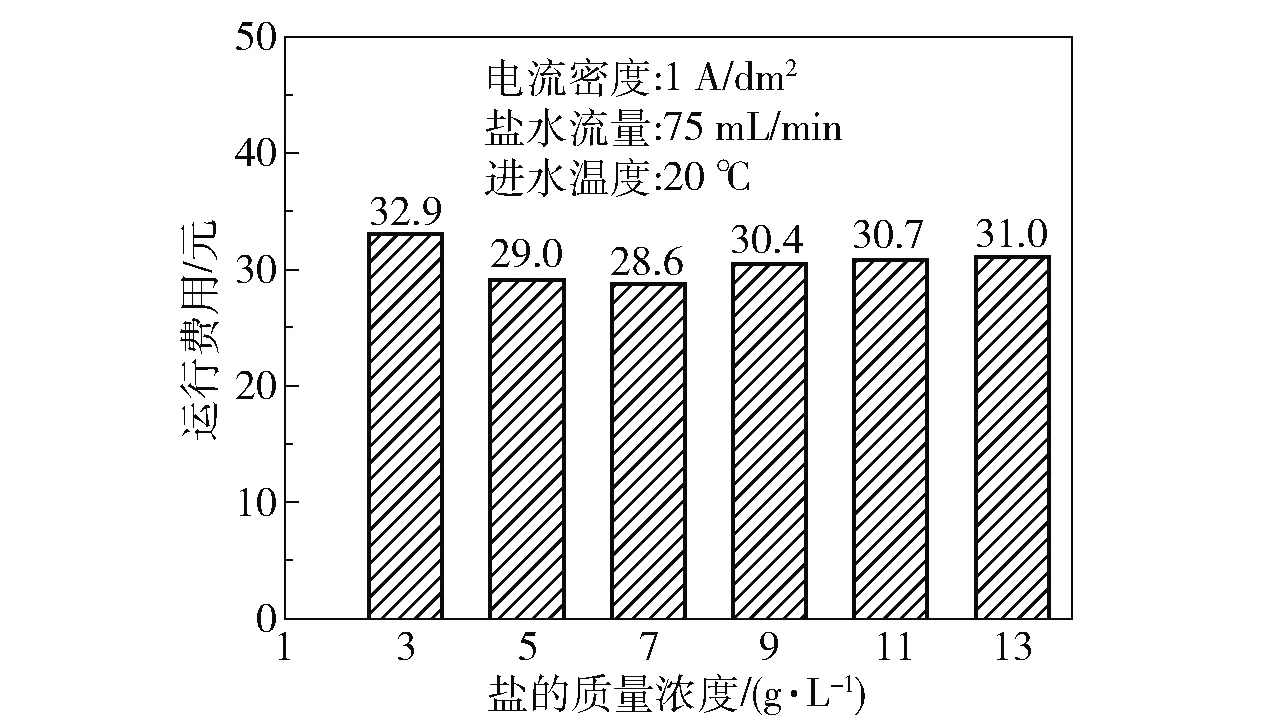
图6 运行费用随盐的质量浓度的变化Fig.6 Variation in operating cost as a function of salt mass concentration
2.1.3电流密度
电流密度是决定出水中有效氯的质量浓度的关键参数,本实验考察的电流密度为0.5~3.0 A/dm2,电流密度对电解效果的影响如图7所示。
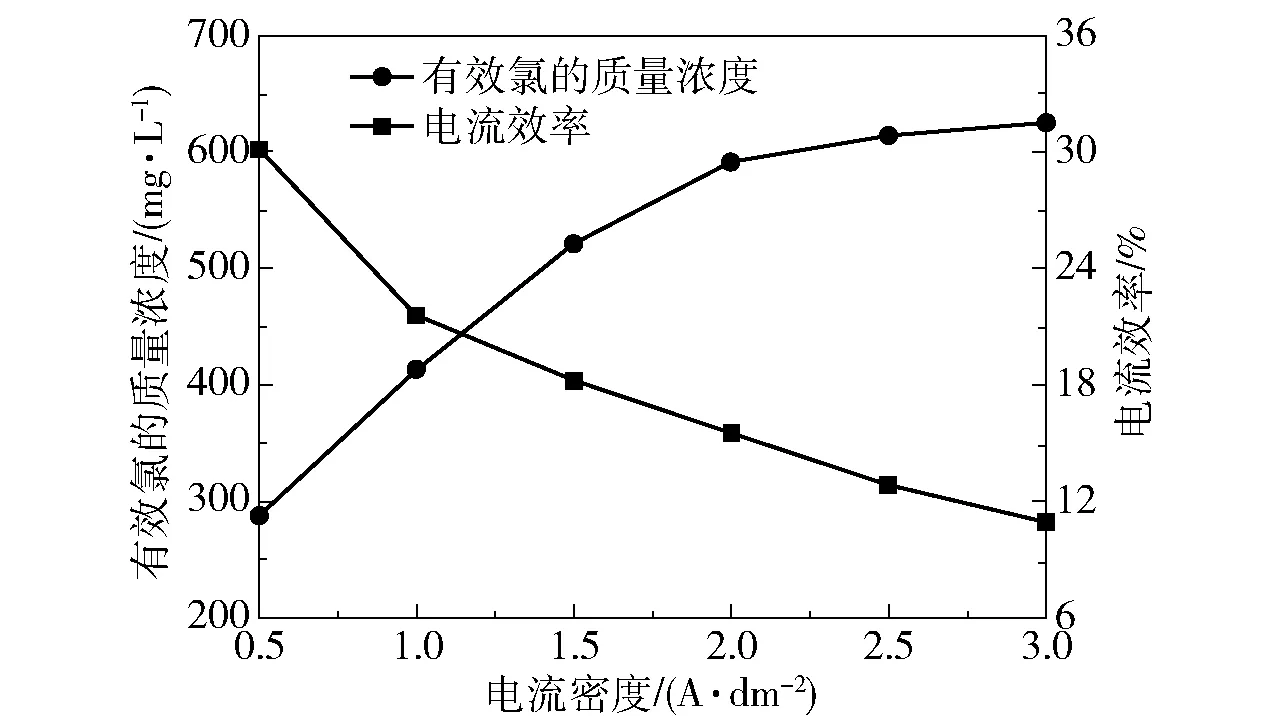
图7 电流密度对电解效果的影响Fig.7 Effect of current density on electrolysis
由图7可知,随着电流密度的增大,有效氯的质量浓度不断增大,在电流密度从0.5 A/dm2增大到2.0 A/dm2的过程中,有效氯的质量浓度呈线性上升趋势,而电流密度从2.0 A/dm2增大到3.0 A/dm2的过程中,有效氯的质量浓度的增长开始变得缓慢。原因是阳极表面生成的氯气在析出过程中会部分附着在电极表面,从而在一定程度上阻碍了电化学反应的进行。电流效率随着电流密度的增大而减小,这是因为在实验中发现,电流密度越大,反应产热越严重,加快了氯气的溢散速率,从而导致电流效率下降。
图8表明了电流密度与运行费用的关系,当电流密度为1.0 A/dm2时运行费用最低,因此选择电流密度1.0 A/dm2作为最佳实验参数。

图8 运行费用随电流密度的变化Fig.8 Variation in operating cost as a function of current density
2.1.4进水温度
电解过程中,进水温度会影响溶液中离子的运动和气体溢散的速度等,本实验的进水温度为15~40 ℃,图9显示了进水温度与电解效果的关系。
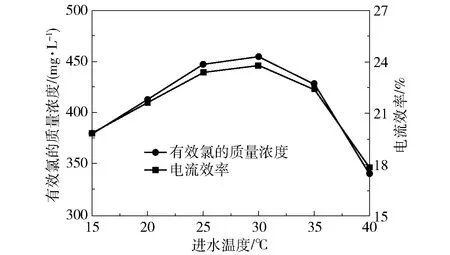
图9 进水温度对电解效果的影响Fig.9 Effect of inflow temperature on electrolysis
由图9可知,当进水温度为30 ℃时,有效氯的质量浓度和电流效率最高,分别为455 mg/L和23.8%。高温和低温环境都不利于有效氯的生成。在15~30 ℃时,随着进水温度的上升,有效氯的质量浓度和电流效率逐渐增大,这是因为随着温度的升高,溶液中离子的吸脱附效率和生成产物的转移速率逐渐增大,适当提高温度有助于氯离子被氧化;在30~40 ℃时,随着温度的上升,有效氯的质量浓度和电流效率逐渐减小,在低浓度的盐溶液中温度升高加快了氯气的溢出速率,同时促使已经生成的次氯酸钠发生分解反应。此外,温度过高还会导致如下歧化反应发生[15]。
(7)
(8)
图10表明了进水温度与运行费用的关系。由图可知,进水温度为30 ℃时运行费用最低,为24.8元,因此选择进水温度30 ℃作为最佳实验参数。
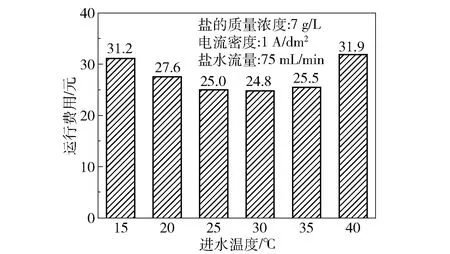
图10 运行费用随进水温度的变化Fig.10 Variation in operating cost as a function of inflow water temperature
2.2 表观动力学
利用方程ln(a/(a-x))=kt对相关实验数据进行动力学拟合,得到盐的不同初始质量浓度下ln(a/(a-x))与电解时间的关系(图11)和决定系数R2(表1)。

图11 盐的不同初始质量浓度下ln(a/(a-x))与电解时间的关系Fig.11 The relationship between ln(a/(a-x)) and electrolysis time for different initial salt mass concentrations

表1 盐的不同初始质量浓度下的决定系数R2Table 1 The coefficients of determination for different initial salt mass concentrations
表1中的R2值表明实验数据与一级反应动力学模型的拟合程度都非常好,所以电解食盐水制备次氯酸钠消毒水的反应为表观一级反应过程。
2.2.1盐的初始质量浓度对反应速率常数的影响
根据图11求得盐的不同初始质量浓度下的反应速率常数k值,如表2所示。
由表2可知,表观反应速率常数k与盐的不同初始质量浓度a相关,对数据进行拟合后得到方程:k=0.007a-0.459,R2=0.983,可知k与a的-0.459次方成正比。

表2 盐的不同初始质量浓度下的反应速率常数kTable 2 Reaction rate constants for different initial salt mass concentrations
2.2.2电流密度对反应速率常数的影响
对不同电流密度下盐浓度和电解时间的实验数据与一级动力学方程进行拟合,得到不同电流密度下ln(a/(a-x))与电解时间的关系(图12)和反应速率常数k和R2(表3)。
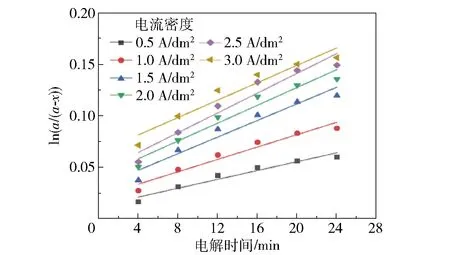
图12 不同电流密度下ln(a/(a-x))与电解时间的关系Fig.12 The relationship between ln(a/(a-x)) and electrolysis time with different current densities
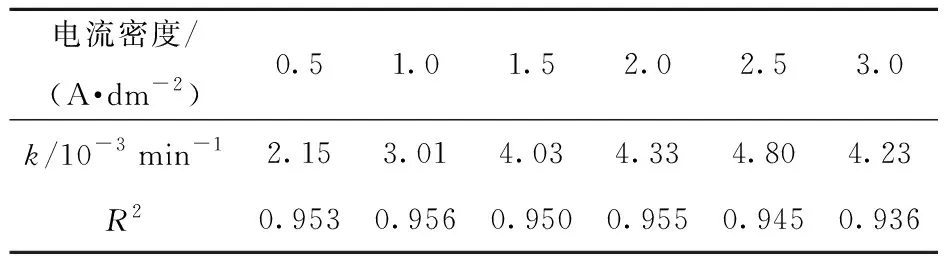
表3 不同电流密度下反应速率常数k和决定系数R2Table 3 Reaction rate constants and coefficients of determination of the effective chlorine formation reaction with different current densities
表3中的R2值表明实验数据与动力学方程拟合效果良好,因此在电流密度J为0.5~3.0 A/dm2内有效氯的生成反应符合一级动力学方程。
由表3可知反应速率常数k随电流密度J的变化而变化,两者存在函数关系。对两组数据进行拟合后,得到方程:k=0.003J0.423,R2=0.912,表明符合程度较高,k与J的0.423次方成正比。
综上所述,有效氯生成反应的表观动力学方程可表达为:-d(a-x)/dt=k1a-0.459J0.423(a-x),其中k1为表观反应速率常数。
3 结论
(1)在无隔膜电解槽中,采用电解法制备有效氯的质量浓度为450~500 mg/L的次氯酸钠溶液时,最优工艺参数为:进水流量75 mL/min、盐的质量浓度7 g/L、电流密度1.0 A/dm2、进水温度30 ℃。此时电流效率(23.8%)较高,运行费用(24.8元)最低。
(2)在本实验条件下,电解氯化钠生成有效氯的动力学反应级数为一级,即反应速率与盐的质量浓度的一次方成正比。
(3)表观反应速率常数k与初始氯化钠的质量浓度a的-0.459次方成线性关系,与电流密度J的0.423次方成线性关系,即反应动力学方程可写为:-d(a-x)/dt=k1a-0.459J0.423(a-x)。
