顶空气相法测定木质素中甲氧基含量
2021-05-06韦笑笑蒙丽丹覃程荣王双飞
刘 义 韦笑笑 蒙丽丹 卫 威,* 覃程荣 王双飞
(1.广西大学轻工与食品工程学院,广西南宁,530004;2.广西清洁制浆造纸与污染控制重点实验室,广西南宁,530004)
木质素是植物界中含量仅次于纤维素的天然大分子高聚物[1]。作为一种来源丰富、可再生的天然高分子聚合物,木质素具有广阔的应用前景,在木材化学、植物生化等相关领域都引起了越来越多的关注。木质素是一种由苯基丙烷结构单元通过醚键和C—C键连接而成的具有三维空间的高聚物[2]。苯基丙烷结构单元存在3 种类型[3],即愈创木基型(G)、紫丁香基型(S)和对羟苯基结构单元(H),其分别在苯环上含有1、2和0个甲氧基。木质素结构中含有许多官能团或功能基,如羧基、羟基、甲氧基和羰基等。甲氧基是木质素结构中的特征官能团,它们在木质素中的含量和分布与木质素的种类及分离方法有关。一般针叶木中甲氧基含量为14%~16%,阔叶木中甲氧基含量为19%~22%,草本类植物中甲氧基含量为14%~15%。木质素中准确的甲氧基含量不仅能够提供木质素的基本结构信息,还可以反映出化学改性过程的结构变化[4-5]。
甲氧基含量的测定[6-9]方法有化学法(质量法和容量法)与仪器分析法(色谱法、核磁共振法和电化学法等)。测定原理是使试样与氢碘酸(HI)作用,反应生成碘甲烷[10],采用不同方法测定生成碘甲烷含量,从而确定甲氧基含量[11-13]。目前应用较为广泛的是化学法中改进的溴化法[7],该方法具有准确度较高、操作简便等优点,但需要使用特殊定制的气密性玻璃器皿和较多的有毒化学试剂,且整个流程耗时较久。Goto 等人[10,14]使用了碳水化合物和木质素模型化合物研究了木质素甲氧基与碘离子形成碘甲烷的酸催化反应机理;发现碳水化合物的存在会影响甲氧基含量的测定,特别是一些木质素含量低的原料,如纸浆等;另外碳水化合物可能通过充当路易斯碱来干扰碘甲烷的形成速度,还会与HI 直接反应生成碘甲烷,影响测定结果。Li等人[11]以顶空气相法测定木质素中的甲氧基含量,该方法对木质素中甲氧基含量的测定具有良好的测量精度(RSD<0.69%)和准确度(RSD<3.5%),但引入NaOH 去中和过量的HI 会有副产物生成。Sumerskii 等人[8]建立了一种顶空同位素稀释(HS-ID)GC-MS 定量分析木质素中甲氧基和乙氧基的方法,该方法显示出了较好的精密度和准确度,但同位素的使用导致其不能广泛推广进行实验研究。
基于上述内容,本研究对顶空气相法进行了改进优化,以期建立一种简便、准确、可用于木质素及相关物质中甲氧基含量的高效测定方法。本实验选用柠檬酸钠作为终止反应剂,它是一种弱酸强碱盐,具有良好的pH 调节及缓冲性能;同时还选用涵盖木质素基本结构单元的G 型、S 型、H 型和5-5 缩合型等12种木质素模型化合物作为研究对象;使用模型化合物具有结构确定、可模拟木质素中的给定结构单元的优点,而不受真实木质素样品中存在的其他结构的干扰。
1 实 验
1.1 实验原料和试剂
实验使用的12种模型化合物结构式见图1,其中化合物IX、X、XI在实验室合成,其余均购自上海阿拉丁生化科技股份有限公司。云杉木粉,取自实验室。
氢碘酸、氨水、铁氰化钾,购于上海阿拉丁生化科技股份有限公司;柠檬酸三钠、过硫酸钠、氢氧化钠,购于天津市大茂化学试剂厂;硫酸亚铁、盐酸、抗坏血酸、乙酸乙酯、石油醚、丙酮,购于天津市致远化学试剂有限公司;碘甲烷,购于天津市风船化学试剂科技有限公司;硼氢化钠,购于成都金山化学试剂有限公司;无水硫酸钠,购于广州时金华大化学试剂有限公司。
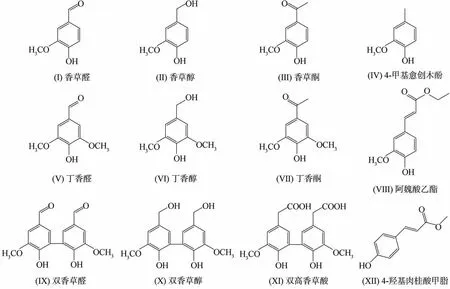
图1 12种木质素模型化合物结构式Fig.1 The structural formulas of 12 lignin model compounds
1.2 实验仪器
安捷伦7697A 顶空进样器;安捷伦8890 气相色谱系统;Bruker AVANCE III HD。
1.3 实验方法
1.3.1 HS-GC实验方法
根据Li等人[11]方法,采用HS-GC法测定木质素样品中甲氧基含量,并进行适当的改进。具体操作步骤为:将0.5 mL 质量分数57%的氢碘酸(HI)与10.0~20.0 mg 木质素样品(木粉40 mg)混合,置于20 mL顶空样品瓶中,用隔片密封;样品瓶置于油浴中,130℃加热30 min;然后冰浴冷却至室温,用注射器将1 mL 0.75 g/mL 柠檬酸钠(Na3C6H5O7·2H2O)溶液注射到密封的样品瓶中,中和多余的HI;立即放入顶空自动采样器进行HS-GC 检测。HS 条件为:烘箱温度50℃,定量环温度60℃,输送线温度70℃,GC循环时间7 min,样品瓶平衡时间15 min,加压时间0.25 min。气相色谱条件为:HP-5 毛细管柱(30 m×0.32 mm×0.25 μm) 30℃保 持5 min, 高 纯 氮 气(99.999%)载气流量3.8 mL/min,氢气和空气流速分别为40 mL/min和400 mL/min。检测器温度250℃,分流模式50∶1,进样口温度200℃。
1.3.2 标准曲线绘制
准确称取0~20 mg香草醛,按照1.3.1中的方法分别测定生成的碘甲烷(CH3I)峰面积,绘制香草醛物质的量与CH3I峰面积的标准曲线。
1.3.3 定量限[15-16]
按照1.3.1 中的方法,将CH3I 标准品逐步稀释,分别移取10 μL 稀释后的溶液和0.5 mL 质量分数57%的HI 置于20 mL 顶空样品瓶中,用隔片密封。其他条件保持不变,进行HS-GC 检测,按信噪比10∶1确定定量限。
1.3.4 重复性测试[11]
准确称取6份相同的香草醛,参照1.3.1中的方法进行平行测定,计算相对标准偏差(relative standard deviation,RSD)。
1.4 3种模型化合物的合成及1H、13C NMR表征
1.4.1 双香草醛(Ⅸ)的合成[17-19]
称取2.0 g 香草醛溶于200 mL 蒸馏水中,加热搅拌使其充分溶解;加入0.15 g 七水合硫酸亚铁(Fe-SO4·7H2O)和1.6 g 过硫酸钠(Na2S2O8)继续搅拌,反应5 min 后停止加热,生成的沉淀物待冷却至室温后用洗净的G5砂芯坩埚进行过滤,保留全部沉淀物。将上述沉淀物用25 mL 3 mol/L NaOH 溶液溶解,再向溶解液里加入15 mL 6 mol/L HCl 溶液进行第二次沉淀;过滤沉淀,用100 mL 热水分多次洗涤沉淀,洗净后放入真空干燥箱中直至干燥为止。所得双香草醛的合成见化学方程式(1)。
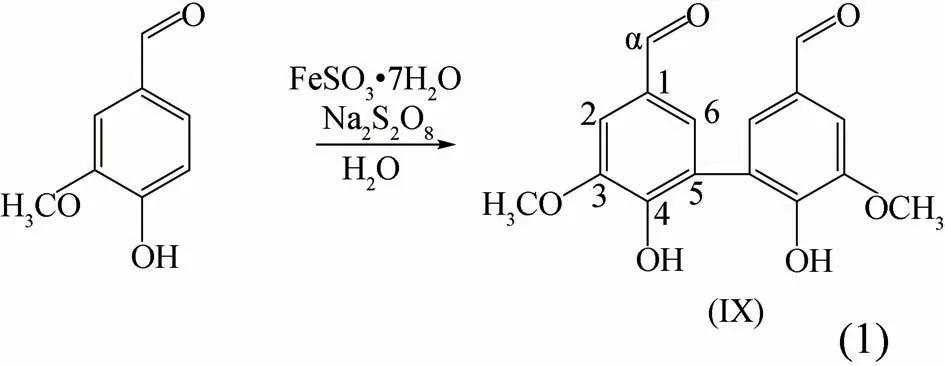
产物核磁共振结果显示为:1H NMR (500 MHz,DMSO,δ):9.81 (s,Hα),7.44 (s,H2,H6),3.94 (s,OCH3);13C NMR (500 MHz, DMSO,δ):191.64 (s, Cα),150.88 (s, C4), 148.62 (s, C3), 128.66 (s, C1), 128.24 (s,C5),125.04(s,C6),109.62(s,C2),56.51(OCH3)。
1.4.2 双香草醇(X)的合成[20]
称取6.0 g 双香草醛溶于100 mL 0.5 mol/L NaOH中(冰浴),缓慢加入3.6 g 硼氢化钠。室温下搅拌30 min,用HCl 酸化调至pH 值=7;反应结束后过滤收集沉淀,产品在真空80℃下干燥过夜。所得双香草醇(X)得率为90%。合成双香草醇(X)的化学方程式见式(2)。
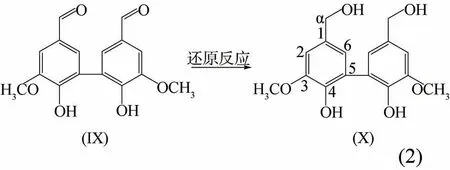
产物核磁共振结果显示为:1H NMR (500 MHz,DMSO,δ): 6.88 (s,H6),6.67 (s,H2),4.41 (d,Hα),3.81 (s,OCH3);13C NMR (500 MHz, DMSO,δ): 147.94(s, C4), 142.78 (s, C3), 133.08 (s, C1), 126.14 (s, C5),121.83 (s, C6), 109.68 (s, C2), 63.54 (s, Cα), 56.25 (s,OCH3)。
1.4.3 双高香草酸(Ⅺ)的合成[21]
称取3.0 g 4-羟基-3-甲氧基苯乙酸(高香草酸)溶于30 mL 蒸馏水和5 mL 浓氨水中,再缓慢加入6.0 g 铁氰化钾,搅拌均匀。5 min 后加入1.0 g 抗坏血酸(L-Ascorbic acid),用HCl 酸化调至pH 值=7;随后用乙酸乙酯萃取,萃取液用无水硫酸钠干燥后,旋转蒸发至干燥。再用石油醚-乙酸乙酯进行重结晶。所得双高香草酸的合成见化学方程式(3)。
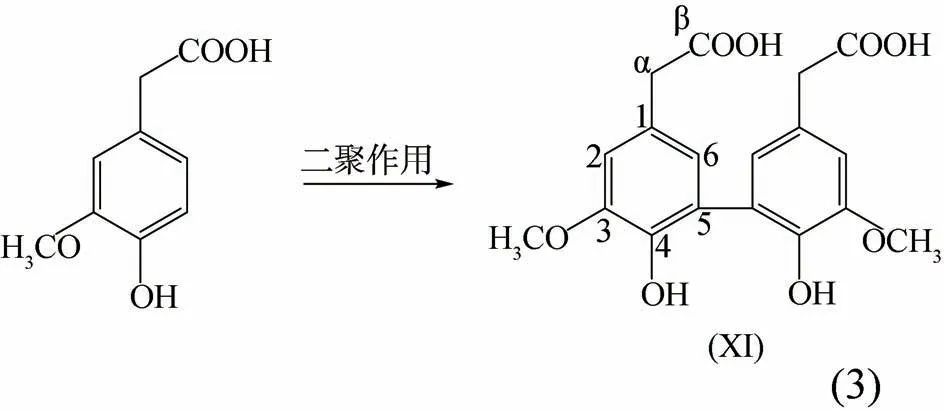
产物核磁共振结果显示为:1H NMR (500 MHz,DMSO,δ):6.83(s,H6),6.60(s,H2),3.46(d,Hα),3.80 (s, OCH3);13C NMR (500 MHz, DMSO,δ):147.93 (s, C4), 142.83 (s, C3), 126.11 (s, C1), 125.39 (s,C5),124.25(s,C6),112.26(s,C2),56.34(s,OCH3)。
2 结果与讨论
2.1 香草醛物质的量与CH3I 峰面积标准曲线与仪器定量限
图2 为香草醛物质的量与CH3I 峰面积标准曲线。如图2所示,香草醛物质的量与CH3I峰面积线性关系良好,通过计算得到标准曲线方程为y=94755x+143.7,R2=0.9995(其中x为木质素模型物香草醛物质的量,mmol,y为CH3I 峰面积)。通过逐步稀释碘甲烷标准溶液,使之信噪比接近10∶10。定量限测定结果表明,在本方法中定量限为1.52 μg(信噪比为10.2∶1)。
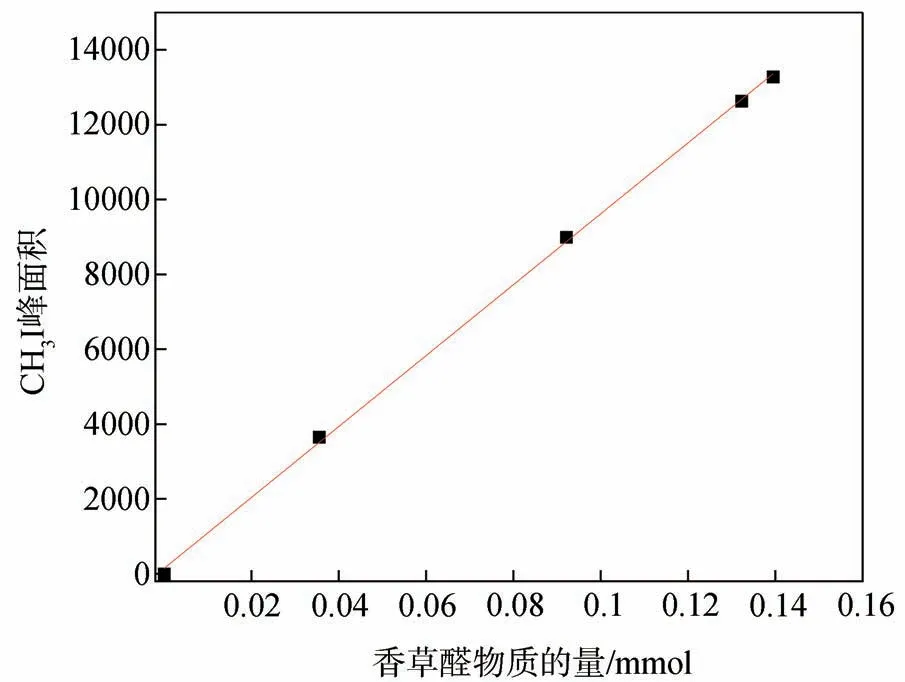
图2 香草醛物质的量与CH3I峰面积标准曲线Fig.2 The standard curve of vanillin molality with iodomethane peak area
2.2 香草醛样品重复性测试
图3 为香草醛样品重复性测试色谱图。由图3 可知,在空白样品测试中未出现CH3I 峰,说明仪器稳定,实验中所使用试剂等不会引入系统误差。且6组平行样中(V1~V6)出峰时间(即保留时间)一致,峰面积接近(结果见表1),重复性良好,峰面积RSD为1.70%。
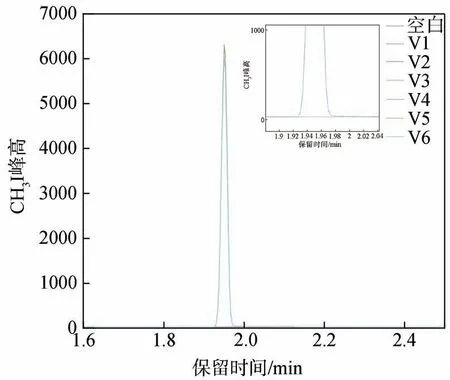
图3 香草醛的重复性测试顶空气相色谱图Fig.3 HS-GC chromatogram of repeated test of vanillin
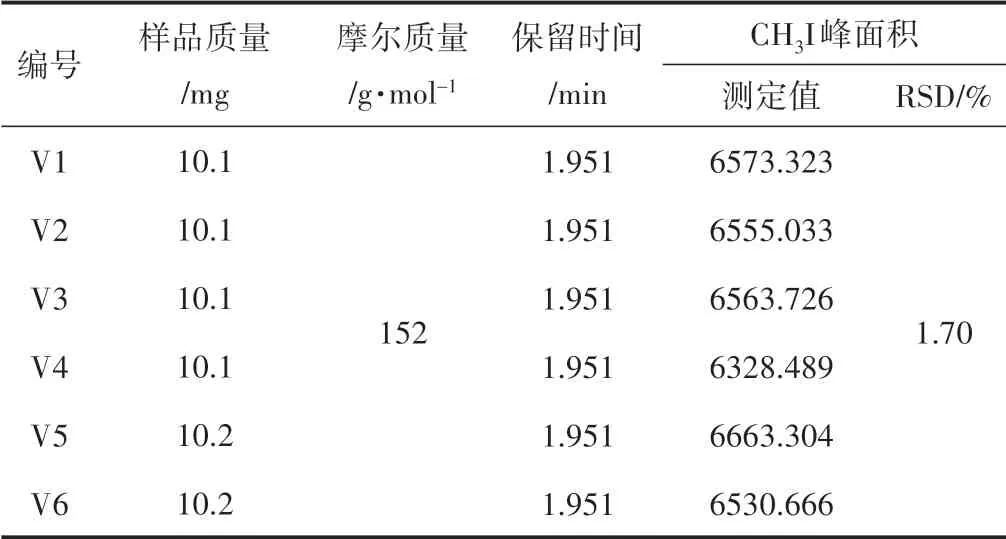
表1 香草醛的重复性测试结果Table 1 The repeatability test results of vanillin
2.3 12种模型物中甲氧基含量的测定
表2 为12 种模型物中的甲氧基含量。从表2可以看出,模型物IX、模型物X 甲氧基含量测定值低于理论值,可能的原因是2 种模型物在HI 中溶解性不好,不能与之充分反应,导致最终测定值偏小;其次,5-5 结构在木质素中含量较少,尤其是双香草醛含量更少,可认为对测定结果影响不大。其他10 种模型物中甲氧基含量测定值与理论值相比的RSD<3%,说明改进的顶空气相测定木质素甲氧基含量的方法准确、可靠。
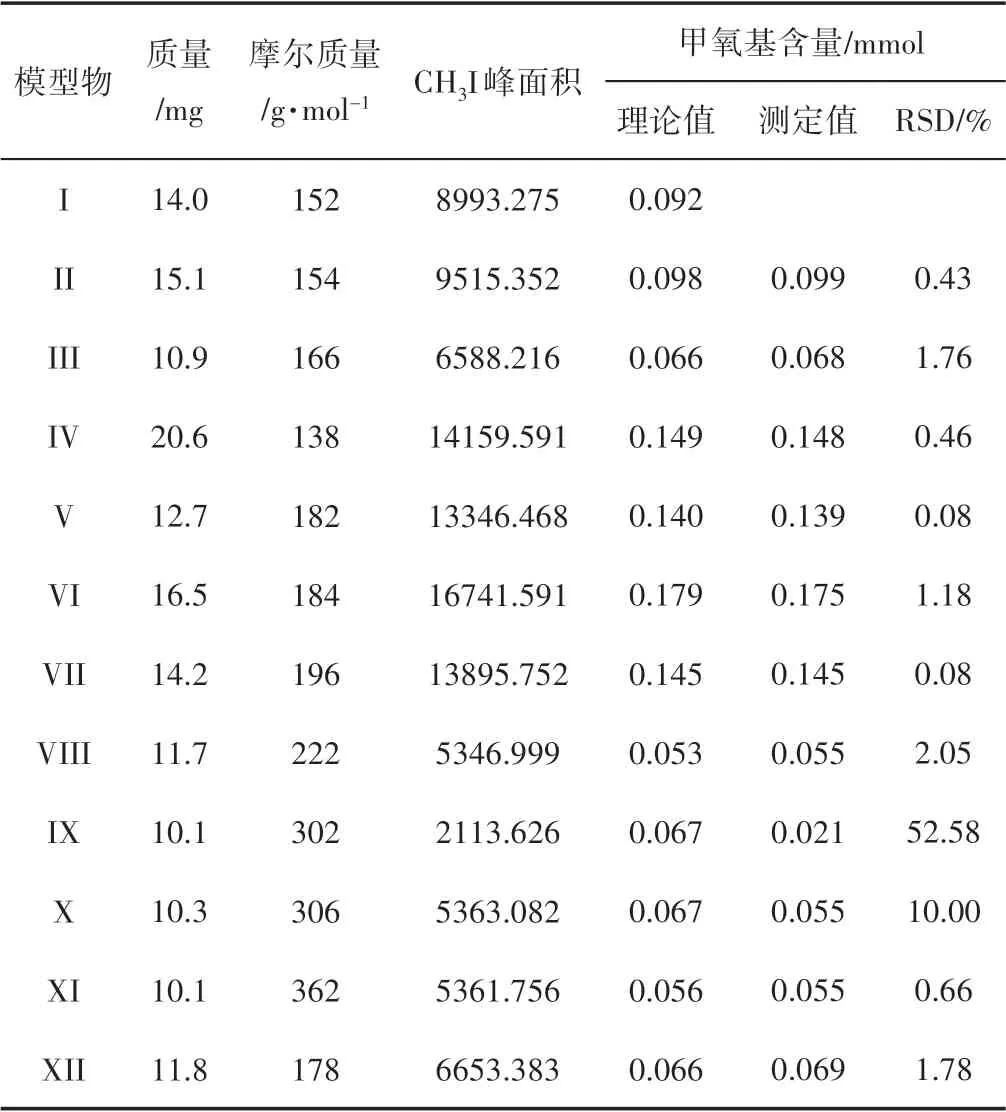
表2 12种模型物中的甲氧基含量Table 2 The content of methoxyl in lignin model compounds
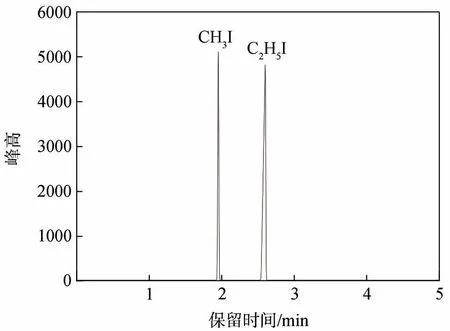
图4 阿魏酸乙酯的顶空气相色谱图Fig.4 HS-GC chromatogram from ethyl ferulic acid
图4 为模型物阿魏酸乙酯的顶空气相色谱图。由图4可以看出,模型物VIII(阿魏酸乙酯)与HI反应不仅生成CH3I,还会有大量副产物碘乙烷(C2H5I)生成,因此以CH3I 作为内标[9-10]测定甲氧基含量可能存在一定的误差。综上,本研究采用外标法计算木质素中甲氧基含量比较合理。
2.4 丙酮抽提云杉木粉的甲氧基含量测定
准确称取40 mg 40~60 目云杉木粉(水分10.06%,Klason木质素含量为27.91%)丙酮抽提28 h,之后操作与1.3.1 中的方法相同。同时以滴定法的结果作对照,具体测定结果见图5。
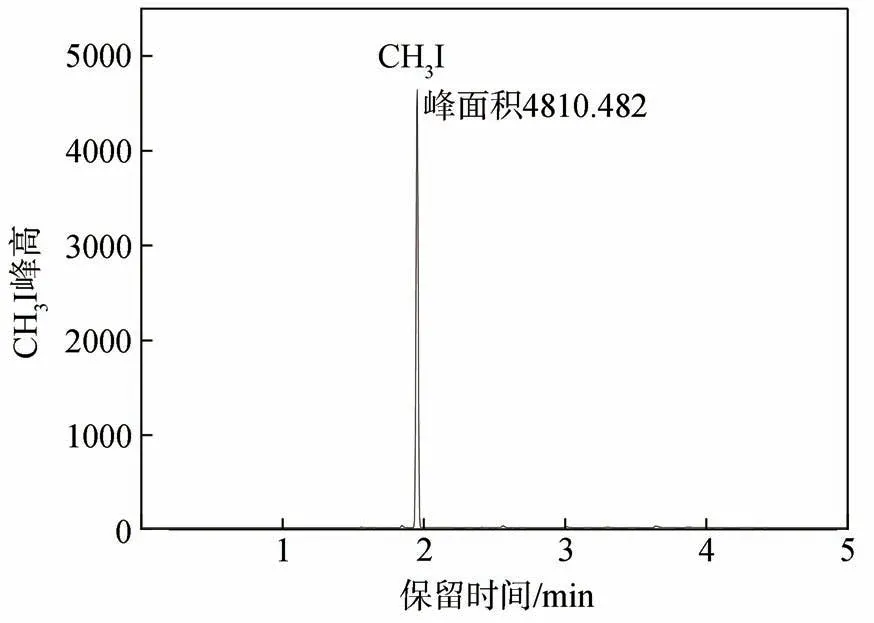
图5 云杉木粉顶空气相色谱图Fig.5 HS-GC chromatogram from spruce wood powder
从图5 可知,通过本方法测定丙酮抽提后云杉木粉(以Klason 木质素计) 的甲氧基含量为4.6560 mmol/g,同时使用滴定法测定的甲氧基含量为4.6028 mmol/g,与本方法测定值的RSD<1%。表明本方法对于直接测定植物纤维原料木质素中甲氧基含量也是合理的。
3 结 论
本研究通过向木质素中注入柠檬酸钠溶液来中和过量的氢碘酸(HI),然后使用顶空气相色谱间接测定12种木质素模型物甲氧基含量。
3.1 选用12 种木质素模型化合物和丙酮抽提后云杉木粉验证改进后测定方法的准确性和可靠性。结果表明,模型物IX、模型物X 中甲氧基含量测定值低于理论值,因其在木质素结构中所占比例较低,不影响最终测定结果;其他10 种模型物中甲氧基含量测定值与理论值的RSD<3%。
3.2 丙酮抽提后云杉木粉(以Klason 木质素计)甲氧基含量为4.6560 mmol/g,以滴定法作为对照测定的甲氧基含量为4.6028 mmol/g,两者RSD<1%。因此,改进后的顶空气相色谱法准确、可靠,可以实现快速测定原料中甲氧基含量。
