头孢呋辛酯胃黏附微丸的制备
2021-03-25申丽先张媛婷张娟
申丽先,张媛婷,张娟
(1.天津红日药业股份有限公司,天津 301700 ;2.大庆师范学院生物工程学院,黑龙江大庆 163712)
头孢呋辛酯是一种β-内酰胺类抗生素,属于时间依赖型抗菌素,抗菌效果随着血药浓度高于最低抑菌浓度的时间延长而增加。临床上广泛用于治疗呼吸道感染、尿路感染、淋球菌型感染等的治疗。文献表明,在胃中滞留时间延长,有利于头孢呋辛酯的溶出[1]。
本文以头孢呋辛酯为模型药物,制备1 次/天给药的胃黏附微丸,增加药物在胃内的滞留时间,使药物缓慢到达最佳吸收位点,保持血药浓度平稳,增加药物的杀菌效果,提高生物利用度。
1 仪器与试剂
1.1 仪器
高效液相色谱系统(日本JASCO 公司);JBZ-300 型多功能微丸包衣造粒机(辽宁医联新药研究所);BS110S 分析天平(德国Sartorius 仪器公司);HL-2 型恒流泵(上海精科实业有限公司);KQ-100型超声分散机(昆山市超声仪器有限公司);SZ-93自动双重纯水蒸馏器(上海亚荣生化仪器厂);ZRS-8L 多功能溶出仪(天津天大天发科技有限公司);UV-2000 紫外-可见分光光度计(尤尼柯上海仪器有限公司)
1.2 药品与试剂
头孢呋辛酯(联邦制药有限公司,批号:322112030);微晶纤维素(江苏省常熟市药用辅料有限公司);卡波姆(型号934 P,上海申兴制药厂);聚乙烯吡咯烷酮(型号K30,天津市博迪化工有限公司);十八醇(天津博迪化工股份有限公司);甲醇(色谱纯)山东禹王实业有限公司;磷酸二氢铵(天津市博迪化工有限公司);浓盐酸(沈阳经济技术开发区试剂厂);无水乙醇(山东禹王化工有限公司);试剂均为分析纯。
2 方法与结果
2.1 微丸质量考察指标
2.1.1 样品含量
头孢呋辛酯有(R,R,R)(R,R,S)两种非对映异构体。目前销售的药品是无定型(R,R,R)和(R,R,S)两种非对映异构体的1∶1 等量混合物。液相检测时可以得到头孢呋辛酯A、B 两个异构体峰,二者相对保留时间分别为1.0、0.9。当A 异构体峰面积与头孢呋辛酯A、B 异构体峰面积和之比为0.48~0.55 时,可用两峰面积之和计算头孢呋辛酯浓度,否则需单独计算。
头孢呋辛酯溶液室温放置易降解,测量时应尽快,最好小于3 h,或将溶液放置于4 ℃冰箱当天使用[2]。
2.1.1.1 色谱条件
色 谱 柱:DiamonsilRC18(250 mm×4.6 mm,5 μm);流动相:0.2 mol/L 磷酸二氢铵溶液-甲醇(55∶45);检测波长:276 nm;流速:1.0 mL/min;柱温:25 ℃;进样量:20 μL。
2.1.1.2 微丸含量测定
取头孢呋辛酯胃黏附微丸适量,研细,精密称取细粉适量(约相当于头孢呋辛酯125 mg),置100 mL 量瓶中,加甲醇25 mL,超声溶解,流动相稀释至刻度,摇匀,滤过。取续滤液5 mL,置25 mL 量瓶中,用流动相稀释至刻度,摇匀,立即精密量取20 μL,注入液相色谱仪,记录色谱图;另精密称取头孢呋辛酯对照品适量,同法测定。按外标法以峰面积计算样品含量n,公式如下:
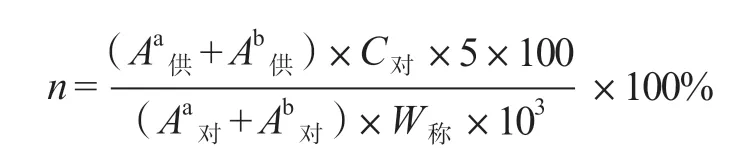
C对——对照品浓度,mg/mL;
W称——称样量,g。
2.1.2 体外释放度测定
取头孢呋辛酯胃黏附缓释制剂(相当于含头孢呋辛酯250 mg),采用第二法桨法[3],以0.1 mol/L 盐酸溶液900 mL 为释放介质,转速为50 r/min,依法操作,在0.5 h、1 h、2 h、4 h、6 h、8 h、10 h 时,分别取溶液5 mL,并及时在操作容器中补充释放介质5 mL。将取出的溶液用0.8 μm 滤膜滤过,分别精密量取续滤液适量,用释放介质定量稀释制成每1 mL 约含15 μg 药物的溶液,作为供试品溶液,照紫外分光光度法[4],在280 nm 测定溶液吸光度,并由随行标准曲线计算不同时间的累积释放量。实验过程中,整个溶出装置和取出的样品都应注意避光。
2.1.3 黏附性能的测定
SD 大鼠禁食供水饲养24 h 后处死。取胃,沿胃大弯剪开,小心除去胃中内容物,取1 cm×2 cm 胃组织平铺于载玻片上。分别在胃粘膜撒上约100 粒微丸,用生理盐水润湿后,将载玻片置于相对湿度92.5%的密闭容器内保湿30 min。载玻片取出固定在45 °斜面上,用pH 值1.2 稀盐酸—氯化钠溶液冲洗胃粘膜表面(22 mL/min)5 min 后,计数胃粘膜表面滞留微丸数,计算微丸黏附率[5-6]。
2.2 头孢呋辛酯胃黏附微丸制备
本文以卡波姆为黏附材料、十八醇为缓释材料、微晶纤维素为填充剂进行头孢呋辛酯胃黏附微丸的制备。经过尝试,微丸载药量可达到50%。
采用挤出滚圆的方式进行头孢呋辛酯胃黏附微丸的制备,按处方量称取头孢呋辛酯原料药,加入适量的卡波姆、十八醇、微晶纤维素,过80 目筛混匀,加入一定比例的乙醇-水(含有适量PVP),捏合至软材,将软材置于挤出滚圆机内,经挤出机筛板(孔径0.9 mm)挤出,条状物料置滚圆机内,调节转速和滚圆时间,使条状物切断成颗粒并滚圆,取出微丸置于40 ℃烘箱干燥,过筛得24~30 目的目标微丸。
2.2.1 黏附材料用量筛选
采用2.2 工艺参数制备含有不同含量卡波姆的微丸(固定载药量50%、十八醇10%,以微晶纤维素为填充剂)。考察卡波姆0%、5%、7.5%、10%、12.5%、15%含量时对微丸圆整度、黏附效果的影响。结果,随着卡波姆含量增加,软材的弹性增大,挤出时物料呈长条状不易断开。含量小于12.5%时,制备的微丸较不加入卡波姆的处方微丸粒径均匀。12.5%含量时制备的微丸表面不太光滑,有少量短棒状出现,15%含量制备的微丸出现大量棒状、长条状。
筛选24~30 目的微丸进行黏附率测定,结果见图1。随卡波姆含量的增加,黏附效果增强,10%含量黏附率为96.41%,因此兼顾微丸圆整度,将卡波姆含量确定为10%。
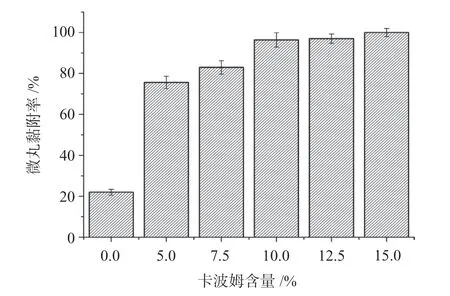
图1 不同含量卡波姆对微丸黏附性能的影响Fig.1 Effect of different percent of Carbomer on the adhesion property
2.2.2 缓释材料用量筛选
采用2.2 工艺参数制备含有不同含量十八醇的微丸(固定载药量50%、卡波姆10%,以微晶纤维素为填充剂)。考察不同含量十八醇对微丸释放、黏附的影响,结果见图2、图3。

图3 不同含量十八醇对微丸黏附性能的影响Fig.3 Effect of the amount of octadecanol on the adhesion behavior
从图2 可以看出,随着十八醇量的增加,药物释放减慢。不含十八醇的含药微丸前期释放太快,4 h 释放将近60%,后期释放减慢。含有15%十八醇的含药微丸体外释放较慢,10 h 释放小于80%。十八醇含量为5%或10%时药物释放曲线符合10 h缓释要求。
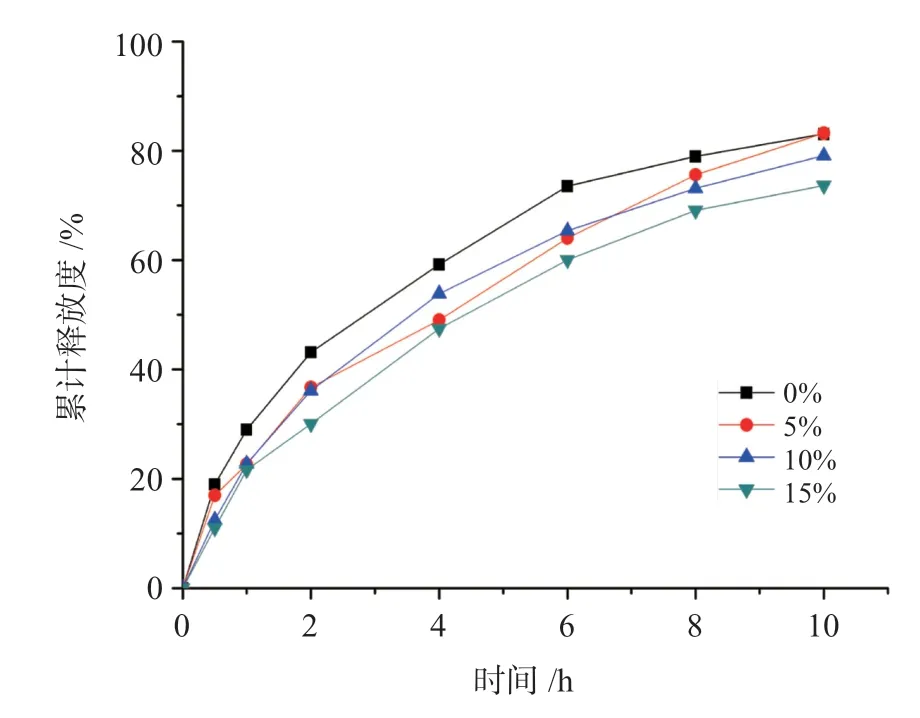
图2 不同含量十八醇对微丸释放度的影响Fig.2 Effect of the amount of octadecanol on drug release
从图3 可知,处方中十八醇的含量对微丸黏附性能影响不大。
2.3 处方工艺重现性考察
固定处方:50%药物,10%卡波姆,10%十八醇,30% MCC,采用2.2 工艺参数制备3 批头孢呋辛酯胃黏附微丸,并进行体外释放度、体外黏附效果考察,结果见图4、图5。结果显示,筛选的处方工艺具有良好的重现性。制备的微丸圆整度好,体外释放度、黏附率均符合要求。
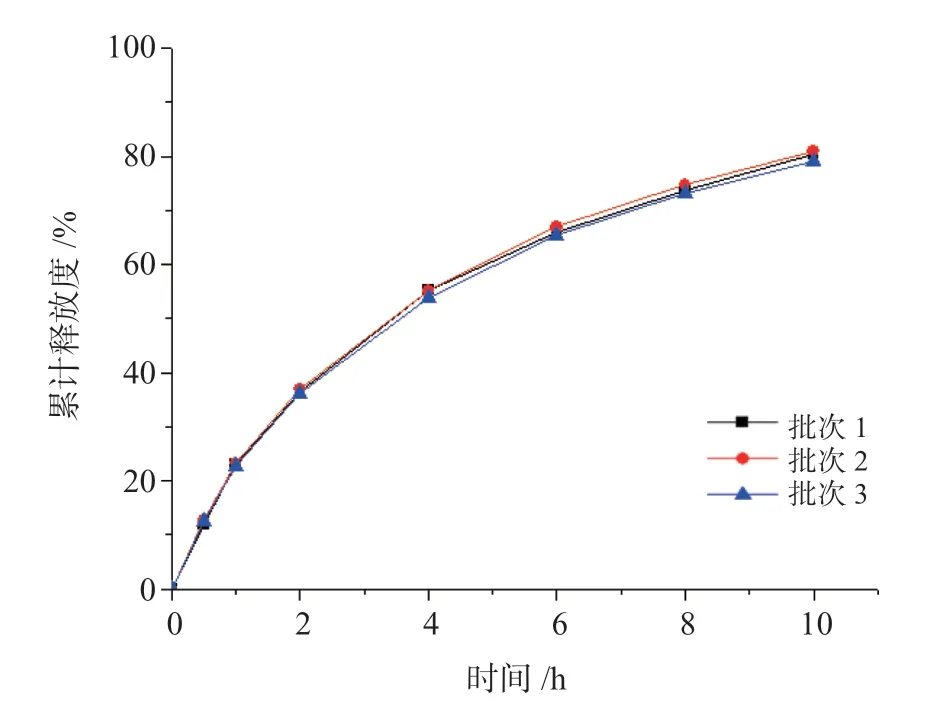
图4 三批微丸的体外释放度结果Fig.4 The release profiles of three batches of pellets
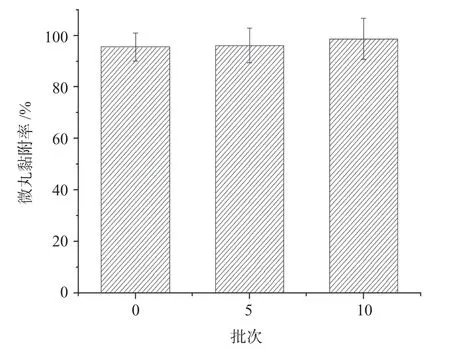
图5 三批微丸的体外黏附效果Fig.5 The adhesiveness property of three batches of pellets
3 讨论
胃黏附制剂直接借助于某些高分子材料对生物粘膜产生的粘合力而黏附于胃粘膜上皮部位,从而延长药物在胃内的滞留时间和释放时间,促进药物吸收,提高生物利用度[7],同时具有靶向、避免首过效应、增加依从性等优点。
头孢呋辛酯是一种时间依赖型抗菌素,血药浓度超过所针对细菌的最低抑菌浓度的时间越长,杀菌效果越好,并且头孢呋辛酯在小肠上端部位吸收最佳,所以本文以头孢呋辛酯为模型药物进行胃黏附微丸的制备。
卡波姆作为一种辅料已被多国药典收载,并已广泛用于制药工业,是一种公认的无毒的黏附材料。亦有许多文献报道显示,卡波姆的黏附性能要优于其他黏附材料。因此选用卡波姆为胃黏附微丸的黏附材料[8]。
4 结论
本文采用挤出滚圆的方法,以卡波姆为黏附材料、十八醇为缓释材料、微晶纤维素为填充剂进行了头孢呋辛酯胃黏附微丸的制备。通过考察了黏附材料、缓释材料的用量对微丸体外黏附效果、体外释放度的影响,优化了微丸处方。确定的处方工艺重现性好,可达到10 h 的缓释效果,体外黏附率高。
