改性粉煤灰对燃煤电厂脱硫废水中氯离子的吸附性能
2021-03-15刘凌寒高良敏张金昕王硕包文运向朝虎吴晔
刘凌寒,高良敏, *,张金昕,王硕,包文运,向朝虎,吴晔
(1.安徽理工大学地球与环境学院,安徽 淮南 232001;2.大唐环境产业集团股份有限公司,江苏 南京 211106)
中国目前有91%的电厂采用石灰石−石膏湿法烟气脱硫技术[1]。湿法脱硫技术会产生大量废水,其中就含有高浓度的Cl−,这对后期的中水回用会造成一定的影响,因此实现脱硫废水的零排放是目前亟需解决的问题。在脱硫系统运行时,吸收塔内浆液中的Cl−会逐渐富集,对脱硫设备和周边环境都会造成很大的危害,同时也会对输水管道产生腐蚀作用[2]。目前处理脱硫废水的方法包括化学沉淀法、生物物理法、蒸汽浓缩蒸发法等,但这些方法对Cl−的去除效率不是太高[3]。现如今,吸附法因操作简便、适用性广而被认为是一种低投入和效果佳的好方法。学者们研究了许多吸附剂的结构修饰,包括将更合适的表面官能团引入到吸附剂基质中[4]。
粉煤灰作为一种常见的工业固体废弃物,因其物理特点与化学组成等特性而成为适用于废水处理的材料[5]。对粉煤灰改性是目前固废吸附材料的一大研究热点,即利用粉煤灰与其他物质结合,如与类水滑石混合时对Cl−的去除率可达到88.89%[6],通过对粉煤灰的改性可以增强其吸附能力,Visa等人[7]在粉煤灰中加入NaOH和十六烷基三甲基溴化铵(HTAB)来处理污染物,发现其比表面积增加,表面电荷性质发生变化,增强了对污染物的吸附性能。
虽然目前粉煤灰在废水处理方面的应用有一定的研究报道,但对燃煤发电厂脱硫废水中 Cl−的去除及其最优参数等的研究还不够全面。本文采用HNO3与粉煤灰混合搅拌,添加发泡剂和助溶剂,然后运用高温煅烧对粉煤灰进行改性,很好地利用了HNO3和双氧水能够氧化粉煤灰,并与发泡剂和助溶剂在粉煤灰内部发生反应产生大量气泡并制造大量孔隙这一特点。通过改变反应温度、投加量、pH、反应时间等反应条件,利用不同吸附模型拟合来研究其对燃煤电厂脱硫废水中高浓度Cl−的吸附性能,然后通过X射线衍射仪(XRD)和红外光谱仪(FTIR)来分析改性前后及吸附反应后粉煤灰的变化特征,进一步探讨改性粉煤灰对脱硫废水中Cl−的吸附机理,以期为粉煤灰资源化利用、以废治废提供一定的参考。
1 实验
1.1 材料
脱硫废水取自天津某电厂初沉池进水口,经过一般过滤处理后的水质指标如下:pH 6.97,Ca2+1 565 mg/L,Mg2+20 733 mg/L,Pb2+1.08 mg/L,Cl−7 133 mg/L,F−82.5 mg/L,悬浮物 241 mg/L,Cr3+2.12 mg/L,Ni2+0.94 mg/L。
粉煤灰来自安徽省淮南市某电厂。首先称取一定质量的粉煤灰于研钵中,按每克粉煤灰 9 mL的量添加1.80 mol/L HNO3溶液,反应120 min。按粉煤灰质量的30%添加CaCO3作为发泡剂,再加入相当于粉煤灰质量8%的CaO作为助熔剂,研磨至均匀后加入一定量的双氧水,再搅拌,最后置于马弗炉内,920 °C煅烧60 min。自然冷却后研磨至粉末状进行后续实验。
1.2 表征方法
采用日本理学SmartLab SE型X射线衍射仪(XRD)和美国赛默飞Nicolet iS50型傅里叶变换红外光谱仪(FTIR)对粉煤灰改性前后以及吸附前后的物相组成、晶体结构、官能团等变化进行研究。
1.3 批量吸附实验及方法
在一系列容积为250 mL的锥形瓶中装入100 mL脱硫废水,设置以下反应条件:温度25 ~ 45 °C,粉煤灰质量浓度 5 ~ 35 g/L,pH 4 ~ 8,Cl−起始浓度 1 425 ~ 7 133 mg/L,反应时间 0 ~ 400 min,振荡速率180 r/min。pH用0.1 mol/L NaOH和0.1 mol/L HCl来调节。Cl−的测定参照GB/T 11896-1989《水质 氯化物的测定 硝酸银滴定法》,做3组平行试验。平衡吸附量qe(单位:mg/g)的计算如式(1)所示,Cl−去除率w按式(2)计算。

式中,m表示吸附剂的用量(单位:g),V表示水样体积(单位:L),ρ0表示Cl−的初始质量浓度(单位:mg/L),ρe表示平衡时 Cl−的质量浓度(单位:mg/L)。
1.3.1 吸附等温学研究
采用Langmuir[8]、Freundlich[9]、Temkin[10]三种等温吸附模型来分析数据,分别见式(1)、(2)和(3)。

式中,qm(单位:mg/g)表示吸附剂的最大吸附量,KL是Langmuir平衡常数,KF和n分别是Freundlich平衡常数和吸附强度,k1和k2是Temkin平衡常数。
1.3.2 吸附热力学研究
平衡吸附分配系数Kd(单位:mL/g)由式(6)计算[11],ΔG0(单位:J/mol)由式(7)计算,ΔS0[单位:J/(mol·K)]、ΔH0(单位:J/mol)分别是熵变、焓变,可由式(8)拟合计算得出[12]。

式中,R是气体摩尔常数,即8.314 J/(mol·K),T是反应温度(单位:K)。
2 结果与讨论
2.1 单因素实验分析
2.1.1 改性粉煤灰投加量的影响
在pH为6.97,室温(25 °C)下以180 r/min振荡400 min,从图1可以看出,改性粉煤灰质量浓度从5 g/L增大到35 g/L时吸附量逐渐减少,5 g/L时的吸附量最大,达到65.53 mg/g,到了15 g/L时吸附量下降到51.62 mg/g。随着改性粉煤灰投加量的继续增大,Cl−的去除率增大在质量浓度为25 g/L时,Cl−的去除率达到最大(56%),并且随着投加量的继续增大,去除率基本趋于稳定。因此可以得出改性粉煤灰吸附Cl−的最佳投加量为25 g/L。随着粉煤灰投加量增大,吸附点位增多,吸附Cl−的量增大,但单位质量吸附剂的脱氯量减少。同时投加量增大也会使吸附剂与溶液不能充分混合,其孔隙或吸附位点不能与被吸附物质充分接触,进而导致吸附量不断减小[13]。如图1所示,随着投加量的增大,吸附量整体呈现下降趋势,投加浓度在25 g/L之后吸附量仅为37.56 mg/g,这可能是因为改性粉煤灰内部还有许多吸附位点没有被Cl−占据,吸附没有达到饱和状态[14]。
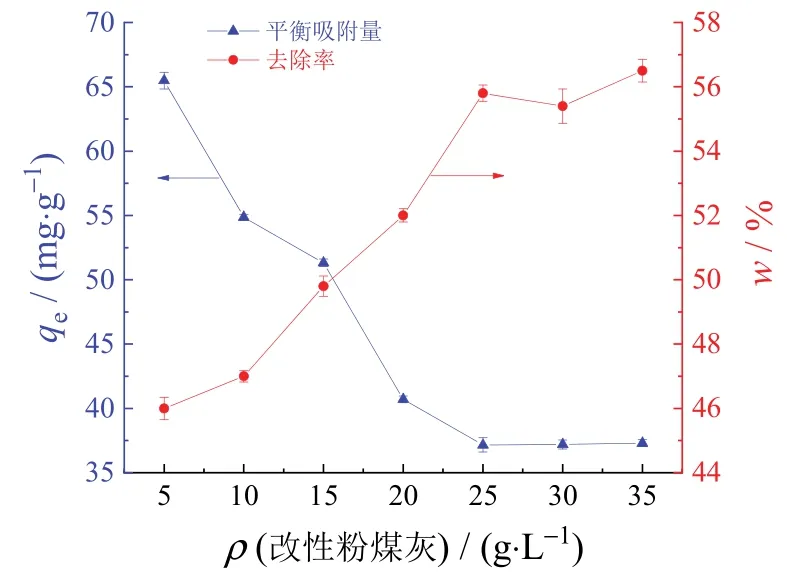
图1 改性粉煤灰投加量对Cl−吸附量和去除率的影响Figure 1 Effect of modified fly ash dosage on adsorption amount and removal of Cl−
2.1.2 pH的影响
在25 °C下投加1.0 g改性粉煤灰,以180 r/min振荡反应400 min。pH是控制吸附过程的重要的因素之一,它能够通过改变粉煤灰表面的电荷来影响其吸附能力。由图2可知,pH在4.0 ~ 8.0范围之间变化时,改性粉煤灰对Cl−的吸附量呈现不同特征,在酸性条件下的吸附效率高于碱性条件,而酸性条件下pH为5时吸附量最大,达到80.9 mg/g。中等酸度条件下的吸附量比强酸条件下大,可见pH在一定程度上会改变粉煤灰的活性位点。随着pH升高,OH−增多,与Cl−形成竞争吸附。低pH时含有高浓度的H+,过高的H+浓度会抑制Cl−的吸附。通过XRD分析可知,粉煤灰中含有大量金属氧化物(如Al2O3、Fe2O3、MgO等),它们在酸性条件下会解离而产生大量正电荷,从而增强对Cl−的吸附能力[15]。然而,Al2O3在酸浓度过高的情况下会发生钝化,致使Al3+不能很好地与Cl−发生离子交换、电中和等化学反应。
2.1.3 反应时间的影响
在pH为6.97,温度为25 °C,搅拌转速为180 r/min的条件下,加入1.0 g改性粉煤灰振荡反应不同时间。由图3可以看出,前50 min反应很快,因为吸附剂表面存在大量吸附Cl−的位点。随着反应的进行,由于吸附剂表面部分位点已经被占据,位点数急剧下降。在第50 ~ 200 min之间,吸附量增长较为缓慢,280 min后吸附位点达到饱和。通常情况下,被吸附物质会在吸附剂表面形成大约一层分子厚度的薄层[16]。因此在该实验参数条件下,适宜的反应时间在280 min左右。
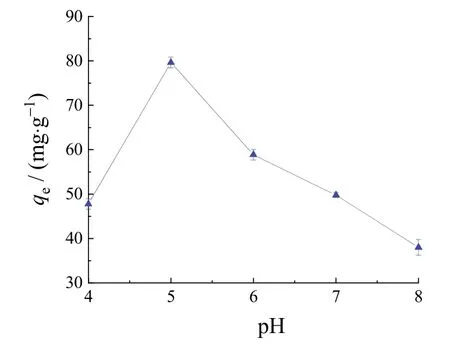
图2 pH对Cl−吸附量的影响Figure 2 Effect of pH on adsorption amount of Cl−
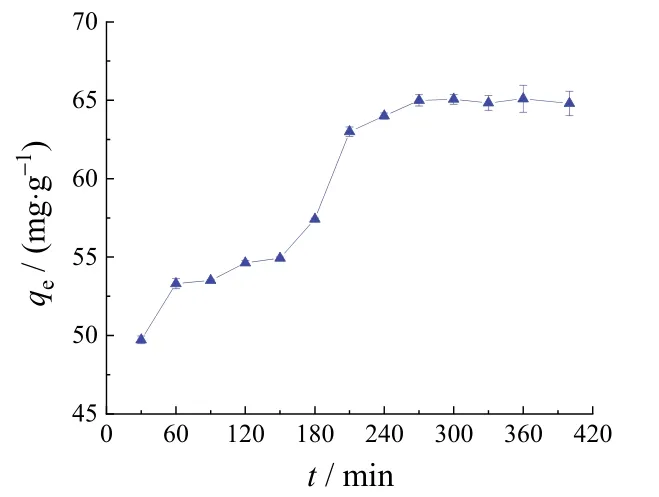
图3 反应时间对Cl−吸附量的影响Figure 3 Effect of reaction time on adsorption amount of Cl−
2.2 吸附等温学
先前已有研究表明温度对吸附过程确实存在着一定的影响[17],因此分别在不同温度梯度下,利用Langmuir、Freundlich、Temkin这3种模型来研究改性粉煤灰对Cl−的等温吸附过程,结果见图4和表1。单从表2的决定系数(R2)来看,这3种模型都能够描述改性粉煤灰对Cl−的吸附过程。在25 °C和45 °C时,Langmuir模型描述吸附过程更加准确,35 °C下Freundlich模型更合适。Temkin模型在3个温度下的适用性均差一点。
在25 °C下,Langmuir模型的R2(0.993)大于Temkin模型的R2(0.980)及Freundlich模型的R2(0.965),表明此温度下产生的化学吸附过程占比大。在35 °C下,Freundlich模型的R2(0.983)大于Langmuir模型的R2(0.973)和Temkin模型的R2(0.957),表明此温度下化学吸附不是唯一的,还存在其他形式的吸附过程。在45 °C时,Langmuir模型的R2(0.993)大于Temkin模型的R2(0.980)和Freundlich模型的R2(0.989),表明此时化学吸附能力很强。对于Langmuir模型,KL越大,表明化学吸附能力越强,可见45 °C时KL最大,说明45 °C下的饱和吸附量应该最大。从理论最大吸附量来看,也是45 °C时最大。Temkin模型的R2在0.957 ~ 0.980之间,也能很好地描述等温吸附过程。综合来看,采用Langmuir模型描述该实验的等温吸附过程更具优势。此结果也表明在一定温度范围内,随着温度的升高,吸附剂对氯离子的吸附量不断增大,吸附量与反应温度呈正相关,这与Huang等人[18]的研究结论相似。

图4 改性粉煤灰在不同温度下吸附Cl−的吸附等温线Figure 4 Adsorption isotherms for adsorption of Cl− by modified fly ash at different temperatures

表1 改性粉煤灰吸附Cl−的等温吸附参数Table 1 Isothermal adsorption parameters for modified fly ash to adsorb Cl−
2.3 吸附热力学
如表2所示,随温度升高,ΔG0的绝对值增大,说明改性粉煤灰吸附Cl−反应在25 ~ 45 °C内是自发的。ΔH0是正值,表明整个吸附反应是吸热的。ΔS0是正值,表明Cl−在粉煤灰表面的反应比较随机,且对粉煤灰具有很高的亲和力,这对去除Cl−具有一定的作用。可能是因为随着温度的升高,在吸附过程中溶液与吸附剂之间界面反应的机性增大[19]。
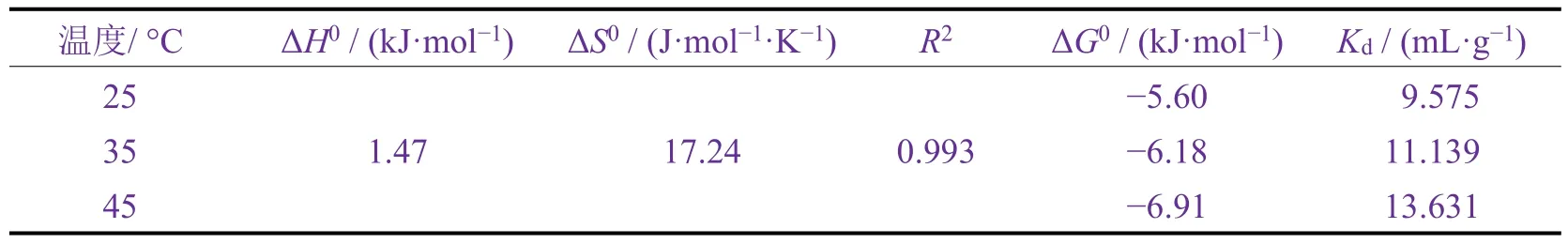
表2 改性粉煤灰吸附Cl−的热力学参数Table 2 Thermodynamic parameters for modified fly ash to adsorb Cl−
2.4 表征分析
为了进一步研究 Cl−被改性粉煤灰吸附的机理,分别对未改性粉煤灰及改性粉煤灰吸附废水前后进行XRD和FTIR分析。
2.4.1 XRD分析
从图5可以看出,改性粉煤灰在吸附前后的XRD谱图有很大差别。通过MDI Jade6软件进行物相分析并与JCPDS标准卡片对比,得出粉煤灰的主要成分有石英和莫来石,前者主要由SiO2组成,后者由3Al2O3·2SiO2组成。加酸高温以及发泡处理后,莫来石和石英的衍射峰均减小,可能是由于改性使得Si─O键和Al─O键得以打开,最终激活了SiO2/Al2O3这样的稳定物质[20]。粉煤灰吸附脱硫废水后莫来石和石英的衍射峰均有一定程度的增大,这也就证明了活性Al2O3和SiO2能够在一定程度上增强吸附性能。物质成分的改变令Si与Al等正价元素能够与Cl−很好地发生离子交换反应,改性后的粉煤灰在2θ为64°和67°处有明显的CaO峰,说明助溶剂中的Ca成功负载到了粉煤灰内部,Ca2+与Cl−能够发生化学反应,从而减少废水中的Cl−。

图5 未改性粉煤灰(a)、改性粉煤灰(b)及其吸附废水后(c)的XRD谱图Figure 5 XRD patterns for unmodified fly ash (a) and modified fly ash before (b) and after (c) adsorbing wastewater
2.4.2 FTIR分析
为了更清楚地了解吸附剂的特性官能团以及彼此独立化学键的吸收带,采用傅里叶用红外光谱仪测得未改性粉煤灰及改性粉煤灰吸附废水前后的相关官能团。如图6所示,在高频区3 639 cm−1和3 405 cm−1附近的吸收峰是由OH在吸附剂表面的伸缩振动引起的[21],OH的伸缩振动幅度在粉煤灰改性后加大,与Cl−竞争和阳离子的反应,也就表明在该区域内化学吸附作用不强,物理吸附作用占据主导地位。在低频区1 427 cm−1和1 124 cm−1附近的伸缩区域是由Si─O─Si做反向对称拉伸运动造成的[22]。吸附剂吸附反应后没有出现明显的新的吸收带,表明吸附过程中存在物理吸附作用[23]。在868.4 cm−1和709.7 cm−1吸收峰附近,从原粉煤灰到改性吸附前再到改性吸附后,吸收峰减弱明显,这可能是 Si─O弯曲振动导致的吸收峰减弱。可以看出Cl−与Si、Al等元素发生了离子交换反应,因此粉煤灰经过酸改性、高温改性以及发泡处理后降低了SiO2和Al2O3的聚合度,提高了对废水溶液中Cl−的吸附能力。这种现象可以归因于Si─O和Al─O的逐渐断裂[24]。

图6 未改性粉煤灰(a)、改性粉煤灰(b)及其吸附废水后(c)的傅里叶变换红外光谱图Figure 6 FTIR spectra for unmodified fly ash (a) and modified fly ash before (b) and after (c) adorbing wastewater
3 结论
(1) 改性粉煤灰吸附Cl−的最佳投加量为25 g/L,此时Cl−的吸附率最高,为56%。在pH为5时吸附量最大,并约在280 min时达到吸附平衡。采用Langmuir模型描述改性粉煤灰对Cl−的等温吸附过程最准确,反应属于吸热反应。粉煤灰中主要有莫来石和石英成分,吸附反应后Si─O和Al─O发生断裂,改性后粉煤灰表面的吸附位点增多,孔隙增加,粒径减小,物理吸附过程得以增强。
(2) 改性粉煤灰对Cl−的吸附机理主要是H+能够溶解Al2O3、SiO2等物质形成配合物或者聚合物的吸附架桥,同时,生石灰CaO能够通过碱性激发和反极化作用提高粉煤灰的活性,双氧水更是通过产生更多的表面氧化基团来增加吸附位点。
