内镜下黏膜剥离术治疗直肠神经内分泌肿瘤疗效分析
2021-03-15曾艳丽张卫平唐丽敏
曾艳丽,张卫平,唐丽敏
(漯河市中心医院消化内科,河南 漯河 462000)
神经内分泌肿瘤(neuroendocrine neoplasm,NENs)泛指所有起源于肽能神经元和神经内分泌细胞的肿瘤,可分为神经内分泌瘤(neuroendocrine tumor,NET) 和神经内分泌癌(neuroendocrine carcinoma,NEC),它是一种特殊类型肿瘤,可发生于全身多个部位,但胃肠道系统多见,胃肠道系统中又以直肠多发[1-2]。直肠神经内分泌肿瘤起源于肠黏膜隐窝深部的嗜铬细胞,能分泌具有生物活性的胺和神经肽,既往认为其是一种罕见病,但近年其发病率有上升趋势[2]。直肠神经内分泌肿瘤起病隐袭,常于体检肠镜或因腹泻、腹痛、大便性状改变而行肠镜检查时发现,因此早发现、早诊断、早治疗是降低其远处转移风险和提高患者生存率的有效方法。本研究选取行内镜下黏膜剥离术(endoscopic submucosal dissection,ESD)治疗的12例直肠神经内分泌肿瘤患者的临床资料进行回顾性分析,报道如下。
1 对象与方法
1.1 对象 回顾性分析2015年4月—2019年10月漯河市中心医院收治的12例直肠神经内分泌肿瘤患者的临床资料,患者瘤体直径<1.5 cm,其中男5例,女7例,年龄38~74岁,中位年龄55.8岁,其中4例无明显症状,于健康体检时发现,8例分别有不同程度的腹痛、腹泻、大便性状改变行肠镜检查时发现,其中腹痛或腹部不适6例,腹泻5例,大便性状改变7例,术前常规行腹部CT或MRI、超声检查,除外周边侵犯和远处转移,同时内镜检查和治疗无明显禁忌。
1.2 方法
1.2.1 治疗方法 (1)使用器械:PENTAX-i10电子胃镜,OLYMPUS H260Z电子胃镜,高频电发生器 Dual刀(OLYMPUS KD-650Q),一次性注射针(VDK-IN-23-160-2504-A)。(2) ESD操作过程:术前行聚乙二醇电解质散(舒泰神北京生物制药股份有限公司),二甲硅油(四川省自贡鸿鹤制药有限责任公司)清洁肠道,静脉麻醉下行ESD。患者取左侧卧或仰卧位,麻醉成功后:①确定病变范围并标记边界:结合内镜下染色和放大内镜ME-NBI观察,确定病变范围,距离病灶边缘3~5 mm处电凝标记。②黏膜下注射:沿标记外缘分多点行黏膜下注射,注射液为1∶10 000甘油果糖+肾上腺素+少许亚甲蓝,抬起病灶。③切开和黏膜下剥离:使用Dual刀于标记点外侧缘黏膜行环周切开,在透明帽辅助下用Dual刀逐步剥离瘤体,剥离过程中严格止血。病灶剥离后对创面显露血管进行预防性止血处理,必要时钛夹闭合创面。剥除标本展开用大头针固定于标本展示板上。
1.2.2 切除标准 病灶整块切除率是指病灶在内镜下一次性被整块切除;病灶完整切除率是指病理标本在侧切缘及基底切缘均为阴性。
1.2.3 术后观察与处理 术后严密观察患者出血、穿孔发生情况。术后出血是指术后24 h~1个月出现需内镜干预的出血;手术穿孔是指手术中或手术后有内镜或腹部CT证实的肠道穿孔。如果确诊为术后出血或穿孔,必要时再次行内镜干预或外科处理。术后3个月、6个月、1 a、3 a定期复查肠镜,腹部CT或MRI,如有阳性发现并证实为NET则定为复发。
2 结果
12例直肠神经内分泌肿瘤均行ESD治疗,病灶整块切除率为100.0% (12/12),病灶完整切除率为83.3%(10/12),其中1例垂直切缘阳性(8.3%),1例瘤体紧邻侧切缘(8.3%),2例患者(16.6%)均行二次扩大切除,术后标本病理未见明显肿瘤细胞,其余10例患者术后病理水平切缘及垂直切缘均为阴性,病理分级显示G1期8例,G2期2例,所有病理均无脉管浸润;1例术后排出少量暗红色血液,给予药物对症处理后好转,无穿孔发生。术后3、6、12个月随访,以后每年随访。肠镜、CT、MRI检查发现,12例患者均未见淋巴结及远处转移,患者生存率100%,目前仍在密切随访中。典型影像学表现见图1-2。
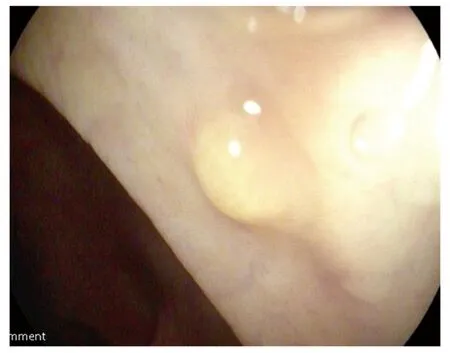
图1 白光下观察直肠神经内分泌瘤患者
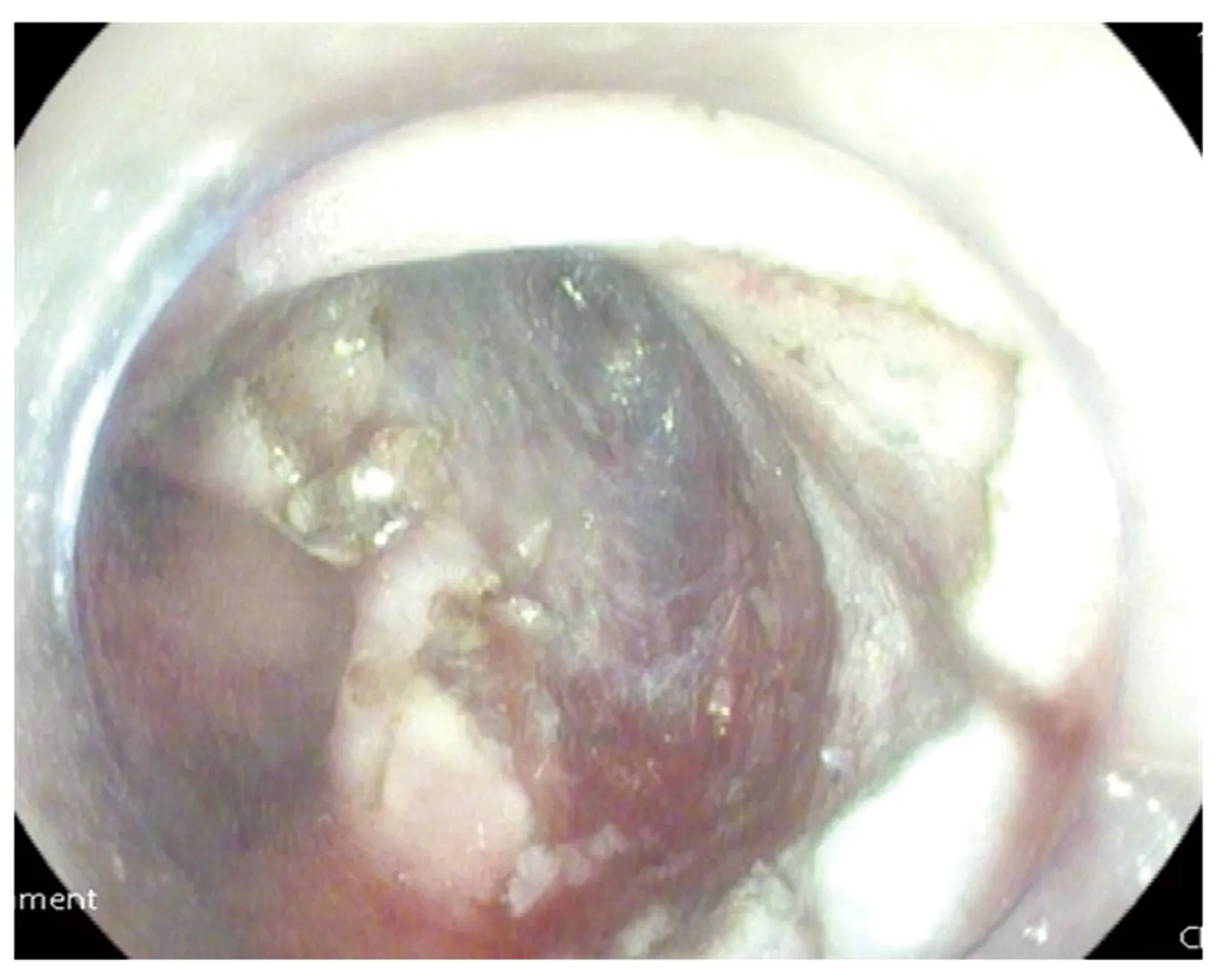
图2 直肠神经内分泌瘤ESD切除术后,剥离创面。
3 讨论
NENs是一组具有某种特质的异质性肿瘤,以胃肠道多发,而胃肠道神经内分泌肿瘤则以直肠最为多见,直肠神经内分泌瘤常为无功能性肿瘤,生长缓慢且无明显的异位内分泌功能,故患者早期常无明显临床症状,或合并其他非特异性症状,如腹痛、腹泻、大便性状改变等,同时病灶多较小,常被误诊为息肉,因此需行肠镜内镜检查及活检,必要时行超声内镜检查,对早期肿瘤的发现尤为重要。
目前,对于直肠神经内分泌肿瘤的治疗尚存在较多争议,一般对于直径<1 cm的直肠NENs建议局部切除,包括内镜ESD治疗及外科手术治疗,当直肠NENs>2 cm时建议外科手术治疗[3]。临床研究[4-5]表明,ESD创伤小,术中可以大范围切除病灶,且术后复发率低。对于直肠NENs患者而言,采用ESD治疗的手术时间短且手术费用低,术中对于多个病灶能够一次性清除,同时对于同一患者而言能够行多次ESD治疗。另外,ESD术后所获得的病理标本较完整,能够给病理学分级等评估提供准确的参考,有利于治疗方案的制定。严丽军等[6]回顾性分析58例直肠NENs患者临床资料发现,ESD作为一种有效且安全的治疗方法,在直肠NENs疾病的治疗过程中能够给予明确的病理学评估,并且可以根治一些病变(符合适应证),而且术中完整切除的患者其术后需要进行补救外科手术的发生率极低。本研究中12例直肠神经内分泌肿瘤患者,G1期10例,G2期2例,直径均<2 cm,行内镜黏膜剥离切除后,病灶整块切除率为100.0%(12/12),完整切除率为83.3%(10/12),1例术后排出少量暗红色血液,给予对症处理后好转,无穿孔、感染等并发症发生,1例垂直切缘阳性,1例瘤体紧邻侧切缘,但二次扩大切除后,标本病理未见肿瘤细胞,可能是高频电切除过程中,边缘可能残存的肿瘤细胞被高频电灼烧破坏;所有病例均无周围淋巴结浸润及远处转移,生存率为100%。其中2例瘤体直径>1.0~1.5 cm,其余瘤体直径均<1 cm,因此,对于G1期瘤体直径稍小的直肠神经内分泌肿瘤,应尽早行肠镜检查,明确诊断,同时ESD是直肠神经内分泌肿瘤治疗比较理想的选择,避免患者行外科手术的创伤,这与王瑞刚等[7]研究结果一致。本研究中,其中1例切缘阳性患者,瘤体直径约1 cm,但由于病例数较少,无法就瘤体大小与完整切除率进行统计分析。田园等[8]研究认为,对于肿瘤<1 cm的直肠神经内分泌肿瘤患者,选择ESD治疗是安全且临床疗效满意,但瘤体直径>1.5~2.0 cm的直肠神经内分泌肿瘤患者,可行ESD治疗,术后应依病理决定是否需进一步治疗。
综上所述,G1期直肠神经内分泌肿瘤早期临床表现无特异性,因此内镜诊断为其主要诊断手段,病理是其诊断“金标准”,对无淋巴结及远处转移,病变局限于黏膜下且直径<1.5 cm者,ESD是其首选治疗方法,对于病变未侵犯黏膜肌且直径>2 cm者,可优先考虑ESD治疗,创伤小,住院时间短,住院费用少,且能保留肠道功能,但术后应密切随访,必要时行手术扩大治疗。但由于本研究为回顾性分析,且样本量较小,部分病例尚在继续随访中,因此对肿瘤复发率、肿瘤分级、肿瘤完整切除率的统计可能存在误差,这些问题有待进一步扩大样本、多中心联合及长时间随访来进一步证实。
