金属有机框架材料对Cr(Ⅵ)离子的吸附去除研究进展
2021-03-12李茹霞钟文彬谢林华谢亚勃李建荣
李茹霞 钟文彬 谢林华 谢亚勃 李建荣
(北京工业大学环境与生命学部环境化工系,绿色催化与分离北京市重点实验室,北京 100124)
0 引 言
随着现代工业化的不断深入发展,水污染问题日益严重,对人类生存和可持续发展造成了极大的威胁[1]。主要水污染物包括重金属离子[2]、染料[3]、含氯有机物[4]等对环境和生物具有危害性的离子和化合物。重金属离子在生物体内难降解、易积累、生物毒性大[5],通过食物链进入人体后可引起急性或慢性中毒。恶性重金属污染事件时有报道,重金属污染已成为我国严重且亟须解决的热点问题。金属铬(Cr)是一种常用的金属元素,广泛应用于金属加工、制革、制漆等方面[6]。铬的广泛应用及不达标排放导致铬离子在水、土壤等环境中的含量日益上升,威胁生态和民众健康。铬离子在自然条件/自然界中,通常以+3和+6两种价态存在[7],Cr(Ⅲ)离子是人体营养必需的微量元素之一,在人体正常的碳水化合物及脂肪的代谢过程中具有重要作用[8]。但因Cr(Ⅲ)离子可以非特异性地与DNA结合,其在人体内含量过高时可能会导致基因突变或恶性肿瘤。整体而言,低浓度的Cr(Ⅲ)离子毒性较低,危害性较小。而且,环境中的Cr(Ⅲ)离子易以Cr(OH)3沉淀形式从水中去除。相比之下,Cr(Ⅵ)离子毒性大,进入人体后易导致呼吸道感染甚至基因突变和癌症[9]。因此,环境中Cr(Ⅵ)离子的去除研究受到广泛关注。在水溶液中Cr(Ⅵ)离子的存在形式主要受到水的酸碱性(pH值)和Cr(Ⅵ)离子浓度的影响。如图1所示,当浓度较大(约 1 mg·g-1以上)时,Cr(Ⅵ)在宽范围 pH 值下以Cr2O72-离子形式存在;当浓度较低时,Cr(Ⅵ)离子的存在形式受pH值影响明显:酸性条件下(pH<6.5)主要存在形式为铬酸(H2CrO4)或铬酸氢根离子(HCrO4-),中性和碱性条件下(pH≥6.5),主要以CrO42-离子形式存在[10]。常见水体接近中性,Cr(Ⅵ)含量不高,Cr(Ⅵ)在水中主要以CrO42-离子形式存在。目前,Cr(Ⅵ)离子的去除方法主要有化学沉淀法[11]、离子交换[12]、吸附[13]等,但多数已有处理方法都存在一定的不足。例如,化学沉淀法通过引入还原剂将Cr(Ⅵ)离子转化为Cr(Ⅲ)离子,再加入碱将Cr(Ⅲ)离子转化为Cr(OH)3沉淀,实现铬的去除。虽然该方法简单易行,但难以将Cr(Ⅵ)离子的浓度降低到饮用水标准(Cr(Ⅵ)浓度:0.05 μg·g-1,生活饮用水标准GB5749-2006)之下,且处理过程中会产生大量的污泥[14];离子交换法所使用的化学试剂量过高、分离比较困难且成本高[15]。

图1 水中Cr(Ⅵ)存在形态在不同pH值和浓度下分布图[10]Fig.1 Distribution of Cr(Ⅵ)in water under different pH values and concentrations[10]
吸附法是利用吸附剂对重金属离子进行吸附、配位等原理实现对重金属离子的去除。此方法具有成本低、操作简单、高效、吸附量大且部分吸附剂具有良好的循环再生性的优点[16-17],被广泛应用。用于重金属离子去除的常见吸附剂包括沸石[18]、活性炭[19]、介孔二氧化硅[20]、生物吸附剂[21]等。以往研究显示,在酸性条件下,大多数吸附剂对Cr(Ⅵ)离子的去除效果比在中性或碱性条件下更好。这主要是因为在酸性条件下吸附剂的外表面和/或孔内表面易被溶液中H+离子质子化而带正电,对带负电的HCrO4-或Cr2O72-离子亲和性高。在碱性条件下,同为负电性的OH-和CrO42-离子在吸附剂中易发生竞争吸附,导致吸附剂对CrO42-吸附能力较弱。因此,文献中关于Cr(Ⅵ)离子吸附的研究主要是对HCrO-4和Cr2O72-离子的去除(高浓度时为Cr2O72-,低浓度时为HCrO4-),而对 CrO42-离子去除的研究报道较少[22]。Cr(Ⅵ)离子的常见检测方式有多种。对于酸性溶液,使用广泛的是二苯碳酰二肼分光光度法测定Cr(Ⅵ)离子的浓度[23]。其原理为在酸性条件下具有强氧化性的Cr(Ⅵ)离子将二苯碳酰二肼氧化成二苯缩二氨基脲,生成的二苯缩二氨基脲与Cr(Ⅲ)离子(Cr(Ⅵ)离子的还原产物)反应形成紫红色配合物,该配合物的最大吸收峰波长在540 nm处,浓度可通过紫外可见吸收光谱法检测。碱性条件下,CrO42-的浓度也常采用紫外可见吸收光谱法检测,最大吸收峰波长在372 nm处。另外,电感耦合等离子体(ICP)原子发射光谱法检测金属离子含量具有检测限低、样品处理简单等特点,可用于测定溶液中各种形态含铬离子的浓度。
目前,研究用于Cr(Ⅵ)离子去除的材料多种多样,主要包括纳米级零价铁(nZVI)和多孔碳基材料。铁基纳米复合材料因吸附能力强、表面积体积比大、磁性强、生物相容性好、性价比高、可重复使用等优点,在污水处理领域得到了广泛的应用[24],采用液相还原法制备的nZVI由于具有高比表面积及存在大量的表面活性位点,因此可有效地还原并去除Cr(Ⅵ)离子。例如,Zhang等[25]通过硼氢化物还原硫酸亚铁制备了具有较高比表面积(183 m2·g-1)和特征形态的nZVI。由于该材料的表面带正电荷,电负性的Cr(Ⅵ)离子可被迅速吸附到nZVI表面,表面的Fe0快速氧化成Fe2+,同时提供大量电子将Cr(Ⅵ)还原为Cr(Ⅲ);生成的Cr(Ⅲ)氧阴离子(Cr2O42-)与 Fe2+很快地形成FeCr2O4沉淀,对Cr(Ⅵ)的去除能力可达123.9 mg·g-1。碳纳米管、多壁碳纳米管(MWCNTs)和石墨烯基材料及其复合材料一直是Cr(Ⅵ)离子去除材料的研究热点,但是这类材料可重复使用性较差,因而在实际应用中受到了限制。例如,Bhaumik等[26]采用原位化学氧化聚合法制备了聚吡咯包裹的氧化多壁碳纳米管纳米复合材料PPy/OMWCNTs。由于其表面质子化位点与Cr(Ⅵ)离子之间存在静电作用,PPy/OMWCNTs对Cr(Ⅵ)离子表现出良好的吸附能力,最优条件下吸附量可达294.18 mg·g-1。然而,在其他常见离子(如 Zn2+、Ni2+、Cu2+、F-、NO3-、CO32-、SO42-)存在的情况下,PPy/OMWCNTs对Cr(Ⅵ)离子的吸附去除能力下降。而且,该材料是否可以循环使用未被验证。Huang等[27]通过简单的热解-碳化过程得到氟氮共掺杂磁性炭(FN-MCs),并用于去除水溶液中的Cr(Ⅵ)离子。相对于单独添加氟或氮的碳材料,FN-MCs对Cr(Ⅵ)离子的去除率明显提高,中性溶液中最大吸附量达188.7 mg·g-1。这一吸附量与文献中性能良好的碳基吸附剂的相当。FN-MCs对Cr(Ⅵ)离子的高吸附性能归因于氟原子和氮原子的同时掺入增加了该吸附剂表面的负电荷密度。不过,FN-MCs经多次循环使用后,其对Cr(Ⅵ)离子去除效果也逐渐下降。活性炭(AC)具有高的比表面积、机械强度及介孔和微孔共存的特征[28],在酸性条件下,AC质子化的孔表面具有活性位点,可与Cr(Ⅵ)离子发生静电相互作用,从而实现吸附去除效果。不过,AC对金属离子的吸附一般没有选择性。
可见,多数吸附剂的重金属离子去除性能都存在一些不足,如吸附量较低、选择性较差、循环使用性不好等。金属有机框架材料(metal-organic frameworks,MOFs)是一类由金属离子/簇与有机配体通过配位键作用形成的晶态多孔材料,具有结构多样、比表面积大、孔径可调、孔表面特征易设计调控等特点,在吸附[29-30]、分离[31-32]、催化[33-34]、传感[35-36]等领域具有应用潜力。在吸附分离方面,污染物的吸附去除是重要且具有现实意义的研究内容之一。污染物种类繁多,结构和性质千差万别,包括空气中的氮氧化物、硫化物、挥发性有机物(VOCs)、氨气、一氧化碳、臭氧,和水中的重金属离子、抗生素、染料、放射性物质、持久性有机污染物(POPs)等。对特定污染物的有效吸附去除很大程度上依赖于吸附剂孔洞与污染物分子或离子在大小、形状和性质上的匹配。MOF材料的结构多样和易设计调控的特性为这类材料在不同污染物吸附去除的应用上提供了极大的优势。尤其对于一些在环境中浓度低但具有极大危害的污染物,常规方法难以将其有效去除,而通过对MOF结构的理性设计或修饰,提升其对污染物的吸附亲和力,最终有望实现污染物的深度去除。近年来,利用MOF材料吸附去除水中重金属离子成为该领域的研究热点之一[37-38]。一些MOF在Cr(Ⅵ)离子吸附方面已表现出很大的潜力(表1)。尽管已有一些关于MOF材料去除各类重金属离子的全面性综述[39],但针对Cr(Ⅵ)去除的研究工作未被较详尽地总结。本文将重点介绍和评论近年来利用MOF材料吸附去除Cr(Ⅵ)离子的研究工作。
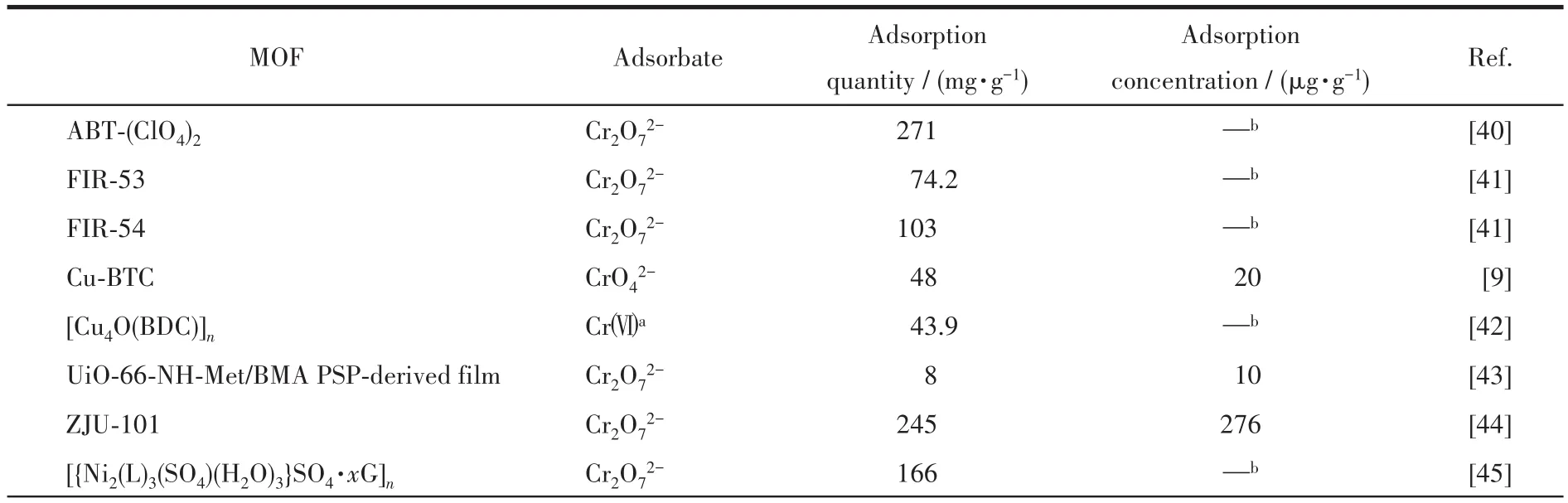
表1 一些MOF材料对Cr(Ⅵ)吸附的性能比较Table 1 Cr(Ⅵ)adsorption performance of some reported MOFs
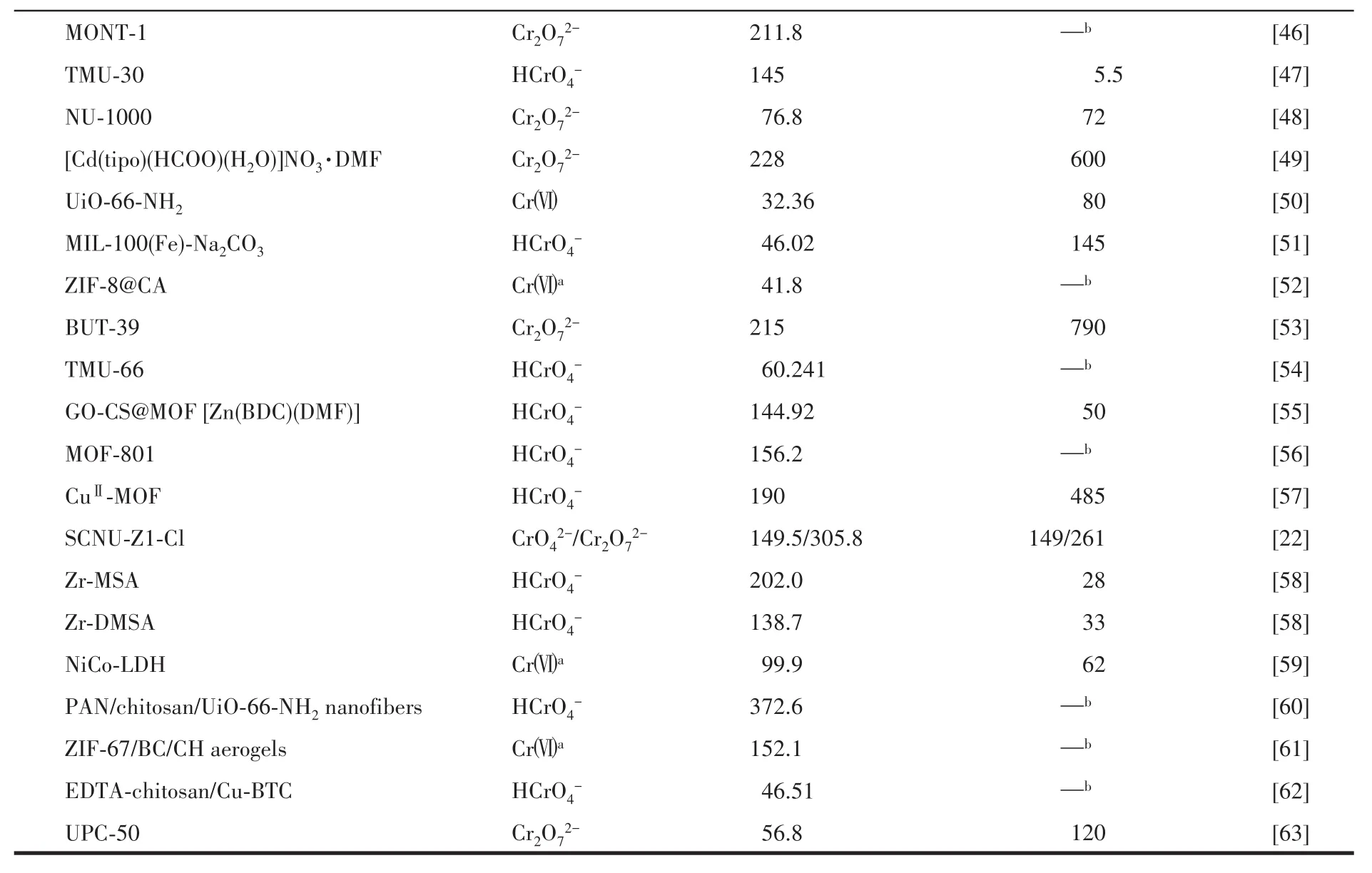
续表1
1 锆基MOF对Cr(Ⅵ)的吸附
锆基MOF(Zr-MOF)因其优异的水稳定性及其具有的多样的Zr6团簇基多孔框架结构而得到广泛的研究[64-66],是一种可用于水中的Cr(Ⅵ)离子吸附去除的潜在材料。已有研究表明,Zr6簇上端基配位的H2O或OH-位点可以通过氢键作用结合各种阴离子[53]。
MOF在Cr2O72-离子的捕获方面具有很大的潜力,但是MOF材料的再生往往需要与高浓度的阴离子(如 Cl-、NO3-等离子)进行交换,这将不可避免地出现大量含铬的固体废物以及需要二次分离工作。为了避免这些问题,Lin等[48]筛选了6种具有较大比表面积且有良好水稳定性的中性框架MOF,即HKUST-1、ZIF-8、MIL-100(Fe)、UiO-66、UiO-67和NU-1000,用于去除水中的Cr2O72-离子。通过对比6种MOF对Cr2O72-离子的吸附性能,发现NU-1000具有最高的吸附能力(76.8 mg·g-1),并且其对Cr2O72-吸收能力和吸附效率优于商业有售的活性炭(图2a),且在高浓度竞争离子(NO3-、SO42-、Cl-)的存在下仍具有很高的选择性。作者对其吸附机理研究发现,锆基MOF材料中Zr6节点上的配位水和羟基是重要的吸附位点。NU-1000中的Zr6簇是8-连接节点,而同样由Zr6簇构筑而成的UiO系列MOF(UiO-66,UiO-67)是12-连接网络结构,其Zr6节点上没有端基配位的水分子或羟基。NU-1000比UiO-66和UiO-67具有明显更高的Cr2O72-吸附量的原因,可认为是由于其具有丰富的活性位点、较高的比表面积、较大的孔径及框架与Cr2O72-离子之间存在静电作用。此外,吸附Cr2O72-离子的NU-1000经酸化甲醇(含2.5 mol·L-1HCl)进行索氏提取再生后,至少重复使用3次后吸附效率基本不变(图2b),对Cr2O72-离子的吸附表现出良好的再生能力。

图2 (a)不同吸附剂对Cr2O72-的吸附效率;(b)NU-1000对Cr2O72-吸附的可重用性[48]Fig.2 (a)Adsorption capacities of some materials for Cr2O72-;(b)Cyclic adsorption performance of NU-1000 for Cr2O72-[48]
He等[53]设计了一种功能化的T型配体并将其与锆盐进行反应,构建了一种新型Zr(Ⅵ)-MOF(BUT-39),BUT-39对Cr2O72-离子具有高效检测和快速捕获的能力。BUT-39具有独特的多孔框架结构,其结构中Zr6簇为少见的低对称性9-连接节点。由于Zr6簇为9-连接,其表面有端基配位的H2O/OH-基团,这些基团能够通过氢键、配位键等作用力来结合各种阴离子。同时,T型配体上苯并咪唑基团中的咪唑N原子是碱性的,可在酸性溶液中质子化,也有利于Cr2O72-的富集,进而导致了BUT-39较高的Cr2O72-吸附量(215 mg·g-1),但由于其 Zr6簇与 Cr2O72-之间存在的氢键、配位键等强相互作用,BUT-39对Cr2O72-离子吸附的循环再生性较差。
目前,多数已报道的研究集中在MOF材料对水溶液中Cr(Ⅵ)离子的去除,同时研究MOF材料对Cr(Ⅵ)离子吸附和降解双重功能的报道较少[67]。Yang等[58]采用绿色水相法(图3b)制备了3种fcu拓扑结构型Zr-MOF,3种Zr-MOF的有机配体上含有不同数量的硫醇基团(图3b),以研究MOF材料孔道表面硫醇基团的引入和数量对其Cr(Ⅵ)离子去除性能的影响。实验结果显示在pH=3时,Zr-SUC对Cr(Ⅵ)去除效率只有90%,而Zr-MSA、Zr-DMSA由于孔表面含有大量的硫醇基团,可实现Cr(Ⅵ)离子的完全去除。这验证了硫醇基团可提升MOF材料的Cr(Ⅵ)吸附去除性能。此外,作者还发现在添加Cr(Ⅵ)后Zr-MSA和Zr-DMSA悬浊液的颜色迅速从白色变为棕色和浅棕色,最后变为浅绿色。XPS测试分析结果显示含有硫醇基团的2种MOF材料中被吸附的铬离子均以Cr(Ⅲ)形式存在,表明硫醇基团具有还原作用,将Cr(Ⅵ)逐渐还原成Cr(Ⅲ)(图3a)。硫醇基团氧化成磺酸根基团,与Cr(Ⅲ)离子之间存在静电相互作用,吸附在MOF孔道内(图3c)[68-72]。作者还对比了含有硫醇基团的2种MOF材料Zr-MSA和Zr-DMSA的Cr(Ⅵ)吸附性能。实验结果显示Zr-MSA的Cr(Ⅵ)吸附量及吸附速率要高于Zr-DMSA,这可认为是由于Zr-DMSA孔洞中过多的硫醇基团阻碍了Cr(Ⅵ)离子在孔内的扩散,导致其Cr(Ⅵ)吸附能力和吸附速率不如Zr-MSA。因此,活性硫醇基团的存在与MOF孔隙率之间达到平衡才能获得MOF材料的最佳Cr(Ⅵ)吸附效果。
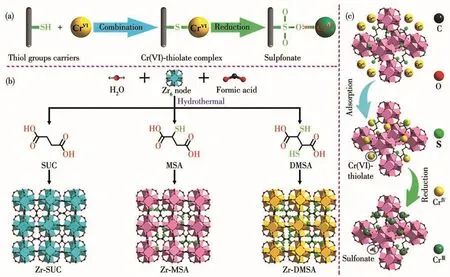
图3 (a)含硫醇化合物降解Cr(Ⅵ)的示意图;(b)无硫醇与含硫醇基团的UiO型MOF的水相合成;(c)含硫醇的MOF对Cr(Ⅵ)的吸附和降解[58]Fig.3 (a)Schematic representation of degradation mechanism of Cr(Ⅵ)by thiol-containing compounds;(b)Synthesis of thiol-free and thiol-tagged Zr-MOFs isostructural to UiO-66;(c)Adsorption and degradation of Cr(Ⅵ)by thiol-tagged Zr-MOFs[58]
Zheng等[56]以长度相对较短的富马酸为配体,制备了fcu拓扑结构型的Zr-MOF材料MOF-801,其框架中孔洞很小但孔表面上的μ3-OH基团密度很高。作者还对MOF-801及2个具有相同fcu拓扑结构的Zr-MOF(UiO-66和UiO-1,4-NDC)进行了Cr(Ⅵ)吸附研究和性能对比(图4)。3种MOF中UiO-66和UiO-1,4-NDC孔表面μ3-OH位点密度要明显低于MOF-801。作者通过对3种MOF的吸附研究发现MOF-801对Cr(Ⅵ)的吸附性能明显优于UiO-66和UiO-1,4-NDC(图4b和4c)。MOF-801对Cr(Ⅵ)在pH=4时吸附量最高,达156.2 mg·g-1。XPS分析结果表明MOF-801对HCrO4-的良好吸附性能源于HCrO4-与μ3-OH之间形成的氢键作用(图4d)而非静电作用。这也很好地解释了MOF-801的吸附性能明显高于UiO-66和UiO-1,4-NDC。另外,他们还证实MOF-801经过甲醇-乙酸洗脱4次后仍能保持稳定的Cr(Ⅵ)吸附能力。
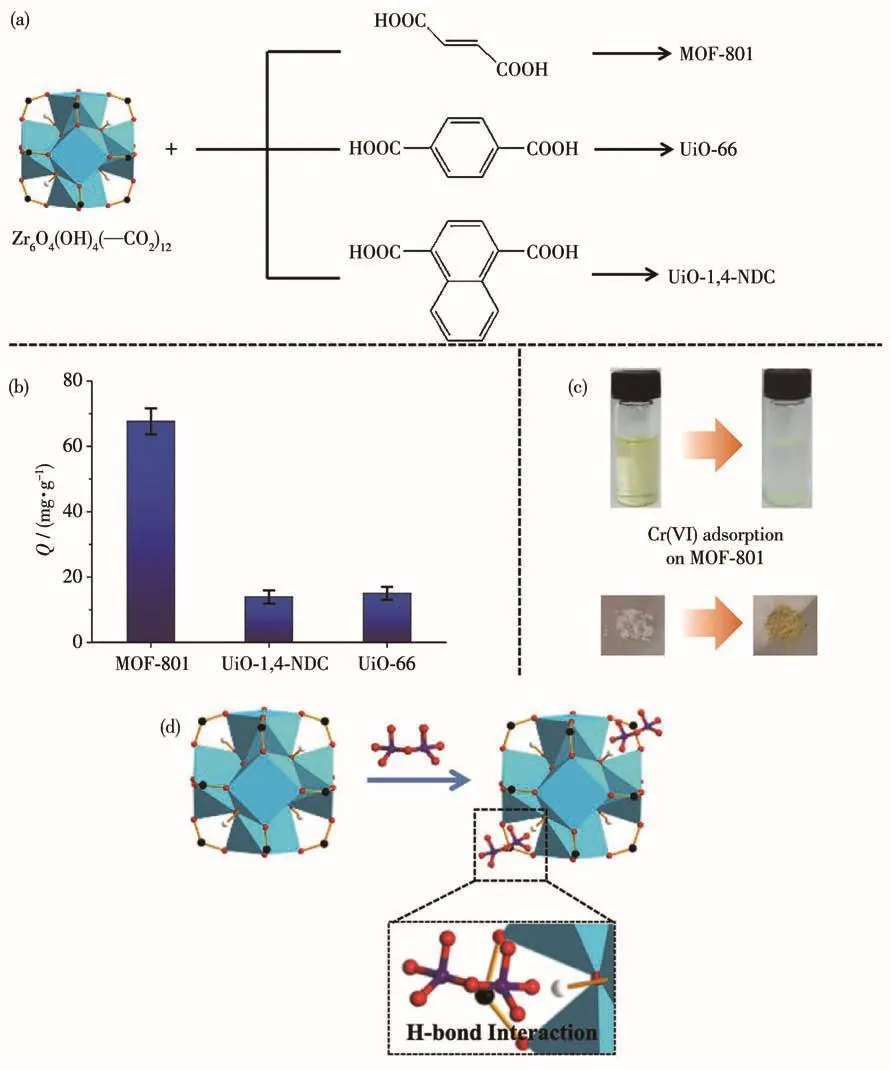
图4 (a)合成MOF-801、UiO-66和UiO-1,4-NDC的Zr6O4(OH)4(—CO2)12簇与有机配体;(b)MOF-801、UiO-66和UiO-1,4-NDC在相同条件下的Cr(Ⅵ)吸附量;(c)MOF-801样品吸附Cr(Ⅵ)前后实物照片;(d)Cr(Ⅵ)通过氢键作用吸附到MOF-801孔道中的机理示意图[56]Fig.4 (a)Synthesis of MOF-801,UiO-66 and UiO-1,4-NDC from Zr6O4(OH)4(—CO2)12clusters and organic ligands;(b)Cr(Ⅵ)adsorption capacities of MOF-801,UiO-66 and UiO-1,4-NDC under the same conditions;(c)Photos of MOF-801 samples before and after Cr(Ⅵ) adsorption;(d)Schematic representation of mechanism of Cr(Ⅵ)adsorption by MOF-801 with hydrogen bonding interaction[56]
2 阳离子框架型MOF对Cr(Ⅵ)的吸附
对于水中阴离子类污染物的去除,具有较好的水稳定性的阳离子框架型多孔材料具有非常大的潜力。阳离子框架型MOF是MOF材料的一个子类,通常由中性的有机配体和金属离子构建而成。这类由阳离子框架和未配位可交换的阴离子组成的MOF具有通过阴离子交换机理来实现吸附特定阴离子的能力[45,73-76]。
Li等[40]制备了一种由畸变八面体和四面体笼组成的三维阳离子框架型MOF:[Ag2(btr)2](ClO4)2·3H2O(ABT-(ClO4)2;btr=4,4′-bis(1,2,4-triazole)),可通过阴离子交换方式吸附Cr2O72-离子。以Ag+为中心制备出的ABT-(ClO4)2沿晶体学(111)方向具有直径约为0.78 nm的一维通道,且孔笼和通道内存在着高度无序的ClO4-离子和晶格水分子。这一开放的框架结构为其他阴离子进入孔道提供了条件。作者发现该MOF对水中Cr2O72-的吸附量可达到 271 mg·g-1。Cr2O72-浓度较低(14.7 μg·g-1)时,该MOF对Cr2O72-也具有良好的去除能力,经过48 h处理后Cr2O72-的浓度降低至0.09 μg·g-1。机理研究显示Cr2O72-与孔道中的ClO4-发生了交换(图5)。离子交换后,阳离子框架晶态结构仍保持完好,表明离子交换过程是由单晶到单晶(简称为SC-SC,即ABT-(ClO4)2转变为ABTCr2O7)转换形式发生的。此外,由于Cr2O72-与阳离子框架具有较强的作用力,当该MOF处在含有BF4-、CF3SO3-、NO3-、Cr2O72-离子的混合溶液中时,只对Cr2O72-有吸附效果,故ABT-(ClO4)2对Cr2O72-的吸附具有良好的选择性。另外,当Cr2O72-与ClO4-交换后,ABT-(ClO4)2转变为ABT-Cr2O7,该材料在紫外线照射下的荧光消失,这一特性表明该MOF材料具有检测Cr2O72-的应用潜力。

图5 ABT-(ClO4)2经离子交换转变为ABT-Cr2O7示意图[40]Fig.5 Schematic representation of transformation from ABT-(ClO4)2to ABT-Cr2O7by ion exchange[40]
Desai等[45]合成了一种由中性配体支撑Ni(Ⅱ)金属节点的三维水稳定阳离子框架型MOF,[{Ni2(L)3(SO4)(H2O)3}SO4·xG]n(1-SO4;L=三-(4-咪唑基苯基)胺;G=DMF,H2O),并研究了其对重铬酸根(Cr2O72-)和高锰酸根(MnO4-)的吸附能力(图 6)。在该 MOF 中,自由的硫酸根离子通过与骨架之间的弱作用占据在多孔框架内。在进行Cr2O72-与MnO4-离子吸附时,作者通过EDX(能量散射X射线谱)和FTIR分析发现吸附过程中框架中游离的SO2-离子与CrO2-、MnO-4274离子进行了交换,并且在交换过程中MOF材料完成由1-SO4到 1-Cr2O7、1-MnO4的 SC-SC的转变。将 1-SO4用于含有ClO4-、NO3-、BF4-或CF3SO3-的 K2Cr2O7或KMnO4水溶液进行竞争吸附实验,发现1-SO4对Cr2O72-、MnO4-离子的吸附具有良好的选择性。进一步研究发现Cr2O72-离子浓度为 1 μmol·L-1时,该MOF材料对Cr2O72-离子的吸附量可达 166 mg·g-1。他们还在Cr2O72-、MnO4-两种离子的竞争吸附实验中发现该MOF材料对MnO4-离子的亲和力更强。Ding等[46]制备了一种具有吸附/分离和荧光传感功能的多孔金属有机框架{[Ag(μ3-abtz)]NO3·0.125H2O}n(MONT-1),该材料可以对Cr2O72-离子进行检测和吸附,Cr2O72-离子浓度为 8 μmol·L-1时吸附量高达211.8 mg·g-1。由于该材料框架中存在自由的NO-3离子,Cr2O72-离子的吸附是通过阴离子交换实现的。作者还发现离子交换后的MONT-1可以浸泡在硝酸盐溶液中实现Cr2O72-离子的解吸。这一过程中可明显观察到随着Cr2O72-的释放,固体样品的颜色由橙色变为淡黄。进行5次吸附-解吸后,该MOF仍可保持73%的Cr2O72-释放效率。

图6 1-SO4框架中SO42-离子与Cr2O72-或MnO4-离子交换示意图及晶体颜色变化照片[45]Fig.6 Schematic representation of the ion exchange of SO42-in 1-SO4with Cr2O72- or MnO4- ions and the photos of the crystal samples showing color change[45]
最近,Deng等[22]合成了一种以Ni(Ⅱ)为金属中心,3,5-二(1-咪唑基)苯基-2H-四唑为配体,具有直径为1.5 nm的管状孔道,BET(Brunauer-Emmett-Teller)比表面积高达1 636 m2·g-1的阳离子框架型MOF(SCNU-Z1-Cl),并将其应用于捕获水中有害阴离子污染物。在该MOF结构中,沿c方向存在着1.5 nm×1.5 nm的一维六边形管状孔道(图7a),且孔道内存在着未配位的Cl-离子。对CrO42-、Cr2O72-、MnO4-、ReO4-的吸附研究发现其框架内未配位的Cl-离子可以与这些阴离子发生离子交换,实现对这些有害阴离子的去除。待吸附离子浓度在100~500 μg·g-1时,该材料对CrO42-、Cr2O72-、ReO4-的吸附量分别可达到126、241、318 mg·g-1,均大于根据Langmuir单层吸附模型计算得出的理论值(图7c)。如图7d所示,当体系中同时存在其他阴离子时,SCNU-Z1-Cl对上述离子的吸附具有良好的选择性。作者认为这是由于吸附过程中不仅发生阴离子交换,还存在着这些离子和MOF框架之间较强的阴离子-π作用和氢键作用(图7b),故吸附量大于理论值。对于MnO4-吸附,过程中不仅存在阴离子交换还有氧化还原反应,所以MnO4-离子的吸附量高达292 mg·g-1,是已知MOF材料中的最高值。此外,解吸实验显示该MOF对CrO42-、Cr2O72-离子的吸附能力在4次吸附-解吸循环后仍能保持80%。
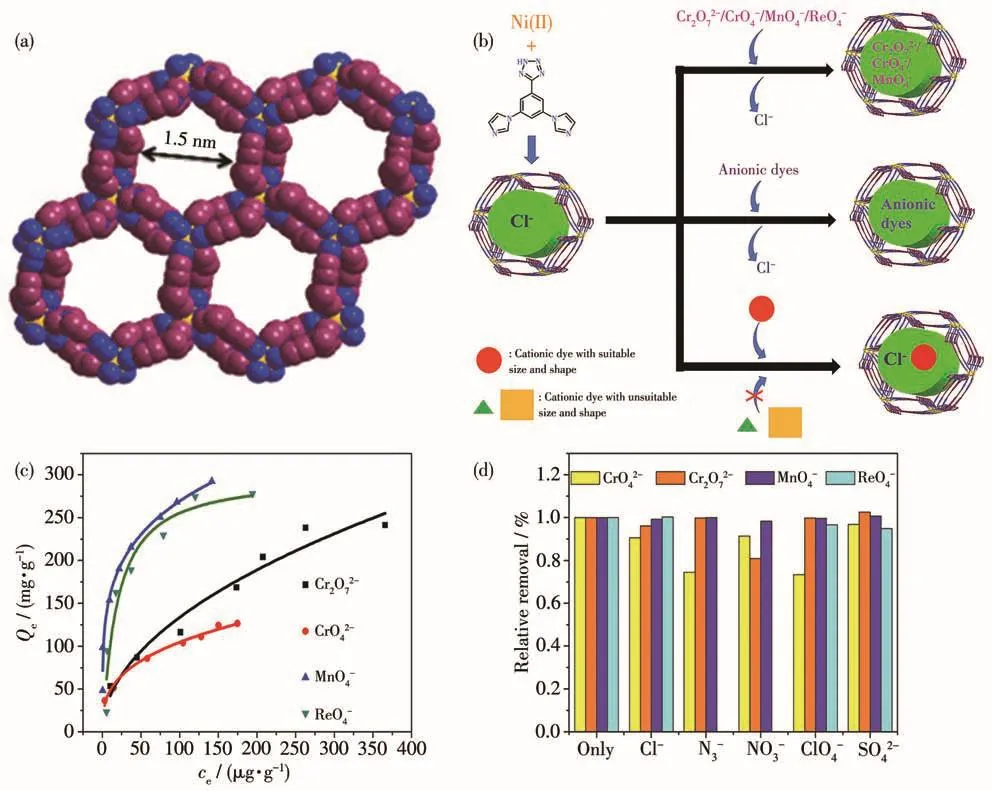
图7 (a)SCNU-Z1-Cl的框架结构图;(b)SCNU-Z1-Cl在水中吸附氧阴离子和染料的示意图;(c)SCNU-Z1-Cl对4种氧阴离子的吸附等温线;(d)竞争阴离子存在下SCNU-Z1-Cl对CrO42-、Cr2O72-、MnO4-、ReO4-的去除效率[22]Fig.7 (a)Framework structure of SCNU-Z1-Cl;(b)Schematic representation of adsorption of anions or dyes in water by SCNU-Z1-Cl;(c)Adsorption isotherms of SCNU-Z1-Cl for four types of anions;(d)Removal efficiency of SCNU-Z1-Cl for CrO42-,Cr2O72-,MnO4-,ReO4-in the presence of competing anions[22]
Shao等[57]制备了一例 CuⅡ-MOF{[Cu(L)0.5(bpe)(H2O)]NO3·0.5H2O}n。该材料框架内存在较大的空腔,空腔中填充着游离的NO3-离子,这一结构特征为阴离子交换实现对Cr(Ⅵ)离子的吸附提供了有利条件。在pH=6时(此时Cr(Ⅵ)以HCrO4-形式存在水溶液中),该MOF对Cr(Ⅵ)离子去除效果最好,吸附量可达189.3 mg·g-1。有意思的是,作者发现该MOF对Cr(Ⅵ)离子的去除机理并非常见的离子交换过程。HCrO4-离子与NO3-离子发生交换后(形成化合物Ⅱ),HCrO4-进一步取代了框架上配位的水分子与金属离子发生了配位(形成化合物Ⅲ)(图8)。配位反应打破了离子交换的平衡,促进了HCrO-离子与NO-43离子的交换。这种配位反应驱动的吸附机理使得该MOF具有良好的Cr(Ⅵ)去除效果。不过,当体系中有其他一价阴离子(如NO3-,HCO3-离子)存在时,其Cr(Ⅵ)离子吸附性能会受到影响。例如体系中有CO32-离子存在时,CO32-离子经过水解产生HCO3-离子,HCO3-离子的存在导致该MOF材料的Cr(Ⅵ)离子吸附去除率下降23%,但仍可从溶液中去除大部分Cr(Ⅵ)。由于HCrO4-离子与金属离子之间较强的配位作用,该MOF吸附HCrO4-后只有在较苛刻的条件下(100℃和1 g·L-1KNO3溶液)才能够实现解吸。
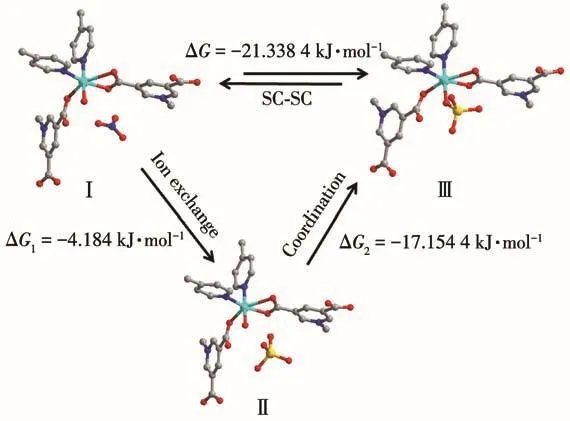
图8 {[Cu(L)0.5(bpe)(H2O)]NO3·0.5H2O}n到{[Cu(L)0.5(bpe)(H2O)](HCrO4)·0.5H2O}n的可逆SC-SC离子交换-配位取代过程示意图[57]Fig.8 Schematic representation of reversible SC-SC transformation from{[Cu(L)0.5(bpe)(H2O)]NO3·0.5H2O}nto{[Cu(L)0.5(bpe)(H2O)](HCrO4)·0.5H2O}nwith ion exchange and coordination substitution processes[57]
3 后修饰的MOF对Cr(Ⅵ)的吸附
多数MOF对重金属离子的吸附量较低,通过后修饰的方法改变MOF孔道表面性质以提升其吸附能力的方法受到广泛关注。Zhang等[44]以MOF-867为起始原料,通过后合成修饰将配体上吡啶N原子甲基化,成功制备了ZJU-101,在此过程中MOF-867的框架结构得到保持。修饰后该MOF能在短时间内从水溶液中选择性地吸附Cr2O72-。在Cr2O72-离子浓度范围为 50~500 μg·g-1时,作者测定了这 2 种MOF材料的Cr2O72-离子吸附能力,发现MOF-867对Cr2O72-的吸附量只有 53.4 mg·g-1,而 ZJU-101 对Cr2O72-吸附量高达 245 mg·g-1,约是 MOF-867 的 5倍。Cr2O72-吸附量明显提升的原因是经后合成修饰后,ZJU-101孔道内存在的平衡离子(NO3-离子)可通过离子交换的机理实现Cr2O72-的吸附去除(图 9a)。ZJU-101是当时已报道多孔材料中Cr2O72-吸附量最高的。而且,即使吸附体系中存在多种阴离子(Cl-、Br-、NO3-、SO42-、F-)且这些干扰离子极大过量(浓度是Cr2O72-的12倍)时,ZJU-101对Cr2O72-的吸附效率仍然高达81%,而ZJU-101的比表面积要比MOF-867小很多(图9b)。作者认为这种高选择性来源于带负电的Cr2O72-与带正电荷的框架之间较强的静电相互作用以及Cr2O72-离子尺寸与该MOF的孔径匹配协同作用(图9c)。
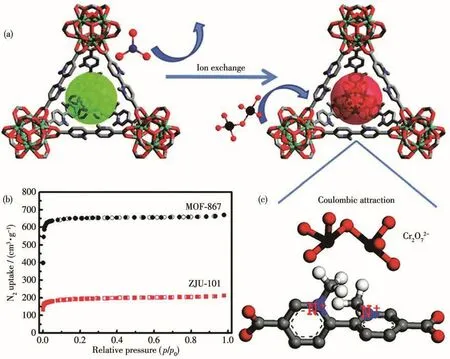
图9 (a)ZJU-101中离子交换过程示意图;(b)MOF-867和ZJU-101在77 K下的N2吸附-脱附等温线;(c)带正电荷的配体与Cr2O7 2-离子之间的静电相互作用示意图[44]Fig.9 (a)Schematic representation of ion exchange process in ZJU-101;(b)N2adsorption-desorption isotherms of MOF-867 and ZJU-101 at 77 K;(c)Schematic representation of electrostatic interaction between positively charged ligand and Cr2O7 2-ion[44]
Aboutorabi等[47]制备了一种以Pb2+离子为金属中心,具有1D菱形孔道(0.71 nm×0.68 nm)的MOF材料TMU-30。该MOF框架上存在带正电的异烟酸N-氧化物,这一基团作为Cr(Ⅵ)离子的吸附位点导致了TMU-30在水相中对Cr(Ⅵ)的快速高效吸附性能(图10a)。尽管pH值不同时,Cr(Ⅵ)离子在水溶液中的存在形式也不同,TMU-30可在pH=2~9的宽范围内快速、高效地吸附水中所有形式的Cr(Ⅵ);在pH>9时,TMU-30的晶体结构开始发生变化。相比之下,多数吸附剂只能在特定pH值下对特定离子形态的Cr(Ⅵ)实现有效吸附。作者通过XPS分析发现TMU-30对Cr(Ⅵ)离子的吸附是由于异烟酸上的N-氧化基团(INO)的氮原子与Cr(Ⅵ)离子的氧原子之间形成了一种较强的静电相互作用,从而对Cr(Ⅵ)离子具有良好的吸附效果。不过,TMU-30不能选择性地吸附CrO42-、MoO42-和WO42-离子中的某一种。另外,由于TMU-30中Pb2+为金属中心,而Pb2+是一种高毒性重金属离子,因此TMU-30难以作为一种实际应用的Cr(Ⅵ)离子吸附剂。受该工作启发,Shokouhfar和Aboutorabi等[54]通过混合配体策略在高稳定的Zr-MOF(UiO-66)结构中引入N-氧化基团来提高其对水溶液中Cr(Ⅵ)的吸附能力。他们采用以盐酸或者是苯甲酸为配位调节剂将特定数量的含N-氧化基团配体引入到UiO-66结构中,分别合成了UiO-66、UiO-66-30%、UiO-66-50%、UiO-66-70%(百分比代表结构中含N-氧化基团配体含量)和TMU-66(含N-氧化基团配体数量为100%)。这几种材料的Cr(Ⅵ)离子吸附性能测试结果显示,随着结构中含N-氧化基团配体比例的增加,材料对Cr(Ⅵ)离子吸附效果逐渐提升,其中TMU-66对Cr(Ⅵ)离子吸附吸附量最高(图10b)。XPS分析结果显示,TMU-66对Cr(Ⅵ)离子的吸附位点中除了N-氧化物基团还有Zr6簇单元。

图10 (a)TMU-30的框架结构图及其对Cr(Ⅵ)的吸附等温线[47];(b)UiO-66、UiO-66-30%、UiO-66-50%、UiO-66-70%和TMU-66对Cr(Ⅵ)离子的吸附等温线[54]Fig.10 (a)Framework structure and Cr(Ⅵ) adsorption isotherm of TMU-30[47];(b)Cr(Ⅵ) ion adsorption isotherms of UiO-66,UiO-66-30%,UiO-66-50%,UiO-66-70% and TMU-66[54]
4 MOF基复合材料对Cr(Ⅵ)的吸附
MOF作为吸附剂应用于水溶液中污染物的去除得到了广泛关注,但是由于MOF材料合成出来后通常以粉末形态存在,分散在水中后不易处理和回收,这极大地限制了这类材料在实际中的应用[77]。因此将MOF与其他功能材料整合制备的MOF基复合材料是解决这一问题的潜在方法,且目前已有一些相关研究工作。
Zhang等[43]通过后合成修饰(PSM)策略将UiO-66-NH2用甲基丙烯酰胺基团功能化再采用光聚合的方法与丙烯酸酯单体进行共聚,制备出MOF基衍生膜。首先,他们将UiO-66-NH2与甲基丙烯酸酐通过PSM反应得到甲基丙烯酰胺基团功能化的UiO-66-NH2(UiO-66-NH-Met)。然后,在光引发剂苯基二(2,4,6-三甲基苯甲酰)氧化膦的存在下,将UiO-66-NHMet与甲基丙烯酸丁酯(BMA)在紫外光下进行共聚,成功制备了一种对溶液中Cr(Ⅵ)离子具有良好分离能力的方形薄膜(PSP-衍生膜)(图11a和11b)。研究PSP-衍生膜对水中重金属离子Cr(Ⅵ)的去除能力的同时,他们也对另外3种薄膜,即BMA的自聚合产物PBMA、MOF/PBMA(等量UiO-66代替UiO-66-NHMet)以及活性炭/PBMA(等量活性炭代替UiO-66-NH-Met),进行了性能分析和对比。实验结果显示纯聚合物膜PBMA对Cr(Ⅵ)离子的分离能力差;MOF/PBMA共混膜中,聚合物与粒子相容性差,形成了非选择性空隙,故其对Cr(Ⅵ)离子截留率也较低;活性炭/PBMA中,活性炭虽然具有多孔性,但其孔表面对Cr(Ⅵ)离子没有合适的结合位点,故对Cr(Ⅵ)离子去除效果较差;PSP-衍生膜对Cr(Ⅵ)离子的分离效果最优。作者认为这是由于:(1)将MOF颗粒掺入聚合物中会带来具有极化表面的孔隙和通道,同时保持聚合物的可加工性;(2)具有可聚合官能团的纳米MOF粒子分散性好,可通过共价键固定在聚合物中,不存在粒子聚集,从而避免了聚合物和/或MOF粒子之间形成无分子选择性的缺陷;(3)MOF与单体的共聚使得粒子与聚合物之间的相互作用更加紧密,从而在分子水平上实现同质性。此外,光诱导后合成聚合方法的优点在于其适应性广且操作简单易控制,这一材料制备方法可能对新型MOF基膜材料和具有实际应用优势成型材料的发展起到推动作用。
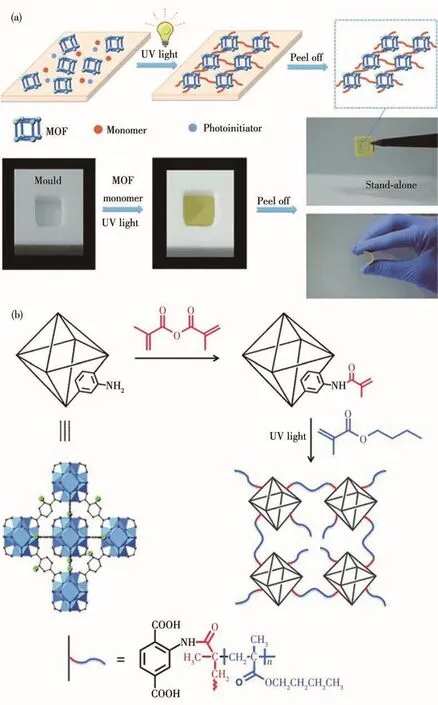
图11 (a)甲基丙烯酸酐对UiO-66-NH2进行后合成改性,然后用紫外光照射与BMA进行聚合流程示意图及所制备膜的照片;(b)UiO-66-NH2后合成修饰与光聚合结构转化示意图[43]Fig.11 (a)Schematic representation of the process where UiO-66-NH2is post-synthesized and modified with methacrylic anhydride,and then irradiated with ultraviolet light to polymerize it with BMA and photos of the prepared film;(b)Schematic representation of post-synthetic modification and photopolymerization of UiO-66-NH[43]2
Fang等[51]合成了4种含或不含矿化剂的微孔MOF材料MIL-100(Fe),比较了这4种材料的稳定性及其对Cr(Ⅵ)离子的吸附性能。MIL系列的MOF合成过程中常使用2种传统的矿化剂,即氢氟酸(HF)和四甲基氢氧化铵(TMAOH),来提高其结晶度。虽然TMAOH有助于提高MIL-100(Fe)的纯度,但其具有较高的腐蚀性和潜在的毒性[78]。HF可以提高MOF的产率和结晶性,但HF更具有强腐蚀性和在环境中的持久性,是极危险和不友好的化学试剂[79]。寻找更理想的矿化剂,安全、环保地制备这类MOF材料具有重要意义。碳酸钠具有成本低、对生态系统无危害的优点,是合成这类MOF的一种潜在矿化剂。在该工作中,作者通过不同矿化剂制备了MIL-100(Fe)-Na2CO3、MIL-100(Fe)-TMAOH 和MIL-100(Fe)-HF。他们发现MIL-100(Fe)-Na2CO3比MIL-100(Fe)-TMAOH、MIL-100(Fe)-HF以及未加矿化剂制备的MIL-100(Fe)具有更高的孔体积和比表面积,对Cr(Ⅵ)吸附能力也最高,在Cr(Ⅵ)初始浓度为400 mg·L-1,pH=4时达最大吸附量45 mg·g-1。而且MIL-100(Fe)-Na2CO3在酸性或中性溶液中对Cr(Ⅵ)的物理吸附足够稳定,但可通过稀NaOH(0.01 mol·L-1)水溶液进行解吸再生,4个吸附-解吸附循环后其对Cr(Ⅵ)的吸附效率依然保持70%。Samuel等[55]通过将MOF材料[Zn(BDC)(DMF)]、氧化石墨烯(GO)和壳聚糖(CS)混合,制备出新型纳米复合材料GO-CS@MOF。其中GO为MOF提供一个稳定的晶体生长基底,加入的壳聚糖为重金属离子的吸附提供更多的结合位点。GO-CS@MOF结构中含有大量的氨基(—NH2)和羟基(—OH)基团,氨基在酸性条件下容易质子化,有利于通过静电作用吸附HCrO4-。吸附实验结果表明该复合材料在pH=3.0时对Cr(Ⅵ)离子的吸附量高达144 mg·g-1。此外,在Cr(Ⅵ)离子吸附过程中,由于GO-CS@MOF结构中存在还原性的羟基,部分Cr(Ⅵ)离子可被还原成低毒性的Cr(Ⅲ)离子。
壳聚糖具有良好的生物相容性、可再生能力、生物降解性以及丰富的氨基和羟基,从而有利于吸附重金属离子和阴离子有机污染物[80],但纯壳聚糖气凝胶的力学性能较差,作为吸附剂在水相中易发生水解,因此,提高壳聚糖力学性能和水稳定性是提高其吸附能力的关键。Li等[61]采用一种简单易行的方法合成了细菌纤维素/壳聚糖(BC/CH)复合气凝胶。随后,在BC/CH气凝胶上原位生长MOF材料ZIF-67,得到了ZIF-67/BC/CH复合气凝胶(图12a)。BC与壳聚糖之间存在的强氢键相互作用使复合气凝胶的力学性能和水稳定性得到了提高。同时,由于ZIF-67晶体的高负载率,使得ZIF-67/BC/CH气凝胶的比表面积大大增加。在pH=6时,该ZIF-67/BC/CH气凝胶对Cr(Ⅵ)和Cu(Ⅱ)离子表现出最大吸附能力。作者发现BC/CH气凝胶的金属离子吸附能力高于纯BC气凝胶,这归因于BC的—OH基团和壳聚糖的—NH2基团对金属离子的螯合作用。此外,在BC/CH气凝胶中引入ZIF-67后,材料对2种金属离子的吸附能力明显提升(图12b),作者认为这是MOF引入后比表面积和吸附位点的增加导致的。不过,ZIF-67/BC/CH气凝胶的金属离子吸附性能易受水中其他物质影响。作者发现该材料在自来水或河水中的离子吸附能力比在去离子水中有所下降,这可能是受到自来水或河水中各种无机离子(如Ca2+、Mg2+等)和有机物的影响,这些物质会与Cr(Ⅵ)和Cu(Ⅱ)离子发生竞争吸附。此外,作者还证实吸附了Cr(Ⅵ)和Cu(Ⅱ)的ZIF-67/BC/CH气凝胶分别用NaOH溶液(1 mol·L-1)和 HCl溶液(1 mol·L-1)进行洗脱后可以重复使用,循环使用5次后,对Cr(Ⅵ)和Cu(Ⅱ)离子的去除效率分别保持在初始值的72%和81%,表明该ZIF-67/BC/CH气凝胶具有良好的可重复利用性。

图12 (a)ZIF-67/BC/CH气凝胶制作示意图;(b)BC、BC/CH、ZIF-67/BC/CH气凝胶对Cu(Ⅱ)、Cr(Ⅵ)的吸附能力[61]Fig.12 (a)Schematic representation of preparation process of ZIF-67/BC/CH aerogel;(b)Absorption capacities of BC,BC/CH,and ZIF-67/BC/CH aerogel for Cu(Ⅱ) and C(Ⅵ) ions,respectively[61]
最近,Mahmoud等[81]利用微波辅助技术对MIL-88A(Fe)进行后合成改性,制备了介孔材料nFe3O4@MIL-88A(Fe)/APTMS,3-氨基丙基三甲氧基硅烷(APTMS)中氨基基团的存在明显增强了该复合材料对Cd(Ⅱ)、Pb(Ⅱ)及Cr(Ⅵ)离子的去除能力。当pH<4时,nFe3O4@MIL-88A(Fe)/APTMS带有正电荷,与溶液中的Cr(Ⅵ)阴离子之间存在引力作用,故对Cr(Ⅵ)具有较高的去除效率和选择性,且连续5次循环处理后,这些离子的去除率仅下降3%。Jamshidifard等[60]通过微波加热法制备了PAN/壳聚糖/UiO-66-NH2(PAN代表聚丙烯腈)复合纳米纤维,可通过吸附和膜过滤法去除水溶液中的金属离子。为获得PAN/壳聚糖/UiO-66-NH2纳米纤维对金属离子的最大吸附量,他们对纳米纤维基质中MOF材料UiO-66-NH2的含量(质量分数)进行了优化。如图13a所示,当MOF含量为10%时,MOF微晶在纳米纤维基质中均匀分布,且PAN/壳聚糖/UiO-66-NH2纳米纤维中吸附位点(UiO-66-NH2中具有功能化官能团如羧基、氨基以及最高比表面积)的增加导致其对Pb(Ⅱ)、Cd(Ⅱ)和Cr(Ⅵ)三种金属离子吸附能力增加;若进一步增加MOF含量(15%),MOF微晶会在纳米纤维基体中聚集,导致其表面积减小,金属离子向纳米纤维内孔扩散受阻,金属离子有效吸附位点减少,最终导致材料对金属离子的吸附能力下降。如图13b所示,该复合材料对Cr(Ⅵ)离子吸附能力在pH=3时达到最大。这是由于在较低pH时,带正电的纳米纤维(氨基质子化)和带负电荷的HCrO4-之间存在较强的静电作用。pH值升高将导致纳米纤维的电荷密度降低,其对Cr(Ⅵ)离子的吸附能力也降低。由于具有较大的比表面积和丰富的有机官能团(如可与金属离子配位的羧基、氨基、羟基等),该PAN/壳聚糖/UiO-66-NH2复合纳米纤维对Cr(Ⅵ)离子吸附量高达372.6 mg·g-1,高于文献中大多数MOF材料和纳米纤维。作者对金属离子吸附机理的研究发现,吸附过程主要分为2个阶段:第一阶段主要是纳米纤维表面的传质,第二阶段则是纳米纤维内孔和膜内的扩散。该材料也具有良好的可再生性,循环使用5次后吸附量才开始出现下降。不过,在相同吸附条件下,PAN/壳聚糖/UiO-66-NH2在 Pb(Ⅱ)、Cd(Ⅱ)及 Cr(Ⅵ)离子共存的三元体系的水溶液中对Pb(Ⅱ)的吸附能力高于其对Cd(Ⅱ)、Cr(Ⅵ)离子的吸附能力。作者认为3种离子的电负性差异导致了Pb(Ⅱ)与该复合材料之间的亲和力强于Cd(Ⅱ)和Cr(Ⅵ)。另外,在吸附剂内部孔隙中Pb(Ⅱ)离子的扩散性最好。作者还通过静电纺丝法制备了PVDF/PAN/壳聚糖/UiO-66-NH2(PVDF代表聚偏氟乙烯)纳米纤维膜,用于水溶液中金属离子过滤去除。研究发现当纳米纤维膜厚度为50 μm、UiO-66-NH2含量为10%时具有高的水通量和高的金属离子截留率(图13c和13d)。在最优条件下合成的PVDF/PAN/壳聚糖/UiO-66-NH2纳米纤维膜对金属离子具有超长去除时间(18 h)和稳定的膜通量(图13e和13f),表现出良好的重金属离子去除应用潜力。

图13 MOF含量(a)和pH值(b)对PAN/壳聚糖/UiO-66-NH2纳米纤维离子吸附能力的影响;膜厚度(c)和MOF含量(d)对PVDF/PAN/壳聚糖/UiO-66-NH2纳米纤维膜金属离子截留率的影响;长时间渗透过程中膜的水通量(e)和金属离子截留率(f)的变化[60]Fig.13 Effect of MOF content(a)and pH value(b)on ion adsorption capacities of PAN/chitosan/UiO-66-NH2nanofiber;Effect of film thickness(c)and MOF content(d)on ion adsorption capacities of PVDF/PAN/chitosan/UiO-66-NH2 nanofiber membrane;Change of water flux(e)and metal ion rejection(f)of PVDF/PAN/chitosan/UiO-66-NH2 nanofiber membrane during 24 hours of permeation [60]
5 结论
MOF材料对Cr(Ⅵ)离子及其他重金属离子的吸附去除表现出了其独特的优势,成为近年来研究热点之一。尤其是MOF材料可以通过配体设计、后合成等手段进行功能化修饰,提升其对Cr(Ⅵ)或其他重金属离子的吸附作用力。吸附作用力的增强有利于提升MOF材料对低浓度重金属离子的吸附去除能力,这是很多其他类型材料难以实现的。而且一些MOF材料具有氧化还原活性,在吸附Cr(Ⅵ)离子的同时能将其还原成毒性相对小的Cr(Ⅲ)离子,这一特性也是很多其他吸附剂不具备的。不过,尽管MOF材料在Cr(Ⅵ)等重金属离子吸附去除方面取得了很大的进展,MOF材料的实际应用仍存在一些挑战。例如,对于Cr(Ⅵ)等重金属离子的吸附,大多数MOF材料只能在特定pH值下才能表现出较大的吸附量,然而很多MOF材料在酸性、碱性甚至中性水溶液中的稳定性不高。因此,提升MOF材料对Cr(Ⅵ)等重金属离子的吸附能力的同时提升其稳定性是今后研究的重点。在提高MOF材料的水、酸、碱稳定性方面,提升MOF结构中金属配体间的配位键强度是关键。前期的工作已经证实一些高价金属离子与含氧配体形成的MOF具有较好的稳定性,如锆羧酸盐、锆酚盐、铬羧酸盐、铁羧酸盐等类型的MOF。由pKa大的唑类配体构筑的MOF,如锌咪唑盐、镍吡唑盐等类型的MOF也表现出良好的水稳定性。一些研究工作也显示,提升MOF孔内表面和/或晶体外表面的疏水性也有利于提升MOF的水稳定性。不过,提升MOF的疏水性可能影响MOF对水中重金属离子的吸附亲和力。通过在配体上引入特定官能团改变配体整体电子结构,提升MOF稳定性的同时增强MOF对重金属离子的吸附作用也值得探索。当然,提升MOF稳定性只是其实际应用需要解决的问题之一。如何降低MOF的制备成本,如何将细小的MOF微晶制成机械稳定性好的块体或薄膜用于重金属离子吸附去除,如何确保MOF材料自身的金属离子不在应用过程中泄漏而带来新的安全问题等,都有待更多的研究突破来解决。
