泽兰不同部位UPLC 特征图谱和酚酸类成分含量测定研究
2021-03-10李国卫何民友索彩仙吴文平
李国卫,何民友,周 密,索彩仙,梁 慧,吴文平,魏 梅
(广东一方制药有限公司/广东省中药配方颗粒企业重点实验室,广东 佛山 528244)
《中国药典》2020 年版收载泽兰为唇形科植物毛叶地瓜儿苗Lycopus lucidus Turcz. var. hirtus Regel的干燥地上部分,夏、秋二季茎叶茂盛时采割,晒干。具有活血调经、祛瘀消痈、利水消肿的功效,用于治疗月经不调、经闭、经痛、产后瘀血腹痛、水肿[1]等症。泽兰始载于《神农本草经》,列为中品,历代本草书籍皆有记载[2-3],泽兰主要生长在沼泽地、水边、沟边等潮湿处,亦见有栽培品,分布于黑龙江、河北、山西、河南、江苏、江西、四川等地。泽兰的化学成分包括酚酸类、黄酮类、萜类和甾体类等结构类型化合物,其主要活性成分为酚酸和黄酮类化合物[4-7]。现代研究表明泽兰具有抗肝炎病毒、扩张血管及治疗心血管疾病等药理作用,其中有效成分咖啡酸、迷迭香酸有着抗菌消炎、抑制血小板聚集的作用[8-13]。传统经验上常以叶的颜色、气味、外观性状等划分规格等级,因此,可依据不同药用部位进行质量评价。
《中国药典》2020 年版泽兰药材项下的质量控制标准仅限于薄层定性,有关特征图谱或含量测定研究的文献报道较少[14-19],因此,本文建立泽兰药材特征图谱以及酚酸类成分的含量测定方法,并围绕不同产地泽兰药材及其茎、叶部位中含有活性成分的分布进行分析评价,以期建立更加全面合理的中药材质量评价方法,为泽兰药材标准化种植、合理利用药材资源及药材质量标准全面提升提供数据支撑。
1 仪器与材料
Waters H-Class 型超高效液相色谱仪(美国沃特世公司);Agilent SB C18(2.1 mm × 100 mm,1.8 μm);ME204E型万分之一天平,XP26型百万分之一天平(梅特勒-托利多公司);Milli-Q 型超纯水机(美国默克公司);KQ500D 型超声波清洗器(昆山市超声仪器有限公司)。
迷迭香酸对照品(含量:90.5%,批号:111871-201706)、咖啡酸对照品(含量:99.7%,批号:110885-201703)均为中国食品药品检定研究院提供;乙醇为分析纯;磷酸、乙腈为色谱纯;水为超纯水。9 批泽兰药材经广东一方制药有限公司魏梅主任中药师鉴定为唇形科植物毛叶地瓜儿苗Lycopus lucidus Turcz. var. hirtus Regel 的干燥地上部分,将每批药材的茎、叶分开,备用,来源信息见表1。

表1 泽兰药材信息表Tab. 1 Lycopus lucidus medicine information table
2 方法与结果
2.1 色谱条件
以Agilent SB C18(2.1 mm×100 mm,1.8μm)为色谱柱;以乙腈为流动相A,0.05%磷酸为流动相B,梯度洗脱(0 ~3 min,10%→13%A;3 ~9 min,13%A;9 ~10 min,13% →15%A;10 ~15 min,15% →20%A;15 ~24 min,20% →30% A;24 ~26 min,30%→90%A);流速为0.4 mL/min;柱温为40 ℃;检测波长为330 nm;进样体积为1 μL。
2.2 对照品溶液的制备
精密称取咖啡酸对照品、迷迭香酸对照品适量,加甲醇制成每1 mL 含咖啡酸6.256 μg、迷迭香酸80.473 μg 的混合对照品溶液。
2.3 供试品溶液的制备
取泽兰药材粉末(过三号筛)适量,取约0.5 g,精密称定,置具塞锥形瓶中,精密加入70%乙醇20 mL,称定重量,超声处理(功率:250 W,频率:50 kHz)30 min,再称定重量,补重,摇匀,滤过,即得。
2.4 特征图谱的建立及评价
2.4.1 精密度试验 取同一供试品溶液,按“2.1”项下色谱条件连续进样6 次,以迷迭香酸色谱峰为参照峰(S),计算得各特征峰相对保留时间和相对峰面积RSD 值均小于3%,表明仪器精密度良好。
2.4.2 重复性试验 取泽兰药材供试品(S3)共6份,按照“2.3”项下方法制备供试品溶液,按“2.1”项色谱条件进样测定,以迷迭香酸色谱峰为参照峰(S),计算得各特征峰相对保留时间和相对峰面积RSD 值均小于3%,表明方法重复性良好。
2.4.3 稳定性试验 取同一供试品溶液,按“2.1”项下色谱条件,分别在0、2、4、6、8、12 h 进样测定,以迷迭香酸色谱峰为参照峰(S),计算得各特征峰相对保留时间和相对峰面积RSD 值均小于3%,表明供试品溶液在12 h 内稳定性良好。
2.4.4 特征图谱分析与评价 (1) 共有峰的确定 取9 批泽兰药材(S1 ~ S9)及其对应的茎(J1 ~ J9)、叶(Y1 ~ Y9),按“2.3”项下方法制备供试品溶液,按“2.1”项下色谱条件进样测定,记录色谱图。采用 《中药色谱指纹图谱相似度评价软件》 (2012 版)分别对9 批泽兰药材、茎、叶特征图谱进行共有峰标识,以S1 号图谱作为参照图谱,以“平均数”法作为对照图谱生成方式,全谱峰匹配分别生成9 批泽兰药材、茎、叶的共有特征图谱,共标定了4 个共有峰,同时分别生成对照图谱R1、R2、R3,结果见图1 ~ 4。经对照品指认,确定峰1 为咖啡酸,峰3 为迷迭香酸,结果见图4。因峰3 分离效果好、出峰稳定,故选定为参照峰S。
(2) 相似度评价 分别以泽兰药材、茎、叶生成的共有模式(R1、R2、R3)为对照图谱,9 批次泽兰药材与其对照图谱的相似度均在0.90 以上,说明泽兰药材、茎、叶组内具有较好的相似性,结果见表2。R1 与R2 的相似度为0.869,R1 与R3 的相似度为0.983,R2 与R3 的相似度为0.835,结果显示,茎与药材/叶之间的差异较大,而药材与叶的相似度较高,样品比较接近。

图1 泽兰药材特征图谱Fig. 1 Atlas of Lycopus lucidus medicinal herbs

图2 泽兰茎特征图谱Fig. 2 Atlas of Lycopus lucidus stem

图3 泽兰叶特征图谱Fig. 3 Lycopus lucidus leaf feature map
(3) 聚类分析 将9 批泽兰药材、9 批泽兰茎、9 批泽兰叶共有峰峰面积除以称样量后,运用SPSS 20.0 软件进行聚类分析,采用组间平均数联结法,以平均Euclidean 距离为度量标准。27 个样品被分为三类,I 类包括J1~J9,即泽兰茎的9 批样品聚为一类;Ⅱ 类包括S1、S2、S3、S4、S6、S7、S8、S9、Y4、Y6、Y7、Y8、Y9,即泽兰药材的8 批样品和泽兰叶的5 批样品聚为一类;Ⅲ类包括Y1、Y2、Y3、Y5、S5,即泽兰叶的4 批样品和泽兰药材的1批样品聚为一类,结果见图5。

图4 对照品与供试品色谱图Fig. 4 Chromatograms of reference and test products

表2 泽兰UPLC 特征图谱与对照图谱(R1、R2、R3)相似度评价结果Tab. 2 Evaluation result of similarity between Lycopus lucidus UPLC feature map and control map (R1, R2, R3)

图5 聚类分析结果Fig. 5 Cluster analysis results
(4) 主成分分析 将9 批泽兰药材、9 批泽兰茎、9 批泽兰叶共有峰峰面积相对于称样量量化后,用SPSS 20.0 软件进行主成分分析,得出相关矩阵的特征值及其贡献率,见表3。

表3 主成分特征值及贡献率结果Tab. 3 Principal component characteristic values and contribution rate results
结果显示,只有1 个主成分的特征值大于1,即3.087,其方差贡献值达79.683%,故主成分1 可代表泽兰特征图谱共有峰的大部分信息。由表4 可知,第1 主成分主要反映了来自原始指标色谱峰1、峰2、峰3、峰4 的信息。前3 名变量的权重值分别为0.923(峰1 咖啡酸)、0.893(峰2)、0.880(峰3 迷迭香酸),即可判定峰1、峰2、峰3 在区分泽兰不同药用部位特征图谱占了决定性作用。针对第1 个主成分对泽兰药材、茎、叶进行评价,计算得分,结果见表5。排名前9 的样品中,叶有6 批,药材有3 批(S3、S4、S5:河南省南阳市);排名倒数9 名的均为泽兰茎的样品。总体来说,同一产地泽兰叶品质最优,药材居中,茎最差,且茎与叶、药材差异明显;河南省南阳市产地的泽兰药材样品综合得分排名较靠前,说明河南省南阳市产地的泽兰药材整体品质较优。

表4 主要因子载荷矩阵表Tab. 4 Main factor load matrix table

表5 综合得分排序表Tab. 5 Comprehensive score ranking table
2.5 含量测定方法与评价
2.5.1 线性试验 精密称取咖啡酸对照品适量,置于50 mL 容量瓶中,加甲醇稀释至刻度,制成每1 mL 含30.005 μg 的储备液;精密称取迷迭香酸对照品适量,置于25 mL 容量瓶中,加甲醇稀释至刻度,制成每1 mL 含1 011.464 μg 的储备液。分别精密量取咖啡酸储备液、迷迭香酸储备液0.1、0.5、1.0、2、5 mL 于10 mL 容量瓶中,精密加入甲醇稀释至刻度,摇匀,注入液相色谱仪,按照“2.1”项下色谱条件测定峰面积,以峰面积积分值为纵坐标(Y),对照品浓度为横坐标(X)进行线性回归,计算各成分回归方程、相关系数(r)、线性范围,见表6,结果显示咖啡酸、迷迭香酸的线性关系良好。

表6 咖啡酸、迷迭香酸线性关系考察结果Tab. 6 Investigation results of linear relationship between caffeic acid and rosmarinic acid
2.5.2 精密度试验 取同一供试品溶液,按“2.1”项下色谱条件连续进样6 次,测定咖啡酸峰面积、迷迭香酸峰面积的RSD值均小于3%,表明精密度良好。
2.5.3 稳定性试验 取同一供试品溶液,按“2.1”项下色谱方法分别于0、2、4、6、8、12 h 进样测定,咖啡酸峰面积、迷迭香酸峰面积的RSD 值均小于3%,表明供试品溶液在12 h 内稳定性良好。
2.5.4 重复性试验 取泽兰药材供试品(S3)共6份,按“2.3”项下方法制备供试品溶液,按“2.1”项下的色谱条件进行测定,计算得咖啡酸、迷迭香酸含量RSD 值均小于3%,表明方法重复性良好。
2.5.5 加样回收试验 取已测质量分数泽兰药材(S3)约0.25 g,精密称定分为三组,每组平行3 份。分别按0.5 ∶1、1 ∶1、1.5 ∶1 加入对照品,按照“2.3”项下制备方法制备供试品溶液,按“2.1”项下色谱条件进样测定,计算加样回收率,结果咖啡酸的平均加样回收率为97.63%(RSD = 0.68%,n = 9),迷迭香酸的平均加样回收率为99.31%(RSD = 1.52%,n = 9),见表7,表明该方法准确度良好。
2.5.6 含量测定结果 取27 个泽兰样品,分别按“2.3”项下方法制备供试品溶液,按“2.1”项下的色谱条件进样测定,计算咖啡酸、迷迭香酸含量,结果见表8。由表可知,同一产地泽兰中咖啡酸、迷迭香酸含量均为:叶>药材>茎;不同产地泽兰样品中的咖啡酸含量波动相对较稳定(RSD 范围为5.81% ~ 14.02%),而迷迭香酸含量波动较大(RSD范围为28.42% ~ 45.19%),说明不同产地泽兰咖啡酸、迷迭香酸含量具有一定的差异性,但迷迭香酸含量差异更显著;按泽兰药材咖啡酸和迷迭香酸总含量来看,以河南省南阳市产地的泽兰药材含量较高且稳定,其次是河南省驻马店市,江苏淮安、宿迁两产地含量均较低。
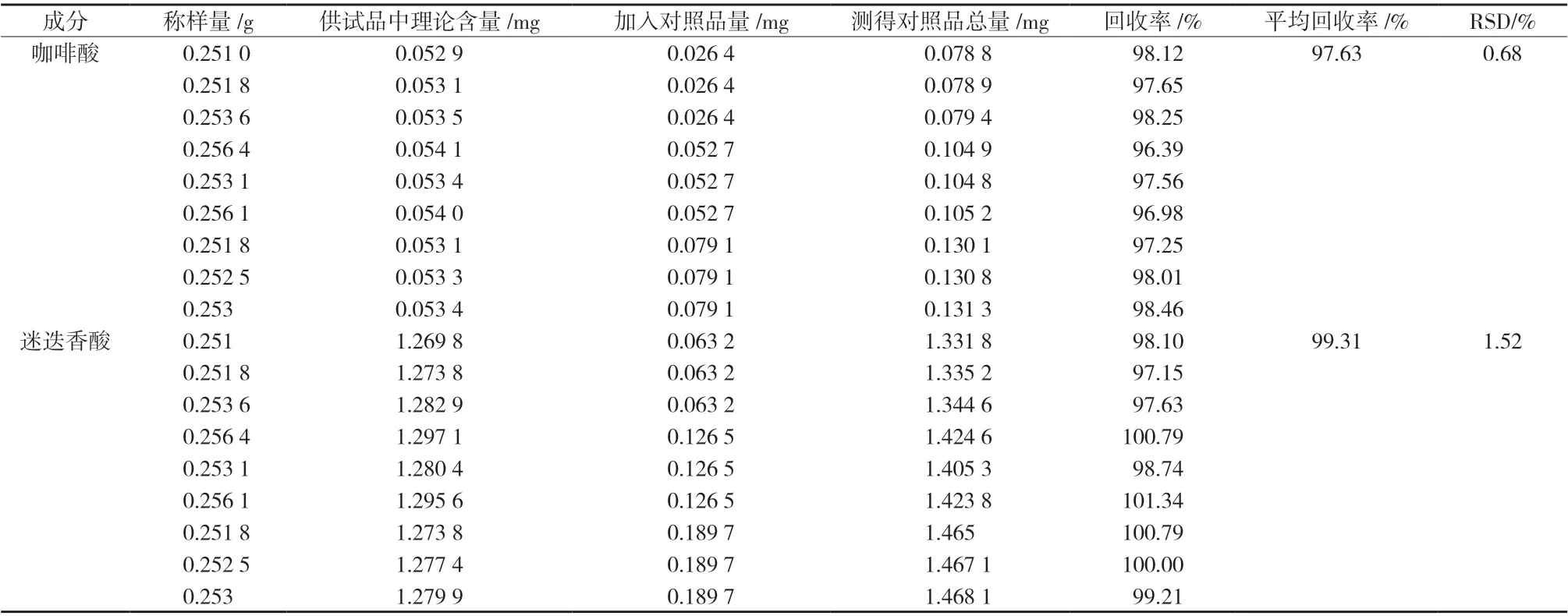
表7 加样回收试验结果Tab. 7 Recovery test result

表8 泽兰不同部位含量测定结果Tab. 8 Determination results of different parts of Lycopus lucidus
3 讨论
3.1 分析方法的优化
本研究分别对流动相体系、检测波长、提取溶媒、提取方式、提取时间等条件进行了考察,最终选取效果最好的乙腈-0.05%磷酸溶液为流动相,330 nm 为检测波长,70%乙醇超声提取30 min 作为泽兰的供试品溶液制备方法。
3.2 特征图谱结果的分析
本研究采用UPLC 法,建立了泽兰特征图谱方法,该方法简便、快捷和准确。9 批泽兰药材及其茎、叶特征图谱共确定了4 个共有峰,指认了其中的峰1为咖啡酸,峰3 为迷迭香酸;相似度、聚类分析、主成分分析结果一致,表明泽兰不同药用部位具有一定的差异性,茎与叶/药材相似度较低,差异较大,能明显区分出来即单独聚为一类;而叶与药材相似度良好,即叶分布较散,部分样品与药材聚在一起,由得分散点图可知,得分较低的叶样品与药材得分差不多,可判定不同产地泽兰叶的品质差异较大,品质较差的叶与药材难以区分出来。
3.3 含量测定结果的分析
2020 年版《中国药典》中“泽兰”项下未收载含量测定指标,本研究主成分分析结果显示,前3 名变量的权重值分别为0.923(峰1 咖啡酸)、0.893(峰2)、0.880(峰3 迷迭香酸),即可判定峰1、峰2、峰3 在区分泽兰不同药用部位中占决定性作用,因峰1、峰3 已指认出成分,且咖啡酸和迷迭香酸为泽兰活性成分[9-11],故本研究以咖啡酸、迷迭香酸为含量测定指标,对27 个泽兰样品进行研究。由结果可知,同一泽兰样品中咖啡酸、迷迭香酸含量为叶>药材>茎,与《中国药典》规定“夏、秋二季茎叶茂盛时采割”一致,推测泽兰活性成分主要富集于叶中。因此,为确保临床疗效,建议保持药材的完整性,采收过程中尽量避免叶片的掉落与损失。不同产地泽兰咖啡酸、迷迭香酸含量存在一定的差异,其中迷迭香酸含量差异显著;整体来说,以河南省产地的泽兰药材总含量较高且稳定,江苏产地总含量较低。
4 结论
本研究建立了不同产地以及不同部位泽兰UPLC特征图谱,并同时测定泽兰不同部位中酚酸类成分(咖啡酸、迷迭香酸)的含量, 该方法简单、稳定、可靠,重复性好,可为泽兰药材的质量评价提供参考依据。综合分析,以河南省产地的泽兰药材总含量较高且稳定,江苏产地总含量较低。 建立不同产地以及不同部位泽兰UPLC 特征图谱,并同时测定泽兰不同部位中酚酸类成分(咖啡酸、迷迭香酸)的含量,为泽兰药材的质量控制及评价提供参考。
