Cu-In-S纳米线促进电催化二氧化碳还原制备一氧化碳
2021-01-21钟达忠郝根彦李晋平
钟达忠,郝根彦,李晋平,赵 强
(太原理工大学 a.化学化工学院,b.气体能源高效清洁利用山西省重点实验室,太原 030024)
随着化石能源的不断消耗,大气中二氧化碳浓度增加以及环境污染问题越来越严重[1-2]。利用太阳能等可再生能源发电再电催化还原二氧化碳可以有效地缓解能源危机和温室效应[3-4]。然而,二氧化碳还原和析氢的热力学电位接近,而且二氧化碳还原是一个动力学缓慢的过程。相对于二氧化碳还原,动力学有利的析氢反应更容易发生,这导致二氧化碳还原的活性和选择性往往较低。一氧化碳是重要的化工原料,将二氧化碳还原至一氧化碳具有重要的意义。目前报道的能够有效地将二氧化碳还原至一氧化碳的催化剂多为贵金属Au[5-7]、Ag[8]和Pd[9-11]等。但是,贵金属昂贵稀少的缺点限制了其进一步的大规模应用。开发廉价高效的二氧化碳还原催化剂是提升二氧化碳还原活性和选择性的有效途径。铜由于能够进一步将一氧化碳还原成烃类和醇类,被广泛认为是潜在的能够广泛应用的二氧化碳还原催化剂。但是多晶铜的析氢活性较高,催化二氧化碳还原得到一氧化碳的活性和选择性依然较低。CuIn双金属合金也是一种高效的二氧化碳还原催化剂[12-13]。铟的引入能够有效地促进二氧化碳在铜上的还原。此外,金属硫化物被报道具有较好的二氧化碳还原的活性[14-15]。CdS纳米棒被报道具有很好的将二氧化碳还原至一氧化碳的活性[15],其具有硫空位的(0002)晶面被认为能够有效促进二氧化碳活化[15]。然而,CdS毒性较高,对人体和环境伤害较大,不利于其大规模应用。为了开发廉价高效的环境友好型二氧化碳还原催化剂,我们通过在铜上引入硫元素来提升铜的表面粗糙度,提升其电化学活性面积,提升电催化反应的电流密度。通过进一步引入铟制备Cu-In-S,In的引入能够有效抑制析氢,提高二氧化碳还原至一氧化碳的选择性。得到的Cu-In-S和Cu-S在-0.8 V vs.RHE的电压下电流密度都能够达到-6.23 mA/cm2左右,与Cu NWs的-1.23 mA/cm2的电流密度相比有了明显的提升。同时,Cu-In-S的CO法拉第效率明显提升,其在-0.8 V vs.RHE的电压下到达最高约75%的CO法拉第效率。
1 实验部分
1.1 试剂
从阿拉丁购买获得CuCl2·2H2O,葡萄糖(分析纯)购自天津化学试剂一厂,十六胺(95%)购自安耐吉化学,正己烷(99%)购自元立公司,硫脲(99%)购自国药。所有试剂在使用前没有进一步纯化。所有实验用水为高纯水(18.25 MΩ/cm).
1.2 合成Cu NWs
参考文献[16]制备Cu NWs. 85.5 mg氯化铜和99 mg葡萄糖溶解在40 mL水中,然后加入0.54 g十六胺搅拌5 h形成天空蓝的溶液,再将此溶液转移至100 mL的反应釜中在120 ℃反应24 h.所得样品经过清洗分散在正己烷中。
1.3 合成Cu-S和Cu-In-S
取10 mg Cu NWs分散在含有22.84 mg(0.3 mmol) 硫脲和30.08 mg(0.1 mmol) 硝酸铟的40 mL PEG600溶液中,在无氧条件下180 ℃回流120 min,制备得到Cu-In-S.不添加硝酸铟制备得到Cu-S.
1.4 电极的制备
将1 mg催化剂和10 μL 5%的Nafion超声分散在490 μL乙醇中,形成均匀的悬浮液。将50 μL悬浮液滴涂在面积为0.5 cm2的玻碳电极上,催化剂负载量为0.2 mg/cm2;在空气中干燥后,进行活性测试。
1.5 结构表征
在Bruker D8 Discover衍射仪上获得X射线衍射图像(XRD)。 扫描电子显微镜照片(SEM)在Hitachi SEM(SU8010,Japan)上获得。 透射电子显微镜(TEM)图像是在JEM-2100(Japan)上获得的。
1.6 活性测试
电化学测试在三电极体系下进行,带隔膜的定制的密闭H型反应池作为反应器,电解液为二氧化碳饱和的0.1 mol/L KHCO3,Ag/AgCl(KCl饱和)和Pt片分别作为参比电极和对电极。测试过程中利用气相色谱对反应的产物进行检测。
2 结果与讨论
2.1 催化剂的制备与结构表征
如图1(a),(b)所示,扫描电镜图说明成功制备了均一分散的Cu纳米线(Cu NWs).光学图片(图1(a)中插图所示)为分散在正己烷中的Cu NWs,其表现出暗红色,说明成功得到金属铜。透射电镜图表明得到的Cu NWs直径约为20~30 nm(图1(c)).高倍透射电镜对应的晶格条纹来自Cu(111)晶面,进一步说明制备得到的为金属铜(图1(d)).XRD衍射图(图1(e))也进一步说明成功得到了金属Cu.
进一步通过液相硫化反应,以硫脲作为硫源,在Cu NWs上引入S制备得到了Cu-S纳米线结构,如图2(a)所示。称取10 mg Cu NWs分散在含有22.84 mg硫脲的40 mL PEG600溶液中,在排空空气的条件下加热至180 ℃,回流120 min,冷却至常温,通过清洗干燥得到了Cu-S.通过扫描电镜照片(图3(a),(b))可以看出,硫化之后Cu NWs长度变短了,但是依然保持棒状结构,其表面变得更加粗糙,这样有利于暴露更多的反应位点,促进电催化反应的进行。图3(c)透射电镜图进一步表明其依然保持棒状结构,表面由原来的光滑表面变得更加粗糙。高倍透射电镜(图3(d))可以观察到晶面间距为0.3 nm的晶格条纹,这和Cu2S的(101)晶面能够很好地对应,说明S引入之后成功制得了Cu2S.为了进一步考察Cu和S元素的分布状态,我们进行了元素分布能谱表征,如图3(e)所示。结果表明,Cu和S元素是均匀分布的,说明我们成功得到了结构均一的Cu-S,S元素均匀掺入到Cu中。

图1 Cu NWs的(a),(b)扫描电镜图(插图为Cu NWs的光学照片),(c)透射电镜图和(d)高倍透射电镜图(插图为黄色框区域的FFT变换),(e)Cu NWs的XRD衍射图Fig.1 (a),(b) Scanning electron microscopy, (c) Transmission electron microscopy, and (d) High resolution transmission electron microscopy images of Cu NWs. (Inset in a: optical photograph of Cu NWs, inset in d: FFT image). (e) XRD pattern of Cu NWs.
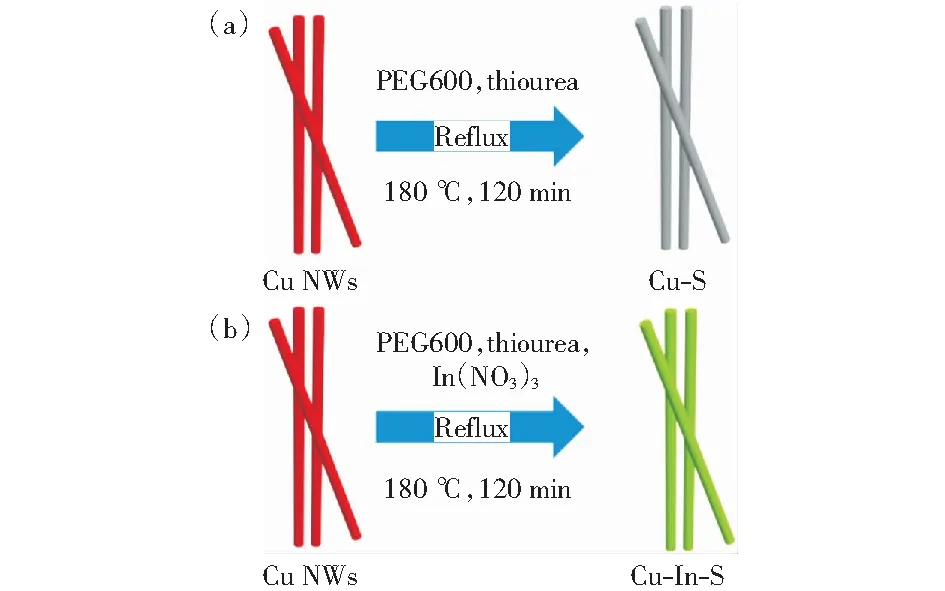
图2 (a)Cu-S和(b)Cu-In-S的制备过程Fig.2 Preparation of (a) Cu-S and (b) Cu-In-S

图3 Cu-S的(a,b)扫描电镜图,(c)透射电镜图,(d)高倍透射电镜图和(e)元素分布图Fig.3 (a,b) Scanning electron microscopy, (c) transmission electron microscopy, and (d) high resolution transmission electron microscopy images of Cu-S. (e) Elements mapping of Cu and S
类似的,我们取10 mg Cu NWs分散在含有22.84 mg硫脲和30.08 mg硝酸铟的40 mL PEG600溶液中,在无氧条件下180 ℃ 回流120 min,冷却至常温状态,通过清洗干燥得到了Cu-In-S(图2(b)).通过扫描电镜对其表面结构进行表征,从图4(a),(b)可以看出,Cu-In-S展现出类似于Cu-S的表面结构,其长度比Cu NWs稍短,但是其表面变得更加粗糙,有许多堆积的小颗粒。此结果说明In的引入并没有引起其形貌的进一步改变,S元素的引入对形貌和粗糙度的改变起着关键作用。我们进一步通过透射电镜表征对其结构进行分析,如图4(c),(d)所示,透射电镜结果同样说明了其表面结构变成类似于Cu-S的粗糙表面。高倍透射电镜可以看到晶格间距为0.32 nm的晶格条纹,对应于CuInS2的(112)晶面,说明In和S的引入生成了CuInS2.同样的,我们考察了Cu、In和S三种元素的分布情况,如图4(e)所示,Cu、In和S是均匀分布的。

图4 Cu-In-S的(a,b)扫描电镜图,(c)透射电镜图,(d)高倍透射电镜图和(e)元素分布图Fig.4 (a,b) Scanning electron microscopy, (c) transmission electron microscopy, and (d) high resolution transmission electron microscopy images of Cu-In-S. (e) Elements mapping of Cu, In, and S
为了进一步明确制备的Cu-S和Cu-In-S的结构,对其进行了X-射线衍射表征。如图5所示,可以看出Cu-S主要以Cu2S的形式存在。同时引入In和S后,得到的Cu-In-S的X-射线谱图衍射峰和CuInS2的PDF卡片(PDF#65-2732)基本吻合,说明Cu-In-S是以CuInS2的结构存在。X-射线衍射的结果和高倍透射电镜的结果也具有很好的一致性。
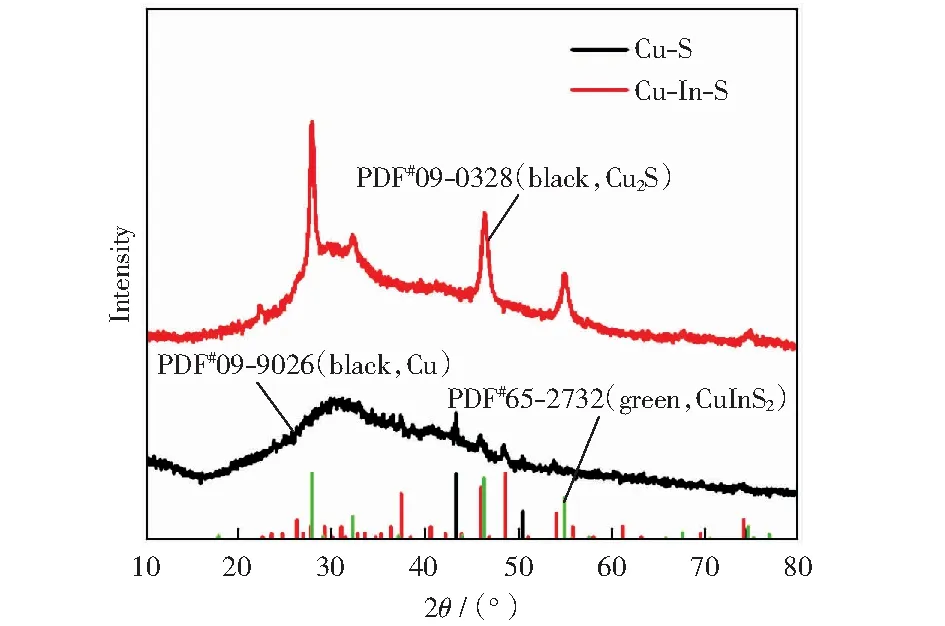
图5 Cu-S和Cu-In-S的X-射线衍射图谱Fig.5 X-ray diffraction patterns of Cu-S and Cu-In-S
2.2 催化剂的活性测试
将Cu NWs、Cu-S和Cu-In-S滴涂在玻碳电极上对其活性进行测试,分别以Ag/AgCl(KCl饱和)和Pt片作为参比电极和对电极,电解液为CO2饱和的0.1 mol/L KHCO3.通过极化曲线对其CO2还原电流密度进行考察,结果如图6所示。在相同的电压下,相对于Cu NWs,Cu-S表现出明显更高的电流密度,这可能是S的引入导致表面结构更粗糙从而表现出电流密度的提高。同时,我们发现其起始电位也出现了正移,说明S的引入也会有利于二氧化碳还原或者析氢反应的进行。Cu-In-S的极化曲线和Cu-S重合度较高,说明In的引入并没有对催化电流有进一步的影响。
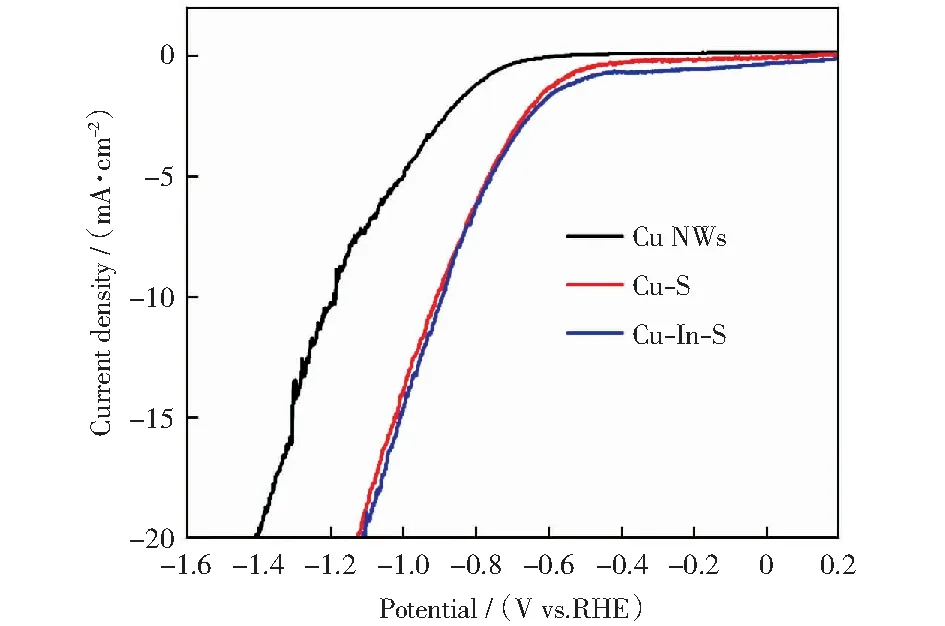
图6 Cu NWs、Cu-S和Cu-In-S的极化曲线Fig.6 Linear sweep voltammetry curves of Cu NWs, Cu-S, and Cu-In-S
为了探究Cu-S和Cu-In-S表现出较高电流密度的原因,进一步进行了电化学活性面积的测试,以双电层电容代表电化学活性面积的大小。如图7所示,Cu-In-S和Cu-S表现出相似的电化学活性面积,和其类似的表面结构结果相吻合。Cu-S和Cu-In-S表现出比Cu NWs高的电化学活性面积,说明S的引入导致电化学活性面积变大,有效地促进了电催化电流密度的提高。
根据极化曲线,选择-0.5~-1.0 V的电压进行法拉第效率测试。如图8(a),法拉第效率测试显示Cu NWs在所测试的电压范围内基本都是产氢的,其CO法拉第效率低于10%.同时,引入S之后,产物分布并没有观察到明显的变化,CO的选择性依然较低,说明S的引入对产物分布并没有太大的影响,其主要是促进了催化剂电化学活性面积的提高,从而提升催化电流密度。然而,如果同时引入了In,其产物分布则发生了明显的变化,Cu-In-S的CO选择性有了明显的提升(图8(c)).改变引入In的量,发现制备过程中适当的In引入量(0.1 mmol)得到的Cu-In-S表现出最好的反应活性(图8(c)).测试电压从-0.5 V升到-1.0 V,Cu-In-S的CO法拉第效率表现出先上升后下降的趋势,其在-0.8 V表现出最大的CO法拉第效率,为75%.说明In的引入能够有效地促进二氧化碳的还原,提升其二氧化碳还原活性。图9为In的引入量为0.05和0.15 mmol时制得的样品的反应活性测试结果。

图7 Cu NWs、Cu-S和Cu-In-S的电化学活性面积Fig.7 Electrochemical surface area test for Cu NWs, Cu-S, and Cu-In-S
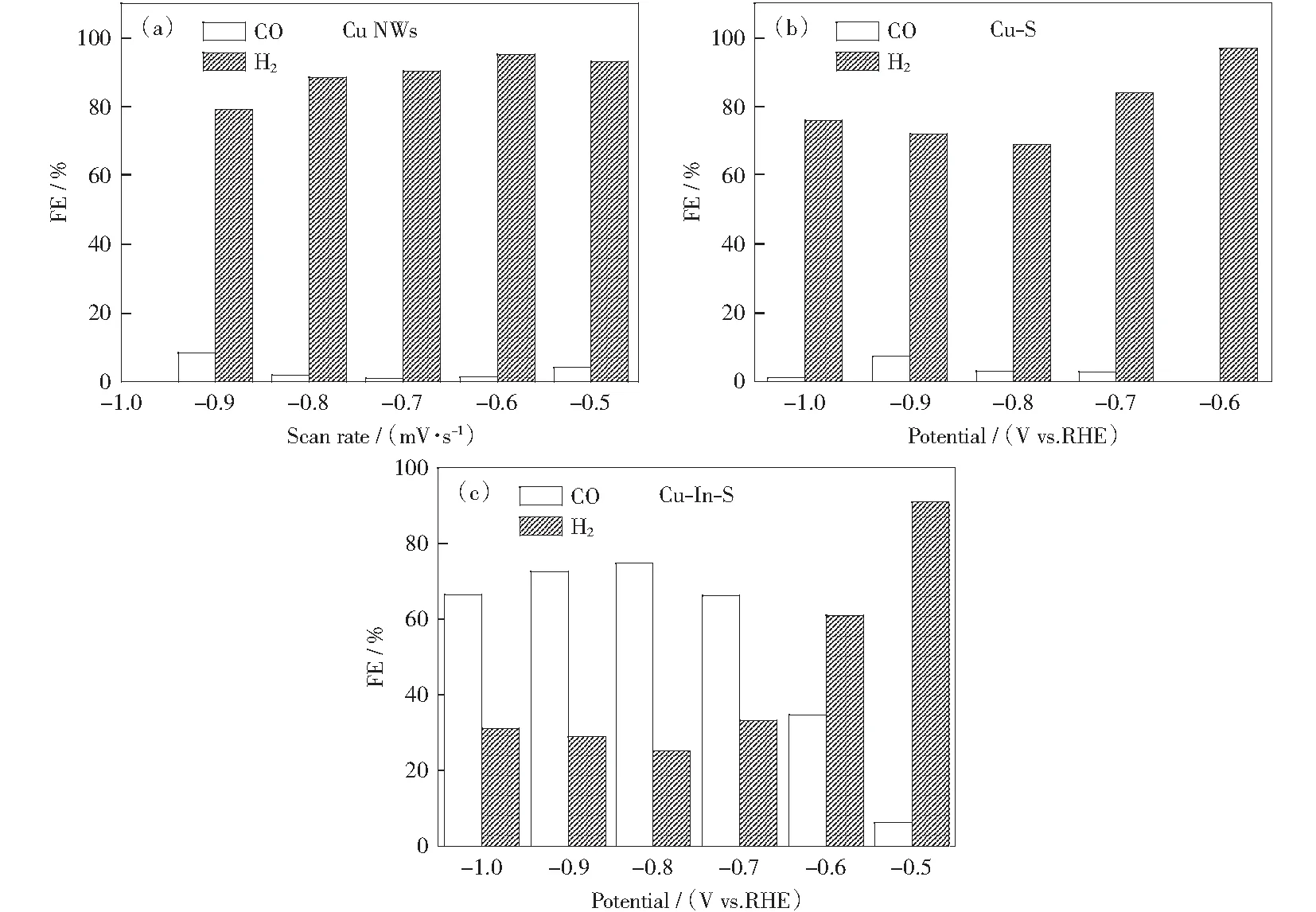
图8 (a)Cu NWs,(b)Cu-S和(c)Cu-In-S的CO2还原活性测试Fig.8 CO2 reduction activity of (a) Cu NWs, (b) Cu-S, and (c) Cu-In-S
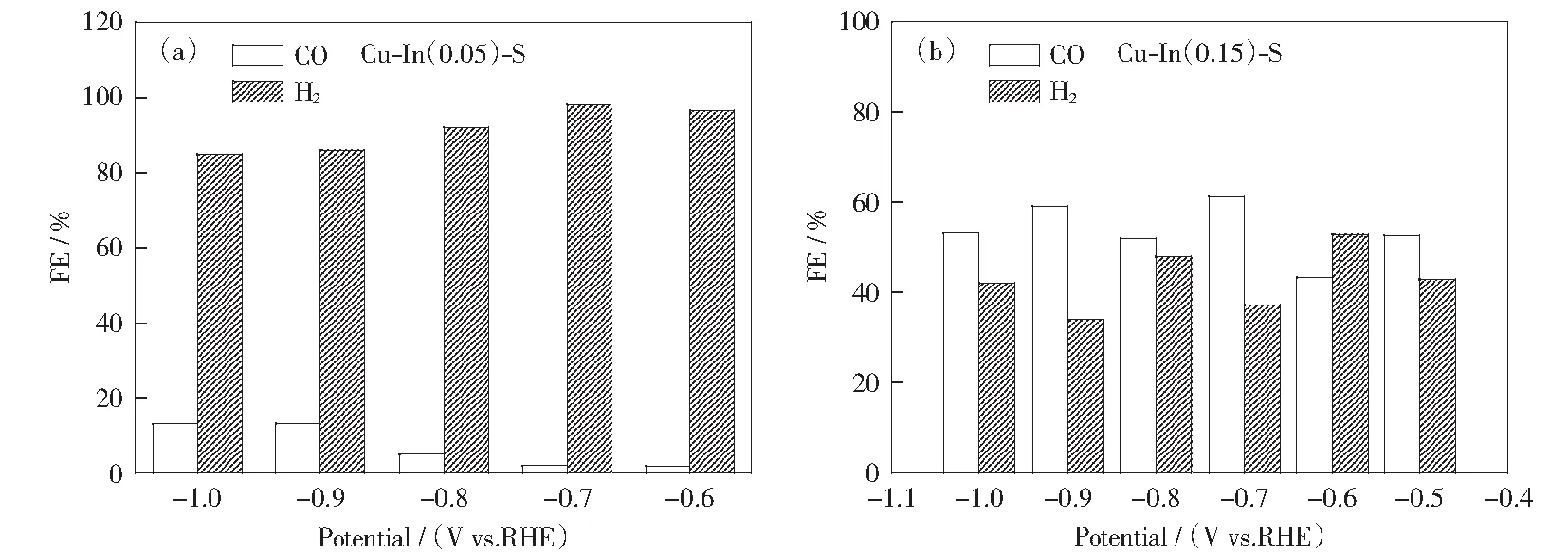
改变加入的硝酸铟量为0.05 mmol制备获得,Cu-In(0.15)-S为改变加入的硝酸铟量为0.15 mmol制备获得图9 (a)Cu-In(0.05)-S和(b)Cu-In(0.15)-S的CO2还原活性测试Fig.9 CO2 reduction activity of (a) Cu-In(0.05)-S and (b) Cu-In(0.15)-S
需要注意的是,Cu NWs和Cu-In-S催化性测试。Cu-In(0.05)-S为反应得到的产物中CO和H2气体产物的法拉第效率接近100%,说明其基本没有液相产物。而对于Cu-S而言,它可能会产生少量的甲酸[17]。
3 结论
本文成功制备了Cu NWs、Cu-S和Cu-In-S的棒状纳米结构,Cu-S和Cu-In-S表现出较为粗糙的表面,S的引入对粗糙表面的构建起着关键作用。将它们用于电催化二氧化碳还原,Cu-In-S表现出较好的二氧化碳还原能力,其在-0.8 V vs.RHE电压下表现出最高的一氧化碳法拉第效率,为75%;In的引入是促进其法拉第效率提升的原因。同时,Cu-In-S和Cu-S在-0.8 V vs.RHE电压下电流密度都能够达到-6.23 mA/cm2左右,相对Cu NWs的-1.23 mA/cm2有了明显的提升。
