新型冠状病毒肺炎治疗过程中糖皮质激素的应用(附2例报告)
2020-12-17廖付军鲍海龙李洁琪吴叶婷杨京李伟
廖付军,鲍海龙,李洁琪,吴叶婷,杨京,李伟
1 贵州医科大学附属医院,贵州贵阳550004;2 贵黔国际总医院
2019年12月以来,湖北省武汉市部分医院陆续发现了多例有华南海鲜市场暴露史的不明原因肺炎病例,现已证实为2019新型冠状病毒(2019-nCoV)感染引起的急性呼吸道传染病,即新型冠状病毒性肺炎(COVID-19)。COVID-19疫情在我国范围内迅速蔓延,并引发严重的公共卫生事件。截至2020年2月29日,我国已确诊的COVID-19患者累计达79 251例,其中重症患者达7 664例,死亡患者达2 835例[1]。新英格兰医学杂志纳入中国1 099例COVID-19患者对人口统计学特点及临床特征进行分析,结果表明COVID-19症状、影像学特点以及疾病的严重程度呈现多样性,入院时发热占比仅为43.8%,20.8%的患者入院时未见影像学改变,这给诊疗过程带来很高的难度;另外发现其中204例(18.6%)患者接受了糖皮质激素治疗,在重症患者中的比例(44.5%)高于非重症患者(13.7%),在这204例患者中,有33例(16.2%)进入ICU,17例(8.3%)接受有创通气治疗,5例死亡(2.5%)[2]。而目前国内对于糖皮质激素在COVID-19治疗过程中的应用存在争议,部分专家考虑糖皮质激素的不良反应及治疗COVID-19疗效的不确定性,对其持保守态度;相反,部分专家认为糖皮质激素已广泛应用于严重感染治疗,早期应用可影响重症肺炎的发生发展,提高治愈率、降低死亡率,对其持开放态度。本研究在观察糖皮质激素治疗效果的同时,结合2例患者的用药情况探讨新型冠状病毒肺炎治疗过程中糖皮质激素的用药时机、疗程、剂量及不良反应等,现报告如下。
1 临床资料
2020年1月30日,贵州医科大学附属医院感染科隔离病房收治的COVID-19患者2例,为两姊妹,分别编号为患者A(妹妹)、患者B(姐姐)。
患者A,女,53岁,因“咳嗽、咳黄绿色脓痰2 d”入院。自述长期居住武汉,1月21日返回贵阳探亲,1月28日无明显诱因出现咳嗽、咳痰,无发热及呼吸困难,未自行服药。1月30日首次在贵州医科大学附属医院发热门诊就诊,考虑其流行病学史,为进一步诊治,于同日入院接受治疗。患者有高血压病史3年、糖尿病病史1年,否认食用野味,未去过华南海鲜市场。入院体格检查结果显示:体温37.1 ℃,心率108次/分,心律齐无杂音,血压160/86 mmHg,咽不红,扁桃体无肿大,双下肺可闻及少量湿啰音。血常规检查显示:白细胞(WBC)5.59×109/L,中性粒细胞(N)绝对值4.08×109/L,淋巴细胞(L)绝对值0.97×109/L。首次肺部CT检查提示患者右下肺感染。
患者B,女,61岁,因“发热、咳嗽1 d”入院。自述长期居住武汉,1月21日返回贵阳探亲,1月29日无明显诱因出现咳嗽,呈干咳无痰,发热,最高体温37.8 ℃,伴腹泻,无呼吸困难,未自行服药。1月30日在贵州医科大学附属医院发热门诊就诊,考虑其流行病学史,为进一步诊治,于同日入院接受治疗。患者无其他疾病史,否认食用野味,未去过华南海鲜市场。入院体格检查结果显示:体温38 ℃,心率91次/分,心律齐无杂音,血压153/74 mm Hg,咽不红,扁桃体无肿大,右下肺可闻及少量湿啰音。血常规检查显示:WBC 11.2×109/L,N绝对值8.94×109/L,L绝对值2.07×109/L。首次肺部CT检查结果显示:右下肺见多发片状磨玻璃高密度影,边界不清,考虑感染病变;右肺上叶、左肺下叶结节,右肺中叶、左肺上叶纤维化灶。
2 治疗方法及结果
患者A入院第1天检查结果显示:降钙素原0.02 ng/mL、血沉27 mm/h、血糖7.3 mmol/L、CRP 1.65 mg/L,余血常规、大小便常规、肝肾功、凝血、心肌酶学及心肌标志物检查未见明显异常,甲流、乙流病毒核酸检测阴性,胸部CT平扫见右下肺感染(图1a)。给予吸氧、头孢孟多酯抗感染、重组人干扰素α1b雾化吸入、利巴韦林静滴抗病毒等治疗方案,采集咽拭子予2019-nCoV核酸检查。入院第3天,患者出现呼吸困难,咳嗽咳痰症状较前加重,并出现体温升高至38.0 ℃,复查胸部CT见双肺斑片渗出影较前明显增加(图1b),两次2019-nCoV核酸检查结果均呈阳性,血气分析提示氧分压69.7 mm Hg、二氧化碳分压47.2 mm Hg。加用洛匹那韦/利托那韦、盐酸阿比多尔片及胸腺法新抗病毒,血必净清热解毒及抗全身炎症反应,甲强龙40 mg静脉滴注抗炎,免疫球蛋白冲击治疗,头孢孟多酯升级为莫西沙星抗感染,并予以无创呼吸机辅助呼吸。入院第6、7天,患者无明显呼吸困难,氧分压108 mm Hg,二氧化碳分压42.9 mm Hg。复查胸部CT,结果显示双肺渗出影较前增高、密度较前增高、部分病灶较前减少(图1c)。入院第8~10天,患者呼吸困难症状逐渐缓解,体温降至37.3 ℃以下,复查胸部CT,结果显示双肺渗出影较前略有吸收(图1d)。入院第11~14天,患者呼吸困难、咳嗽症状较前明显缓解,2019-nCoV核酸检测第1次转阴,停用甲强龙,复查肺部CT,结果显示双肺渗出影较前减少(图1e)。入院第16天,复查胸部CT见病灶明显吸收(图1f),两次2019-nCoV核酸检测转阴,无发热,达到第六版新冠肺炎诊治指南出院标准,予以出院。

图1 患者A不同时间点胸部CT影像
患者B入院第1天检查结果显示:降钙素原<0.02 ng/mL、血沉22 mm/h、血糖6.52 mmol/L,CRP 17.38 mg/L,余血常规、大小便常规、肝肾功、凝血、心肌酶学及心肌标志物检查未见明显异常,甲流、乙流病毒核酸检测阴性,胸部CT平扫见右下肺见多发片状磨玻璃高密度影,边界不清,右肺上叶、左肺下叶结节,右肺中叶、左肺上叶纤维化灶(图2a)。给予吸氧、头孢孟多酯抗感染、重组人干扰素α1b雾化吸入抗病毒、利巴韦林静滴等治疗,采集咽拭子予2019-nCoV核酸检查。入院第3天,患者出现呼吸困难、咳嗽咳痰症状较前加重,并出现体温升高至38.5 ℃,复查胸部CT见双肺渗出影较前明显增加(图2b),两次2019-nCoV核酸检查结果均呈阳性,血气分析提示氧分压53.4 mm Hg、二氧化碳分压43.6 mm Hg,加用洛匹那韦/利托那韦、盐酸阿比多尔片及胸腺法新抗病毒,血必净清热解毒及抗全身炎症反应,甲强龙40 mg静脉滴注抗炎,免疫球蛋白冲击治疗,头孢孟多酯升级为莫西沙星抗感染,沙丁胺醇、乙酰半胱氨酸雾化吸入,并予以无创呼吸机辅助呼吸。入院第6、7天,患者无创呼吸机辅助下氧分压72.3 mm Hg、二氧化碳分压40 mm Hg,复查胸部CT,结果显示双肺渗出较前进展、部分病灶较前减少(图2c)。在治疗2 d后,因患者本人考虑激素的不良反应,拒绝使用甲强龙抗炎,遂停止使用。入院第8~15天,患者在无创呼吸机辅助呼吸下仍感呼吸困难,血气分析提示氧分压59.2 mm Hg、二氧化碳分压46.7 mm Hg,经ICU医生会诊后转入ICU隔离治疗,并进行气管插管,予以有创呼吸机辅助呼吸,并在之前治疗基础上继续使用甲强龙40 mg静脉滴注进行抗炎治疗。入院16~20天,患者血气分析提示氧分压94.8 mm Hg、二氧化碳分压44.6 mm Hg,复查胸部CT,结果显示双肺渗出较前略有吸收(图2d),予以脱机并转出ICU。入院第21~24天,患者呼吸困难症状明显缓解,体温恢复正常,2019-nCoV核酸检测第1次转阴,减量并逐渐停用甲强龙,复查肺部CT,结果显示双肺渗出较前减少(图2e),并予以加用磷酸氯喹片口服。入院第25天复查胸部CT,结果显示病灶明显吸收(图2f),两次2019-nCoV核酸检测转阴,无发热,达到第六版新冠肺炎诊治指南出院标准,予以出院。
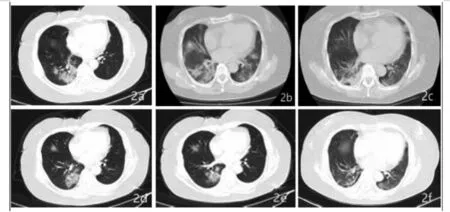
图2 患者B不同时间点胸部CT影像
3 讨论
本研究中两例患者同时发病,具有典型聚集发病特点,同时具备COVID-19典型影像学特点,参照第六版新冠肺炎诊疗指南,入院时均考虑为普通型患者[3],同时使用指南推荐的抗病毒药物治疗,包括α-干扰素雾化吸入、洛匹那韦/利托那韦口服、利巴韦林静脉滴注等,并同时使用了糖皮质激素甲强龙40 mg静脉滴注抗炎。整个诊治过程中,患者A(妹妹)使用甲强龙后未再继续出现进展恶化情况,而患者B(姐姐)在使用2 d后因考虑激素的不良反应停止使用,随后出现病情迅速进展恶化,转入ICU行呼吸机辅助呼吸等生命支持,直至继续使用糖皮质激素后病情逐渐趋向稳定,撤除呼吸机后转出ICU至康复出院。A和B患者均是在呼吸频率增快、有呼吸困难症状、血气分析提示氧分压明显下降情况下使用激素治疗,且使用的是40 mg小剂量甲强龙治疗。当然,出现两种结局,也可能与患者B(姐姐)开始肺部感染较患者A(妹妹)严重有一定的关系,这一点可从初始入院时肺部CT检查结果得到证实。最新国内指南指出,目前对抗病毒药物多种联合使用无确切有效的证据,反而因多种病毒药物的不良反应而对患者产生不利影响,因此不做常规推荐。对于激素的使用,指南指出,当出现肺内渗出增加、低氧血症进一步加重、各类细胞因子明显上升、患者向危重型转变迹象的时候,可酌情小剂量使用激素1~2 mg/kg,使用时间3~5 d[4]。
新冠肺炎病毒颗粒可吸附在呼吸道黏膜,并在扩散后感染其他细胞,在体内诱发一系列细胞免疫反应,引起外周血白细胞、淋巴细胞、巨噬细胞等免疫细胞变化,产生各种细胞因子,包括白细胞介素(IL)、干扰素、肿瘤坏死因子(TNF)超家族、集落刺激因子、趋化因子、生长因子等,其中一部分细胞因子促进炎症激活,导致炎症反应,这一炎症反应综合征被称为细胞因子风暴[5]。新冠肺炎病毒感染后,一般可通过机体免疫反应清除病毒,但失控的、过度的免疫级联反应反而对人体组织和器官造成伤害,部分患者出现急性呼吸窘迫综合征和感染性休克,最终导致多器官功能衰竭,出现死亡。因此,因糖皮质激素具有很强的抗炎症反应和免疫抑制作用,而被广泛应用于新冠肺炎患者的临床治疗。但Lancet近期发表的一篇文章质疑使用糖皮质激素治疗新冠肺炎的效果,因为目前没有确切的证据表明患者获益[6],该文章的发表为激素的使用蒙上一层阴影,因此我们国家专门为糖皮质激素的使用发布了专家共识[7],认为糖皮质激素的适应症应为:年龄≥18岁;新型冠状病毒感染核酸检测阳性;症状(包括发热、咳嗽或其他相关感染症状)发生10 d以内,影像学证实为肺炎且快速进展;静息未吸氧状态下,患者血氧饱和度(SpO2)≤93%或呼吸急促(呼吸频率≥30次/分钟)或氧合指数≤300 mm Hg。
目前对病毒性肺炎的病理生理改变过程,一般认为分为三个时相:第一时相,即病毒侵入及复制阶段,冠状病毒在感染者体内迅速复制,引起高热和流感症状,也可以称作为病毒血症时期;第二时相,机体过度免疫反应阶段,此阶段会释放大量细胞因子,形成细胞因子风暴;第三时相,炎症反应或者炎症风暴导致机体组织损伤阶段,因失控的免疫反应导致炎症介质大量释放,损害机体及器官组织[5]。因此,从病理生理角度的发展规律来理解激素的治疗时机,我们认为应该在第二时相和第三时相比较合适。在病毒复制的第一时相内使用激素可能对患者并没有获益,反而因激素的不良反应而带来危害。从药理机制看,糖皮质激素是抑制第二时相及第三时相的药物,可用于病毒性肺炎的治疗。糖皮质激素抗炎作用强,但不良反应也很明显,它虽然可抑制炎症,但也抑制了免疫反应和人体免疫系统对于病毒的清除作用,同时长期使用糖皮质激素导致股骨头坏死、糖尿病、消化道出血、二重感染、结核播散、电解质紊乱等,并留下后遗症,既往SARS期间多有报道,近期也有病例报道糖皮质激素在新型冠状病毒肺炎使用后出现糖尿病[8]。因此,糖皮质激素是一把“双刃剑”,我们该慎重对待使用激素,参照指南结合患者实际情况正确合理使用这把“双刃剑”。
综上所述,在COVID-19治疗过程当中,当肺部炎症、低氧血症进一步加重,有向危重型转变的时候,可考虑使用小剂量糖皮质激素。
