4-氨基-2,6-二甲氧基嘧啶的绿色合成工艺研究
2020-10-31赵云德朱林飞
赵云德 朱林飞 丁 靖,2
(1.江苏天和制药有限公司,江苏 扬州 225200;2.南京工业大学,江苏 南京 211816 )
4-氨基-2,6-二甲氧基嘧啶(4-amino-2,6-dimethoxypyrimidine,ADMP)是一种重要的药物中间体,可用于合成长效磺胺药(4-氨基-N-(2,6-二甲氧基-4-嘧啶基)苯磺酰胺)。该药物凭借制备成本低、使用方便和抗菌谱广等优点,广泛地应用于畜牧、养殖等行业,具有良好的市场前景[1-4]。因此,研究磺胺药中间体4-氨基-2,6-二甲氧基嘧啶的合成工艺具有重要意义和价值。
4-氨基-2,6-二甲氧基嘧啶现有的合成方法主要有:(1) 巴比妥酸法,即首先利用三氯氧磷将巴比妥酸氯化为三氯嘧啶,然后经过氨化、甲氧基化等步骤,得到4-氨基-2,6-二甲氧基嘧啶和2-氨基-4,6-二甲氧基嘧啶混合物。该工艺主要存在分离困难、产物纯度低等问题,制约了其实际生产应用;(2) 氰乙酸乙酯法,即首先通过氰乙酸乙酯、尿素和乙醇钠反应生成4-氨基-2,6-二羟基嘧啶钠盐(ADHP-Na),然后利用冰醋酸酸化生成4-氨基-2,6-二羟基嘧啶(ADHP)。在二甲基苯胺催化作用下,以三氯氧磷为氯化试剂,将4-氨基-2,6-二羟基嘧啶氯化生成4-氨基-2,6-二氯嘧啶,再经过甲氧基化生成ADMP。虽然该工艺路线较为成熟,但以三氯氧磷为氯化剂会产生大量的含磷废水,生产1吨ADMP约产生40吨含磷废水,对环境造成严重危害[5,6]。近年,随着环保要求的不断提高,诸多企业由于无力处理氰乙酸乙酯工艺过程中所产生的含磷废水已停产停业。同时,市场对长效磺胺药的需求逐年增长,因此亟待开发出一条新型环保的ADMP合成工艺路线。本文采用4-氨基-2,6-二羟基嘧啶钠盐(ADHP-Na)为反应原料,以碳酸二甲酯(DMC)为绿色甲基化试剂一步合成ADMP[7-10]。系统考察了反应条件对ADMP得率的影响,提出了可能的O-甲基化反应机理。该工艺路线的成功开发,可完全避免含磷废水的产生,为ADMP的绿色合成提供了一条可行性路径。
1 实验部分
1.1 试剂和仪器
十六烷基三甲基溴化铵(CTAB),聚乙二醇-400(PEG-400),碳酸钾(K2CO3),甲醇(CH3OH),均购自国药上海化学试剂公司,未经处理直接使用;DMC,二甲基甲酰胺(DMF),四丁基溴化铵(TBAB),均购自阿拉丁生化科技股份有限公司,未经处理直接使用;4-氨基-2,6-二羟基嘧啶(ADHP),去离子水,均实验室自制。
岛津SPD-15C液相色谱仪(日本岛津公司,C18液相色谱柱);布鲁克ACF-400核磁共振仪(德国布鲁克公司,400 MHz);瑞利WQF-510A傅里叶转化红外光谱仪(中国背景瑞利分析仪器有限公司);DF-101S数显电动搅拌器(巩义市英峪高科仪器厂)。
1.2 4-氨基-2,6-二甲氧基嘧啶的制备
以ADHP-Na为原料合成ADMP路线如图1所示。取60 mL DMF溶剂置于100 mL三颈烧瓶,加入3.42 g(20 mmol) ADHP-Na、一定量K2CO3和相转移催化剂CTAB。一定反应温度下向上述反应体系中逐滴加入DMC,恒温反应数小时。反应结束后,冷却、过滤,去离子水洗涤3次,得到淡黄色固体。

图1 以ADHP-Na为主要原料合成ADMP路线示意图Fig.1 Schematic diagram of the synthesis of ADMP from ADHP-Na
1.3 4-氨基-2,6-二甲氧基嘧啶合成过程中产物分析方法
采用HPLC测定ADMP合成过程中原料ADHP-Na和产物ADMP含量。色谱柱采用AT LiCHROM SiO2(5 μm),流速设定为1 mL/min,流动相采用甲醇和0.01%氨水混合物(体积比65∶35),检测波长为254 nm。
2 结果与讨论
以DMC为甲基化试剂,DMF为溶剂,K2CO3为固体碱催化剂,CTAB为相转移催化剂,在150 ℃和 10 h 的反应条件下,以ADHP-Na为原料合成ADMP。ADHP-Na转化率和ADMP收率如表1所示。由表1可知,以ADHP-Na为甲基化反应原料,同时加入催化剂K2CO3和相转移催化剂CTAB,ADHP-Na转化率为85.1%,ADMP收率为29.8%。当仅加入相转移催化剂CTAB时,虽然ADHP-Na转化率很高(90.2%),但是ADMP收率仅为26.5%。而当只加入催化剂K2CO3时,ADHP-Na转化率为30.2%,ADMP收率为10.9%。当二者均不加入时,ADHP-Na基本不与DMC反应。因此,可以看出催化剂K2CO3和相转移催化剂CTAB的加入对ADHP-Na甲基化反应的转化率与收率具有明显的影响。
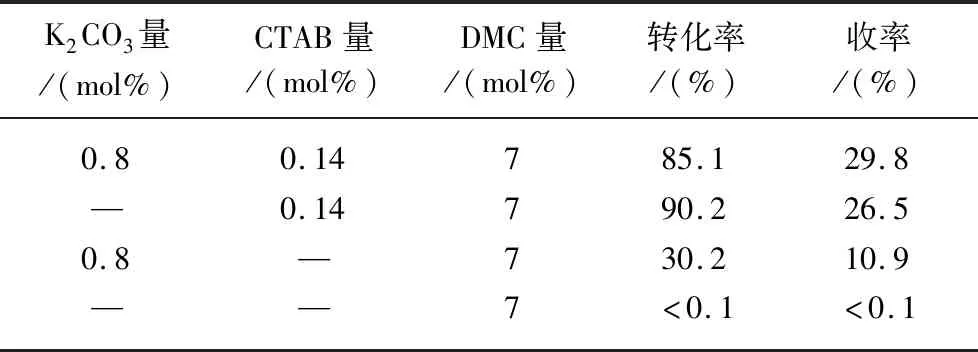
表1 催化剂的加入对反应性能的影响Tab.1 The effect of the addition of catalysts on catalytic performance
以ADHP-Na为原料和DMC为绿色甲基化试剂制备ADMP的过程主要受相转移催化剂CTAB用量、固体碱催化剂碳酸钾用量、反应温度和反应时间等因素的影响,通过单因素实验和正交实验得到最佳反应条件。实验过程中,通过液相色谱对目标产物进行定量分析,进而计算出目标产物ADMP收率。
2.1 单因素实验
2.1.1 CTAB用量对反应性能的影响
在反应温度150 ℃,反应时间10 h,催化剂为K2CO3,相转移催化剂为CTAB,n(ADHP-Na)∶n(K2CO3)∶n(DMC)=1∶0.8∶7条件下,考察了CTAB用量对ADHP-Na转化率和ADMP收率的影响,实验结果如图2所示。
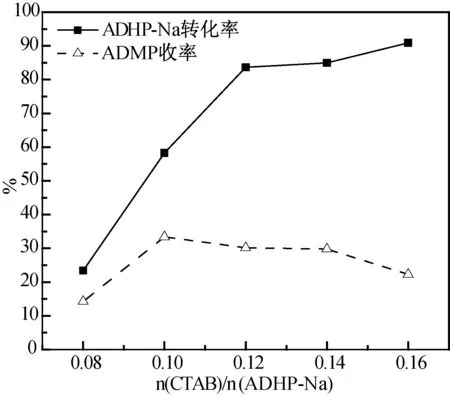
图2 CTAB用量对反应性能的影响Fig.2 Effect of CTAB dosage on reaction performance
由图2可知,随着CTAB用量增加,ADMP收率先增加后减小。当n(CTAB)∶n(ADHP-Na)=0.1∶1时,反应性能达到最佳,此时ADMP收率为33.4%。当进一步增加CTAB用量,ADHP-Na转化率增加,但是ADMP收率急剧下降,这说明CTAB用量过大会导致副反应的发生。DMC可在ADHP-Na结构上的N位和C位进行甲基化和甲氧羰基化反应,更容易发生甲氧羰基化反应。同时,CTAB用量越多,导致进入DMF相的反应离子对就越多,从而发生甲氧羰基化反应的可能性越大,因此ADHP-Na转化率增加的同时ADMP收率反而下降。综上,选择n(CTAB)∶n(ADHP-Na)=0.1∶1。
2.1.2 K2CO3用量对反应性能的影响
在反应温度150 ℃,反应时间10 h,催化剂为K2CO3,相转移催化剂为CTAB,n(ADHP-Na)∶n(CTAB)∶n(DMC)=1∶0.1∶7条件下,考察了K2CO3用量变化对ADMP合成反应性能的影响,实验结果如图3所示。由图3可知,随着K2CO3用量的增加,ADMP收率出现先保持不变后减少的现象,ADHP-Na转化率先减少后增加,当n(K2CO3)∶n(ADHP-Na)=0.8∶1时,ADMP收率最高(55.9 %),此时ADHP-Na转化率为58.3%。当n(K2CO3)∶n(ADPH-Na)=(0.4~0.8)∶1时,随着K2CO3用量的增加,ADMP收率基本不变,但其选择性由38.9%上升至55.9%。这主要是少量K2CO3催化剂的加入可以提高O-甲基化反应产物的选择性。但当n(K2CO3)∶n(ADHP-Na)>0.8∶1时,随着K2CO3量增加,ADHP-Na转化率增加,ADMP选择性降低。这说明过量K2CO3的加入利于甲氧羰基化反应的进行。由此可见,K2CO3用量过多或过少都不利于产物ADMP的生成。因此,最佳n(K2CO3)和n(ADHP-Na)比为0.8∶1。

图3 K2CO3用量对反应性能的影响Fig.3 Effect of K2CO3 dosage on reaction performance
2.1.3 DMC用量对反应性能的影响
图4为DMC用量对反应性能影响的结果。由图4可知,在反应温度150 ℃,反应时间10 h,催化剂为K2CO3,相转移催化剂为CTAB,n(ADHP-Na)∶n(K2CO3)∶n(CTAB)=1∶0.8∶0.1条件下,随着DMC用量增加,ADMP收率先增加后基本保持不变。当n(DMC)∶n(ADHP-Na)=7∶1时,ADMP收率最高(33.4%)。由于DMC沸点为90 ℃,在反应温度为150 ℃时,DMC会剧烈汽化并挥发,因此需要加入过量DMC以满足反应需求。研究发现,当n(DMC)∶n(ADHP-Na)=7∶1时,此时体系内DMC数量已满足实际反应需求。进一步增加DMC用量,对ADHP-Na转化率和ADMP收率的影响不大。因此最终选择n(DMC)∶n(ADHP-Na)=7∶1。

图4 DMC用量对反应性能的影响Fig.4 Effect of DMC dosage on reaction performance
2.1.4 反应温度对反应性能的影响
在反应时间10 h,投料比(摩尔比)为ADHP-Na∶CTAB∶DMC∶K2CO3=1∶0.1∶7∶0.8条件下,考察反应温度变化对反应性能的影响,结果如图5所示。由图5可知,随着反应温度升高,ADMP收率先增加后减少。当反应温度为130 ℃时,ADMP收率最高,为40.0%。较低的反应温度不利于DMC活化。同时,当反应温度由130 ℃进一步提高时,DMC会急剧汽化,从而造成有机相中DMC含量的降低,不利于反应的进行,导致ADHP-Na转化率和ADMP收率的降低。

图5 反应温度对反应性能的影响Fig.5 Effect of temperature on reaction performance
2.1.5 反应时间对反应性能的影响
在反应温度130 ℃,催化剂为K2CO3,相转移催化剂为CTAB,n(ADHP-Na)∶n(CTAB)∶n(DMC)∶n(K2CO3)=1∶0.1∶7∶0.8条件下,考察反应时间对甲基化反应性能的影响,结果如图6所示。随着反应时间增加,ADMP收率先增加后基本保持不变,当反应时间为10 h时,ADMP收率为40.0%。进一步增加反应时间,ADMP收率增加不明显。因此选择反应时间为10 h。
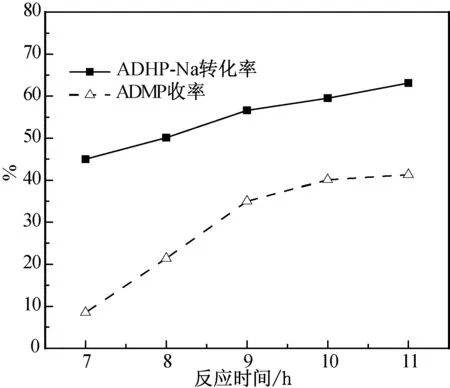
图6 反应时间对反应性能的影响Fig.6 Effect of time on reaction performance
2.2 正交优化实验
为了更加准确地确定反应最佳条件,在单因素实验基础上,以n(ADHP-Na)∶n(DMC)(A)、反应温度(℃)(B)、反应时间(h)(C)、n(ADHP-Na)∶n(K2CO3)(D)为因素,进行4因素3水平的L9(34)正交试验,正交试验结果如表2。由表2可知,影响反应各因素的显著性顺序为:反应温度>n(ADHP-Na)∶n(K2CO3)>反应时间>n(ADHP-Na)∶n(DMC)。优选方案为:A1B2C2D2,即反应时间10 h,投料比(摩尔比):ADHP-Na∶CTAB∶DMC∶K2CO3=1∶0.1∶7∶0.8,反应温度130 ℃。在此优选工艺条件下,进行了三次平行实验,ADMP收率分别为39.2%、40.1%和41.2%,平均收率为40.2%。

表2 正交试验结果L9(34)Tab.2 Results of orthogonal test L9(34)
2.3 产物结构表征分析
2.3.1 FT-IR分析
为确认合成产物的化学结构,判断是否成功合成目标产物ADMP,对其进行了红外光谱测定,图7为合成产物ADMP的红外谱图。由图7可知在3 451 cm-1和3 309 cm-1处出现的双峰为伯氨基的N-H 伸缩振动峰,峰型尖锐,与同样可能在附近出现的羟基峰有明显区别,由此可判断化合物含有伯氨基;3 153 cm-1处出现的吸收峰是嘧啶环上的C-H伸缩振动峰,640 cm-1~800 cm-1出现的多个较强吸收峰为嘧啶环上的C-H面外弯曲振动峰,2 794 cm-1~2 990 cm-1出现的一系列特征峰为甲氧基上的C-H伸缩振动峰;1 049 cm-1处的特征峰为=C-O-C伸缩振动峰,芳醚的对称伸缩振动峰一般出现在900 cm-1~980 cm-1,因此954 cm-1处出现的峰为芳醚的C-O-C对称峰,判断化合物有甲氧基;1 648 cm-1和1 606 cm-1处的强特征吸收峰为C=N 的伸缩振动峰,1 151 cm-1,1 220 cm-1,1 296 cm-1等特征吸收峰为C-N伸缩振动峰,1 364 cm-1和1 452 cm-1出现的特征峰为嘧啶环骨架吸收振动峰。由此可初步判定化合物为4-氨基-2,6-二甲氧基嘧啶。

图7 合成产物ADMP的红外谱图Fig.7 IR spectrum of ADMP
2.3.21H NMR分析
为确认产物化学结构,判断是否成功合成目的产物ADMP,使用1H NMR对其表征分析测定,图8为ADMP的1H NMR谱图。由图8可知,在化学位移δ=2.50处为溶剂峰DMSO,δ=3.35处为样品中残存的水峰。δ=6.63处为与嘧啶环相连的氨基上的2个氢(7号位)的特征峰,δ=3.38处为嘧啶环骨架上1个氢(3号位)的特征峰,δ=3.75、3.74处双重峰为两个甲氧基上6个氢(9号位和11号位)的特征峰。谱图各峰位置与相关文献报道一致,各峰积分面积比与氢个数比基本一致[28],因此进一步判断合成产物为ADMP。

图8 ADMP氢核磁谱图Fig.8 1H NMR spectrum of ADMP
2.4 反应机理分析
大多数酚类与DMC发生甲基化反应的机理为:碱性催化剂使酚类去质子化形成PhO-,然后PhO-进攻DMC的甲基碳或羰基碳,发生甲基化或甲氧羰基化反应。从电负性来看,羰基碳的电负性更高,因此甲氧羰基化反应更易进行,温度较低时更趋向于发生甲氧羰基化反应,这也是大多数DMC甲基化反应都在较高温度下进行的原因。对于氨基与DMC的反应来说,氨基是强给电子基可以进攻亲核试剂,不需碱或酸催化剂活化,本身就可以进攻DMC。在固液相反应时,只需相转移催化剂增强氨基与DMC的接触即可进行反应,因此本反应体系中ADMP选择性不高。ADHP-Na本身就是一种羟基钠盐,羟基已经去质子化,可以直接进攻DMC,因此不加固体碱K2CO3也能发生O-甲基化反应生成ADMP。但是不加入相转移催化剂CTAB时,DMC和ADHP-Na很难直接接触,因此转化率低。
ADHP-Na与DMC发生O-甲基化反应的反应机理示意图如图9。以ADHP-Na上的1个羟基钠盐为例解释,反应的时候两个羟基钠盐都反应,以Q+代表CH3(CH2)15N+(CH3)3。ADHP-Na不溶于DMF,因此很难与溶剂中DMC接触。相转移催化剂CTAB(Q+Br-)与ADHP-Na相互作用形成离子对,使原料进入有机相与DMC接触反应。原料中的嘧啶氧负离子进攻DMC的甲基碳,发生甲基化反应生成ADMP。DMC的离去部分分解为二氧化碳和甲醇钠,相转移催化剂CTAB再生。在本反应中起主要催化作用的是相转移催化剂CTAB,它能促进ADHP-Na和DMC接触。固体碱K2CO3的作用一般是使原料去质子化,但是ADHP-Na本身已经是去质子化形式,因此不需K2CO3原料也能与DMC反应。故K2CO3在体系中不起主要催化作用,但是一定量的K2CO3能提高ADMP的选择性。在同时有氨基和羟基参与反应时,一定量的K2CO3能提高O-甲基化反应选择性。

图9 DMC与ADHP-Na发生O-甲基化反应反应机理示意图Fig.9 Schematic diagram of the reaction mechanism of O-methylation reaction between DMC and ADHP-Na
3 结论
(1) 开发了一条以ADHP-Na为原料、DMC为绿色甲基化试剂,经过O-甲基化反应合成ADMP的工艺路线。
(2) 以ADHP-Na为原料合成ADMP的反应中,催化剂K2CO3和相转移催化剂CTAB的引入对甲基化反应的转化率与收率具有明显的影响。O-甲基化反应中相转移催化剂CTAB起主要催化作用,CTAB可以促进原料和DMC接触,并且一定量的固体碱K2CO3可以提高ADMP的选择性。
(3) 考察了甲基化反应中催化剂用量、反应时间、投料比、反应温度等对O-甲基化反应转化率和收率的影响。得到较佳的工艺条件为:以DMF为溶剂,投料比(摩尔比):ADHP-Na∶CTAB∶DMC∶K2CO3=1∶0.1∶7∶0.8,在130 ℃下反应10 h,ADMP收率为40.0%,选择性为67.2%。
(4) 提出了O-甲基化反应机理,CTAB与ADHP-Na相互作用使原料进入液相,ADHP-Na中的嘧啶氧负离子进攻DMC上甲基碳发生甲基化反应。
(5) 该工艺反应条件温和、操作方便、绿色环保,可完全避免含磷废水的产生,为ADMP的绿色合成提供了一条可行性路径。
